往期回顾
乳腺肿瘤WHO分类学习笔记(连载1)
乳腺肿瘤WHO分类学习笔记(连载2)
乳腺肿瘤WHO分类学习笔记(连载3)
乳腺肿瘤WHO分类学习笔记(连载4)
乳腺肿瘤WHO分类学习笔记(连载5)
乳腺肿瘤WHO分类学习笔记(连载6)
乳腺肿瘤WHO分类学习笔记(连载7)
乳腺肿瘤WHO分类学习笔记(连载8)
乳腺肿瘤WHO分类学习笔记(连载9)
乳腺肿瘤WHO分类学习笔记(连载10)
乳腺肿瘤WHO分类学习笔记(连载11)
乳腺肿瘤WHO分类学习笔记(连载12)
乳腺肿瘤WHO分类学习笔记(连载13)
乳腺肿瘤WHO分类学习笔记(连载14)
乳腺肿瘤WHO分类学习笔记(连载15)
第7章 男性乳房肿瘤
男性乳房肿瘤WHO分类
上皮性肿瘤
男性乳腺发育症
旺炽性男性乳腺发育症
8500/2 导管内癌,非浸润性,NOS
DCIS
LCIS
乳头PD
8500/3 浸润性(infiltrating)导管癌NOS
介绍
男性乳房是一种未发育的器官,其腺体成分仅限于乳晕后区的导管。男性乳腺上皮表达ER、PR和AR,并在一生中暴露于激素变化。特别是,随着年龄增长,性染色体拷贝数变异非常频繁。
尽管体积小,但男性乳房可发生多种良恶性疾病,发生于很大的年龄范围。良恶性结节的临床和放射学表现可能相似,其中大多数表现为乳晕后肿块。细胞学和组织学术前诊断与女性乳房中的诊断相似。然而,对于个体而言,男性乳房疾病罕见,需要足够的知识来建立诊断、预后和预测标准。
男性乳腺癌罕见(约占所有乳腺癌的1%),但死亡率高。男性乳腺癌的治疗方式与女性绝经后乳腺癌相似。常见复发。过去十年,多机构系列研究揭示了男性乳腺癌的发病机制,包括与女性乳腺癌的差异。分子研究表明,存在大量不同表达的基因,其中AR基因似乎在男性乳腺上皮细胞的肿瘤转化中起着驱动作用。
潜在的进一步挑战可能来自性别重置(性别肯定)*,无论是男变女还是女变男。目前几乎没有证据,但已发表的数据表明,激素刺激可能诱发乳腺癌。
*Sex Reassignment性别重置(gender confirmation性别肯定),旧称变性
性别重置手术是指通过外科手段(组织移植和器官再造)使手术对象的生理性别与其性别认同(旧称心理性别)相符,即切除原有的生殖器官并重建受术者认同性别的体表生殖器官和与之相匹配的第二性征的医疗技术。一般地,性别重置手术的受术者为易性症群体和间性人。根据受术者的需求可分为三种——男变女、女变男、间性人的性别肯定。
Gynaecomastia
男性乳腺发育症
定义
男性乳腺发育症(Gyn)是男性乳房腺体组织的良性弥漫性或局灶性增生。
ICD-O编码
没有
ICD-11编码
GB22 Gyn
相关术语
没有
亚型
旺炽性Gyn;纤维性Gyn
部位
大多数病例位于乳晕后,双侧性。
临床特征
Gyn通常表现为双侧乳晕后区弥漫性或离散性肿块。疼痛或无痛,也可能偶然发现。青春期或新生儿期的生理性Gyn是一种暂时的、通常自限性的增大。通过临床病史、体格检查以及实验室和影像学检查来识别具有潜在病理原因的患者非常重要。脂肪乳症(Lipomastia,假性Gyn)可能与真Gyn相混淆。
流行病学
婴儿、儿童和青少年的Gyn常见,通常是生理性。少数男性(通常年龄>26岁)是病理性,与导致激素失衡的未被充分认识的疾病有关。
病因
大多数病例是由由雄-雌激素比值异常和AR缺失或改变。Gyn可能是由于暴露于外源性雌激素(如膳食植物雌激素)、药物(包括合成代谢类固醇)、内源性雌激素产生增加(由于睾丸或肾上腺肿瘤或雄激素芳构化增加)、肥胖、酒精诱导的肝硬化、肾功能衰竭、衰老和甲状腺功能亢进引起的。雄激素缺乏症(原发性或继发性性腺功能减退症)主要由Klinefelter综合征、化疗、放疗或影响雄激素合成相关酶的药物(螺内酯、甲硝唑)引起。用于治疗前列腺癌的药物或许多AR缺陷(例如导致终末器官耐药的AR不敏感综合征)也会导致Gyn。在超过40%的病例中,未发现病因。
发病机制
雌激素、孕激素和雄激素参与女性乳腺发育症的发病,还涉及通过催乳素、IGF1、IGF2、LH和/或hCG受体介导的其他途径。瘦素及其受体的多态性可能通过改变脂肪细胞芳香化酶的表达或通过上皮成分的旁分泌作用导致Gyn。
表7.01Gyn的病因和发病机制概述
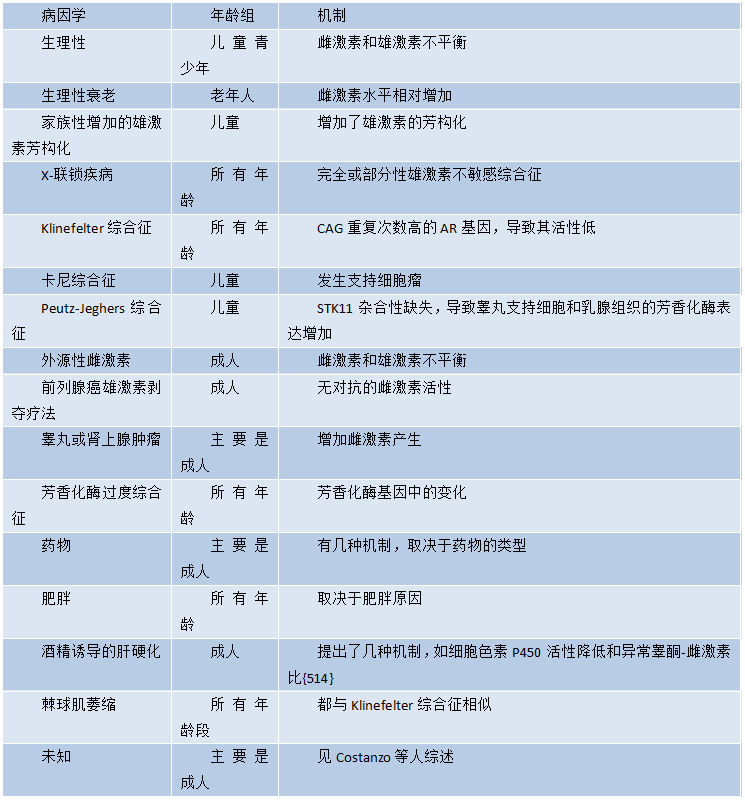
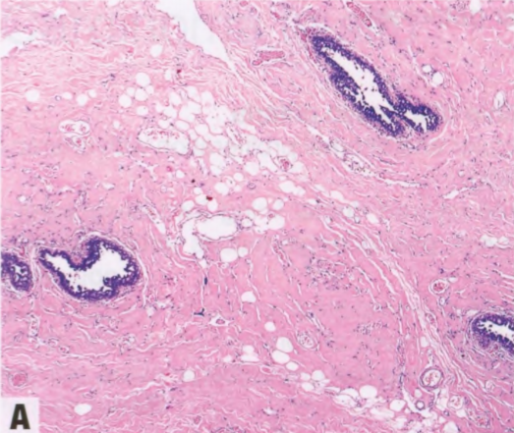

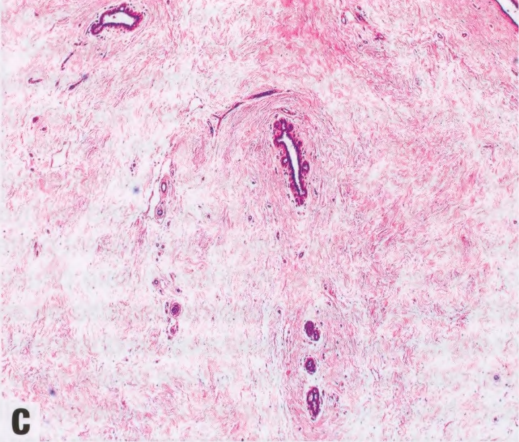
图7.01Gyn。A 旺炽性:乳腺导管周围有PASH。B 旺炽性:导管内衬旺炽性上皮,周围PASH。C 纤维性:特征是纤维间质和扁平上皮衬于导管。
表7.01总结了Gyn的病因和发病机制。Klinefelter综合征患者(47,XXY)在50-70%的病例中表现Gyn。在这种综合征中,AR基因中CAG重复的数量增加,导致其活性降低。重复越多,临床上Gyn越显著。Klinefelter综合征患者可能发生分泌hCG的生殖细胞肿瘤,这是Gyn的另一原因。与Gyn相关的其他遗传综合征包括棘球肌萎缩(通过AR外显子1中CAG重复扩增的类似机制)、完全或部分雄激素不敏感综合征、雄激素过量综合征(由芳香化酶基因或邻近增强子的改变引起)以及PeutzJeghers综合征和Carney综合征(导致睾丸支持细胞和乳腺组织中芳香化酶体表达增加)。

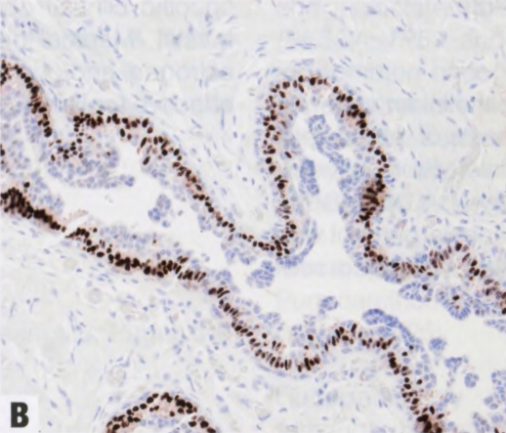
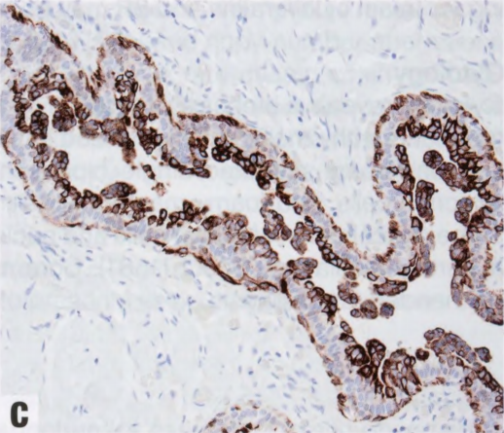
图7.02Gyn。A 导管显示三层衬覆上皮,有深染细胞和小乳头簇。B 中间层ER染色。C 内外层CK5/6染色。
大体检查
Gyn表现为乳头下方离散的、柔软的、橡胶状到质硬的灰色或白色肿块,或界限模糊的硬结区域。
组织病理学
组织病理学表现取决于导管和间质的相对比例。导管数量增加,由特征性的上皮细胞双层和肌上皮细胞外层组成。上皮细胞内层和肌上皮细胞外层可以用CK5/6和CK14来显示,上皮细胞中层呈ER、PR和AR阳性。导管周围是混有脂肪组织的间质。有两种主要的组织学模式,可能共存。旺炽性Gyn的特征是不规则的分支导管,内衬轻-中度增殖的细胞,细胞具有小簇、金字塔形微乳头、偶有真乳头或筛状结构。可能伴有肌上皮增生。周围的间质通常表现为导管周围的同心圆状袖套,可以是松散的、黏液样的或富细胞性(纤维母细胞)。常见PASH。纤维性Gyn的特征是透明变性、少细胞的导管周围间质,由于同心圆状袖套的扩张,通常呈融合模式。还可见中间模式,为旺炽性和纤维性模式的混合。罕见大汗腺化生或鳞状化生。在女性乳房中观察到的多核间质细胞也有描述,见于1型神经纤维瘤病患者。在Klinefelter综合征中,可见致密的透明变性间质,导管很少。
Gyn样增生应区分ADH和DCIS。基底样CK和ER染色可能有帮助。
细胞学
细胞学显示,上皮和间质碎片呈双相分布,其中小-中等扁平导管细胞片段被散在的单双极核包围。梭形细胞、顶泌细胞和泡沫巨噬细胞也可能存在。导管细胞可能出现一些非粘附性和核增大深染。建议进行粗针活检以进行诊断。
诊断分子病理学
与临床无关
诊断标准
必要标准:良性导管和间质增生,具有特征性的间质袖套。
理想标准:典型的三层导管衬覆上皮(两个基底层和一个管腔层);PASH。
分期
与临床无关
预后和预测
Gyn不伴乳腺癌风险。由于大多数Gyn病例在2年内消退,因此通常不需要治疗,除非在突然或有症状Gyn的特定临床背景下。药物治疗包括芳香化酶抑制剂、抗雌激素和/或雄激素治疗。激素治疗对旺炽性和青春期Gyn最有效。
Carcinoma in situ
原位癌
定义
男性乳腺原位癌是局限于乳腺导管的上皮细胞的肿瘤性增殖,涵盖了女性乳腺中观察到的所有原位癌。
ICD-O编码
8500/2 导管内癌,非浸润性,NOS
ICD-11编码
2E65.2&XH4V32乳腺DCIS&DCIS NOS
2E65.0&XH6EH0乳腺LCIS&LCIS NOS
相关术语
没有
亚型
DCIS;LCIS;乳头PD
部位
男性乳腺癌几乎只局限于乳晕后区。
临床特征
男性乳腺原位癌有三种不同的临床情形:作为Gyn的偶然发现,伴发浸润性癌,或纯原位癌伴不同症状和临床特征。症状持续时间从几个月到8年不等。纯原位癌最常表现为老年男性的乳晕后肿块,平均年龄范围为58-65岁,可能双侧性。原位癌罕见于年轻男性和青少年。大导管受累伴有血性乳头溢液。在PD中,乳头乳晕复合体呈现逐渐增大的湿疹样病变。仅通过乳房X线进行诊断可能很困难,而MRI有助于做出正确的诊断。
流行病学
男性乳腺原位癌,几乎全是DCIS,多达46.2%的病例伴浸润性癌。纯原位癌更罕见,最近的数据表明,它占所有男性乳腺癌的10%,占年轻和青春期男孩乳腺癌的18%。小系列报道,Gyn的原位癌发病率为6.76%。PD占所有男性乳腺癌的1.45%。
病因
病因与女性乳腺浸润性癌的病因相似(第82页)。
发病机制
其发病机制与浸润性男性乳腺癌相似(见浸润性癌,第257页)。关于男性原位癌的分子特征的数据很少,并且与DCIS有关,这些数据表明原位癌和相关浸润性癌之间存在密切关系,PIK3CA、TP53和GATA3中存在类似的突变,常见癌基因的拷贝数异常。在极少数病例中,DCIS附近出现柱状细胞样改变,浸润性癌显示相同的突变特征。DCIS中已发现与AR拷贝数增加相关的X染色体异常。
大体检查
纯原位癌表现为不规则肿块,有时为囊性肿块。
组织病理学
尽管在女性乳腺中观察到的所有原位癌也可以在男性乳腺中发现,但绝大多数(97.9%)的男性原位癌是DCIS,而LCIS罕见。大多数纯DCIS具有低或中等核级别,乳头状或微乳头状结构,而伴有粉刺型坏死的高级别DCIS通常伴高级别浸润性癌。DCIS的核分级、组织类型和免疫表型通常与并发浸润性癌的分级和类型相关。DCIS似乎伴有非特殊型(NST)浸润性癌,而罕见LCIS病例可能伴浸润性小叶癌、浸润性癌NST或混合型浸润性癌。原位成分中的ER、PR和HER2状态能反映浸润性成分的状态。
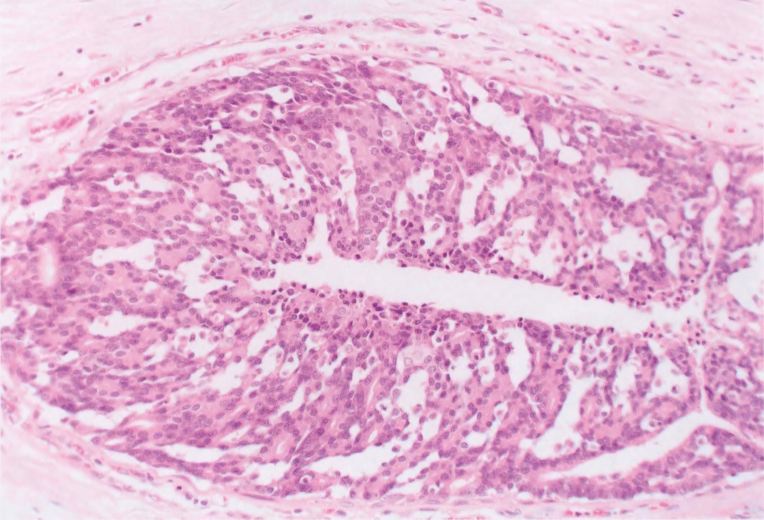
图7.03男性乳腺DCIS。男性乳腺原位癌最常见导管型,如本例所示,具有乳头状和筛状特征。
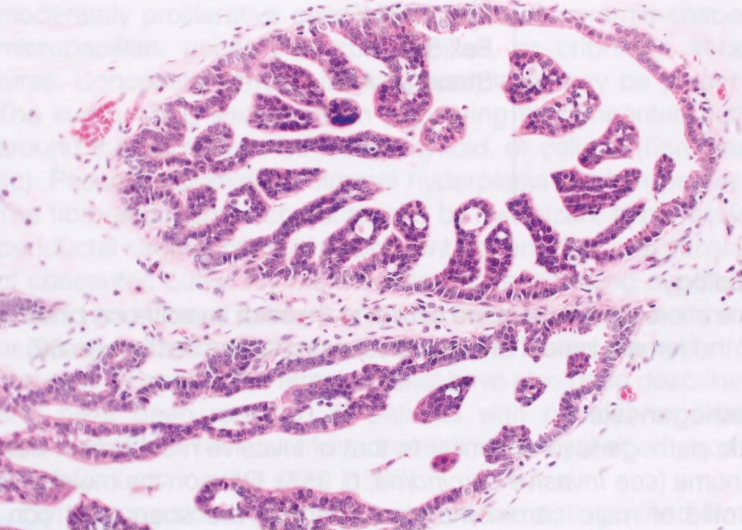
图7.04男性乳腺DCIS。乳头状特征的一个例子。
偶尔,原位癌具有包裹性乳头状癌的特征,可能缺乏肌上皮层。PD与女性乳房相似。柱状细胞样变化可伴有DCIS。这些病例的特征是扩张的导管,内衬单形性轻度非典型细胞,顶端有胞质突起。很少出现微钙化和分泌物。
细胞学
目前还没有关于纯男性原位癌的FNA文献。粗针活检是诊断的首选。
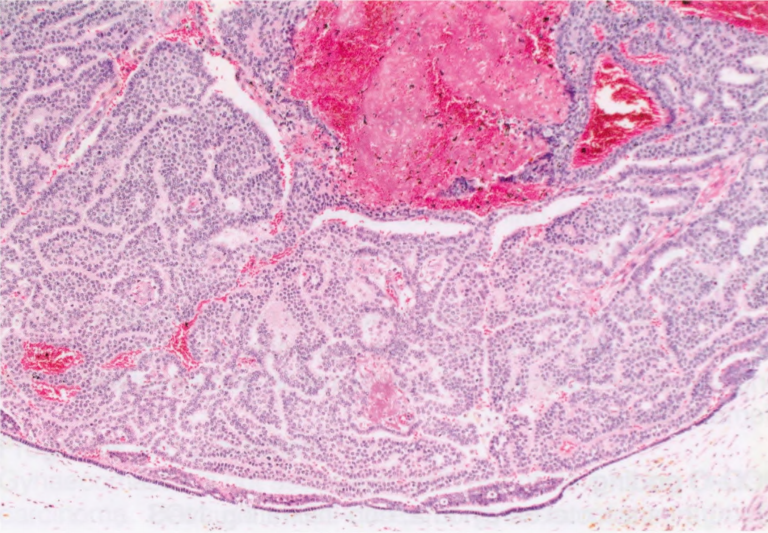
图7.05男性乳腺DCIS。包裹性乳头状癌。
诊断分子病理学
与临床无关
诊断标准
诊断标准与女性乳腺DCIS的诊断标准相似(第80页)。
分期
分期与女性乳腺DCIS的诊断标准相似(第80页)。
预后和预测
伴有浸润性癌的原位癌,治疗方法与浸润性疾病相似。纯DCIS预后好。在一个系列中,31例中有4例复发:1例为DCIS,3例为浸润性癌。有人认为,浸润性癌旁存在DCIS与管腔A组和管腔B HER2富集组的较长总生存期有关。
Invasive carcinoma
浸润性癌
定义
男性乳腺浸润性癌是一种罕见的恶性上皮性肿瘤,其组织学与女性乳腺中的相应肿瘤相似。
ICD-O编码
8500/3 浸润性导管癌NOS
ICD-11编码
2C61.0&XH7KH3乳腺浸润性癌NOS&浸润性导管癌NOS
相关术语
与女性乳腺浸润性癌相似
亚型
与女性乳房中观察到的相同
部位
男性乳腺癌通常局限于乳晕后区。
临床特征
男性乳腺癌通常表现为乳罩下区域的单侧无痛肿块,通常略偏心于乳头。出血或浆液性分泌物可能是首发症状。由于男性乳腺组织通常较少,肿瘤很容易浸润上方皮肤或下方筋膜/肌肉。
流行病学
在美国,男性乳腺癌占所有乳腺癌的<1%,占所有男性癌症死亡的<0.5%。过去几十年,英美加澳的男性乳腺癌发病率有所上升。据报道,以色列发病率最高(每10万男人每年1.24例),泰国的发病率最低(每10万男人每年0.16例)。男性乳腺癌在黑人男性更常见、更年轻也更晚期,乳腺癌特异性死亡率更高。女性乳腺癌有两个年龄峰值,男性乳腺癌的发病年龄略高于绝经后女性的乳腺癌(中位数:68.4岁)。然而,它也累及年轻和青春期的男孩。Klinefelter综合征导致男性患乳腺癌的相对风险为30-50(由于循环雌激素增加);多达男性乳腺癌的5%,死亡率增加57.8倍。患乳腺癌的风险也可能受到与性别重置(性别确认)相关的激素变化的影响,包括男变女和女变男。
病因
导致雌激素相对过量的激素失衡(如肝硬化或Klinefelter综合征)最常与男性乳腺癌的发生有关。正如其他癌症一样,年龄会增加男性患乳腺癌的风险。肥胖也与这种疾病有关,最近体重指数的增加产生了显著影响。隐睾、流行性腮腺炎、睾丸炎、睾丸创伤和前列腺癌也会增加男性患乳腺癌的风险。
大约20%的男性乳腺癌患者有乳腺癌一级家族成员。有女性或男性乳腺癌家族史的男性,乳腺癌的风险增加2-3倍。1/3家族性男性乳腺癌似乎发生在BRCA1/2突变携带者中,其余的与其他基因(如CHEK2和PALB2)有关,而其他病例的潜在遗传机制尚不清楚。在男性乳腺癌中,BRCA2的突变和重排比BRCA1更频繁。大约5-10%的男性BRCA2携带者一生中会发生乳腺癌,而BRCA1携带者的这一比例为1-2%。BRCA1/2男性乳腺癌显示与BRCA1/2女性乳腺癌不同的病理特征,并且它们表现出侵袭性更强的表型。
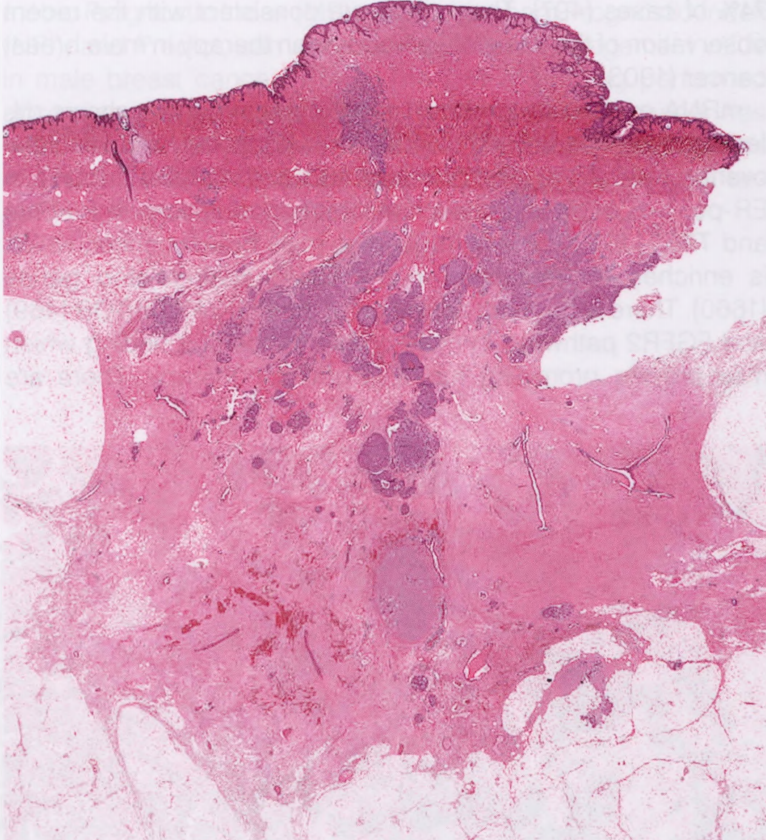
图7.06男性乳腺浸润性癌。男性乳腺浸润性癌最常见于乳晕后区。
电离辐射和电磁辐射、饮酒、吸烟和食用红肉等环境因素与男性乳腺癌发病率的增加有关。大多数研究都没有发现Gyn和男性乳腺癌之间有令人信服的致病联系。
发病机制
确切的发病机制尚不完全清楚,一般认为遗传、激素和环境因素导致激素失衡,雌激素与雄激素的比例相对过高,导致乳腺上皮细胞增殖增强。最近发表的几项分子研究显示了男性和女性乳腺癌之间的差异,男性的管腔型癌比例高于女性,男性乳腺癌中HER2富集、基底样和三阴性亚型的比例几乎是女性乳腺癌的一半。
ER-阳性男性乳腺癌的染色体获得和丢失的模式与ER-阳性女性乳腺癌相似,除外男性乳腺癌的X染色体获得。多数男性乳腺癌具有BRCA2样特征。男性乳腺癌表现出CCND1扩增更频繁,17号染色体上的拷贝数变化更少,16q上的拷贝号丢失更少。AR作为驱动基因在男性乳腺癌中的作用已得到充分证实。AR在男性乳腺癌中高度表达,约74%的病例中出现X染色体非整倍体和随后的AR基因多态性。这些数据与最近观察到的抗雄激素治疗在男性乳腺癌中的价值一致。
男性乳腺癌的mRNA表达谱与女性乳腺癌不同,很少重叠。在ER-阳性、HER2-阴性肿瘤中发现的16q缺失和突变(例如PIK3CA和TP53中的突变)在男性乳腺癌中较少见,其富集了DNA修复相关基因的突变。在男性乳腺癌中,PI3K/AKT/mTOR和FGFR2通路经常激活,这一发现可能为未来的治疗提供有前景的靶点。与女性乳腺癌相比,男性乳腺癌甲基化基因既有相似又有差异,男性乳腺癌甲基化率总体低,但高级别男性乳腺癌ESR1和GSTP1甲基化相对频繁。关于男性乳腺癌中微小RNA数量有限的数据有限,但这些微小RNA与女性乳腺癌中的微小RNA不同。
大体检查
男性乳腺癌通常形成大的星芒状或结节状肿块,也可能累及乳头。
组织病理学
最常见的浸润性男性乳腺癌类型是非特殊型(NST)浸润性导管癌。第二常见的肿瘤是乳头状癌,这与女性乳腺癌不同。浸润性小叶癌极罕见。其他特殊类型,如黏液癌、小管癌和化生性癌,也极罕见。大多数肿瘤为2级。在高级别男性乳腺癌中,可能发现纤维化病灶。
男性乳腺癌通常为ER阳性和/或PR阳性(>90%的病例),AR表达频繁。HER2阳性、三阴性和基底样肿瘤都罕见。乳腺上皮的典型标记物,如GATA3、cyclin D1、mammaglobin、BCL2和GCDFP-15(BRST-2),在大多数男性乳腺癌中表达,并在转移中保持不变。
据报道,前哨淋巴结和腋窝清除标本使用了与女性乳腺癌相同的指南。原发性男性乳腺癌应区分转移癌,包括PSA、PSMA和NKX3-1阳性的转移性前列腺癌。
细胞学
当由经验丰富的细胞病理医师进行FNA时,可以做出准确的诊断。细胞学特征与女性乳腺癌相似。穿刺活检是诊断男性乳腺癌的金标准。
诊断分子病理学
与临床无关


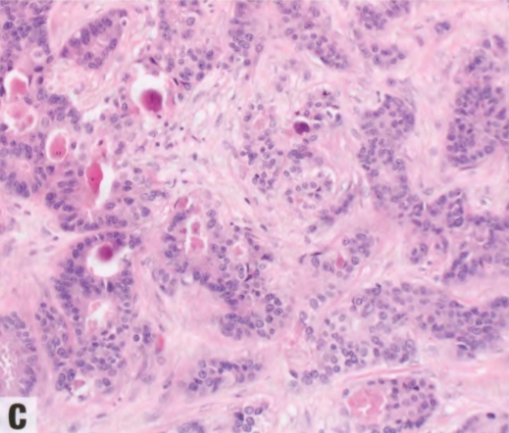
图7.07男性乳腺浸润性癌。A 大多数浸润性癌属于NST。B 浸润性癌NST显示微乳头状特征。C 可能发生微钙化。


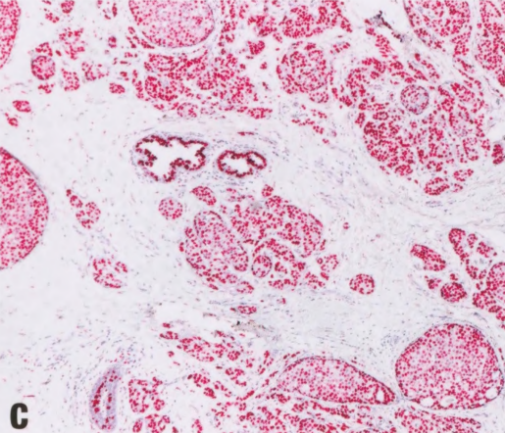
图7.08男性乳腺浸润性癌。ER(A)、PR(B)和AR(C)通常强阳性。
诊断标准
必要标准:诊断标准与女性乳腺癌相同;乳腺上皮的浸润性恶性肿瘤,无外周肌上皮细胞层(可能需要免疫组化),伴或不伴原位癌;ER、PR和HER2免疫组化用于指导分类、治疗和预后。
分期
国际癌症控制联盟(UICC)第八版TNM分类应用于女性乳腺癌。
预后和预测
EORTC 10085/TBCRC/BIG/NABCG国际男性乳腺癌计划的数据表明,大多数男性乳腺癌患者患有T1(48.7%)或T2(38.3%)疾病。40.6%的病例有腋窝淋巴结转移,淋巴结转移数量少(N1:32.2%,N2:5.3%,N3:3%)。据报道,在一小部分病例(5.1%)中出现了远处转移。
临床结局受分期、激素受体状态、核分裂象计数、分级、分子亚型和淋巴结状态的影响。淋巴结阳性对无病生存率和总生存率有不利影响。尽管数据相互矛盾,但人们普遍认为,男性乳腺癌的预后类似于分期和年龄相同的女性乳腺癌。有研究表明,已婚患者的5年生存率明显更高,这表明配偶支持的重要性。
由于报道的男性乳腺癌数量较少,几乎没有预后标记物。然而,与女性乳腺癌一样,激素受体表达和HER2状态被用作治疗反应的预测因素。应用于女性乳腺癌的预后模型,如形态计量预后指数(MPI)、诺丁汉预后指数(NPI)和预测,也可以对男性乳腺癌具有实际管理价值。根据女性乳腺癌标准进行分级的作用受到了挑战,因为核分裂象计数的阈值可能不同。BRCA2样特征可能表明靶向治疗的益处,正如在女性乳腺癌。
未完待续......






























共0条评论