[导读] 编译整理:强子
实用学文献-妇科病理诊断及鉴别诊断中的免疫组化要点(一)
实用学文献-妇科病理诊断及鉴别诊断中的免疫组化要点(二)
实用学文献-妇科病理诊断及鉴别诊断中的免疫组化要点(三)
实用学文献-妇科病理诊断及鉴别诊断中的免疫组化要点(五)
实用学文献-妇科病理诊断及鉴别诊断中的免疫组化要点(六)
实用学文献-妇科病理诊断及鉴别诊断中的免疫组化要点(七)
实用学文献-妇科病理诊断及鉴别诊断中的免疫组化要点(八)
实用学文献-妇科病理诊断及鉴别诊断中的免疫组化要点(九)
实用学文献-妇科病理诊断及鉴别诊断中的免疫组化要点(十)
实用学文献-妇科病理诊断及鉴别诊断中的免疫组化要点(十一)
实用学文献-妇科病理诊断及鉴别诊断中的免疫组化要点(十二)
四. 子宫上皮性肿瘤
1. 子宫内膜腺癌
宫体最常见的上皮性肿瘤为高分化子宫内膜样癌,但也可有诸如浆液性癌、透明细胞癌、癌肉瘤等;后述这些肿瘤相互形态学之间、以及和高级别子宫内膜样癌之间有显著重叠。不过,准确鉴别还是很有意义的,因为不同肿瘤的预后、对放化疗的反应等均有所不同。
子宫的癌最常用免疫组化目的有:(1)区分癌的亚型;(2)排除中肾管或非中肾管来源癌的转移,前者如宫颈或卵巢来源的癌,后者如肺、乳腺等其他部位来源的癌;(3)低分化癌和未分化癌、癌肉瘤的鉴别。最常用的标记物有PAX8、p53、p16、ER、PR、AMACR、Napsin A、HNF1β、WT1。
PAX8与中肾管、甲状腺、肾脏的器官形成有关,对应于这一谱系性转录因子在中肾管发育过程中的作用,相应良性上皮性结构、恶性病变中,均有PAX8的阳性表达。实际工作中PAX8已成为证实相应的癌为子宫及相应中肾管来源应用最多的标记物,尤其癌表现为转移性病变时;也用于排除其他PAX8阴性原发癌(如乳腺癌、肺癌、胃肠道癌)转移至中肾管相应结构的目的。对于子宫和卵巢的浆液性癌、子宫内膜样癌、透明细胞癌均较敏感,在宫颈腺癌中仅极少数阳性。
子宫的子宫内膜样癌一般表达PAX8、ER、PR,p16呈斑片状阳性。子宫肿瘤如出现p16弥漫阳性、且激素受体阴性或局灶阳性,应立即想到浆液性癌、或宫颈管来源肿瘤的可能,其中宫颈管来源肿瘤可表达CEA,而大部分子宫内膜样癌中CEA为阴性。对于疑难病例可进行HPV原位杂交以明确其为宫颈来源腺癌。
子宫的子宫内膜样癌大部分病例p53均为异质性表达,即野生型;但小部分高级别病例中可见弥漫强阳性、或完全缺失。另外,子宫内膜样癌有少部分病例可见错配修复(mismatch repair,MMR)蛋白染色缺失、提示微卫星不稳定(microsatellite instability,MSI)。不管相应标记物表达如何,出现鳞状分化和/或黏液样分化都是提示子宫内膜样分化的形态学线索。
子宫浆液性癌几乎总是会有p53的突变,因此免疫组化为弥漫强阳性、或完全缺失。相反,非典型细胞异质性表达(野生型)p53,更可能是反应性非典型而非浆液性癌,尤其子宫内膜息肉中时更是如此;MIB1增殖指数低也可以进一步支持为反应性的诊断。
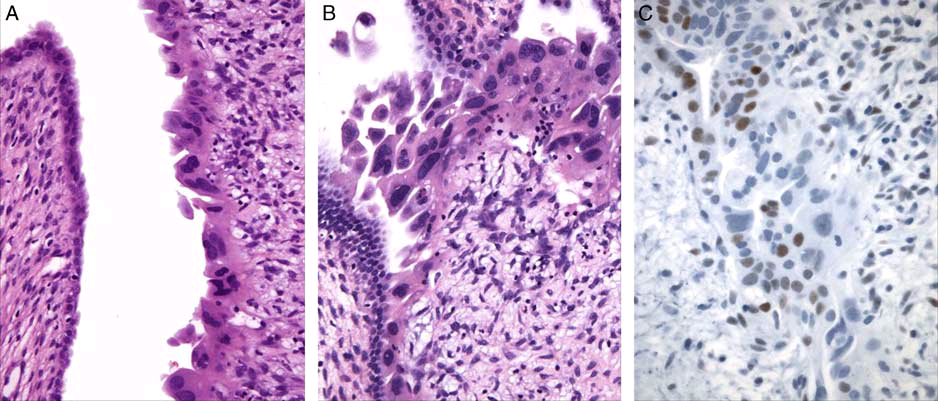
图1. 伴细胞学非典型的子宫内膜息肉;小的息肉碎片或息肉表面中可见有显著细胞学异型性,需考虑浆液性癌可能;免疫组化p53呈异质性表达(即野生型),加之MIB1增殖指数低(未示),支持反应性改变而不支持肿瘤性病变。
浆液性癌中p16常为弥漫阳性,此时不要和宫颈处的腺癌混淆。与卵巢的浆液性癌相反,子宫浆液性癌大部分为WT1阴性,这对于子宫和中肾管上段部分均有浆液性癌的病例来说尤其有帮助。比如,WT1阴性的子宫浆液性癌、同时中肾管上段部分并存有WT1阳性的浆液性癌,则支持为同时双原发肿瘤;相反,子宫和中肾管上段部分并存的肿瘤均为WT1阳性、或均为阴性,则更可能是一处原发、转移至另一处。当然,免疫组化并非100%敏感和特异,具体诊断中还应结合形态学特征及相关预后指标来综合考虑,如肿瘤有子宫深部肌壁的浸润及脉管侵犯等。
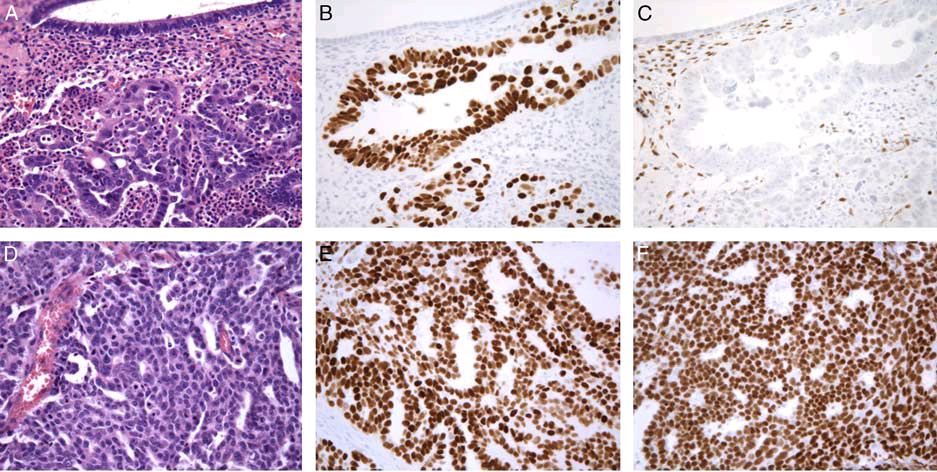
图2. 浆液性癌。本例子宫内膜息肉(A)和网膜(D)中均有浆液性癌成分,且两处的免疫组化均为p53弥漫阳性(B、E)。不过,息肉中的癌WT1阴性(C)而网膜中的癌WT1阳性(F),支持这是两处同时双原发的癌。
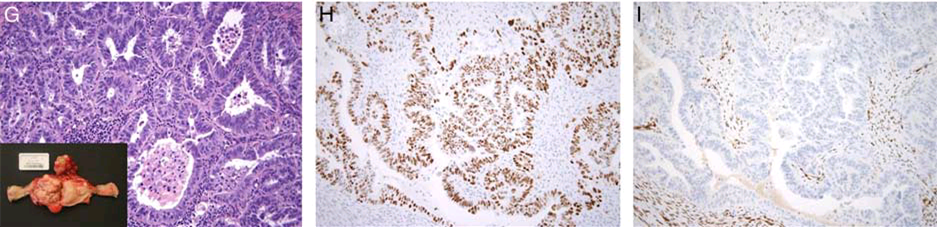
图3. 本例宫腔及卵巢均有肿物,左图示卵巢癌为浆液癌形态,免疫组化p53弥漫阳性,而WT1阴性;子宫处的癌WT1也为阴性(未示),因此卵巢处病变符合子宫浆液性癌转移。
子宫透明细胞癌属于子宫内膜癌中的罕见亚型,且临床一般分期较晚、对化疗效果欠佳。典型情况下,该肿瘤表现为管状乳头状生长,细胞具有高度异型性,细胞之间分界清晰,细胞核大而深染,胞质透明。间质透明样变也是该肿瘤的特征,且可能是较好的形态学线索。
最近有研究称透明细胞癌的发病机制与ARID1A基因有关,大部分透明细胞癌中均有ARID1A的免疫组化着色缺失,不过该抗体实际工作中应用较少。关于该肿瘤,也有其他相关标记物的研究,如Napsin A(高度敏感)、AMACR/p504S(高度特异)、HNF1β(高度敏感,但特异性稍差),不过无一具有完全的敏感性或特异性。综合而言,Napsin A和AMACR阳性,尤其ER、PR为阴性的情况下,则非常支持透明细胞癌的诊断。
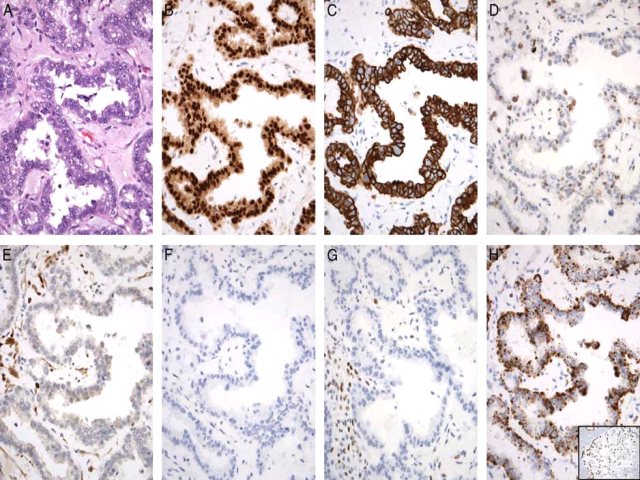
图4. 子宫透明细胞癌,细胞具有显著异型性,呈靴钉样,且有玻璃样变的间质;免疫组化PAX8(B)、CK7(C)、Napsin A(H)、HNF1β(H插图)阳性;p53呈野生型(D),p16(E)、ER(F)、PR(G)阴性。透明细胞癌中AMACR一般也为阳性。卵巢透明细胞癌中免疫组化与此类似。
相应指标在鉴别伴透明细胞特征、伴分泌性改变、伴卵黄囊分化的子宫内膜样癌时也很有帮助。这些病变均可类似透明细胞癌,这些病变中的细胞核特征一般为低级别,而透明细胞癌中的细胞核特征一般为高级别。ER、PR阳性且Napsin A、AMACR、HNF1β阴性或局灶阳性,则不支持透明细胞癌的诊断而支持子宫内膜样癌的诊断。需要注意的是,部分子宫内膜样癌中不表达Napsin A、AMACR的情况下,HNF1β阳性,且表达SALL4、GATA3,则支持卵黄囊分化。最后,p53在浆液性癌中一般为弥漫阳性,但在大部分透明细胞癌中为异质性(野生型)表达;这是一个诊断陷阱,因为部分透明细胞癌也会有p53的突变,因此不能仅凭免疫组化而排除透明细胞癌的诊断。与浆液性癌相反,透明细胞癌中p16一般为局灶阳性或阴性。
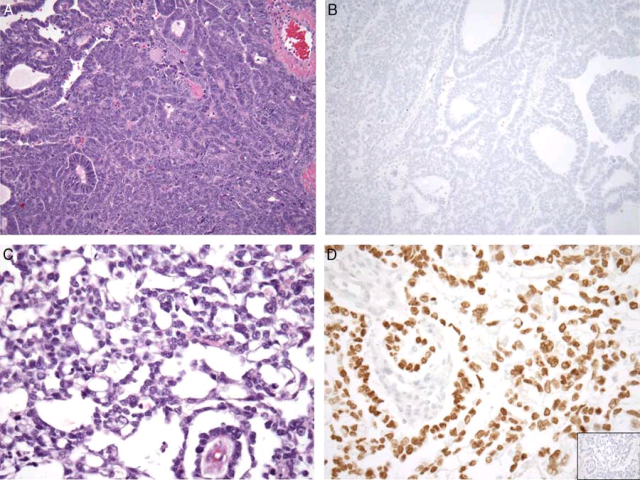
图5. 伴卵黄囊分化的中肾管癌。形态学可见异质性,鉴别诊断需考虑到子宫内膜样癌、浆液癌、透明细胞癌、以及其他罕见的情况。致密腺性成分中,免疫组化p53为野生型表达(未示),SALL4阴性(B),符合子宫内膜样癌;而疏松腺性成分中SALL4弥漫阳性(C、D),符合卵黄囊分化;AFP阴性(D中插图),但该标记物敏感性差。
点击下载英文文献
参考文献
Hirsch MS, Watkins J.A Comprehensive Review of Biomarker Use in the Gynecologic Tract Including Differential Diagnoses and Diagnostic Pitfalls[J].Advances in anatomic pathology,2019,.
DOI:10.1097/PAP.0000000000000238


















共0条评论