往期回顾:
消化系统肿瘤WHO分类第五版学习笔记(一)
消化系统肿瘤WHO分类第五版学习笔记(二)
消化系统肿瘤WHO分类第五版学习笔记(三)
消化系统肿瘤WHO分类第五版学习笔记(四)
消化系统肿瘤WHO分类第五版学习笔记(五)
01. 胃鳞状细胞癌
定义
胃鳞状细胞癌是一种恶性胃上皮肿瘤,表现为鳞状细胞分化,其特征是角质形成细胞型细胞具有细胞间桥和/或角化。
ICD-0编码
8070/3鳞状细胞癌NOS
ICD-11编码
2B72&XH胃恶性肿瘤和鳞状细胞癌NOS
相关术语
无
亚型
无
部位
胃的上部、下部和中部按频率递减的顺序受到影响。
临床特征
其临床特征与其他胃癌相同。
流行病学
可用数据有限。原发性胃鳞状细胞癌占所有胃癌的0.04-0.07%,据报道<100例。
病因
未知
发病机制
已经提出了各种起源,包括通过胃黏膜鳞状细胞化生、多能干细胞、胃黏膜异位鳞状巢或经历鳞状化生的胃癌。
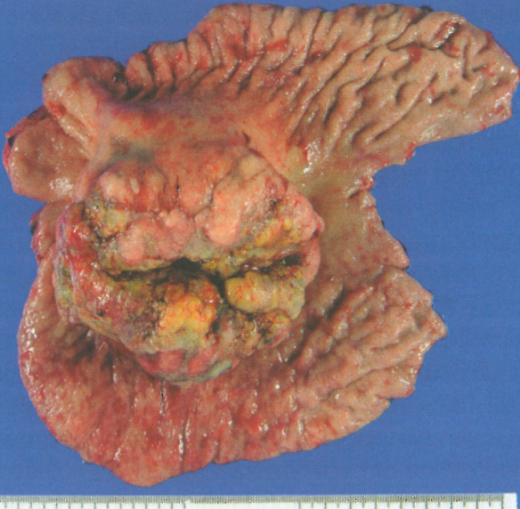
图3.41原发性胃鳞状细胞癌。外观粗糙。
大体表现
宏观外观与其他胃癌相同。
组织病理学
组织学与食管鳞状细胞癌(见食管鳞状乳头状瘤,第30页)和其他器官的组织学相似。肿瘤显示均匀的鳞状细胞分化,在彻底取样时没有任何腺癌或其他组织学成分。必须进行足够的取样以排除另一种成分,排除另一器官鳞状细胞癌的转移也是如此。应排除下段食管鳞状细胞癌的延伸。
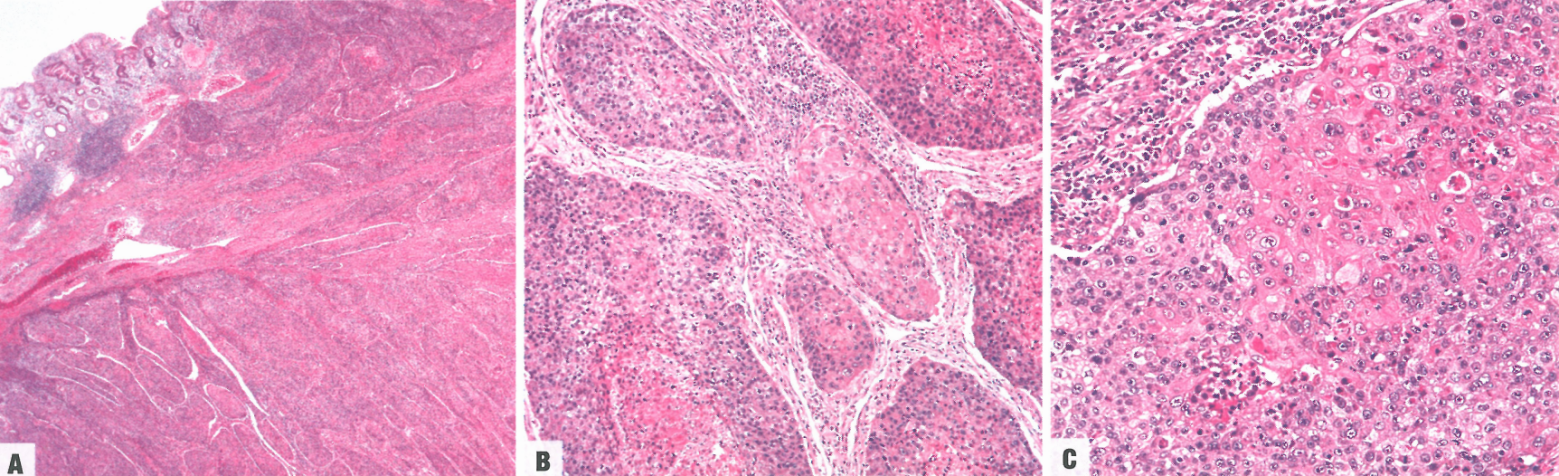
图3.42胃鳞状细胞癌。渗透性胃壁。B显示恶性鳞状细胞浸润巢,伴有大面积坏死。C高倍镜。
细胞学
无临床相关性
诊断分子病理学
没有确凿的数据。
诊断标准
无
分期(TNM)
胃鳞状细胞癌经常出现在晚期,这与预后不良有关。在晚期疾病中,扩散到肝脏是常见的。
预后和预测
由于这种疾病的罕见性,尚未确定具体的预后特征。诊断时的疾病阶段可能是预后的主要决定因素。胃鳞状细胞癌的表现似乎比同一疾病阶段的腺癌更具浸润性。
02. 胃腺鳞癌
定义
胃腺鳞癌是一种原发性胃癌,由腺细胞和鳞状细胞成分组成,鳞状细胞成分占肿瘤的25%以上。
ICD-0编码
8560/3腺鳞癌
ICD-11编码
2B72&XH胃恶性肿瘤和腺鳞癌
相关术语
无
亚型
无
部位
胃腺鳞癌最常见于下三分之一,其次是上三分之一和中三分之一。应排除最常见的食管胃交界处腺鳞癌的延伸。
临床特征
胃腺鳞癌的临床特征与其他类型的癌症相似。大多数肿瘤表现为大肿块,平均大小为5cm。
流行病学
胃腺鳞癌占所有胃癌的0.25%。男性受影响最为严重,平均年龄为60岁。
病因
未知
发病机制
未知
大体表现
大体外观与其他胃癌相似。
组织病理学
胃腺鳞癌由腺癌和鳞状细胞癌以不同比例混合而成。鳞状细胞成分应占肿瘤的25%以上。鳞状细胞成分可能显示食管和其他部位常规鳞状细胞癌中已知的所有细胞学和结构特征。黏液染色有助于突出显示腺体分化区域;p63/p40免疫组织化学可能有助于确定鳞状细胞成分的存在和范围。
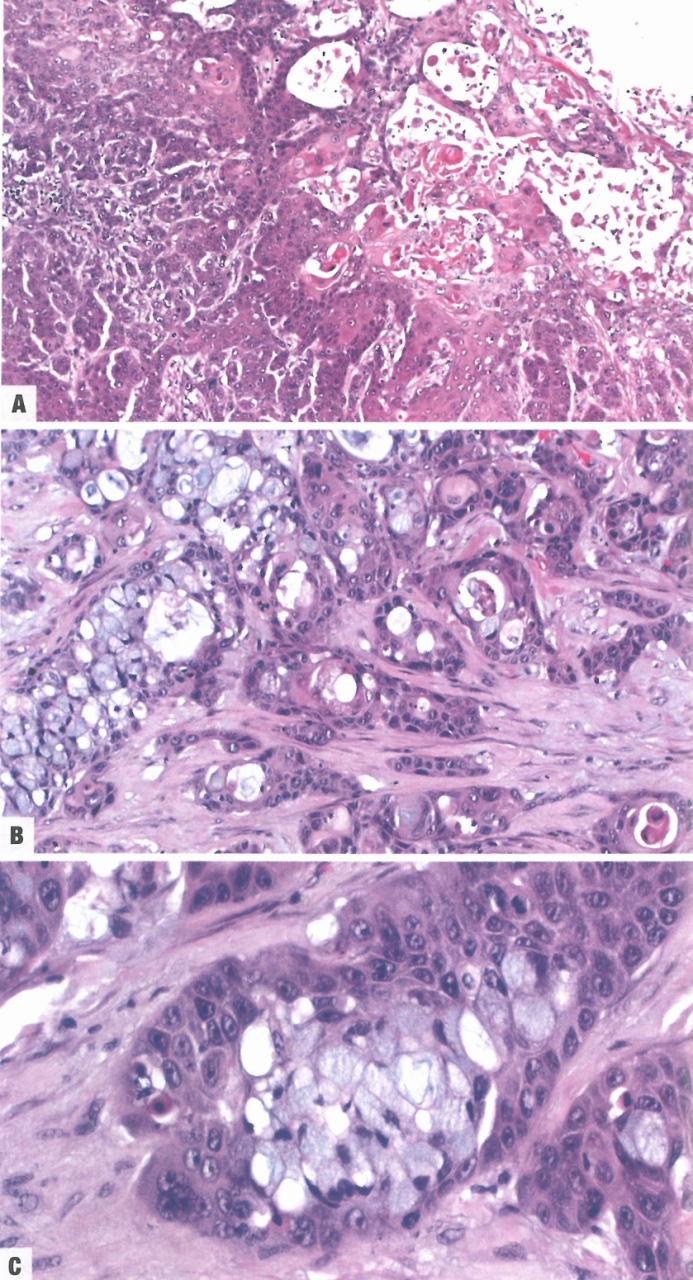
图3.43胃腺鳞癌。A浅表部分可能与胃纯鳞状细胞癌无法区分。B从纯鳞状区域(右)过渡到杯状细胞丰富的腺体区域(左)。C高倍放大显示鳞状细胞巢内杯状细胞样分化,呈现杂交模式。
细胞学
无临床相关性
诊断分子病理学
无临床相关性
诊断标准
必要标准:真正的腺体或黏液细胞分化。
注:单纯鳞状细胞癌鳞状病灶内腺样体或微囊性改变不足以诊断。
分期(TNM)
肿瘤扩散到局部淋巴结和肝脏或腹膜是常见的。淋巴结转移主要来自腺癌成分,但在转移中可能会看到鳞状细胞成分或两种成分。
预后和预测
由于该疾病的罕见性及其普遍的浸润性,尚未确定具体的预后特征。诊断时的疾病阶段是主要的预后决定因素。
03. 胃未分化癌
定义
胃未分化癌是一种由间变性细胞组成的原发性胃癌,没有特定的细胞学或结构分化类型。
ICD-0编码
8020/3癌,未分化,NOS
ICD-11编码
2B72和XH1YY4胃恶性肿瘤和癌,未分化,NOS
相关术语
可接受:间变性癌;多形性癌。
不推荐:巨细胞癌。
亚型
大细胞癌伴横纹肌样表型(/3);多形性癌(/3);肉瘤样癌(/3);破骨细胞样巨细胞癌(/3)
部位
在胃内没有观察到特定的定位,但多个区域的弥漫性受累并不罕见。
临床特征
大多数患者表现为大面积溃疡和广泛性溃疡
坏死透壁性蕈伞样肿块,通常与广泛的同步区域转移有关。大多数最初局限性疾病的患者在诊断和手术后不久就会出现广泛的转移,大多数患者在1年内死于该疾病。
流行病学
可用数据有限。据估计,未分化的横纹肌样癌占所有胃癌的0.1-0.3%,占实体腺癌的5.6%。
病因
未知
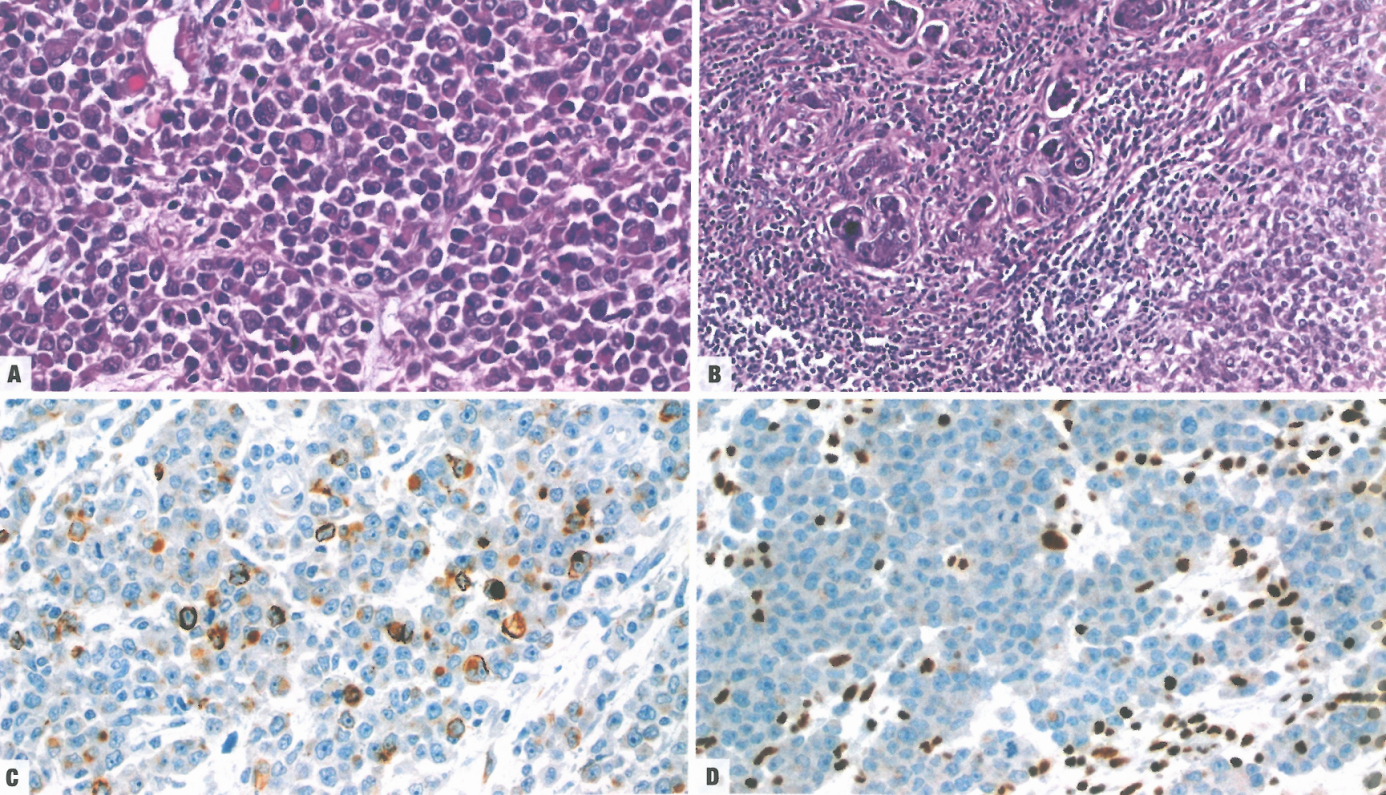
图3.44胃未分化癌。横纹肌样分化。B在大多数充分取样的胃未分化癌中可见少量腺体成分。C广谱角蛋白表达程度不一。D横纹肌样胃未分化癌中SMARCB1的缺失。
发病机制
在其他未分化的肿瘤中,经常存在可变的腺体成分或向腺癌过渡的区域,这表明起源于去分化。在通过去分化起源于其他癌症类型的病例中,基因型基本上由起源的克隆决定。在某些情况下,未分化的表型可能是由SWI/SNF染色质重塑复合物的各种成分驱动的;特别是,SMARCB1(INI1)、SMARCA4和ARID1A的缺失已被报道。在某些情况下,SWI/SNF丢失和错配修复缺陷叠加。
大体表现
该癌是一个大的、溃疡的、坏死的、通常跨壁的蕈伞样肿块,通常累及广泛的区域淋巴结。
组织病理学
间变性癌由弥漫的的中等到大的间变性多边形细胞组成,常见多形性肿瘤巨细胞。数量不等的横纹肌样细胞成分很常见,可能是主要模式;这些细胞经常表现出双核或多核。其他可能局部或作为主要模式的组织学模式包括梭形肉瘤样多形性模式、具有破骨细胞样巨细胞的未分化癌和具有淋巴上皮瘤样特征的癌。根据取样的程度,可能会观察到很少或明显的腺体成分。间质可能是黏液样或黏液性的,通常含有单核炎性细胞。免疫组织化学没有特异性,不同程度地表达广谱角蛋白。EMA染色可能有助于确诊角蛋白表达缺乏的例子。波形蛋白持续表达,通常呈核周点状。胃未分化癌应与具有淋巴间质的EBV相关癌、浸润性淋巴瘤(包括间变性大细胞淋巴瘤)、转移性黑色素瘤、生殖细胞肿瘤、PEC瘤和其他类型的具有上皮样大细胞模式的低分化肉瘤区分开来。
细胞学
胃未分化癌含有没有分化迹象的恶性细胞。
诊断分子病理学
见胃腺癌(原书第85页)。ERBB2(HER2)免疫组织化学被推荐用于所有适合治疗的胃癌,但没有具体的建议。
诊断标准
必要标准:没有分化组织学证据的恶性细胞;模棱两可的免疫组织化学。
分期(TNM)
见胃腺癌(原书第85页)。
预后和预测
由于该实体罕见及其高度侵袭性,尚未发现具体的预后特征。诊断时的疾病阶段可能与预后有关。
04. 胃母细胞瘤
定义
胃母细胞瘤是一种发生在胃固有肌层(通常位于胃窦)的双相肿瘤,通常发生在男童和年轻男性身上。
ICD-0编码
8976/1胃母细胞瘤
ICD-11编码
无
相关术语
无
亚型
无
部位
仅报道了12例,均位于胃固有肌层;胃窦部8例,体部2例,胃底1例。最后1例的确切部位没有报道。
临床特征
大多数患者出现腹痛或上腹痛,有些出现疲劳或便血。部分患者体检时可发现肿块。报告的肿瘤大小在3.8至15cm之间(平均值:7cm;中位数:6cm)。
流行病学
报告的胃母细胞瘤患者年龄在9至56岁之间(平均:24岁;中位数:27岁)。男性似乎占主导地位,迄今为止报告的病例有8例男性和4例女性。
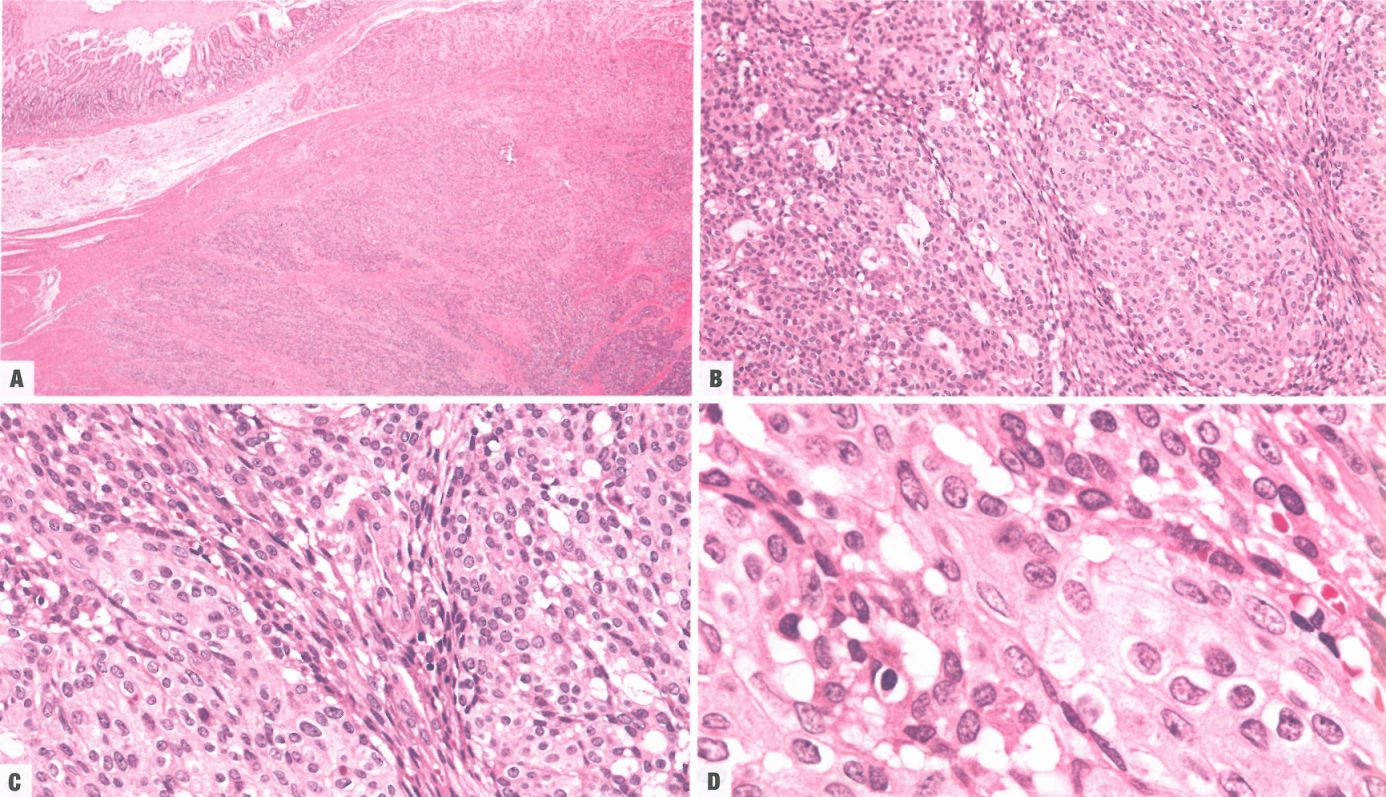
图3.45胃母细胞瘤。A该病变集中在胃固有肌层;注意上覆的胃窦黏膜(胃窦是胃中最易患病的位置);肿瘤在填充固有肌层时形成轻微的丛状小叶。B有上皮巢,梭形细胞索从图像的左上角到右下角呈对角线排列;注意细胞的均匀外观。C这张高倍图像显示了肿瘤的梭形细胞和上皮细胞成分;细胞核小,细胞质苍白。D这张油镜HE图像充分显示了胃母细胞瘤的细胞学特征;注意小核仁,只有在高倍镜下才能看到。
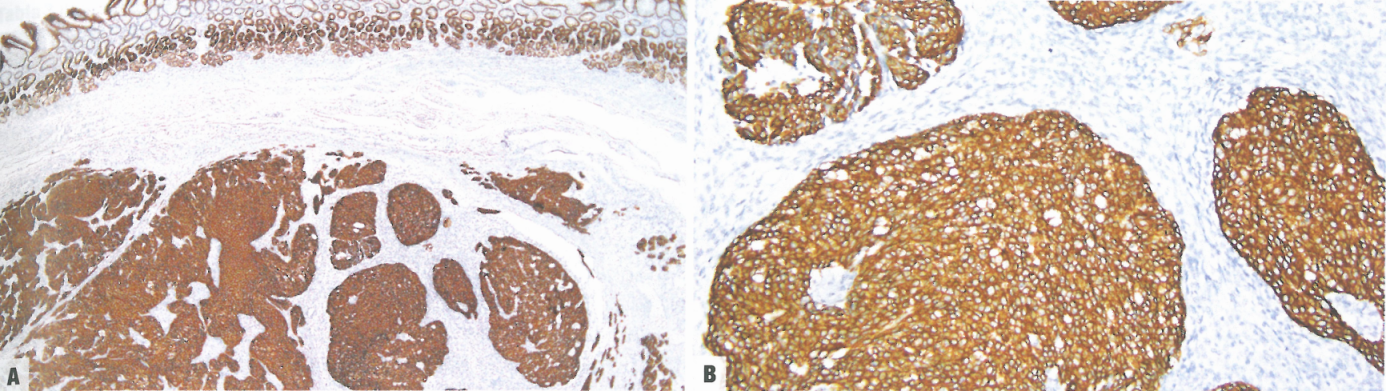
图3.46胃母细胞瘤。A胃母细胞瘤的上皮成分表达细胞角蛋白,但梭形细胞成分不表达(CAM5.2免疫染色)。B细胞角蛋白染色(CAM5.2)标记上皮细胞,但不标记梭形细胞。
病因
未知
发病机制
除了与特征性基因融合(MALAT1-GLI1)有关外,这些肿瘤的发病机制尚不清楚。体细胞MALAT1-GLI1基因融合是丛状纤维黏液瘤的一些例子所共有的,丛状纤维黏液瘤也是胃固有肌层的肿瘤。然而,所有报告的丛状纤维黏液瘤病例都是良性的。因为胃母细胞瘤是双相的,一些例子已经进行了SS18融合的检测,但没有发现融合,从而将这些肿瘤与滑膜肉瘤区分开来。
大体表现
胃母细胞瘤以胃固有肌层为中心,在结节中生长,有些伴有周围硬化。
组织病理学
胃母细胞瘤呈双相组织学,均匀的梭形细胞和均匀的上皮细胞排列成巢状。在肿瘤中,梭形细胞和上皮细胞的比例各不相同。上皮细胞胞质稀少,胞核圆形,核仁不明显。梭形细胞成分单调,细胞细长,通常呈黏液样背景。可能会遇到矿化区域。核分裂在大多数情况下很少见(也有例外),核分裂计数似乎与结果无关。在免疫标记上,上皮成分表达各种全细胞角蛋白,并显示CD56和CD10的局灶性标记,而梭形细胞成分缺乏角蛋白的表达,表达CD56和CD10。重要的是,KIT、DOG1、CD34、SMA、结蛋白、Syn、CgA或S100没有表达。
细胞学
无临床相关性
诊断分子病理学
胃母细胞瘤的诊断需要在肿瘤细胞中证明MALAT1-GLI1融合基因。
诊断标准
必要标准:双相组织学,梭形细胞和上皮细胞巢;MALAT1-GU1融合基因。
分期(TNM)
胃母细胞瘤分期胃腺癌。
预后和预测
大多数患者都接受了肿瘤的手术切除。在11名有可用信息的患者中,7名患者进行了长达14年(168个月)的平稳随访,但报告的中位随访时间仅为12个月。2名患者在就诊时报告有肝转移(其中一名患者也有淋巴结和腹膜扩散),一名患者有淋巴结转移,另一名患者有局部复发。最后一例没有随访。化疗在少数病例中进行了试验,但一直无效。报告的病例数量太低,无法确定预后或预测标记物。
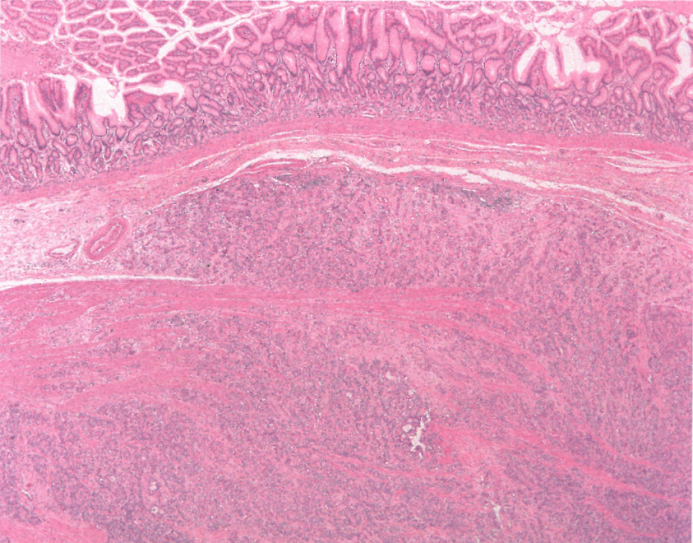
图3.47胃母细胞瘤。这种病变累及胃窦的固有肌层,并形成巢穴,将固有肌层的平滑肌束分开。
05. 胃的神经内分泌肿瘤
定义
胃的神经内分泌肿瘤(NEN)是具有神经内分泌分化的胃上皮肿瘤,包括高分化神经内分泌瘤(NET)、低分化神经内分泌癌(NEC)和混合型神经内分泌-非神经内分泌肿瘤。
ICD-0编码
8240/3神经内分泌肿瘤NOS
8246/3神经内分泌癌NOS
8154/3混合性神经内分泌-非神经内分泌肿瘤(MiNEN)
ICD-11编码
2B72.1&XH55D7胃恶性神经内分泌肿瘤&高分化的神经内分泌癌
2B72.1&XH9LV8胃恶性神经内分泌肿瘤&神经内分泌肿瘤,1级
2B72.1&XH7F73胃恶性神经内分泌肿瘤&中分化神经内分泌癌
2B72.1&XH0U20胃恶性神经内分泌肿瘤&神经内分泌癌NOS
2B72.1&XH9SY0胃恶性神经内分泌肿瘤&小细胞神经内分泌癌
2B72.1&XH0NL5胃恶性神经内分泌肿瘤&大细胞神经内分泌癌
2B72.1&XH6H10胃恶性神经内分泌肿瘤&混合型腺-神经内分泌癌
2B72.1&XH7NM1胃恶性神经内分泌肿瘤&肠嗜铬细胞类癌
2F70.1&XH93H8胃行为不确定的肿瘤&胃泌素瘤NOS
2B72.1&XH0GY2胃恶性神经内分泌肿瘤&胃泌素瘤,恶性
相关术语
可接受:类癌;高分化内分泌肿瘤/癌;低分化内分泌癌;混合性外分泌-内分泌癌;复合类癌-腺癌。
亚型
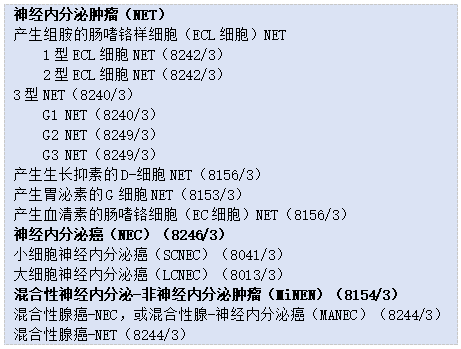
见简表3.04。
部位
NET发生在胃中,根据肿瘤亚型具有部位特异性分布。肠嗜铬样细胞(ECL细胞)NET出现在胃体/胃底,D细胞和G细胞NET出现在胃窦,肠嗜铬细胞(EC细胞)NET同时出现在胃窦和胃体/胃底。NEC和MiNEN可以出现在胃的任何部位,但通常发生在胃窦或贲门区域。
简表3.04胃神经内分泌肿瘤的亚型
临床特征
大多数胃NET不会引起特定症状或局部肿瘤症状,在评估潜在胃部疾病时偶然发现。它们很少与Zollinger-Ellison综合征等分泌综合征有关。
产生组胺的ECL细胞NET:1型ECL细胞NET伴有慢性萎缩性胃炎(通常是自身免疫性,具有针对壁细胞和/或内因子的抗体)和胃酸缺乏引起的高胃泌素血症,以及其他原因引起的高胃泌素血症和(不太常见)大细胞贫血(恶性贫血)。2型ECL细胞NET也伴有高胃泌素血症。该血症多由多发性内分泌腺瘤1型和肥厚性高分泌性胃病中十二指肠或胰腺(罕见)胃泌素瘤引起。3型NET出现在正常的泌酸黏膜中,由于肿瘤生长或转移性扩散,出现不同程度的胃炎和非特异性症状,包括黑便、疼痛和体重减轻。广泛肝转移的患者可能会出现非典型类癌综合征,其特征是皮肤潮红、面部水肿、流泪、头痛和支气管痉挛。罕见的ECL细胞NET与壁细胞泌酸的内在缺陷有关,伴有高胃泌素血症、胃酸缺乏和壁细胞增生。胃分泌组胺的ECL细胞NET的主要临床病理特征总结见表3.06。
表3.06胃神经内分泌肿瘤(NET)1、2和3型的主要临床病理特征
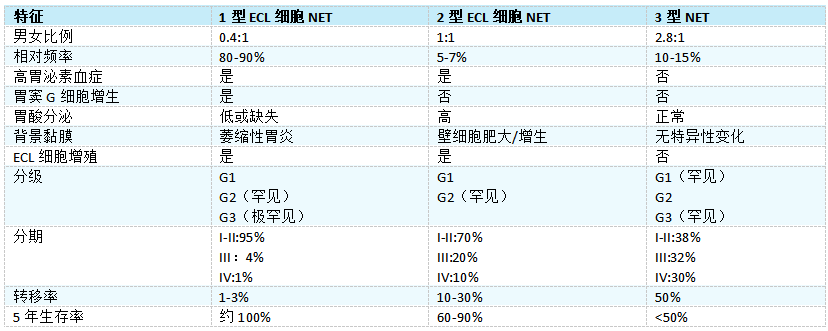
产生血清素的EC细胞NET:这种罕见的肿瘤亚型通常无功能,但可能与腹泻、潮红、三尖瓣返流和哮喘等典型类癌综合征症状有关。
产生胃泌素的G细胞NET:这些肿瘤通常无功能,但少数病例可能导致Zollinger-Ellison综合征;术语“胃的胃泌素瘤”仅用于此类功能性病例,而不用于没有相关临床表现的胃泌素表达肿瘤。
NEC和MiNEN:这些肿瘤表现出非特异性症状,包括消化不良和因肿瘤生长和/或远处转移导致的体重减轻。溃疡性肿瘤可能伴有胃出血、贫血和疼痛;大的幽门病变可能导致梗阻。
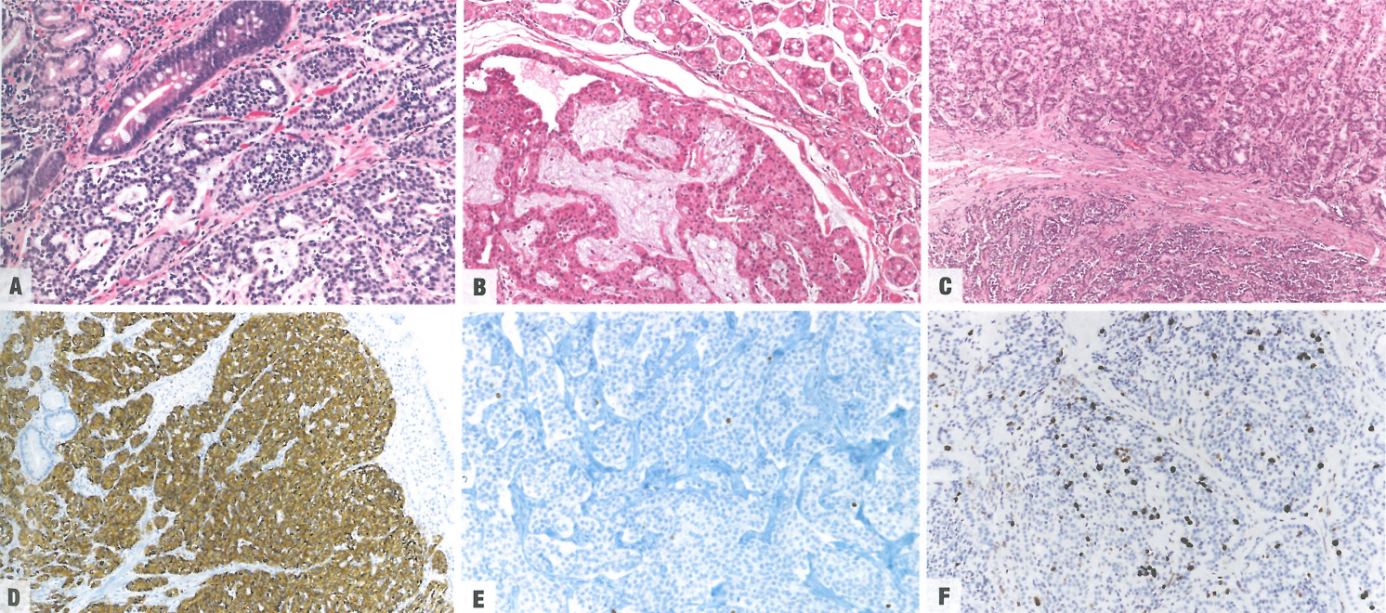
图3.48神经内分泌肿瘤(NET)。A 1型肠嗜铬样细胞(ECL细胞)NET出现在萎缩性胃炎的背景下,表现为假幽门腺化生和肠化生(左上角);肿瘤细胞形成微小叶结构,无坏死,并显示无核仁的单一核。B 在2型ECL细胞NET中,瘤周黏膜不萎缩;特征是高分化的单形态细胞增殖,嗜酸性细胞质形成小梁和缎带,伴细胞外黏液样物质。C 3型NET出现在正常的泌酸黏膜中。D VMAT2免疫染色,1型ECL细胞NET呈弥漫强阳性。E G1 3型NET的Ki-67免疫染色。F G2 3型NET的Ki-67染色。
流行病学
近年来,胃NEN的发病率增加了约15倍,这可能是内镜广泛使用的结果。2012年,美国估计的年龄调整发病率约为每10万人每年0.4例,女性占主导地位,诊断时的平均患者年龄为64岁。欧洲病例也有类似的流行病学特征。尽管胃NET总体上以女性为主,但具体的年龄和性别分布因肿瘤亚型而异。在ECL细胞NET中,类型1是最常见的;它约占所有ECL细胞NET的80-90%,女性更常见。2型约占ECL细胞NET的5-7%,没有性别偏好。3型NET约占所有胃NEN的10-15%,男性更常见。胃窦NET很少见,在一个研究系列中约占胃NEN的5%。胃NEC约占所有胃NEN的21%,男性更常见,占所有消化NEC的20.5%。由腺癌和NEC组成的胃混合癌(MANEC)总体上很少见,约占所有消化道MANEC的20%。
病因
1型ECL细胞NET通常与自身免疫性慢性萎缩性胃炎(针对壁细胞和内因子的自身抗体)有关,但部分病例也与HP感染有关。2型ECL细胞NET发生在胃泌素瘤引起的高胃泌素血症后的1型多发性内分泌腺瘤中。3型NET没有已知的病因。少数ECL细胞NET病例似乎与壁细胞泌酸的内在缺陷有关,这可能是由于质子泵活动异常造成的。除了在一例罕见的原发性胃Merkel细胞癌中存在Merkel细胞多瘤病毒外,尚未发现NEC或MiNEN的具体病因。
发病机制
产生组胺的ECL细胞NET的发病机制:1型和2型ECL细胞NET与不受调节的胃泌素刺激直接相关。潜在的协同因素包括TGF-α和bFGF。MEN1基因异常是2型ECL细胞NET发生所必需的。在17-73%的1型ECL细胞NET和25-50%的3型NET中,也发现了MEN1基因位点标记的杂合性缺失。3型NET的发病机制尚不清楚。关于胃NET基因改变的信息很少。MEN1基因染色体位点标记的杂合性缺失是2型ECL细胞NET的规律。MEN1基因杂合性缺失和/或突变在约30-40%的散发性3型NET中也得到证实。在多发性内分泌腺瘤4型的背景下,已经描述了具有CDKN1B突变和p27(p27Kip1)蛋白水平降低的NET。据报道,一个携带ATP4A基因(编码胃质子泵的A亚基)失活突变的家族已经发生了ECL细胞NET。
NEC和MANEC:NEC和高级别MiNEN(MANEC)的发病机制尚不清楚,可能涉及复杂的遗传学因素。可用数据很少。胃NEC显示多种染色体异常,涉及细胞周期调控基因,如TP53、RB1、FHIT、DCC和SMAD4。一项直接比较研究表明,胃NEC的突变率更高,突变谱与传统胃腺癌不同,557个分析基因中只有40个(7.2%)在两种肿瘤类型中都有突变。在557个分析的基因中,绝大多数(98.2%)仅在NEC中发生突变,包括SMAD4、PIK3CA、KRAS和RB1。TP53和RB1突变有助于区分NEC和G3 NET,其中这些基因更常见的是野生型。胃MANEC的稀疏数据表明,这些肿瘤具有与NEC相似的特征。MANEC两个组分的染色体改变模式和突变谱的相似性表明了单克隆起源。
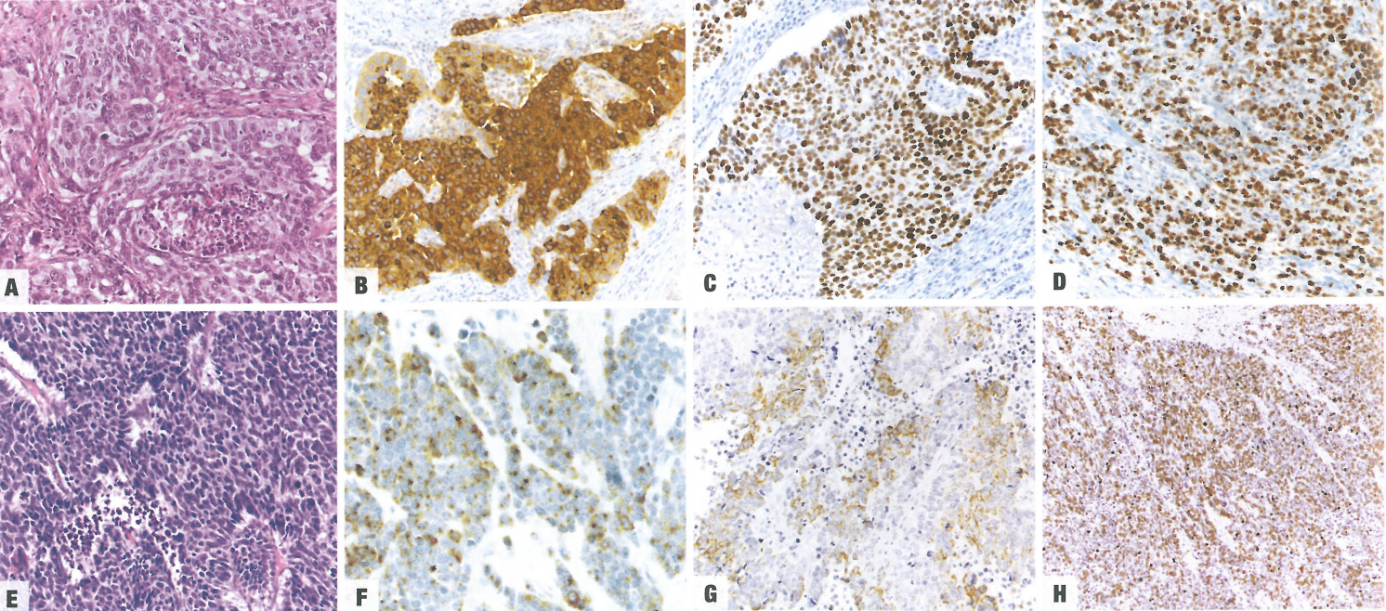
图3.49神经内分泌癌(NEC)。A 大细胞NEC(LCNEC),由具有分散染色质和显著核仁的大细胞组成,排列成片伴坏死。B LCNEC。CgA染色显示胞质呈弥漫性强阳性。C LCNEC。p53阳性。D LCNEC,高Ki-67增殖指数。E 小细胞NEC(SCNEC),实性小细胞成片,核深染,无核仁。F SCNEC,CgA染色,呈典型的核周点状阳性。G SCNEC,CK染色证实其上皮性质,可能局灶阳性。H SCNEC,高Ki-67增殖指数。
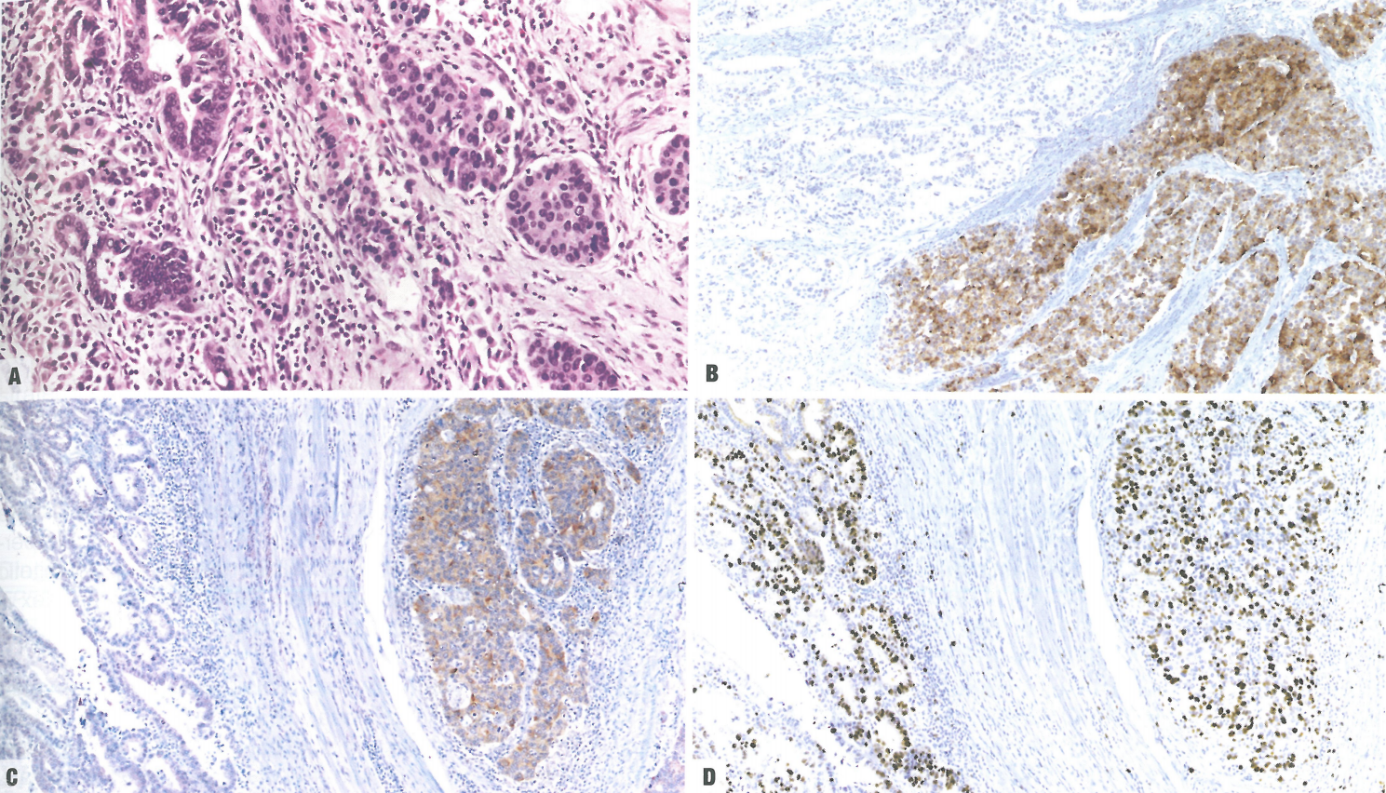
图3.50胃混合性腺-神经内分泌癌(MANEC)。A 贲门MANEC,由腺癌(左侧)和大细胞神经内分泌癌(LCNEC;右侧)组成。B CgA染色显示神经内分泌成分,胞质呈弥漫强阳性,腺癌阴性。C 神经内分泌成分Syn也呈阳性。D 神经内分泌成分呈高Ki-67增殖指数,是MANEC最重要的预后标记物。
大体表现
约60%的病例中,1型ECL细胞NET是多发性,表现为胃体/胃底黏膜的小息肉(<1cm)或结节。2型ECL细胞NET出现在泌酸黏膜中,表现为多发性病变,通常<2cm;严重的肥厚性高分泌性胃病可能导致胃黏膜增厚。3型NET通常是单灶大(约2cm)病变。产生胃泌素的G细胞NET通常是位于胃窦区域的小的黏膜/黏膜下增殖物,最常见于幽门附近。胃NEC可能形成大的蕈样肿块,深入胃壁。MANEC肉眼观类似传统型胃腺癌,通常表现为息肉样或溃疡性狭窄大肿块,平均大小约为5cm。
组织病理学
产生组胺的ECL细胞NET
ECL细胞NET通常显示微小叶和/或小梁结构,没有坏死。它们由高分化细胞组成,具有丰富的嗜酸性细胞质,核呈均质的圆形,缺乏明显核仁。核分裂象很少。在极少数情况下,NET显示出更实性的结构,小梁增大而紊乱,偶尔出现点状坏死;这些肿瘤由较大的细胞组成,具有丰富的细胞质和中重度核异型性,其特征是多态性(polymorphic)、拥挤的核和不规则分布的染色质。核分裂象很多,有时是非典型核分裂象。
1型ECL细胞NET>0.5cm,通常浸润到黏膜肌层之外;罕见病例>1cm并侵犯固有肌层,这种病例可能转移。大多数病例为G1或G2,胃壁浸润和转移扩散程度相似,临床结局也相似。已经描述了非常罕见的1型ECL细胞NET G3病例,占研究系列中所有1型ECL细胞NET的1.6%。背景黏膜萎缩,伴有肠化生和假幽门化生,以及复杂的ECL细胞增生和异型增生变化。在相应的胃窦黏膜中,通常观察到产生胃泌素的G细胞增生,这是高胃泌素血症的形态学对应物。绝大多数1型ECL细胞NET都是低分期。
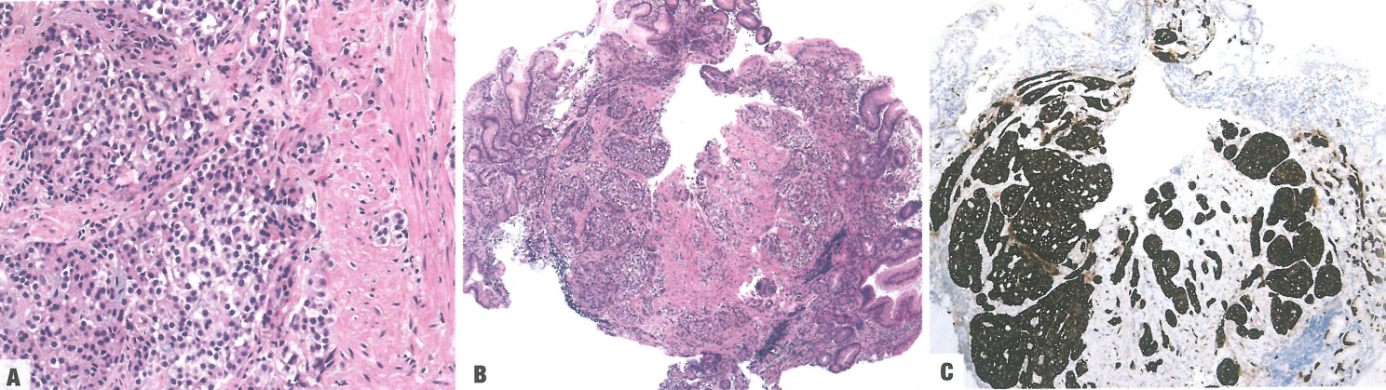
图3.51胃神经内分泌肿瘤(NET)。胃的1型NET病例(A),伴自身免疫性胃炎;低倍镜下,两者的特征清楚(B)。相应的Syn染色(C)也显示自身免疫性胃炎部分的肠嗜铬样细胞(ECL细胞)增生。
2型ECL细胞NET的G1病例主要局限于黏膜/黏膜下层,但分别有30%和10%的患者存在淋巴结和远处转移。背景黏膜增生,并显示多种类型的ECL细胞增生和异型增生。
3型NET的范围从G1到G3,经常深入胃壁并发生淋巴结和远处转移。3型NET通常处于高分期。
与壁细胞泌酸的内在缺陷相关的ECL细胞NET是多发性病变,其特征与1型和2型ECL细胞NET相似。它们的发病也与高胃泌素血症有关;未受累的黏膜显示出独特的泌酸腺肥大和增生变化,伴ECL细胞增生/异型增生。嗜酸腺经常扩张,充满浓缩的物质,衬覆细胞质肿胀的壁细胞(要么深嗜酸性,要么空泡化,胞质顶端突入腺腔内)。与1型ECL细胞NET相似,相应的胃窦黏膜显示产生胃泌素的G细胞增生。已有区域淋巴结转移的报道。
产生血清素的EC细胞NET
胃EC细胞NET的形态特征与回肠EC细胞NET相似,包括具有外周栅栏状排列的圆形细胞巢。肿瘤细胞均匀,具有强嗜酸性细胞质。
产生胃泌素的G细胞NET与胃泌素瘤
产生胃泌素的G细胞NET通常显示细长的小梁状和旋涡状,但部分病例具有更多实性巢。肿瘤细胞均匀,细胞质稀少。
产生生长抑素的D细胞NET
由生长抑素阳性的高分化单形态细胞组成。
NEC
胃NEC由大的、异型增生的小梁或低分化细胞成片组成。它们分为小细胞NEC(SCNEC)和大细胞NEC(LCNEC),与它们更常见的肺部对应肿瘤相似。LCNEC由具有泡状核的大细胞组成,显示显著的核仁和丰富的嗜酸性细胞质。SCNEC由细胞质稀少、核深染且无核仁的肿瘤细胞组成。NEC的核分裂率通常>20个核分裂/mm2,Ki-67增殖指数通常>60-70%,尤其是SCNEC。
MiNEN
MANEC由NEC与并发的腺癌组成。存在广泛坏死的实性或器官样结构,以及非常高的核分裂率,可能提示MANEC的诊断,可用神经内分泌标记物阳性来证实诊断。MANEC的神经内分泌成分通常Ki-67增殖指数>55%。混合性腺癌-NET(原发和转移性肿瘤都是)由管状、乳头状或黏液腺癌区域和G1或G2 NET区域组成。已经描述了与自身免疫性慢性萎缩性胃炎相关的胃混合性腺癌-NET病例。
混合性腺瘤NET
胃混合性腺瘤-NET罕见,由G1或G2 NET伴管状或管状绒毛状腺瘤组成。神经内分泌成分通常位于息肉的深部中央部分,而腺瘤成分占据大部分外周。目前,这些不同寻常的肿瘤不归入MiNEN。
免疫组织化学
胃NET表达通用的神经内分泌标记物Syn和CgA。此外,所有ECL细胞NET表达VMAT2、HDC和SSTR2A。还可能表达血清素、胃饥饿素、生长抑素和α-hCG阳性的散在细胞。ECL细胞表型不能在所有3型NET中得到证实;除了由ECL细胞组成的病例外,这一类别还包括由缺乏特定表型的非典型细胞组成的病例。一些特征,包括SSTR2A和HDC的表达,可能会在罕见的G3 NET中丢失。胃EC细胞NET对血清素、SSTR2A和CDX2呈阳性。产生胃泌素的G细胞NET对胃泌素和SSTR2A呈阳性。产生生长抑素的D细胞NET对生长抑素、CgA、Syn和SSTR2A呈阳性。胃NEC对Syn呈阳性,而CgA可能不存在或仅局部表达(具有典型的核周点状模式)。NEC,特别是SCNEC,也可能对TTF1和ASH1L(ASH1)呈阳性。
分级
胃NEN使用与其他胃肠胰NEN相同的系统进行分级。
细胞学
胃NET体积小,通常多灶,FNA很少用;然而,它可用于诊断黏膜下结节,正如一项针对Zollinger-Ellison综合征患者的研究,其中12例中有11例成功诊断NET。与其他解剖部位一样,表现为均匀的细胞群,核圆形,染色质呈点彩状。胃NEC的细胞学检查与其他高级NEC相同。
诊断分子病理学
TP53和RB1突变可以帮助区分NEC和G3 NET,后者野生型基因更常见。
诊断标准
NET
必要标准:形态均匀细胞群,伴圆形核和细腻点彩状染色质;小梁、腺泡、巢和带状等结构模式;表达Syn和CgA。
NEC
必要:小细胞癌或大细胞癌模式;低分化细胞成片或小梁状排列;高核分裂率和高Ki-67增殖指数。
分期(TNM)
胃NET使用第1章(原书第20页)中介绍的NET-特异性国际癌症控制联盟(UICC)TNM分期系统进行分期。NEC和MiNEN按照腺癌分期。
预后和预测
胃NEN的预后在很大程度上取决于肿瘤亚型、分级和分期;较高级别和分期与发病率增加有关。1型ECL细胞NET的预后极佳,3型NET的预测明显较差。2型ECL细胞NET具有中等预后特征,主要取决于并发的多发性内分泌腺瘤1型相关肿瘤。在1型ECL细胞NET中,分期参数(如大小和胃壁侵犯)似乎比分级更具预测意义。在3型NET中,级别和阶段都与预后相关。胃窦NET通常是惰性的,预后良好。胃NEC和MANEC预后差,生存时间通常以月为单位。在MANEC中,NEC成分及其Ki-67增殖指数决定了结局,就像NEC一样。


























共0条评论