[导读] 编译整理:强子
骨原发肿瘤诊断策略概述(一)
骨原发肿瘤诊断策略概述(二)
骨原发肿瘤诊断策略概述(三)
骨原发肿瘤诊断策略概述(四)
骨原发肿瘤诊断策略概述(六)
骨原发肿瘤诊断策略概述(七)
四. 成骨性肿瘤
1. 骨样骨瘤及骨母细胞瘤
骨样骨瘤及骨母细胞瘤为良性成骨性肿瘤,二者发生部位分别为骨皮质、髓质。二者好发于长管状骨的干骺端、骨干处以及椎骨、手足处的小骨。骨样骨瘤的疼痛可通过非甾体类抗炎药而缓解,但骨母细胞瘤的疼痛则无此特点。还有人提出骨母细胞瘤>20mm,而骨样骨瘤<20mm,当然这一说法有些过于武断。
影像学及组织学上,骨样骨瘤和骨母细胞瘤均境界清楚,骨样骨瘤周边一般会伴显著硬化表现。二者组织学上均为病灶中央更加显著(central nidus)的表现,且二者病灶中央均为不规则、相互沟通的骨小梁,周边为显著骨母细胞,其间穿插富于血管的间质。也可有显著破骨细胞。骨母细胞瘤出现显著细胞学异型性时,最好归为侵袭性骨母细胞瘤,但其临床预后和无非典型细胞者并无差别,因此也可称之为怪异型(bizarre)骨母细胞瘤。也可出现继发性动脉瘤样骨囊肿。
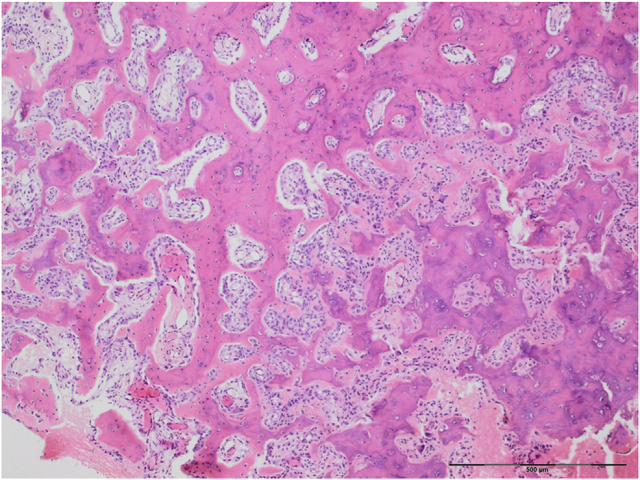
图8. 骨样骨瘤。本图示病灶中央更加显著的表现。可见骨小梁及显著破骨细胞,周围可见胖梭形骨母细胞。骨小梁之间有显著脉管成分。病变周边处为更加成熟的骨组织。这一构型特点也见于骨母细胞瘤。结合影像学特点,这一类病变不太容易误诊为骨肉瘤。
2. 骨肉瘤
A. 概述
骨原发非造血系统肿瘤最常见的即骨肉瘤,其特点即有成骨性恶性细胞。该肿瘤很少发生于4岁之前,10-14岁患者最为多见,但30%发生于40岁以上。骨外骨肉瘤则是根据解剖部位而分的,如发生于和骨组织不相连的软组织时,此时的鉴别诊断需考虑到恶性外周神经鞘膜瘤、伴异源性骨形成的去分化脂肪肉瘤。
骨的高级别骨肉瘤治疗上会进行新辅助化疗,疗效反应对于总生存和无病生存来说都是一个重要的预后只指标。化疗效果好,是指治疗后组织学评估中90%以上的肿瘤坏死。

图9. 术前化疗效果评估,需对标本的一个完整横切面进行组织学评估。

图10. 一例高级别骨母细胞型骨肉瘤,化疗后股骨远端切除标本。肿瘤位于干骺端及骨干处,并累及关节下方。骨皮质受累、骨膜隆起(Codman’s三角),也可见软组织显著受累。
根据肿瘤级别、形态学、解剖部位,骨肉瘤有很多分类,具体如低级别骨肉瘤、高级别骨肉瘤和中央型骨肉瘤、表面骨肉瘤。中央型骨肉瘤最为常见,且大部分为高级别;根据形态学又可分为骨母细胞型(70-80%)、软骨母细胞型(10-15%)、纤维母细胞型/多形性(10%)、血管扩张型(<4%)及其他罕见亚型(如富于巨细胞型、小细胞型、骨母细胞样)。高级别表面型骨肉瘤极为罕见,治疗上与高级别中央型骨肉瘤一致。低级别骨肉瘤也很少见,仅占骨骼骨肉瘤的4%:发生于髓腔者占1%(即低级别中央型骨肉瘤)、发生于骨表面者占3%(即骨旁骨肉瘤)。10-15%的骨旁骨肉瘤可转化为高级别病变,即所谓去分化骨旁骨肉瘤。另一种极为罕见的表面骨肉瘤即骨膜骨肉瘤(periosteal osteosarcoma),详见后述。
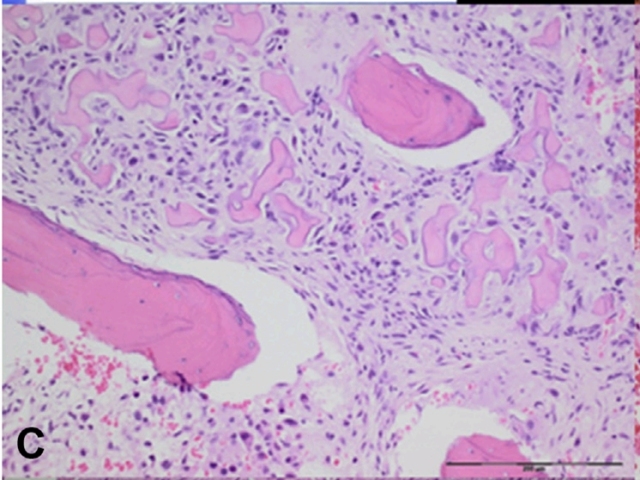
图11. 高级别骨母细胞型骨肉瘤,瘤细胞呈高级别形态,细胞核显著多形性,可见非典型核分裂,并有广泛骨样组织沉积。
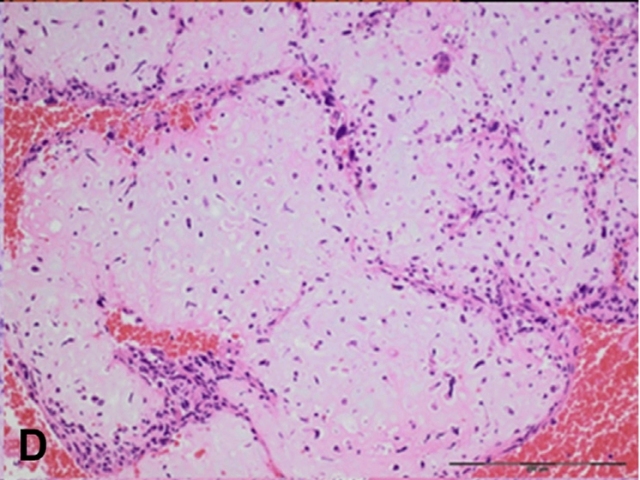
图12. 高级别软骨母细胞型骨肉瘤,镜下为伴软骨母细胞特征的恶性细胞,多形性瘤细胞散在于黏液-透明样软骨基质背景中。细胞核非典型程度、加之基质的透明样表现,因此可诊断为软骨母细胞型骨肉瘤。骨样组织沉积的数量不一,本例中仅为散在。
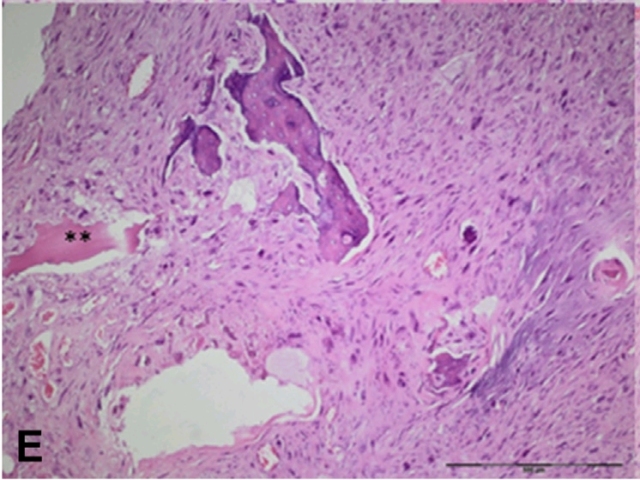
图13. 高级别纤维母细胞型骨肉瘤。镜下为多形性肿瘤细胞,且有骨样组织生成,间质为致密胶原性。可见宿主骨残余。
高度非典型细胞、伴骨样组织沉积,是高级别骨肉瘤的特征,但骨样组织的数量不一。骨母细胞型骨肉瘤中,骨样组织数量一般非常丰富,但血管扩张型骨肉瘤中则数量极少。高级别骨肉瘤的形态学亚型,并无治疗意义,也无疗效预测意义。
需要注意的是,前述怪异型骨母细胞瘤中瘤细胞核浆比低、但体积大,可误判为骨肉瘤。动脉瘤样骨囊肿也可误判为血管扩张型骨肉瘤,反之亦然。
从治疗角度来说,骨原发的高级别纤维肉瘤、或无骨样组织的多形性肉瘤化疗方案与经典型骨肉瘤相同。不过,做出类似诊断前必须排除软组织治疗侵犯骨组织、去分化软骨肉瘤、转移性病变(如肉瘤样肾细胞癌)。如活检中未见骨样基质,则影像学有助于确定病变中的骨形成,可协助诊断骨肉瘤。
软骨母细胞型骨肉瘤很难与经典型软骨肉瘤鉴别。仔细研判软骨细胞非典型的程度、细胞外基质的数量,对于鉴别有一定帮助。一般说来,软骨母细胞型骨肉瘤中细胞核的非典型程度与黏液样基质的数量并不一致,具体如细胞核显著非典型、同时具有大量透明软骨样基质。同时也要结合影像学表现及发病部位进行鉴别。
类似情况下的诊断和鉴别诊断,免疫组化一般无太大帮助:骨肉瘤可以表达CK、S100及其他某些标记物,SATB2对于骨肉瘤也并不特异。
小细胞骨肉瘤极为罕见,此时需注意鉴别Ewing肉瘤、淋巴瘤、癌、间叶性软骨肉瘤、组织细胞肿瘤等。
大部分骨肉瘤为骨原发病变,但也有一小部分、尤其年龄>40岁者可继发于放疗、骨的Paget病、骨纤维结构不良、骨的巨细胞肿瘤、骨的梗死等。
约20%的骨肉瘤患者会有种系性基因突变,最常见为TP53突变而导致Li-Fraumeni综合征、Rb突变导致双侧视网膜母细胞瘤综合征、RECQL4突变导致Rothmund-Thomson综合征。
B. 低级别中央型骨肉瘤
低级别中央型骨肉瘤大部分见于20-30岁,好发于长管状骨,尤其多见于股骨远端、胫骨近端。如完整切除、且不伴高级别成分,则预后较好,出现转移的几率为15%。因此这类病变切除后必须广泛取材。
组织学上表现为中等程度非典型的梭形细胞呈束状排列,可有纤维结构不良型表现;不过,纤维结构不良病例中95%以上可查出GNAS突变,无此突变者则可排除纤维结构不良。需要注意的是,检出GNAS突变并不完全意味着该病例就是纤维结构不良,因为有1%的纤维结构不良会转化为骨肉瘤。因此低级别中央型骨肉瘤中可以检出GNAS突变;不过约40%的低级别中央型骨肉瘤具有MDM2的扩增,并且这一点与GNAS突变是并不共存的。影像学除有助于诊断外,还可用于指导活检部位。
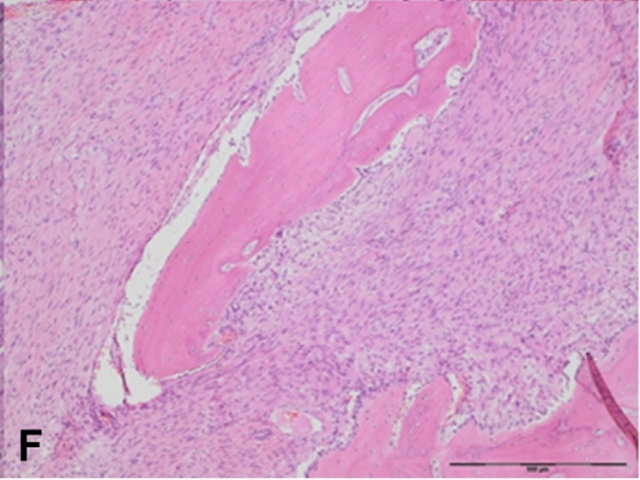
图14. 低级别中央型骨肉瘤。镜下为轻度非典型的梭形细胞呈束状排列,肿瘤内可见宿主骨的不规则骨小梁残余。
C. 表面骨肉瘤
如前所述,表面骨肉瘤又可分为骨旁(parosteal)骨肉瘤、骨膜(periosteal)骨肉瘤,其中骨旁骨肉瘤最为常见,主要发生于30岁左右成人。如完整切除,预后尚好,但如切除不完整,且复发率极高且有转移风险,甚至在多年后转化为高级别病变(有时称之为去分化)。曾有报道称骨旁骨肉瘤复发病例中40%伴有去分化。
该肿瘤80%发生于股骨远端后表面,直接发生于骨膜外表面。约半数骨旁骨肉瘤会有软骨分化,甚至可以广泛软骨分化,具体表现形式可以是散布于肿瘤内,也可表现为软骨帽,并可能因此而误诊为骨软骨瘤。不过,与骨软骨瘤不同的是,骨旁骨肉瘤贴附于皮质骨,与下方髓质骨并无延续。
骨旁骨肉瘤组织学上表现为条索样,细胞形态为具有轻至中等程度非典型的梭形表现,混杂有板层状骨小梁。细胞密度增加、细胞核具有多形性、且具有核分裂,是向高级别转化的特征。不过,低级别与高级别的鉴别也是具有主观性的,有时并不那么容易。目前尚无客观指标来确定骨旁骨肉瘤是否向高级别转化。高级别病变病程更具侵袭性,预后较差。
遗传学上,骨旁骨肉瘤不管是低级别还是高级别,约85%的病例会有MDM2和CDK4的扩增。
骨膜骨肉瘤则是骨肉瘤中较罕见的亚型。临床最多见于20-30岁。形态学上具有显著软骨母细胞形态,骨样组织一般仅为局灶。目前报道中尚未见特异性遗传学改变。
骨膜骨肉瘤相比经典型骨肉瘤来说,预后相对较好,约80%的患者会长期存活,因此有人将其归为中等级别(intermediate)肿瘤。临床治疗方面则主要是新辅助化疗、后进行手术切除。
未完待续
点击下载英文文献
参考文献
Flanagan AM.A diagnostic approach to bone tumours[J].Pathology,2017,49(7):675-687.
DOI:10.1016/j.pathol.2017.08.003




















共0条评论