WHO女生5ed第6章子宫体肿瘤(四)
往期回顾:
5. 子宫平滑肌肉瘤
定义
子宫平滑肌肉瘤是一种子宫肌层平滑肌起源的恶性间叶性瘤,表现为梭形细胞、上皮样或黏液样形态。
ICD-0编码
8890/3 平滑肌肉瘤NOS
ICD-11编码
2B58.1 子宫的平滑肌肉瘤
相关命名
无
亚型
梭形细胞平滑肌肉瘤;上皮样平滑肌肉瘤;黏液样平滑肌肉瘤
部位
大多数子宫平滑肌肉瘤发生在子宫体;大约5%来自宫颈。它们可能位于子宫肌壁内(约占2/3)、黏膜下或浆膜下。
临床特征
患者出现阴道出血、盆腔肿块或盆腔/腹部疼痛。可能发生胃肠道或泌尿道症状,是肿瘤在该区域扩散所致。也可能出现与肿瘤破裂(腹膜出血)或肺转移(呼吸困难)有关的症状。罕见患者出现血液学表现或副肿瘤综合征。
流行病学
平滑肌肉瘤是最常见的子宫肉瘤(约占40-50%),但仅占所有子宫恶性肿瘤的1-2%。患者年龄通常超过50岁。
病因
偶尔与他莫昔酚治疗和盆腔照射有关。
发病机制
子宫平滑肌肉瘤中发现了多种分子异常,包括复杂的染色体数量和结构的异常,但没有一种有诊断价值。最常见的突变基因包括TP53(约30%)、ATRX(约25%)和MED12(约20%)。
大体检查
子宫平滑肌肉瘤通常表现为单个、质软、切面凸起的鱼肉样肿块,平均直径10cm。大约25%的肿瘤小于5cm。切面通常坏死和出血。黏液样肿瘤可能呈胶状且易碎。
组织病理学
认可三种主要亚型。梭形细胞(传统型)平滑肌肉瘤通常是细胞丰富(罕见少细胞),由含有嗜酸性胞质(有时胞质很少)的梭形细胞组成,排列成长的、交织的、通常致密但相对紊乱的束状。核多形性通常很显著,但一部分肿瘤表现出均匀一致的细胞学特征,在低倍镜下貌似温良。梭形细胞和多形性细胞的比例各不相同。可能存在多核肿瘤细胞和破骨细胞样巨细胞。核分裂象计数通常很高(≥4个/mm²,相当于直径为0.55mm、面积为0.24mm²的视野≥10个/10HPF),并有非典型核分裂象。大约1/3病例存在肿瘤细胞性坏死,其特征是从存活肿瘤细胞突然转变为非存活肿瘤细胞。区分肿瘤细胞和梗死型坏死可能很困难,尤其是在早期。为了确诊梭形细胞平滑肌肉瘤,需要存在以下三项特征之二:肿瘤细胞性坏死、显著的细胞学异型性和核分裂象≥4个/mm²(相当于直径为0.55mm、面积为0.24mm²的视野≥10个/10个HPF)。罕见病例中,梭形细胞平滑肌肉瘤可能发生于平滑肌瘤的背景中。
上皮样平滑肌肉瘤相对少见,该肿瘤主要表现为上皮样外观(>50%),由圆形或多角形细胞组成,胞质呈嗜酸性或透明,呈巢状、条索状、结节状或弥漫性模式。可能局灶出现横纹肌样细胞或印戒样细胞。也可能发现假腺样腔隙。肿瘤偶尔可能会广泛透明变性。诊断标准包括中度至重度细胞学异型性和/或肿瘤细胞性坏死或核分裂象≥1.6个/mm²(相当于直径为0.55mm、面积为0.24mm²的视野≥4个/10HPF)。
黏液样平滑肌肉通常细胞量稀少,因为含有丰富的黏液样间质。它们可能显示模糊的束状或结节状生长。可能需要大量取材来确定诊断恶性肿瘤的区域。出现任何程度的细胞学异型性、肿瘤细胞性坏死或核分裂象>0.4个/mm²(相当于直径0.55mm、面积0.24mm²的视野>1个/10HPF)都应诊断为黏液样平滑肌肉瘤。
细胞类型的混合并不罕见。肿瘤通常有浸润性边缘,多达20%的肿瘤存在血管腔侵犯。约1/3病例存在肿瘤细胞性坏死,其特征是存活肿瘤细胞突然转变为非存活肿瘤细胞
肿瘤细胞表达desmin、h-caldesmon(特异性较强)和SMA,但如果肿瘤分化差或呈黏液样,则可能呈弱表达和/或斑片状。常见CD10、EMA和CK的阳性表达,其中EMA和CK阳性在上皮样肿瘤中尤其常见。梭形细胞肉瘤通常表达ER和PR。p16和/或p53的过表达也常见。
细胞学
无临床相关性
诊断性分子病理学
无临床相关性
诊断标准
见简表6.02。
分期
使用FIGO和TNM系统对子宫平滑肌肉瘤进行分期。
预后和预测
这些肿瘤预后不良有关差,即使初始诊断时局限于子宫也是如此。肿瘤<5cm且局限于子宫时,预后较好。合并所有分期,5年总生存率从15%至25%。I-II期肿瘤的女性预后较好,5年生存率为40-70%。对化疗的反应有限。
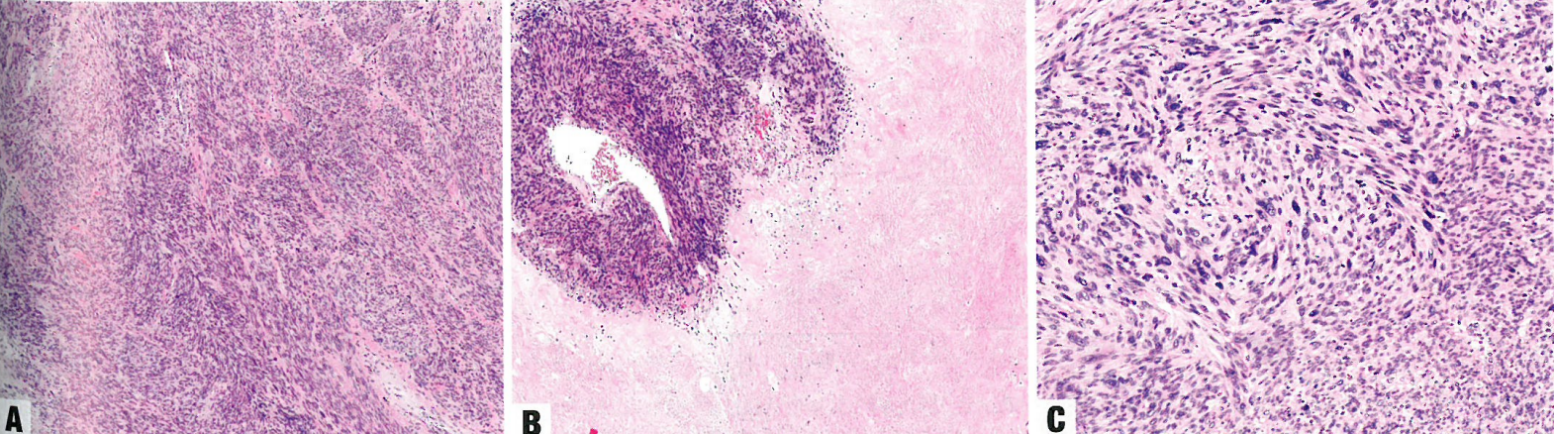 图6.46子宫平滑肌肉瘤,梭形。A 低倍,肿瘤富于细胞,束状生长,核增大深染。B 凝固性肿瘤细胞坏死,存活肿瘤(围绕供血血管)和非存活肿瘤(有明显的肿瘤残影)之间存在明显分界。C 肿瘤细胞呈显著多形性。
图6.46子宫平滑肌肉瘤,梭形。A 低倍,肿瘤富于细胞,束状生长,核增大深染。B 凝固性肿瘤细胞坏死,存活肿瘤(围绕供血血管)和非存活肿瘤(有明显的肿瘤残影)之间存在明显分界。C 肿瘤细胞呈显著多形性。
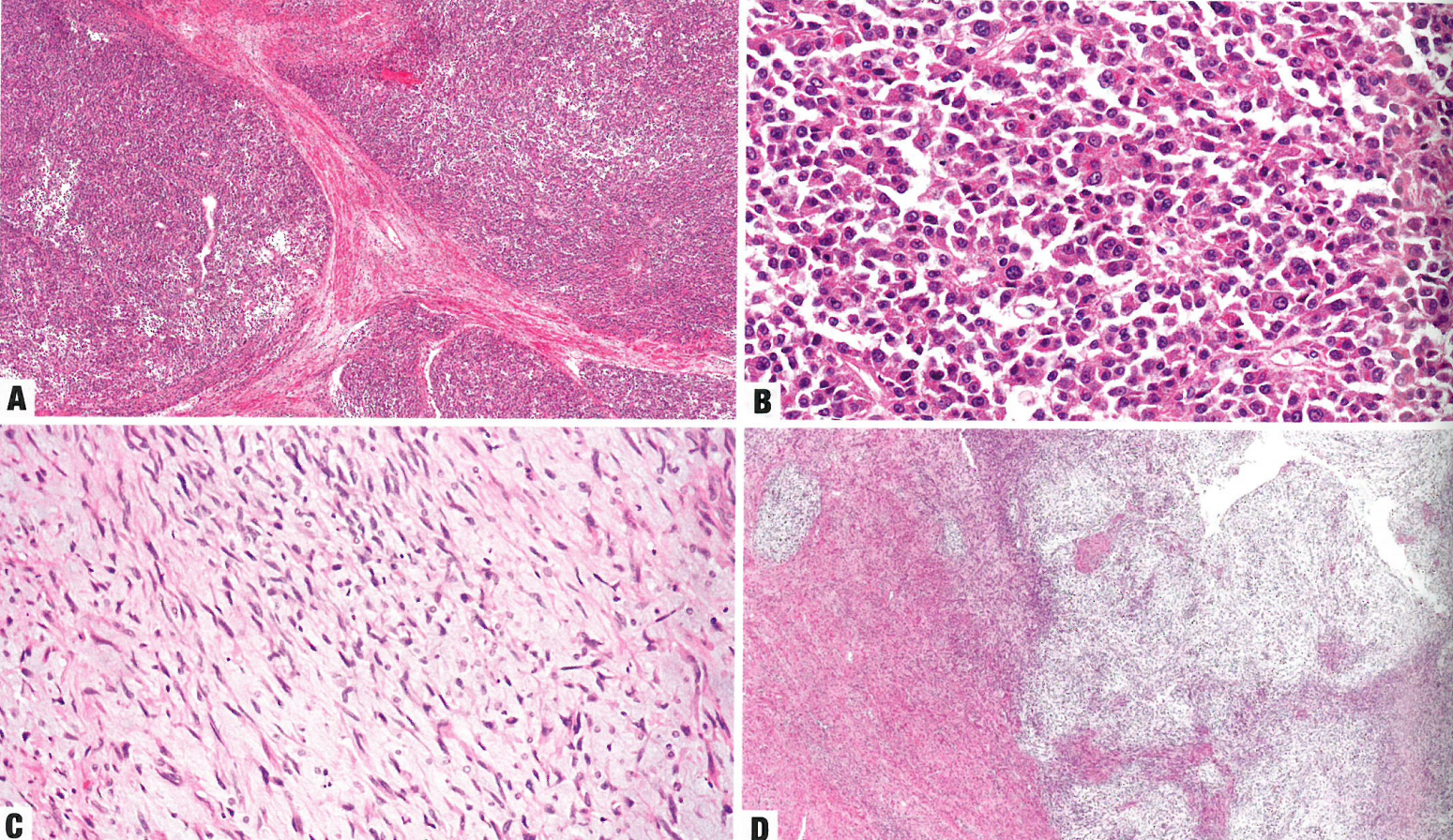
图6.47子宫平滑肌肉瘤。A 上皮样平滑肌肉瘤。肿瘤与子宫肌层的界面不规则,由圆形到多角形的细胞组成,含有颗粒状嗜酸性胞质。注意明显的核异型性和易见核分裂象。desmin和h-caldesmon阳性。B 上皮样平滑肌肉瘤。圆形至卵圆形肿瘤细胞,含有嗜酸性颗粒状胞质,核形不规则。C 黏液样平滑肌肉瘤。肿瘤呈下发性,缺乏明显的细胞学异型性。它与丰富的黏液样物质有关。D黏液平滑肌肉瘤。肿瘤特征是与周围子宫肌层的不规则浸润性界面和明显的黏液样背景。

6. 子宫内膜间质结节
定义
子宫内膜间质结节是一种边界清楚的子宫内膜间质瘤,类似于增殖期子宫内膜间质,缺乏淋巴管血管浸润。
ICD-0编码
9030/0 子宫内膜间质结节
ICD-11编码
2E88&XH8C13 良性子宫内膜间质结节&子宫内膜间质结节
相关命名
可接受:良性子宫内膜间质瘤
亚型
无
部位
肿瘤位于子宫内;可能位于黏膜下、子宫肌壁内或(很少)浆膜下。
临床特征
患者可能出现异常子宫出血、腹痛、子宫增大或盆腔肿块。
流行病学
子宫内膜间质结节是一种罕见的肿瘤。较常见于围绝经期女性(平均患者年龄:53岁;范围:23-86岁)。
病因
未知
发病机制
大约70%的具有经典组织学的肿瘤,以及一些平滑肌分化或性索分化的肿瘤,携带(7;17)(p21;q15)导致JAZF1-SUZ12融合
大体检查
肿瘤边界清楚,呈实性,黄色至褐色,平均大小7cm(范围:1-22cm)。可能息肉样,也可能囊性变。
组织病理学
肿瘤边界清楚,或最多可以有≤3个指状突起,距离边缘<3mm。典型者细胞量非常密集,呈均匀一致的小细胞,胞质稀少(蜕膜化除外),核圆形至椭圆形,核仁不明显,可能围绕小动脉呈旋涡状(可能透明变性)。肿瘤周围可能见到散在的大血管。核分裂象活性通常低,但如果增加也不排除该诊断。可能存在胶原束、泡沫状组织细胞和较少见的胆固醇裂隙。变异的形态学包括平滑肌分化、纤维黏液样改变(显得少细胞)、性索样分化(包括网状结构)、子宫内膜样腺体和横纹肌样或上皮样形态。免疫表达谱等同于低级别子宫内膜间质肉瘤。
细胞学
无临床相关性
诊断性分子病理学
无临床相关性
诊断标准
必要标准:界边界清楚的结节;肿瘤细胞就像增殖期子宫内膜间质;无淋巴管血管浸润
分期
无临床相关性
预后和预测
只要对肿瘤与子宫肌层的交界处进行充分取材以排除肉瘤,患者的预后就很好。
7. 低级别子宫内膜间质肉瘤
定义
低级别子宫内膜间质肉瘤是一种恶性间质瘤,其细胞类似于增殖期子宫内膜间体,显示浸润性(渗透性)生长,伴有或不伴有淋巴管血管浸润。
ICD-O编码
8931/3 子宫内膜间质肉瘤,低级别
ICD-11编码
2B5C0 子宫的子宫内膜间质肉瘤&子宫内膜间质肉瘤,低级别
相关命名
无
亚型
无
部位
这些肿瘤更常见于子宫体,远远多于子宫颈。
临床特征
患者出现异常子宫出血、盆腔疼痛、子宫肿块,和/或肺转移,或附件和淋巴结转移。
流行病学
肿瘤发生的年龄范围很广(平均患者年龄:52岁,范围:16-83岁)。风险因素包括长期摄入雌激素或他莫昔酚和盆腔照射。
病因
未知
发病机制
2/3的低级别子宫内膜间质肉瘤存在涉及多梳家族基因的遗传性融合,其中JAZF1-SUZ12最常见,其次是JAZF1-PHF1、EPC1-PHF1和MEAF6-PHF1。MBTD1-EZHIP(CXorf67)、BRD8-PHF1、EPC2-PHF1和EPCi-SUZ12也有报道,但经验有限(各报告病例<3例),BRD8-PHF1也与高级别肿瘤有关。
大体检查
肿瘤通常形成宫腔内或子宫肌壁内、边界不清的、融合的黄色至褐色结节(大多数5-10cm),常有明显的肌层浸润和/或血管内瘤栓有关,后者有时在子宫旁静脉内更加明显。
组织病理学
肿瘤细胞形成不规则、密集的细胞岛,弥漫性生长,渗透子宫肌层(舌状浸润),可能伴有淋巴管血管浸润(有显著)。核均匀一致,椭圆形至梭形,异型性轻微或没有,胞质稀少,有精致的小动脉网。有时肿瘤细胞在血管周围呈旋涡状排列。核分裂象活性通常低,但也可能核分裂象活跃。可能见到透明斑块、泡沫状组织细胞、囊性变和坏死。常见的变异型特征包括平滑肌分化、纤维黏液样/纤维样改变和性索样分化。奇异形核、上皮样/横纹肌样改变、子宫内膜样腺体和假乳头少见。其他报道的形态学变异(如骨骼肌/脂肪细胞分化和透明细胞变化)在分子确诊的病例中没有发现。
肿瘤通常呈CD10、IFITM1、ER和PR弥漫性强阳性,局灶性cyclin D1阳性(极少数例外)。广谱角蛋白可能阳性。Desmin和h-caldesmonty阳性,通常用于显示平滑肌分化,常见于显示性索样成分,这些成分也表达inhibin、calretinin、melan-A、WT1和CD99。
细胞学
无临床相关性
诊断性分子病理学
有选择的病例,证明特征性基因融合可能有帮助。
诊断标准
必要标准:增殖期子宫内膜间质型肿瘤细胞浸润子宫肌层,伴或不伴淋巴管血管浸润。
分期
低级别子宫内膜间质肉瘤按子宫肉瘤的分期系统,根据FIGO、美国癌症联合委员会(AJCC)和国际癌症控制联盟(UIC系统)进行分期。
预后和预测
低级别子宫内膜间质肉瘤是相对惰性的肉瘤,即使复发,临床病程也很长。分期不是最重要的预后因素,I/II期的5年生存率>90%,而Ⅲ期为50%。有些肿瘤的子宫肌层浸润程度超过子宫内膜间质结节所允许的范围,但与大多数肉瘤相比,其浸润相对有限;这些被命名为浸润有限的子宫内膜间质肿瘤;然而,出于某种目的,它们应该诊断为低级别子宫内膜间质肉瘤,因为它们也可能复发。
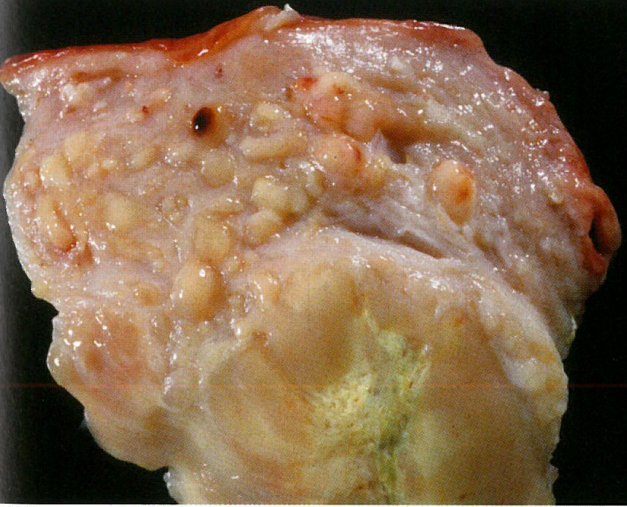
图6.49低级别子宫内膜间质肉瘤,大体表现。褐色大肿块,明显的浸润性生长并进入子宫肌层和血管腔,可见蠕虫状瘤栓。
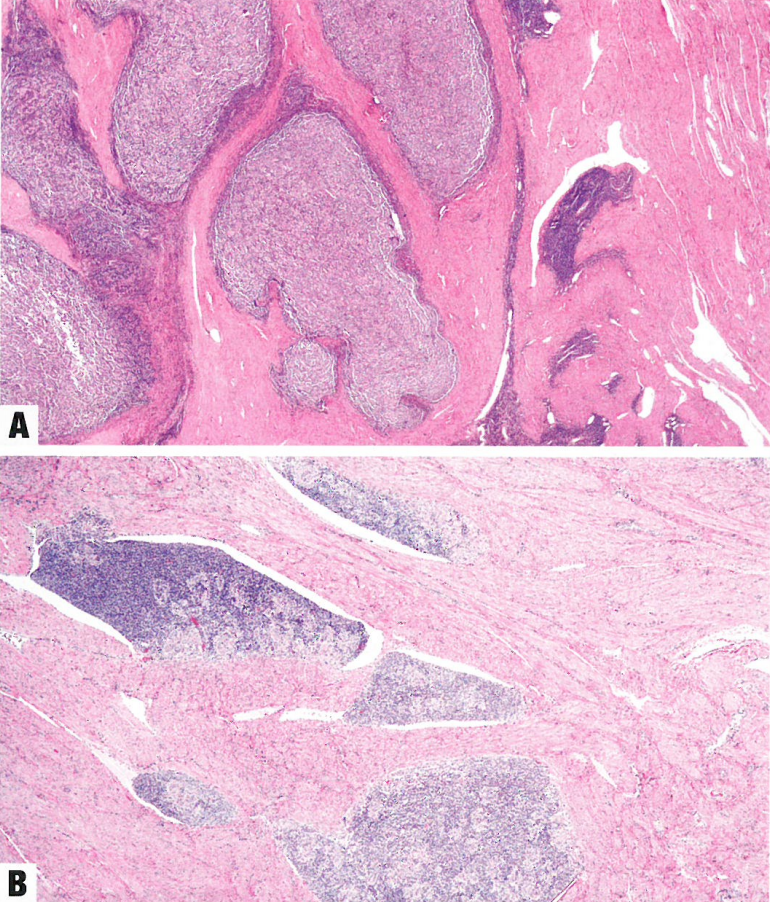
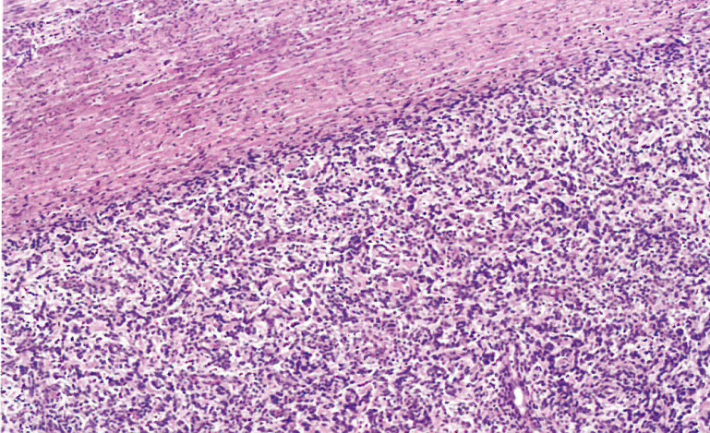
图6.50低级别子宫内膜间质肉瘤。A 肿瘤由蓝色细胞形成不规则的细胞岛,呈舌状浸润模式,没有间质反应。B 可见明显的淋巴管血管浸润。
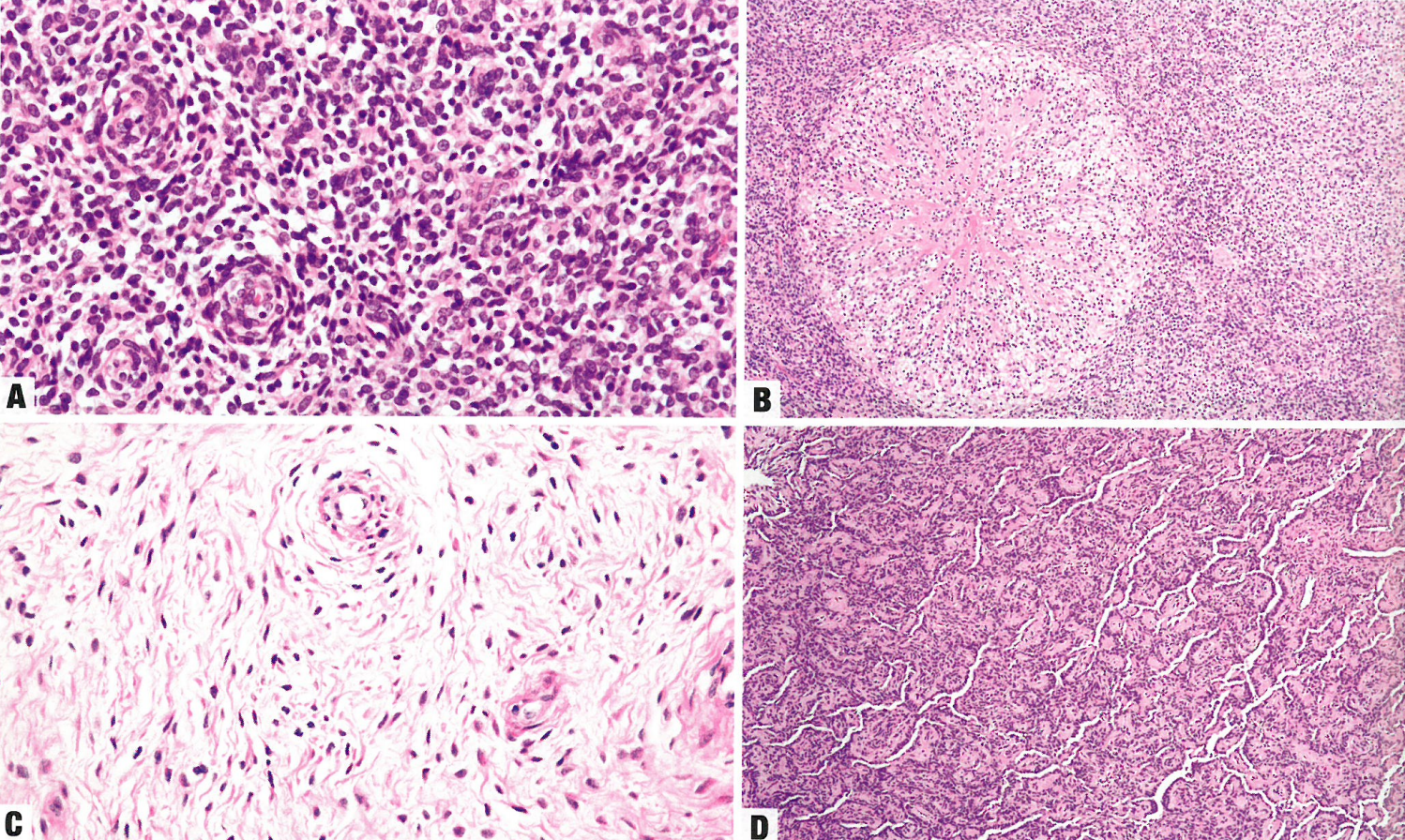
图6.51低级别子宫内膜间质肉瘤。A 小而均匀的细胞,胞质稀少,核卵圆形,没有细胞学异型性。肿瘤细胞在小动脉周围形成局灶性旋涡状排列,就像增殖期子宫内膜间质。B 在子宫内膜恶性肿瘤的背景下,平滑肌分化貌似星爆形态,胶原束向结节周围呈放射状排列,结节内有陷入的圆形细胞。C 与典型的低级别子宫内膜间质肿瘤相反,这例肿瘤细胞稀少。背景有纤细的胶原和小动脉。D 注意广泛的性索样分化伴网状结构。
8. 高级别子宫内膜间质肉瘤
定义
高级别子宫内膜间质肉瘤是一种恶性子宫内膜间质肿瘤,具有均匀一致的高级别圆形和/或梭形形态,有时伴有低级别成分
ICD-0编码
9030/3子宫内膜样间质肉瘤,高级别
ICD-11编码
2BC5.0&XH2CV3 子宫的子宫内膜间质肉瘤&子宫内膜间质肉瘤,高级别
相关命名
无
亚型
无
部位
子宫
临床特征
患者表现为异常子宫出血、盆腔疼痛/压迫感或子宫肿块。
流行病学
这些肿瘤罕见。患者的年龄从14岁到71岁不等,但携带BCOR内部串联重复(ITD)的高级别子宫内膜间质肉瘤的患者通常更年轻(中位年龄:44岁;范围:14-59岁),尽管只有少数病例报道。
病因
未知
发病机制
肿瘤含有YWHAE-NUTM2A/B融合、ZC3H7B-BCOR融合或BCOR ITD。EPC1-BCOR、JAZF1-BCORL1和BRD8-PHF1融合罕见。
大体检查
高级别子宫内膜间质肉瘤通常表现为巨大的宫腔内或子宫肌壁内黄褐色鱼肉样肿块,常见出血和坏死。
组织病理学
肿瘤可能表现为膨胀性、渗透性或浸润性生长,并且可能出现多种侵袭模式。常有淋巴管血管浸润、旺炽的核分裂象活性和坏死。YWHAE-NUTM2A/B融合的肿瘤显示圆形细胞伴嗜酸性胞质和高级别核,核轮廓不规则,空泡状染色质,不同程度的明显核仁。可能伴有纤维黏液样或传统的低级别子宫内膜间质成分。假乳头/腺样结构、横纹肌样形态、假菊形团和性索样分化罕见。高级别成分对Cyclin D1、BCOR、KIT、CD56和CD99呈阳性,对DOG1呈阴性。
ZC3H7B-BCOR高级别肉瘤通常表达Cyclin D1,而只有约50%的病例表达BCOR。CD10通常弥漫性阳性,ER和PR阳性率不一致。它们也可能显示SMA和caldesmon的局灶性表达,但desmin阴性。肿瘤可能显示pan-TRK染色,但与NTRK重排无关。与ZC3H7B-BCOR肿瘤的免疫组化特征不同,BCOR ITD肿瘤(仅报告了少数病例)可能对CD10的阳性率较低,通常对Cyclin D1和BCOR呈弥漫性阳性,对ER和PR呈阴性。还可能表达desmin,但对SMA和caldesmon呈阴性。高级别子宫内膜间质肉瘤NOS伴有低级别子宫内膜间质成分。表6.04总结了所有这些肿瘤的免疫表型。
细胞学
无临床相关性
诊断性分子病理学
证实基因融合或ITD可能有助于诊断。高级别子宫内膜间质肉瘤存在YWHAE-NUTM2A/B融合、ZC3H7B-BCOR融合或BCOR ITD。EPC1-BCOR、JAZF1-BCORL1和BRD8-PHF1融合罕见。
诊断标准
必要标准:单形性高级别圆形和/或梭形细胞;旺炽的核分裂象活性;如有YWHAE-NUTM2A/B或ZC3H7B BCOR融合或BCOR ITD,则Cyclin D1和BCOR免疫染色阳性;如有并存的低级别子宫内膜间质成分,则归入NOS。
理想标准:有选择的病例,验证基因型。
分期
使用FIGO、国际癌症控制联盟(UICC)和美国癌症联合委员会(AJCC)系统的子宫肉瘤分期。
预后和预测
与低级别子宫内膜间质肉瘤相比,高级别子宫内膜间质肉瘤的侵袭性更强。基于蒽环的治疗可能对重现性YWHAE NUTM2A/B肉瘤患者有益。
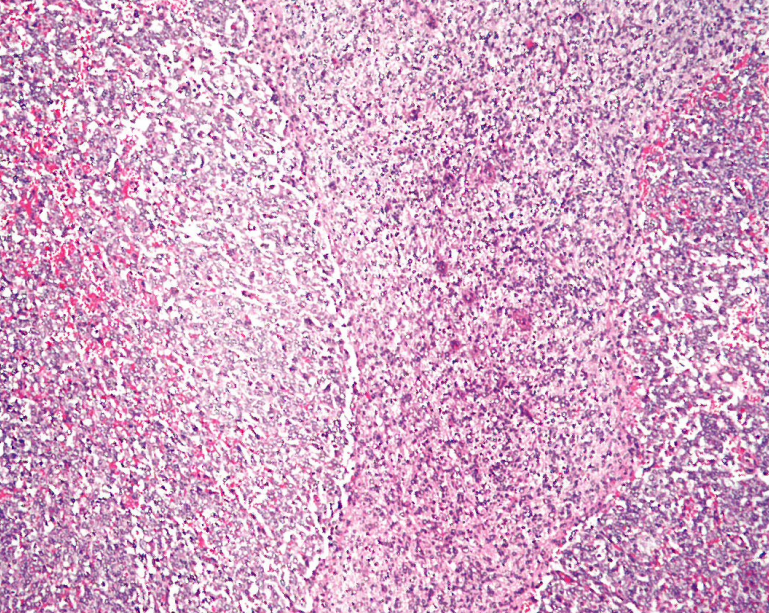 图6.52高级别子宫内膜间质肉瘤NOS。这种高级别肉瘤伴有低级别肉瘤成分,后者表现为低级别子宫内膜间质肉瘤(中心)。
图6.52高级别子宫内膜间质肉瘤NOS。这种高级别肉瘤伴有低级别肉瘤成分,后者表现为低级别子宫内膜间质肉瘤(中心)。
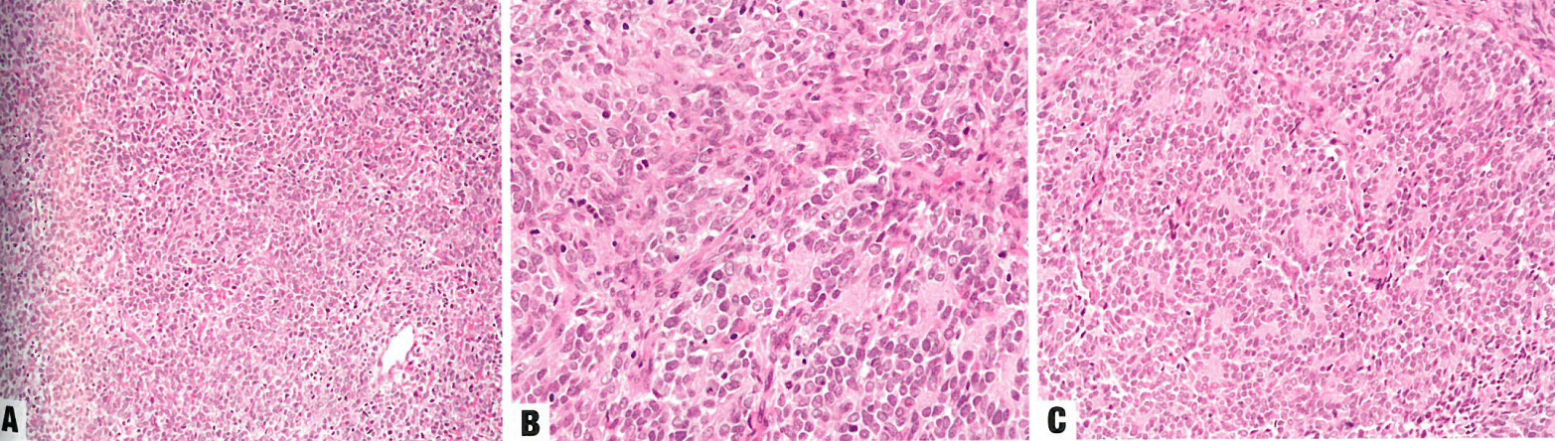
图6.53 YWHAE-NUTM2A/B融合阳性高级别子宫内膜间质肉瘤。A 小圆形肿瘤细胞弥漫性生长,伴纤细血管。B 肿瘤细胞小,有很少嗜酸性胞质,核圆形至成角,颗粒状至空泡状染色质。C 假菊形团形成,可能与原始神经外胚层肿瘤(PNET)混淆,因为二者都表达CD99。然而,高级别子宫内膜瘤表达Cyclin D1和BCOR(PNET都不表达),从而可以区分。
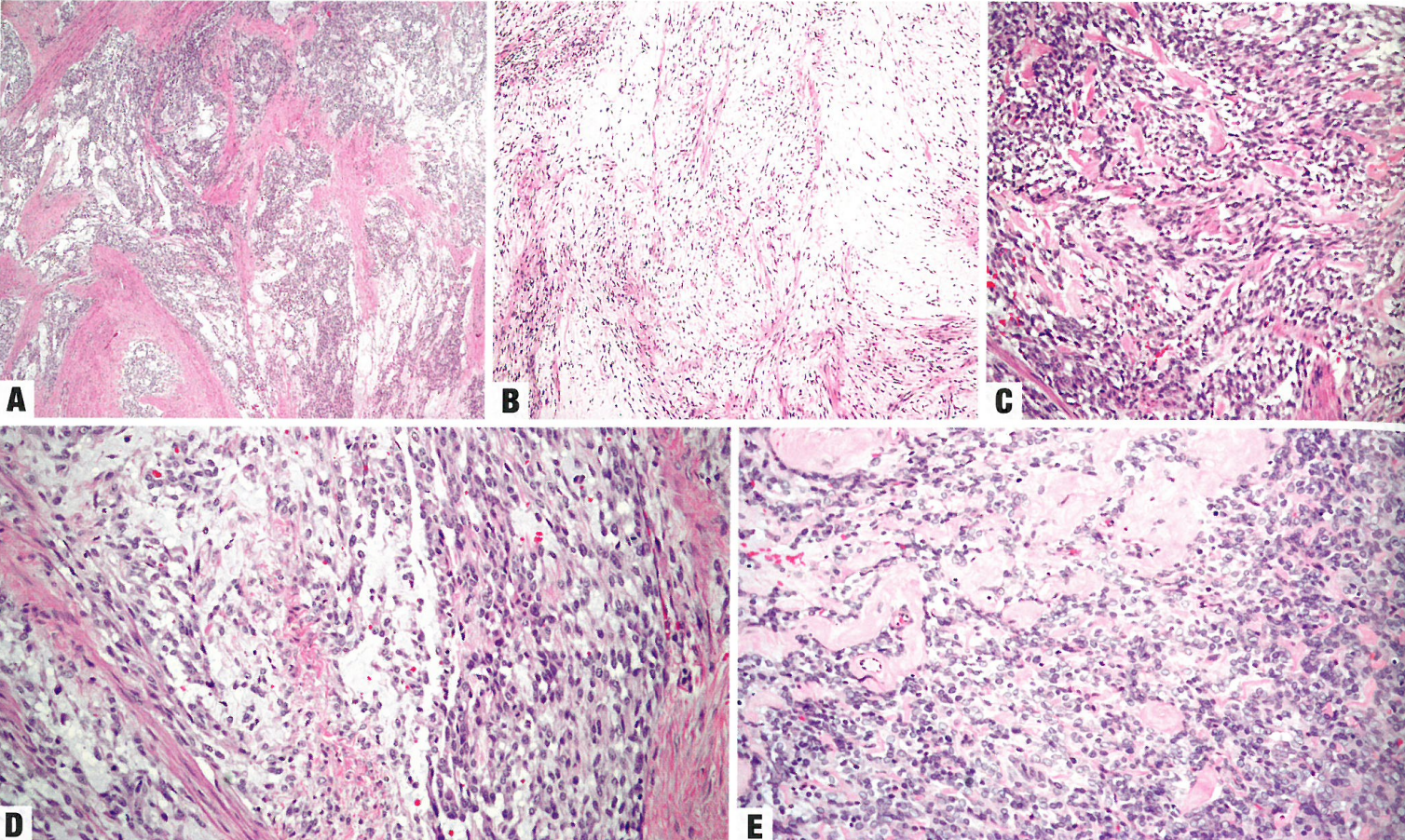
图6.54高级别子宫内膜肉瘤。A-D ZC3H7B BCOR融合的高级别子宫内膜间质肉瘤。A 破坏性浸润子宫肌层,并有丰富的黏液样基质。B 肿瘤由梭形细胞组成,位于背景间质中,很像黏液样平滑肌肉瘤。C 有些病例中,梭形细胞密集,伴有透明斑块。D 少到中等量嗜酸性胞质,椭圆形到梭形核,核相对均匀一致。E BCOR内部串联重复(ITD)高级别子宫内膜间质肉瘤。小圆细胞成分,只有很少梭形细胞成分,陷入略微黏液样间质。
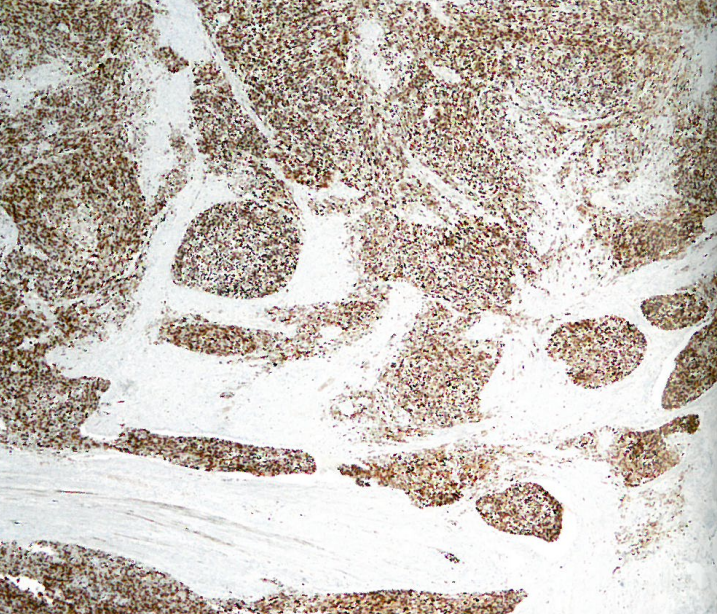
图6.55 ZC3H7B-BCOR融合高级别子宫内膜间质肉瘤。细Cyclin D1呈弥漫性阳性。
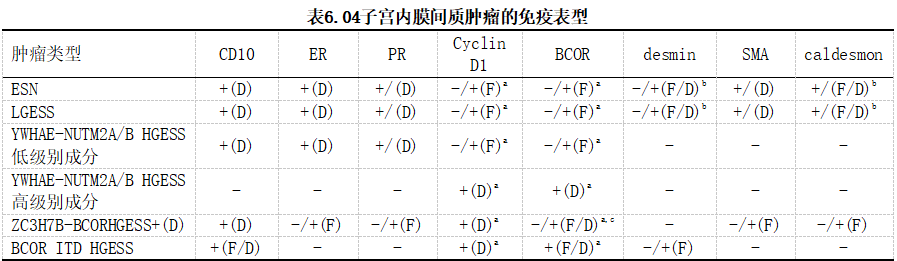
D,弥漫;F,局灶;ITD,内部串联重复;ESN,子宫内膜口间质结节;HGESS,高级别子宫内膜间质肉瘤;LGESS,低级别子宫内膜间质肉瘤
a F(局灶)表示<50%的肿瘤细胞核染色;“D”(弥漫)表示≥70%的肿瘤细胞核染色。
b Desmin和caldesmon仅在变异型平滑肌分化的情况下呈弥漫染色。
c 50%的病变有弥漫染色,染色强度不一
9. 未分化子宫肉瘤
定义
未分化子宫肉瘤是一种恶性间叶性肿瘤,缺乏特定分化细胞系的证据;因此,这是一种排除性诊断。
ICD-O编码
8805/3 未分化肉瘤
ICD-11编码
2B5F.0&XH6HY6 子宫肉瘤,未在其他部位归类&未分化肉瘤
相关命名
无
亚型
无
部位
子宫内膜和/或子宫肌层,罕见于宫颈
临床特征
患者通常是绝经后妇女,出现异常子宫出血、盆腔疼痛/压迫感和与子宫外疾病相关的症状。
流行病学
这些肿瘤罕见。
病因
未知
发病机制
肿瘤显示与生殖道发育、细胞外基质、肌肉功能和增殖相关的RNA表达途径的激活,以及异质性拷贝数的改变。一些肿瘤显示出广泛的染色体获得或缺失;其他肿瘤则接近二倍体。
大体检查
未分化子宫肉瘤形成大的宫腔内息肉样或子宫壁内鱼肉样肿块,伴有出血和坏死。
组织病理学
与软组织对应的肿瘤类似,未分化子宫肉瘤也无法识别分化细胞系。目前认为,它们可能是一组异质性肿瘤,是一种排除性诊断。因此,充分的取材很重要。
未分化子宫肉瘤通常表现为破坏性浸润子宫肌层。过去,将这些肿瘤进一步分类为均匀型和多形型。在具有均匀核特征的肿瘤中,应排除YWHAE NUTM2(FAM22)高级别子宫内膜间质肉瘤。其中一些肿瘤伴有低级别子宫内膜间质成分,并广泛表达Cyclin D1。然而,其他具有多形性组织学的肿瘤也伴有低级别成分,被命名为高级别子宫内膜间叶性肉瘤NOS。因此,目前归入未分化子宫肉瘤类别的肿瘤通常由成片的均匀或多形性的上皮样细胞和/或梭形细胞组成,伴有旺炽性核分裂象活性。常见坏死和淋巴管血管浸润。肿瘤通常呈p53和p16阳性,有些肿瘤ER和/或PR阳性,CD10阳性率不一致。
细胞学
无临床相关性
诊断性分子病理学
可能发现(罕见)YWHAE、JAZF1和NTRK重排,不应归入多形性肉瘤这个类别。
诊断标准
必要标准:均匀或多形性高级间叶性细胞伴旺炽性核分裂象活性;通过广泛取材排除低分化癌、癌肉瘤、腺肉瘤中的肉瘤性过生长,通过ZC3H7B-BCOR、YWHAE-NUTM2(FAM22)和BCOR ITD免疫组织化学排除高级别子宫内膜间质肉瘤和NTRK肉瘤。
理想标准:可能需要排除其他肉瘤携带的融合基因。
分期
使用FIGO、国际癌症控制联盟(UICC)或美国癌症联合委员会(AJCC)系统,按子宫肉瘤进行分期。
预后和预测
这些肿瘤预后不良;然而,核分裂象计数和激素受体表达似乎定义了一组可能实现长期生存的病例。ER和/或PR表达与总体生存率的提高有关。分别与细胞外基质和核分裂象数升高相关的基因表达可能与总生存率和5年生存率的降低有关。
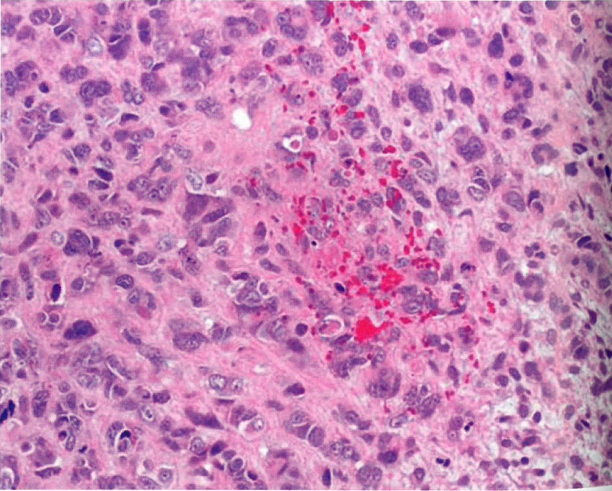
图6.56未分化子宫肉瘤。弥漫性生长方式,明显的核多形性,缺乏任何特定的分化类型。
10. 类似卵巢性索肿瘤的子宫肿瘤
定义
类似卵巢性索肿瘤的子宫肿瘤是一种形态学模式类似于卵巢性索肿瘤的子宫肿瘤,没有可识别的子宫内膜间质成分。
ICD-0编码
8590/1 类似卵巢性索肿瘤的子宫肿瘤
ICD-11编码
2F76&XH8CW8 女性生殖器官的生物学行为不确定的肿瘤&类似卵巢性索肿瘤的子宫肿瘤
相关命名
无
亚型
无
部位
子宫体或罕见于子宫颈
临床特征
这些肿瘤通常发生在中年女性(平均年龄:50岁),通常表现为异常阴道出血或盆腔疼痛,但也可能是偶然发现。
流行病学
罕见(<1%的子宫间叶性肿瘤)。
病因
未知
发病机制
有人假设,这些肿瘤来自多潜能间叶性细胞、子宫内膜间质细胞或移位的卵巢性索细胞,但发病机制尚不确定。波及ESR1或GREB1的重排已有报道,这些重排有多种伴侣,包括NCOA1、NCOA2、NCOA3、CTNNB1、NR4A3和SS18。这些肿瘤不携带低级别子宫内膜间质肉瘤(JAZF1-SUZ12)、成人粒层细胞瘤(FOXL2改变)或Sertoli-Leydig细胞瘤中的分子改变。
大体检查
肿瘤通常位于子宫肌壁内和/或黏膜下,形成平均大小为6cm的息肉样肿块。它们通常边界清楚,主要呈实性,质软到质硬不等,切面呈黄色或褐色。
组织病理学
这些肿瘤通常边界清楚,但有些肿瘤边缘不规则,周围平滑肌被陷入肿瘤中。它们呈片状、条索状、巢状、岛状、小梁状或小管状生长,有时呈网状。胞质少到丰富,可能淡染(包括泡沫状)或嗜酸性,有时形成横纹肌样外观。核呈卵圆形,呈轻微的细胞学异型性,核分裂象活性低,但恶性肿瘤例外,恶性肿瘤可能表现为明显的细胞学异型性和旺炽性核分裂象活性。偶尔可见血管浸润。肿瘤具有多表型免疫组织化学表达谱,不同程度地表达性索标志物(inhibin、calritinin、WT1、CD56、CD99、SF1、FOXL2和melan-a)、上皮标志物、ER、PR、平滑肌标志物(actin、desmin和h-caldesmon)和CD10。
细胞学
无临床相关性
诊断性分子病理学
无临床相关性
诊断标准
必备:性索模式,不含子宫内膜间质瘤成分。
理想:性索间质标记物阳性。
分期
使用FIGO、国际癌症控制联盟(UICC)和美国癌症联合委员会(AJCC)系统,按子宫肉瘤分期。
预后和预测
类似卵巢性索肿瘤的子宫肿瘤的大多数病例是良性,但应当认为具有较低的恶性潜能,因为它们可能会复发。然而,尚未确定明确的预后形态学特征。
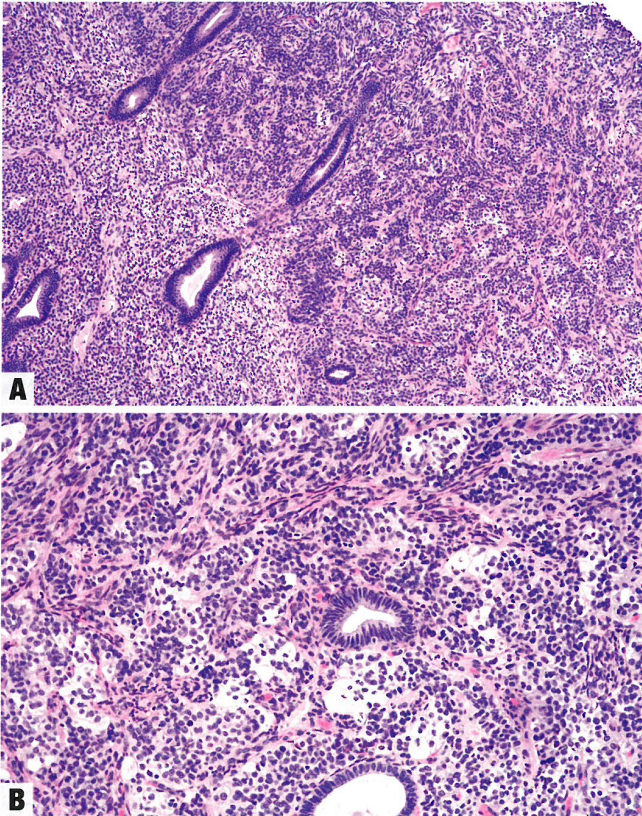
图6.57类似卵巢性索肿瘤的子宫肿瘤。A 肿瘤显示吻合的小梁,在子宫内膜腺体之间生长。B 大多数肿瘤细胞显示嗜酸性胞质,但有些细胞有丰富的淡染空泡状胞质。核小而温和。
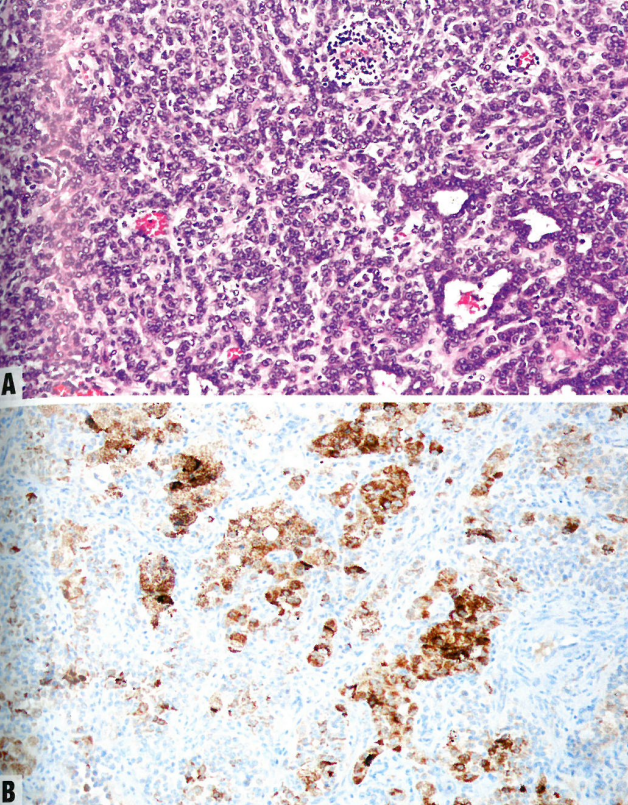
图6.58类似卵巢性索肿瘤的子宫肿瘤。A 肿瘤细胞形成条索和小管。B Melan-A在许多肿瘤细胞中呈阳性。
11. 血管周上皮样细胞肿瘤
定义
血管周上皮样细胞肿瘤(PEComa)是由表达黑素细胞和平滑肌标志物的血管周细胞(PEC)组成的间叶性肿瘤家族的成员。
ICD-O编码
8174/0 血管周围上皮样肿瘤,良性
8174/3 血管周围上胚层肿瘤,恶性
ICD-11编码
2F33.Y&XH4CC6 女性生殖器官的其他特指性良性肿瘤&血管周上皮样肿瘤,良性
2C76.Y&XH9WD1女性生殖器官的其他特指性良性肿瘤&血管周上皮样肿瘤,恶性
相关命名
无
亚型
无
部位
PEComa最常见于子宫体,较少发生在宫颈、阴道、卵巢和阔韧带。
临床特征
患者通常会出现盆腔肿块、异常出血或腹盆腔疼痛。
流行病学
患者年龄范围16-77岁(平均:51岁)。
病因
大多数病例是散发性,但有一部分(约10%)伴有结节性硬化症。
发病机制
TSC1/TSC2的失活突变导致mTOR信号传导上调。一些肿瘤具有TFE3、RAD51B或HTR4-ST3GAL1融合。TSC突变和TFE3融合是相互排斥的。
大体检查
肿瘤边界清楚或有浸润性边缘;大小范围0.2-17cm(平均5.5cm),可能有出血坏死或软化。
组织病理学
传统型PEComa由上皮样细胞和/或梭形细胞组成,具有透明至嗜酸性颗粒状胞质。上皮样细胞排列成不粘附的细胞巢,周围围绕薄壁血管,和/或排列成片状,而梭形细胞通常形成束状。其他特征包括肿瘤细胞的放射状/血管周围分布、多核细胞、富含脂质或横纹肌样胞质的细胞和间质透明变性(如果广泛,肿瘤可以称为硬化性PEComa)。肿瘤可能具有膨胀性、渗透性(舌状)或浸润性生长。罕见的PEComa形成淋巴管平滑肌瘤病样形态的肿块。TFE3易位相关PEComa具有均匀的上皮样细胞,胞质全透明或透明至嗜酸性,形成巢状、腺泡状或实性结构。这两种类型都可以看到不同程度的细胞学异型性和核分裂象活性,以及黑色素(局灶性或弥漫性)。
传统型PEComa表达HMB45、melan-A和平滑肌标志物(SMA、desmin和h-caldesmon),表达强度和范围各不相同。在黑素细胞标记物中,HMB45最敏感,几乎在所有肿瘤中都是阳性,而melan-A特异性更强,至少在一半肿瘤阳性(有时只是局部阳性)。每个平滑肌标志物阳性率相似。组织蛋白酶K在几乎所有肿瘤中都是阳性,只有少数病例表达S100(局灶性)、MITF和酪氨酸酶。一些肿瘤可能表达广谱角蛋白和激素受体。
TFE3易位相关的PEComa呈TFE3、HMB45和组织蛋白酶K弥漫性阳性,Melan A呈局灶阳性至阴性。平滑肌标志物的表达各不相同,但通常弱阳性至阴性。
细胞学
无临床相关性
诊断性分子病理学
在TFE3重排肿瘤中,通过原位杂交或其他方法确认TFE3重排或融合可能有帮助。
诊断标准
必需标准:透明至嗜酸性颗粒状胞质的细胞;薄壁血管围绕细胞巢;HMB45或melan-A的表达以及至少一种肌样标志物阳性。
理想标准:证实TFE3重排肿瘤中的TFE3重排或融合。
分期
恶性PEComa分期按子宫肉瘤进行分期。
预后和预测
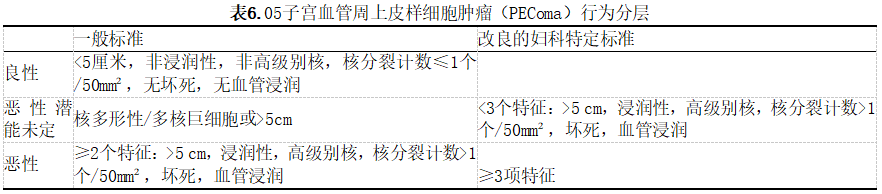
已经提出了三种方法对恶性潜能进行分层(见表6.05)。由于mTOR信号通路的激活,可以考虑使用mTOR抑制剂。有限的数据表明,RAD51B融合的肿瘤可能侵袭性更强。
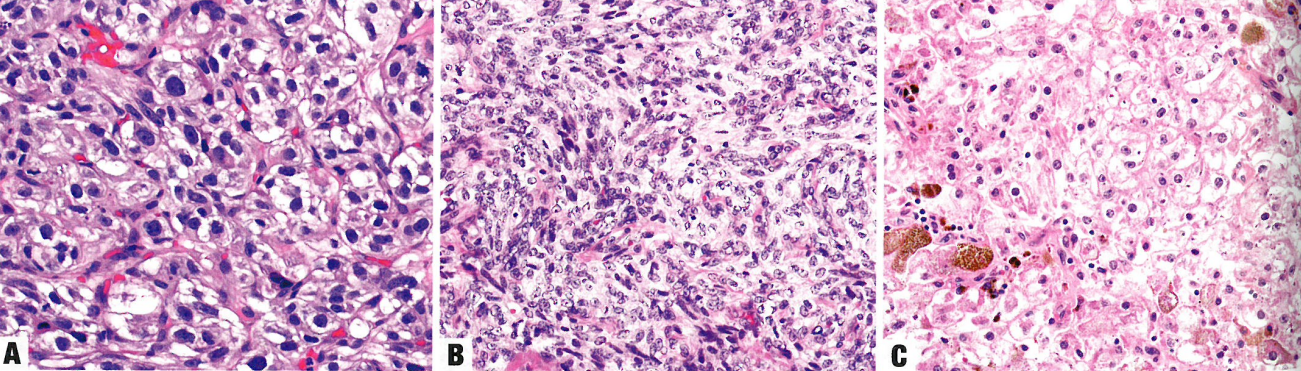
图6.59血管周围上皮细胞瘤(PEComa)。A 传统型PEComa,由上皮样细胞组成,胞质透明至嗜酸性,形成小巢,周围有纤细的血管。B 传统型PEComa主要由梭形细胞组成,含有淡染的嗜酸性颗粒状胞质,形成短束状。C TFE3易位相关的PEComa,由上皮样细胞组成,胞质透明或透明至嗜酸性颗粒,片状生长。可见黑色素。
12. 炎性肌纤维母细胞瘤
定义
炎性肌纤维母细胞瘤(IMT)是一种独特的间叶性肿瘤,由梭形细胞(肌纤维母细胞和纤维母细胞)组成,伴有炎性浸润。
ICD-0编码
8825/1 炎性肌纤维母细胞瘤
ICD-11编码
2F76&XH66Z0 女性生殖器官行为不确定的肿瘤&肌纤维母细胞瘤NOS
相关命名
不推荐:炎性假瘤
亚型
上皮样炎性肌纤维母细胞肉瘤
部位
多个解剖部位报道了IMT,包括腹膜和内脏。在女性生殖道中,IMT通常发生在子宫体,子宫颈很少见。
临床特征
大肿瘤可能会导致异常子宫出血,也可能是子宫切除术或剖腹产时的偶然发现。腹膜中的肿瘤可能会引起与腹盆腔肿块相关的症状,或者偶然发现。
流行病学
子宫IMT罕见(<100例报告病例)。它们通常发生在成年绝经前妇女中(中位年龄:38岁;范围:6-78岁)。有些病例与妊娠有关,并累及胎盘。
病因
未知
发病机制
大多数(约95%)病例呈ALK免疫染色阳性,通常与ALK基因的改变有关。大约75%的病例,FISH检测到ALK重排(2p23.2-p23.1)。常见的融合伴侣包括IGFBP5、THBS1和TIMP3。FISH阴性的肿瘤通常具有复杂的遗传重排,如染色体内倒置,可用RNA测序来检测。ALK阴性子宫IMT罕见,可能被低估,只有一例携带ETV6-NTRK3或RET融合。ROS1和PDGFRB融合尚未在子宫肿瘤中发现。腹膜IMT也经常包含涉及受体酪氨酸激酶的遗传融合;ALK最常见,有可变的5'融合伴侣,其次是罕见的NTRK3融合。报道,伴有上皮形态的侵袭性IMT携带RANBP2-ALK和RRBP1-ALK融合(见下文描述)。
大体检查
子宫IMT的平均大小为7.5cm(范围:1-20cm)。大多数肿瘤位于子宫肌壁内,但也可能在宫腔内息肉样生长。切面表现为胶样、质软或质硬、旋涡状(就像平滑肌肿瘤),边缘经常不规则。约1/3肿瘤出现出血和坏死。
组织病理学
低倍镜下,肿瘤可能边界清楚,也可能显示浸润性边缘。有三种主要的组织学模式,它们可能混合存在的:(1)疏松的黏液样模式,特征是少细胞区域,单个细胞散在分布于丰富的黏液样基质中,呈现结节性筋膜炎样或组织培养样外观(可能貌似黏液样平滑肌肿瘤);(2)束状/致密型,特征是富细胞区域,排列成交叉束状或较少见的网状结构(貌似传统型平滑肌肿瘤或较少见的子宫内膜间质瘤);和(3)透明变性模式,特征是致密胶原化间质,肿瘤细胞不明显。肿瘤细胞呈梭形,含有细腻的嗜酸性胞质和细长的核,均匀分布的或开放的染色质。可能存在神经节样细胞、上皮样细胞和Touton巨细胞。核异型性通常轻微,但可能出现重度异型性。可能存在核分裂象。炎症成分通常以淋巴浆细胞为主,混合其他炎症细胞,在每个肿瘤内炎症强度和分布各不相同。妊娠期可以观察到间质蜕膜化。
具有上皮样形态的ALK阳性IMT已被描述为“上皮样炎性肌纤维母细胞肉瘤”这个术语。这种亚型通常位于腹腔内,大多数起源于肠系膜或网膜。在卵巢中也有描述,但在女性生殖道的其他部位尚未发现。它由成片的圆形上皮样细胞组成,具有空泡状核和嗜酸性胞质,常有丰富的黏液样间质和炎症,以及少量梭形细胞成分。
免疫组织化学
免疫组化,ALK颗粒状胞质阳性对子宫IMT的诊断具有高度敏感性和特异性;然而,阳性程度各不相同,一些肿瘤仅显示局灶性染色。IMT常表达SMA、desmin和caldesmon(因此,如果只考虑这些标记物,常被误诊为平滑肌肿瘤)。也常表达CD10,但角蛋白、S100、CD34和KIT(CD117)阴性。肿瘤通常是p53野生型。
细胞学
无临床相关性
诊断性分子病理学
ALK的免疫组织化学通常足以诊断,有选择的病例中检测融合基因可能有用。
诊断标准
必要标准:形态学温和的梭形细胞伴黏液样和束状生长;淋巴浆细胞性炎症;ALK免疫组织化学表达(有极少数例外)。
理想:ALK重排。
分期
无临床相关性
预后和预测
大多数子宫IMT是良性,仅限于子宫;然而,少数患者会出现子宫外扩散和/或复发。没有足够的证据来确定局限于子宫的肿瘤的预后参数。坏死、肿瘤>7cm、中度至重度异型性、高度核分裂象活性和淋巴管血管浸润与侵袭性病程有关。携带ALK重排的IMT可能对使用酪氨酸激酶抑制剂的靶向治疗有反应。腹膜上皮样炎性肌纤维母细胞肉瘤具有高度侵袭性,其中大量患者快速局部复发并致死。
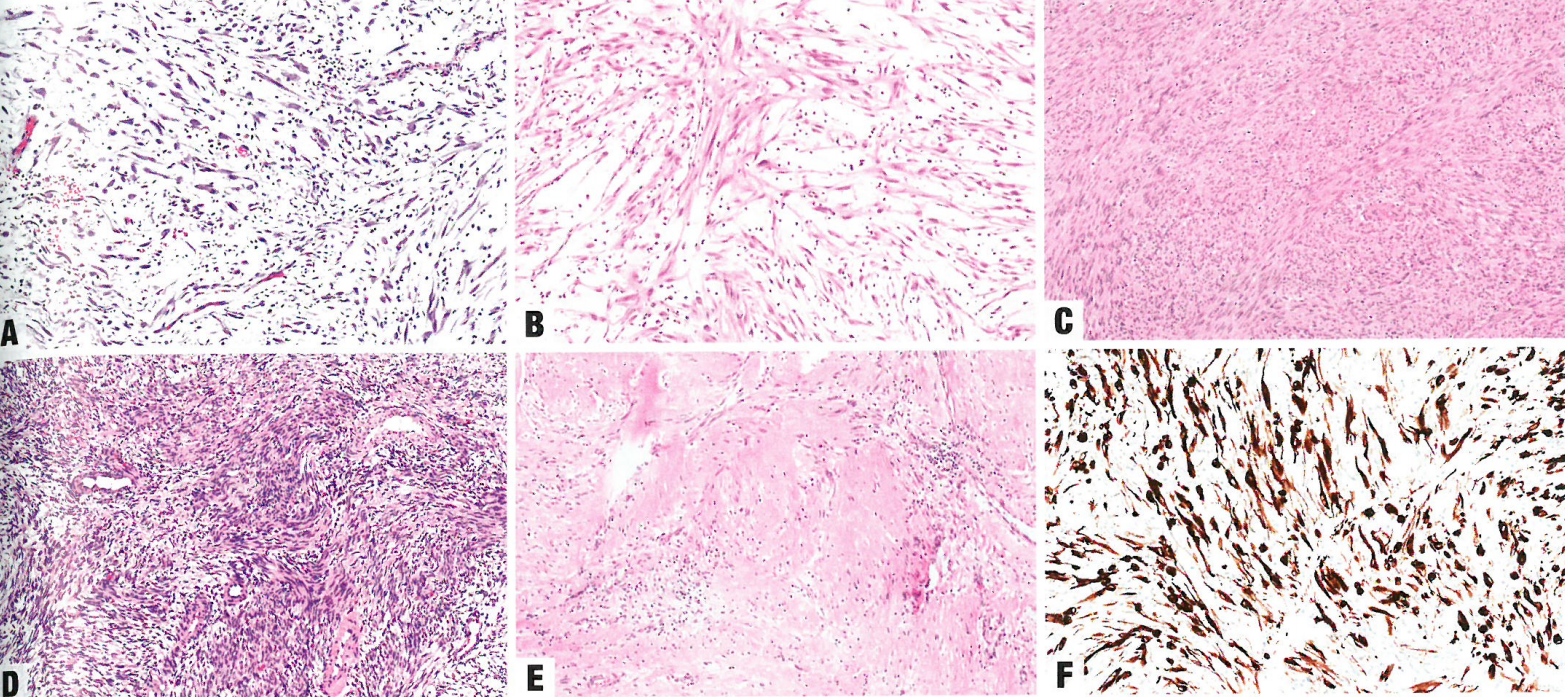
图6.60炎性肌纤维母细胞瘤。A 形态温和的梭形和卵圆形的细胞,陷入黏液样基质中,呈组织培养样外观。注意,淋巴浆细胞浸润遍布肿瘤。B 黏液样模式,少细胞,在黏液样背景下,疏松排列的梭形至上皮样细胞,并有明显的混合性炎性炎症(淋巴细胞、浆细胞、组织细胞和嗜酸性粒细胞)。C 束状模式,可能高度富于细胞,没有可辨认的肿瘤间间质,混合性炎性浸润不太明显。D 与黏液样区域相比,束状结构通常细胞更丰富,炎症更少,很像平滑肌肿瘤。E 透明变性模式,细胞很少,呈散在的梭形细胞和明显的透明变性间质。F ALK呈胞质强阳性。
子宫的其他间叶性肿瘤
子宫体中也可能发生各种其他良性和恶性间叶性肿瘤,包括血管肿瘤、脂肪肿瘤、腺泡状软组织肉瘤、孤立性纤维瘤(在第13章:下生殖道间叶性肿瘤中讨论)、神经鞘瘤和更常见的神经纤维瘤(与神经纤维瘤病相关)、NTRK肉瘤(在第13章:下生殖器间叶性肿瘤中讨论)和巨细胞瘤。
三、混合性上皮-间叶肿瘤
8932/0 腺肌瘤
8932/0 非典型性息肉样腺肌瘤
8933/3 腺肉瘤
13. 子宫体腺肌瘤
定义
腺肌瘤由形态学良性的子宫内膜样腺体、子宫内膜样间质和平滑肌混合形成。
ICD-0编码
8932/0 腺肌瘤NOS
ICD-11编码
2F33.Y&XH4ZH4 其他特指性女性生殖器官的良性肿瘤&腺肌瘤
相关命名
可接受:腺肌瘤性息肉;子宫内膜样腺肌瘤;息肉样腺肌瘤
亚型
无
部位
肿瘤主要位于子宫体,偶尔位于子宫颈。它们可呈息肉样、子宫肌壁内或浆膜下病变。它们也可能发生在阔韧带。
临床特征
腺肌瘤的发病年龄范围很广。大多数患者出现异常阴道出血。
流行病学
没有流行病学数据。
病因
未知
发病机制
一些病例与潜在的子宫腺肌病有关,代表了子宫腺肌病的一种局限化形式;在一项研究中,30.8%的病例存在子宫腺肌病。一项研究发现,这些肿瘤在MED12的外显子2中缺乏突变(子宫平滑肌瘤的特征)。
大体检查
在一项大型系列中,肿瘤的最大径0.3-17cm。肿瘤呈结节状或息肉样,切面主要为实性白色旋涡状,有时伴有小囊肿。
组织病理学
子宫体腺肌瘤是由腺体和囊肿组成的结节或息肉,内衬形态温和的子宫内膜样上皮,周围是子宫内膜样间质和平滑肌,通常以平滑肌为主。上皮成分内可能发生各种化生,包括输卵管化生、黏液性化生和鳞状化生。子宫内膜样间质围绕腺体,但在大部分病变中可能不明显。平滑肌成分通常形态温和,没有细胞数量的增加,通常含有厚壁血管成分,但偶尔细胞丰富,呈上皮样外观,或含有少量奇异形核,没有核分裂象活性。子宫内膜息肉的间质中存在少量平滑肌成分并不少见,这些病例不应称为腺肌瘤。免疫组织化学,子宫内膜样间质成分通常呈CD10阳性,平滑肌成分通常呈desmin、SMA和h-caldesmon阳性。
细胞学
无临床相关性
诊断性分子病理学
无临床相关性
诊断标准
必要标准:由子宫内膜样腺体、子宫内膜样间质和平滑肌组成的结节或息肉。
分期
无临床相关性
预后和预测
这些肿瘤都是良性,患者在子宫切除术、子宫肌瘤切除术或息肉切除术后的结局平安。

图6.61腺肌瘤。边界清楚,实性为主,但可有大小不一的出血灶和囊肿形成。
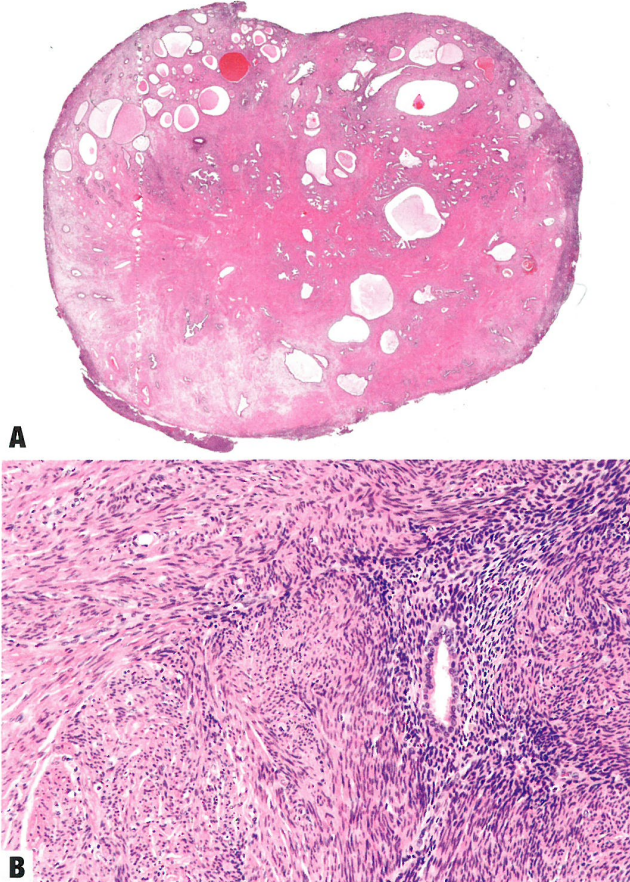
图6.62腺肌瘤。A 低倍,典型腺肌瘤,含有囊腔。B 肌瘤通常由子宫内膜样腺体组成,周围是子宫内膜样间质和平滑肌。
14. 非典型息肉样腺肌瘤
定义
非典型息肉样腺肌瘤是一种息肉样病变,由非典型、结构复杂的子宫内膜腺体组成,位于肌瘤或纤维肌瘤内。
ICD-0编码
8932/0 非典型息肉样腺肌瘤
ICD-11编码
2F33&XH7ZB1 其他或非特指女性生殖器官的良性肿瘤&非典型息肉样腺肌瘤
相关命名
可接受:非典型息肉样腺肌纤维瘤
亚型
无
部位
它们往往发生在子宫下段,但也可能发生在子宫体。
临床特征
患者出现阴道异常出血或不育。
流行病学
患者年龄范围为25-73岁(平均39岁)。大多数患者处于生育年龄。有3例与特纳综合征有关。
病因
未知
发病机制
至少有些病例可能是继发于长期雌激素刺激。未发现特定分子异常;然而,非典型息肉样腺肌瘤与非典型增生和低级别子宫内膜样病变腺癌表现出相似的免疫组织化学和分子特征。
大体检查
非典型息肉样腺肌瘤是一种息肉样、质硬的病变。通常是外生性,也可能出现内生性生长模式。平均大小为2cm,但有报道最大达到6cm。大多数非典型息肉样腺肌瘤是单发,偶尔出现多发性息肉样病变。
组织病理学
非典型息肉样腺肌瘤由不规则的、通常结构复杂的子宫内膜样腺体组成,这些腺体位于肌瘤性或纤维肌瘤性间质内。几乎总有鳞状化生,通常伴有中央坏死。腺体成分可能具有轻度至中度异型性,并可能呈小叶状排列。周围组织由良性富细胞性肌瘤性或纤维肌瘤性间质组成。在刮宫标本中,非典型息肉样腺肌瘤的碎片通常与正常增殖期或分泌期子宫内膜的碎片相混合。间质细胞呈h-caldesmon阴性(与子宫肌层不同),SATB2可能呈核阳性。
细胞学
无临床相关性
诊断性分子病理学
无临床相关性
诊断标准
必要标准:不连续病变,由非典型、通常复杂的子宫内膜样腺体组成,伴有桑椹样鳞状化生,位于良性纤维肌瘤性间质中
分期
无临床相关性
预后和预测
大多数育龄期患者可以通过刮宫和密切随访来治疗。尽管疾病持续存在,女性可能成功怀孕。普通的非典型息肉样腺肌瘤有30%的复发率,但含有更多结构复杂腺体的病变风险更高。对已发表系列文章的全面综述表明,进展为子宫内膜腺癌的风险约为8.8%。几乎所有这些癌都是低级别和微小浸润。
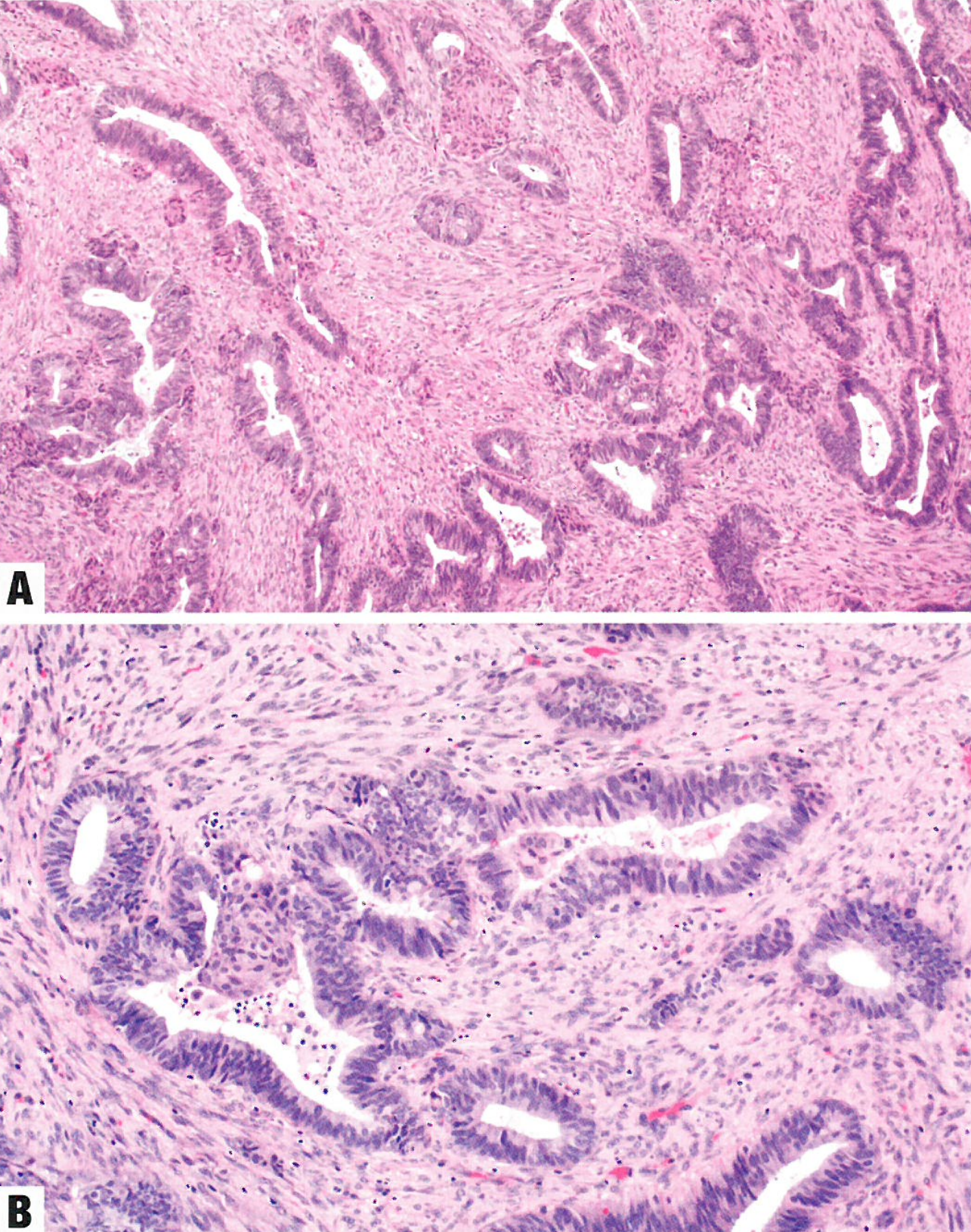
图6.63非典型息肉样腺肌瘤。A 这些病变通常含有不规则的、通常结构复杂的子宫内膜样腺体,常有桑椹样鳞化,位于肌瘤性或纤维瘤性间质内。B 腺体成分可有轻中度异型性,周围组织由良性富细胞性肌瘤性或纤维肌瘤性间质组成。
15. 子宫体腺肉瘤
定义
腺肉瘤是一种由良性上皮成分和恶性间质成分组成的双相肿瘤。
ICD-0编码
8933/3 腺肉瘤
ICD-11编码
2B5D.1&XH5544 子宫体的恶性混合上皮和间叶性肿瘤&腺肉瘤
相关技术
可接受:苗勒腺肉瘤
亚型
腺肉瘤伴肉瘤性过生长
部位
除了发生在子宫,这些肿瘤也发生在子宫颈和阴道(见子宫颈腺肉瘤,原书第388页,和阴道腺肉瘤,原书第417页)。另外,这些肿瘤可发生于子宫外,可能来自子宫内膜异位症(见卵巢腺肉瘤,原书第91页)。
临床特征
患者出现异常子宫出血、子宫增大、盆腔肿块或宫颈外口脱出物。提示复发性息肉的病史并不少见。
流行病学
年龄范围广,但大多数是绝经后患者。
病因
有人认为这种肿瘤来自苗勒间叶性细胞的肿瘤转化,随后刺激良性伴随腺体的反应性生长。
发病机制
发病机制尚不清楚,但有些病例与他莫昔酚的使用有关。
大体检查
肿瘤通常是孤立性、外生性、息肉样肿块,充满宫腔(平均大小:约5-6cm);它们通常在宫颈外口脱垂。小肿瘤可能类似于典型的子宫内膜息肉。大肿瘤常见坏死和出血,特别是在肉瘤性过生长的情况下。
组织病理学
典型的肿瘤具有分叶状结构。腺体呈裂隙样或扩张(僵硬的囊肿),内衬良性子宫内膜上皮或纤毛上皮。腺体周围环绕着一圈明显的肿瘤性间质,与附近的良性组织相比,肿瘤间质通常富于细胞。常有间质增殖和异型性,但可能轻微。肉瘤性成分通常是无法描述的非特殊性同源型组织,但也可能是横纹肌肉瘤分化和罕见的性索分化。肉瘤成分可能远远超过上皮成分(称为肉瘤性过生长);也可能转化为高级别肉瘤。上皮成分可有某种程度的细胞学异型性,常有化生。免疫组织化学显示,肿瘤通常呈CD10、ER和PR阳性,但在肉瘤性过生长时通常呈阴性。腺纤维瘤的诊断已从本版WHO分类中删除,并且认为先前诊断为腺纤维瘤瘤的大多数肿瘤只是低级别腺肉瘤或具有异常形态(即,局灶性叶状结构和/或腺体周围间质细胞增多)的良性子宫内膜息肉或子宫颈息肉。
细胞学
无临床相关性
诊断性分子病理学
这种肿瘤缺乏其他妇科肉瘤中发现的基因组畸变和特异性染色体重排。有些病例检出8q13扩增和MYBL1高级拷贝数的获得,最常见于肉瘤性过生长。少数病例存在NCOA2/3融合。TP53突变少见,与肉瘤性过生长和侵袭性行为有关。
诊断标准
必要标准:恶性间质增生伴非肿瘤性苗勒上皮,通常形成宽大的分叶状结构,突入囊腔内,类似于乳腺叶状肿瘤;富于细胞的间质在腺体周围形成袖套样结构;核分裂象活性(可能轻微或没有)
分期
腺肉瘤的分期不同于其他子宫肉瘤;pT1的命名是基于肌层浸润的存在和深度,而不是肿瘤大小。
预后和预测
与其他妇科肉瘤相比,腺肉瘤的预后通常较好。肉瘤性过生长、深肌层浸润和子宫外复发是不良预后因素。高度异型性也可能导致更差结局。
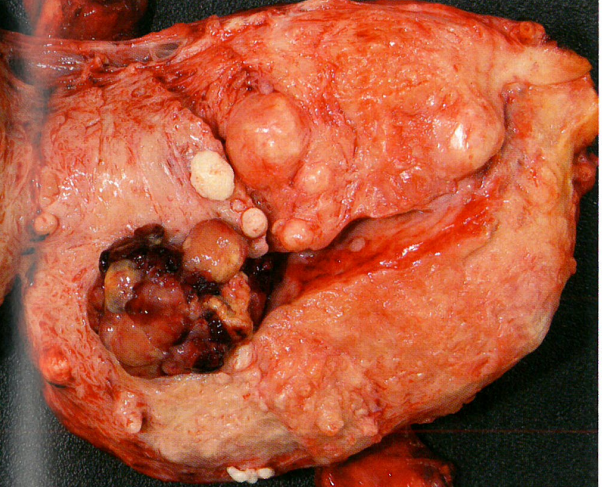
图6.64腺肉瘤。多发性息肉样肿块,有些伴出血,突入宫腔内。
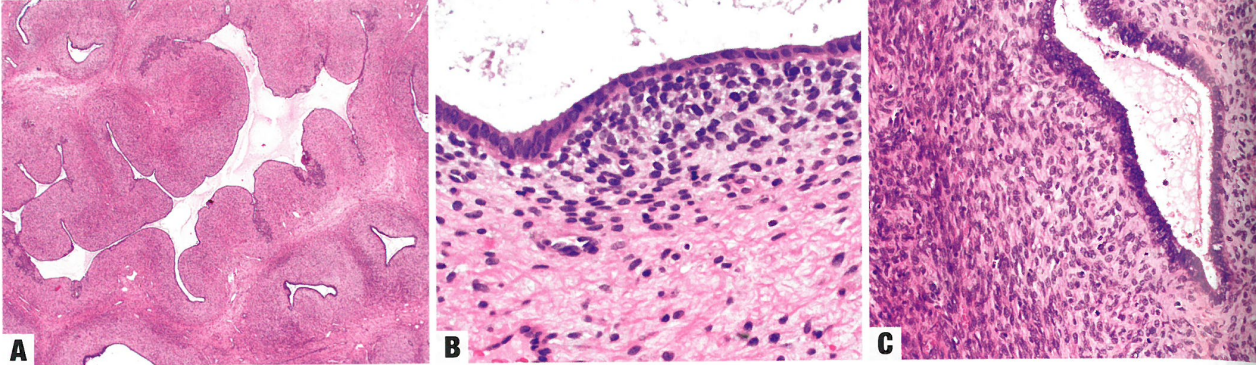
图6.65腺肉瘤。A 低倍,子宫腺肉瘤呈分叶状结构和和腺体周围细胞增多。B 上皮下方密集的核分裂象活跃的富于细胞性间质是其特征。C 高倍,示子宫腺肉瘤间质核分裂象活性。
四、杂类肿瘤
16. 中枢型原始神经外胚层肿瘤/CNS胚胎性肿瘤
定义
中枢型原始神经外胚层肿瘤/CNS胚胎性肿瘤是一种中枢型神经外胚层起源的恶性肿瘤。
ICD-0编码
9473/3 原始神经外胚层肿瘤NOS
ICD-11编码
2B5F.0&XH89C3 子宫肉瘤,未在其他部位归类&中枢原始神经外胚层肿瘤NOS
相关命名
无
亚型
无
部位
这些肿瘤在子宫体中比在宫颈中更常见。
临床特征
症状包括异常子宫出血、盆腔疼痛/压迫感和子宫肿块引起的症状。
流行病学
这些是罕见的肿瘤,发生在中位年龄为55岁(范围:26-81岁)的女性患者。
病因
未知
发病机制
未知
大体检查
这些肿瘤通常形成息肉样鱼肉样肿块,伴有出血。
组织病理学
肿瘤的特征是小圆蓝色细胞,或可能显示神经元/神经胶质分化。有些肿瘤伴有另一种肿瘤类型,如癌、腺肉瘤或癌肉瘤。Syn、CgA和S100通常阳性,大约一半的病例GFAP阳性。常见CD99和FLI1膜阳性。
鉴别诊断
尤因肉瘤(Ewing sarcoma),文献中经常报道为外周型原始神经外胚层肿瘤,不应包括在这一类别中。尤因肉瘤缺乏GFAP免疫表型,有特征性的基因融合,最常见的是EWSR1-FLI1。
细胞学
无临床相关性
诊断性分子病理学
缺乏EWSR1-FLI1融合或其变异融合可能有帮助。
诊断标准
必要标准:恶性小细胞肿瘤伴任何程度的神经胶质分化;排除尤因肉瘤。
分期
按子宫肉瘤分期。
预后和预测
这些肿瘤预后差。
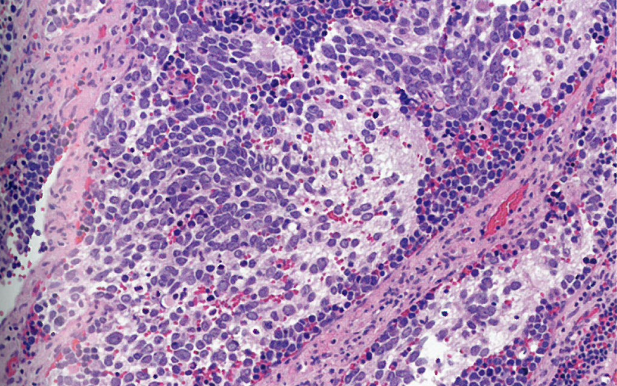
图6.66中枢型原始神经外胚层肿瘤。小圆细胞伴局灶神经纤维,后者符合胶质分化。
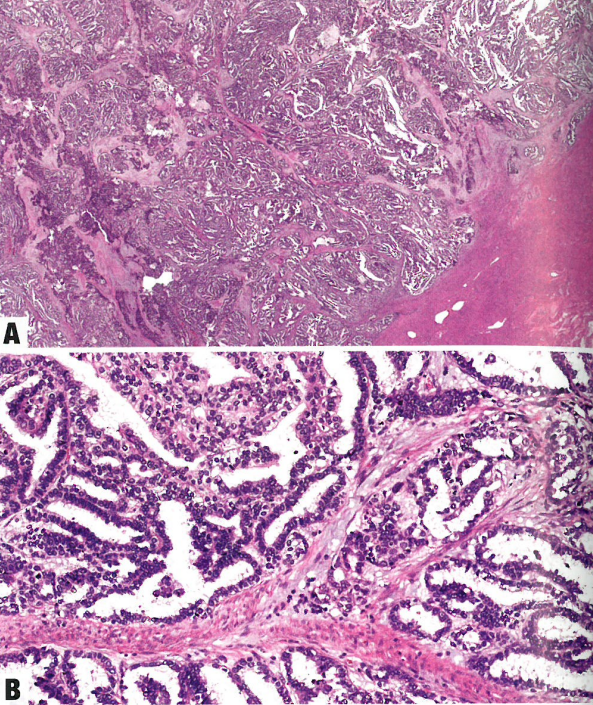
图6.67子宫内膜卵黄囊瘤。A 肿瘤以乳头状结构为主;乳头状结构被覆立方形到柱状细胞,核呈原始形态;存在核上和/或核下空泡。B 更高倍。
第6章完结
责任编辑:华夏病理 本站欢迎原创文章投稿,来稿一经采用稿酬从优,投稿邮箱tougao@ipathology.com.cn
相关阅读
 数据加载中
数据加载中
我要评论

热点导读
-

淋巴瘤诊断中CD30检测那些事(五)
强子 华夏病理2022-06-02 -

【以例学病】肺结节状淋巴组织增生
华夏病理 华夏病理2022-05-31 -

这不是演习-一例穿刺活检的艰难诊断路
强子 华夏病理2022-05-26 -

黏液性血性胸水一例技术处理及诊断经验分享
华夏病理 华夏病理2022-05-25 -

中老年女性,怎么突发喘气困难?低度恶性纤维/肌纤维母细胞性肉瘤一例
华夏病理 华夏病理2022-05-07







共0条评论