介绍
p63基因是p53肿瘤抑制基因的同源物,它是上皮细胞发育所必需的。p63基因位于染色体3q27-29上,包含15个外显子,并与p53具有显著的序列和结构同源性。p63通常在皮肤、食管、扁桃体、尿路上皮、外子宫颈和阴道的复层上皮的基底细胞和祖细胞核中表达,以及胸腺、前列腺、乳房和支气管腺体结构的基底细胞中表达。
p63异构体分为两大组(TAp63和△Np63),p63抗体识别TAp63和△Np63,因此是广谱p63标记物。p40抗体针对△Np63,不识别TAp63。
在什么情况下应该使用p40,而不是p63?
使用最广泛的p63抗体克隆号是4A4,对鳞癌有极好的敏感性(94%~100%),但特异性较低,因为它在肺腺癌中的意外表达(16%~65%),也表达于其他恶性肿瘤,如大细胞淋巴瘤(高达一半),偶见于一些软组织肿瘤。虽然在非鳞状肿瘤中表达通常为弱到中度,但在少数病例中可以观察到强和弥漫性表达。
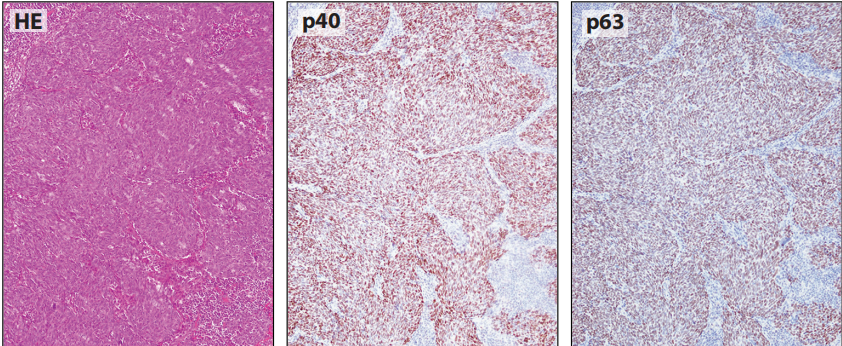 图8-1低分化鳞癌,p40和p63弥漫强性。
图8-1低分化鳞癌,p40和p63弥漫强性。
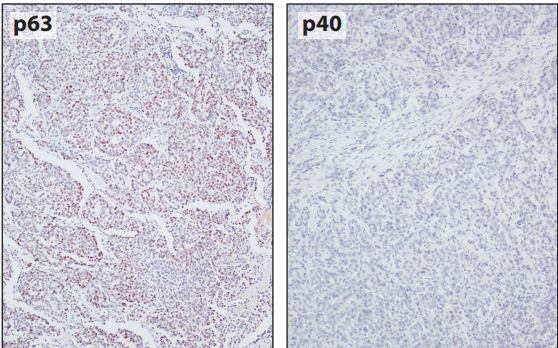
图8-2 p63对鳞癌没有特异性。低分化肺腺癌显示p63的表达相当弥漫性,而p40不表达。
一些研究已经表明,p40具有相当高的敏感性,与p63相似,但特异性更高,是鉴别鳞状细胞分化的可靠标志物(图8-1和8-2)。p40识别鳞癌优于p63。然而,应该记住,如果有鳞状分化的形态学证据(角化或细胞间桥),那么不需要IHC确认。在形态未分化的非小细胞肺癌小活检样本,要用鳞状标记和腺癌标记(如,p40和TTF1)努力区分亚型。如果在相同的肿瘤细胞中p63/p40和TTF1都有表达,且TTF1表达胜过p63/p40,则倾向腺癌。一项研究表明,TTF1和p63共表达常见于ALK阳性腺癌,但没有观察到TTF1和p40共表达。
答:p40应当用于鉴别形态学未分化鳞癌,其准确性优于p63。
在什么情况下应该使用p63来代替p40?
在某些情况下,NUT癌中p63和p40之间的表达不一致。p63弥漫表达,而p40只有很少细胞表达(图8-3)。这可能会导致在使用p40时的诊断陷阱,特别小活检。因此,鉴别诊断包括NUT癌的病例,除了形态学评估和其他IHC标记之外,p63可能比p40更有用(NUT癌详见第14章)。
答:如果在肿瘤的鉴别诊断中考虑了NUT癌,那么p63可能比p40更有用。
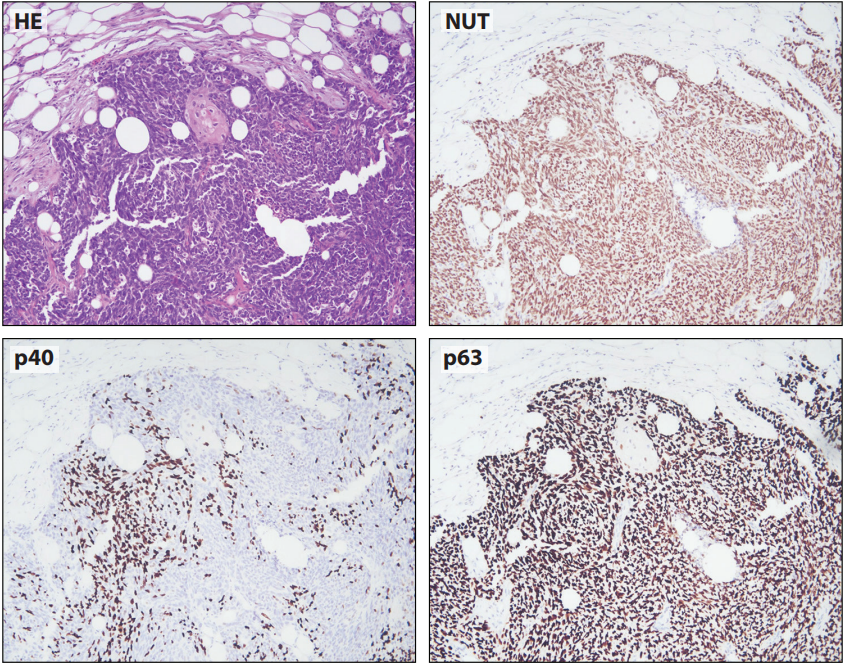 图8-3 NUT肺癌显示局灶性p40和弥漫性p63表达。
图8-3 NUT肺癌显示局灶性p40和弥漫性p63表达。
什么程度的p40/p63染色应该判读为阳性?
在鳞癌中,p40/p63通常有很强的弥漫性阳性(图8-1)。p40和p63阳性阈值应该超过的50%肿瘤细胞核,对鳞癌才有特异性。阳性细胞核小于10%,不应单独用于诊断分类,因为局灶性和弱阳性的p40/p63可见于腺癌和其他类型的肿瘤。10%~50%阳性是一个需要考虑的问题,并取决于临床背景和染色强度,以及形态学特征和其他IHC结果(图8-4)。其他具有鳞状细胞分化的IHC标记物,如CK5/6在有问题的情况下可能是有用的后备(见第9章)。值得注意的是,鳞癌的角化成分通常为p40阴性,因此,其阴性并不排除鳞癌的诊断。然而,考虑到角化是鳞癌的诊断标准,在这种情况下,不需要进行p40免疫染色。
答:鳞癌中常有弥漫强阳性p40(和p63)表达,至少50%的细胞核表达应该判读为阳性。
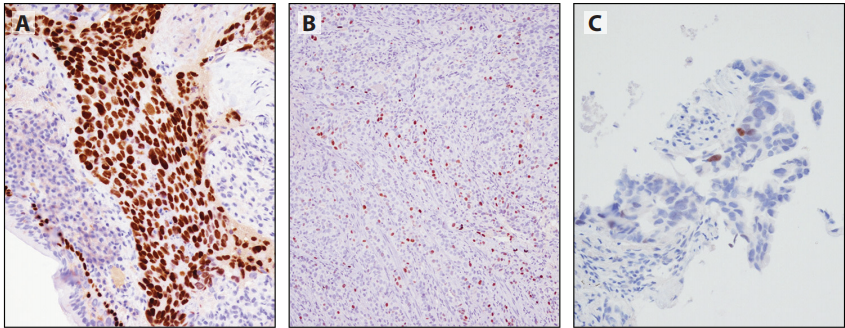 图8-4肺癌中p40表达的不同水平。A:鳞癌,强弥漫性p40染色。B:腺癌,约10%的细胞核呈斑片状染色。C:腺癌,只有非常局灶性的p40染色(<5%的细胞核)。
图8-4肺癌中p40表达的不同水平。A:鳞癌,强弥漫性p40染色。B:腺癌,约10%的细胞核呈斑片状染色。C:腺癌,只有非常局灶性的p40染色(<5%的细胞核)。
结论
在日常实践中,如果形态学特征不足,识别鳞癌或鳞状细胞分化时,p40优于p63(表8-1)。阳性阈值应该是超过50%肿瘤细胞核染色,而局灶性或弱阳性对鳞癌没有诊断价值。可疑病例,应加做其他鳞状标记物,如CK5/6。鳞癌与其他肿瘤类型的区别也应考虑形态学特征和其他IHC标记物(例如,在未分化非小细胞癌中的TTF1表达情况)。
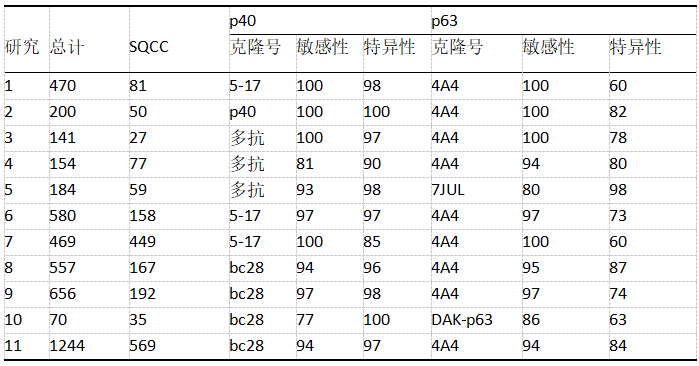
表8-1 p40与p63治疗鳞癌(SQCC)的对比研究
往期回顾:
国际肺癌研究协会免疫组化诊断图谱(IASLC ATLAS of DIAGNOSTIC IMMUNOHISTOCHEMISTRY 2020.9)
国际肺癌研究协会免疫组化诊断图谱——5小活检
国际肺癌研究协会免疫组化诊断图谱——6肺癌切除大标本
国际肺癌研究协会免疫组化诊断图谱——7甲状腺转录因子-1


















共0条评论