[导读] 编译整理:强子
小标本、大风险-部分乳腺病变粗针穿刺活检诊断要点(二)
小标本、大风险-部分乳腺病变粗针穿刺活检诊断要点(三)
小标本、大风险-部分乳腺病变粗针穿刺活检诊断要点(四)
小标本、大风险-部分乳腺病变粗针穿刺活检诊断要点(五)
小标本、大风险-部分乳腺病变粗针穿刺活检诊断要点(六)
随着人民健康意识的提高及影像学技术的进步,乳腺癌筛查已在世界范围内全面推广。这也推动了粗针穿刺活检等微创检查手段的广泛应用。不过,这种情况下病理医师遇到的标本都相对较小或破碎,可造成一定诊断困难。针对这类问题,美国墨菲特癌症中心(Moffitt Cancer Center)病理专家Rosa、Agosto-Arroyo在《Annals of Diagnostic Pathology》杂志就这一问题进行了专门讲述。为便于大家更好的了解相关问题,并指导临床实践,我们将该文要点编译介绍如下。
导管内增生性病变
导管内增生性病变其实包括了一组累及乳腺大导管及终末导管导管内成分的病变,具体可以有多种类型,涉及良性病变(普通型导管增生)、非典型病变(非典型导管增生)、直至导管原位癌。不过,不管增生程度如何,受累导管周围均有肌上皮。由于这类病变发生浸润性癌的风险不同,因此粗针穿刺活检中做出准确判定极为重要。
普通型导管增生
普通型导管增生可发生于任何年龄,患者确诊时年龄平均53岁,但青春期前者罕见。60岁以后者也罕见。临床一般无特殊表现,一般是因间质异常(如假血管瘤样间质增生、纤维囊性改变、放射性瘢痕、复杂性硬化性病变)而活检、在周围乳腺组织中偶见。
镜下表现不一,可自局灶增生、至多灶增生不等;上皮细胞分布不规则,细胞边界清晰,细胞核大小不一。细胞核常出现重叠,并可呈“流水样”,即细胞长轴相互平行。增生的程度不一,可自数层细胞、直至几乎填满管腔、使得管腔扩张的实性增生(旺炽性导管增生)均可出现。也可能出现次级管腔及微乳头状结构。可出现钙化、鳞化及泡沫样组织细胞,核分裂罕见。不过,出现管腔内坏死碎屑者罕见。周围乳腺可出现其他类型的增生性改变,如硬化性腺病、大汗腺化生、非典型小叶增生。
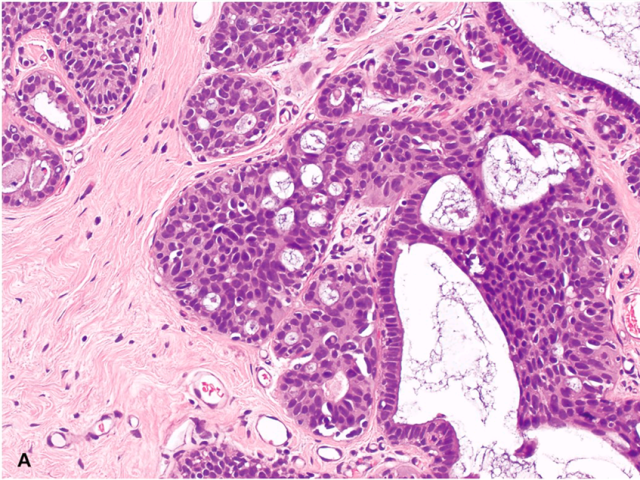
图1. 导管内增生,细胞呈流水样,排列无极性,局灶可见继发腔隙。该例应归为普通型导管增生。
非典型导管增生
非典型导管增生,是形态单一的上皮细胞在导管内均匀分布的增生,其组织学和细胞学特点类似低级别导管原位癌、但尚不足以诊断为后者。非典型导管增生是发生乳腺癌的危险因素,且与导管原位癌、浸润性癌具有相似的分子遗传学改变。非典型导管增生确诊时的年龄平均为58岁,稍大于普通型导管增生。影像学引导粗针穿刺活检标本中的检出率约为4-9%;随着筛查范围的加大、影像学技术的进展,影像学异常情况下活检中非典型导管增生的检出率越来越高:筛查检出的微钙化病变行粗针穿刺活检,约31%含有非典型导管增生。
如前所述,非典型导管增生的组织学和细胞学特点类似低级别导管原位癌、但尚不足以诊断为后者;因此对于导管内增生性病变来说,除非形态学提示需鉴别低级别导管原位癌,否则就不要诊断非典型导管增生。非典型细胞可局灶累及终末导管小叶单位,并混有无非典型的增生细胞。细胞分界清晰,细胞核中等程度增大、深染,有显著核仁。细胞并无普通型导管增生中的旋涡状、流水样及重叠表现。罕见核分裂。结构上可以出现实性、筛状、微乳头状,因此与低级别导管原位癌的鉴别主要是根据定量标准:形态学为低级别导管原位癌,但累及范围不足两个独立导管、或最大径<2mm,则诊断为非典型导管增生;相反,异型增生范围超出上述定量标准则诊断为低级别导管内癌。不过,粗针穿刺活检标本中常很难确定病变范围,因此这种情况可能应诊断为非典型导管增生、或备注非典型导管内增生性病变,并建议完整切除后全面评估。
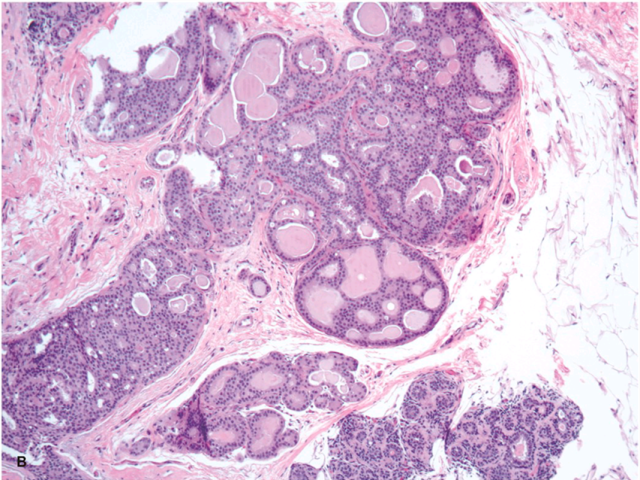
图2. 非典型导管增生,导管内增生的细胞形态单一,具有轻度异型性,局灶有筛状结构。
导管原位癌
导管原位癌具有高度异质性,明确是部分乳腺浸润性癌的前驱病变。近年来导管原位癌的发病率增加,很大原因是由于人群寿命增加、影像学诊断的进展。美国新确诊乳腺癌患者中,导管原位癌约占20-25%。确诊时的年龄平均50-59岁。随着影像学技术应用的增加,导管原位癌病例80-85%为影像学检出,一般为钼靶筛查;约10-15%为其他原因(如可触及异常)而粗针穿刺活检检出。
组织学上,导管原位癌的特点为恶性细胞在导管内增生、累及终末导管小叶单位的整个腔内并使之扩张。周围肌上皮层及基底膜完整,并籍此与浸润性癌鉴别。可根据细胞核的级别、有无坏死、结构特点来进一步分为三组。腺腔内可见分泌物、点状坏死及钙化。有无核分裂并非导管原位癌的必需特征,因为正常及增生的病变中也可见核分裂。
低级别导管原位癌的特点为形态单一的细胞增生,细胞排列均匀,细胞核大致呈圆形、位于中央,核仁不明显。具体标准详见前述。坏死不常见,但出现坏死、包括粉刺状坏死并不妨碍低级别导管原位癌的诊断。由于中间级别、高级别导管原位癌并无前述定量标准,因此根据结构特征和细胞学特征一般诊断相对容易。中间级别的导管原位癌细胞核已失去低级别导管原位癌中形态单一的特征,一般具有轻度至中等程度多形性。高级别导管原位癌细胞多形、分布不规则,细胞核一般大,细胞核大小差异较大(anisonucleosis),细胞核轮廓不规则,染色质粗糙,核仁显著。
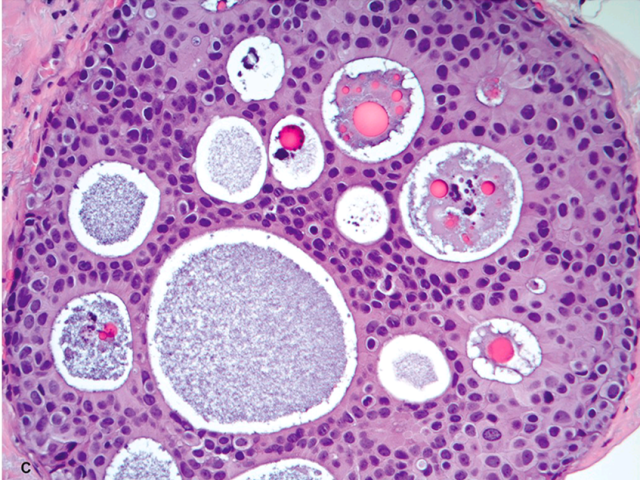
图3. 细胞核为中级别的导管原位癌,细胞核有中等程度多形性,呈筛状结构,围绕管腔的细胞排列有极性。
结构上,导管原位癌呈不同特征。实性型时,肿瘤细胞增生并部分或完全填满导管腔;筛状型时,肿瘤细胞周边出现微小腔隙;微乳头状时导管内衬上皮呈单层,形成叶状、拱形或罗马桥样。相关结构内并无纤维血管轴心,因此可与乳头状构型鉴别。其他少见亚型还有大汗腺型、印戒细胞型、透明细胞型、神经内分泌型、梭形细胞型。罕见情况下,同一终末导管小叶单位可混杂存在导管原位癌、小叶原位癌。
参考文献
Rosa M, Agosto-Arroyo E.Core needle biopsy of benign, borderline and in-situ problematic lesions of the breast: Diagnosis, differential diagnosis and immunohistochemistry[J].Annals of diagnostic pathology,2019,43:151407.
DOI:10.1016/j.anndiagpath.2019.151407
















共0条评论