[导读] 编译整理:强子
某些肾脏肿瘤的少见表现
这一部分所述肿瘤类型其实已经相对明确,此处仅探讨三种类型肿瘤的不常见临床表现,因为这些罕见情况可能会造成显著的诊断陷阱。
高级别及梭形细胞为主的黏液管状和梭形细胞癌
黏液管状及梭形细胞癌(mucinous tubular and spindle cell carcinomas,MTSCs)为上皮成分、并混有梭形细胞成分构成,前者为拉长管状,后者一般无细胞学非典型,且该肿瘤常为黏液样背景。鉴于该肿瘤有IRX5的过表达,因此目前认为其来源于髓袢(loop of Henle)。肾肿瘤诊断中常用的免疫组化对该肿瘤并无特异性,如CK7+、p504s+,因此无法据此鉴别乳头状肾细胞癌。
总之,当黏液管状及梭形细胞癌表现出变异形态学模式时,仅凭形态学和有限的免疫组化指标可能不足以明确该诊断,如与乳头状肾细胞癌存在显著重叠的上皮为主型、梭形细胞为主型。以及伴高级别或去分化特征时。这种情况下常需进行辅助分子检测以对肿瘤准确分类。虽然文献中也有特殊分子表现的报道,但常规临床实践中的应用率高低不一,低级别肿瘤仍常仅凭形态学标准进行诊断。关于该肿瘤分子特征的综合研究发现其存在肿瘤抑制因子(如PTPN14、SAV1)的失活、Hippo信号通路中NF2的失活,具体可见于不到1/3的病例。针对这类基因变异的测序检测尚未在临床实践中得到广泛应用,且随访研究发现,作为Hippo信号通路失活标记的免疫组化YAP1也并无特异性;VSTM2A的原位杂交则相对敏感和特异。目前更普遍的检测方法是对染色体水平拷贝数变异的分析。
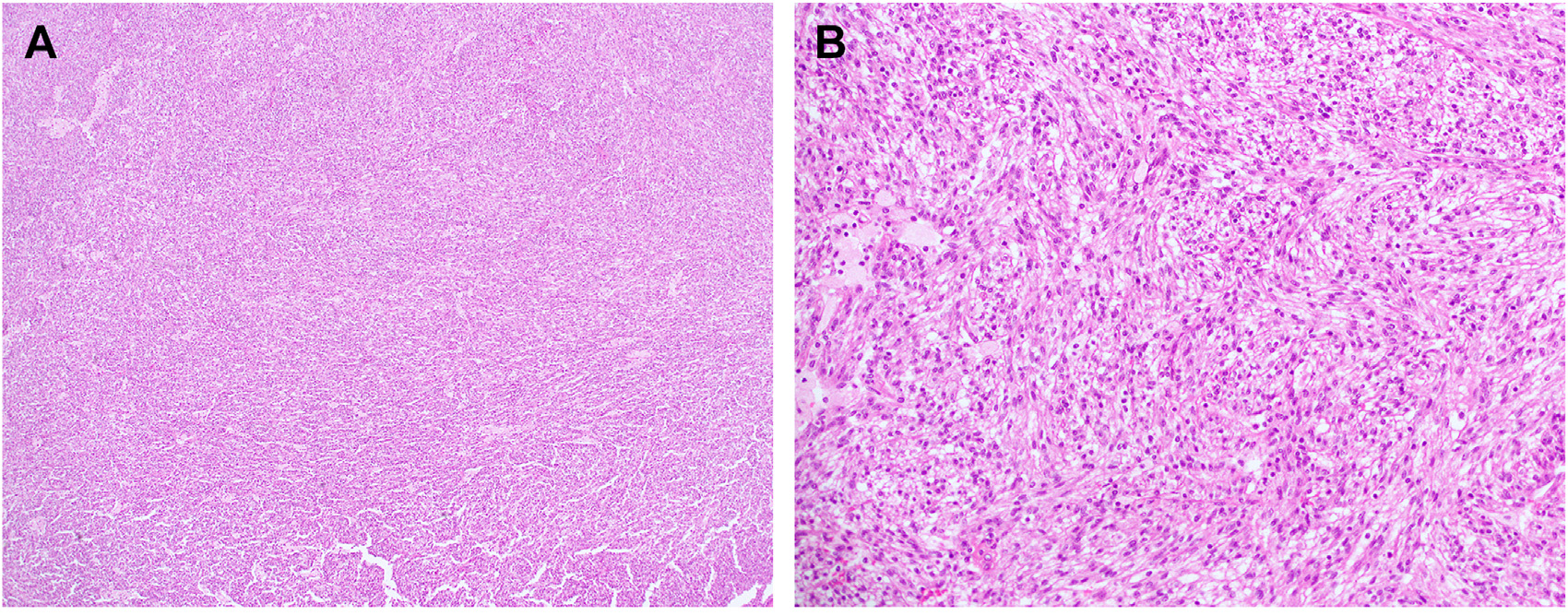 图9.梭形细胞为主的黏液管状及梭形细胞癌。
图9.梭形细胞为主的黏液管状及梭形细胞癌。
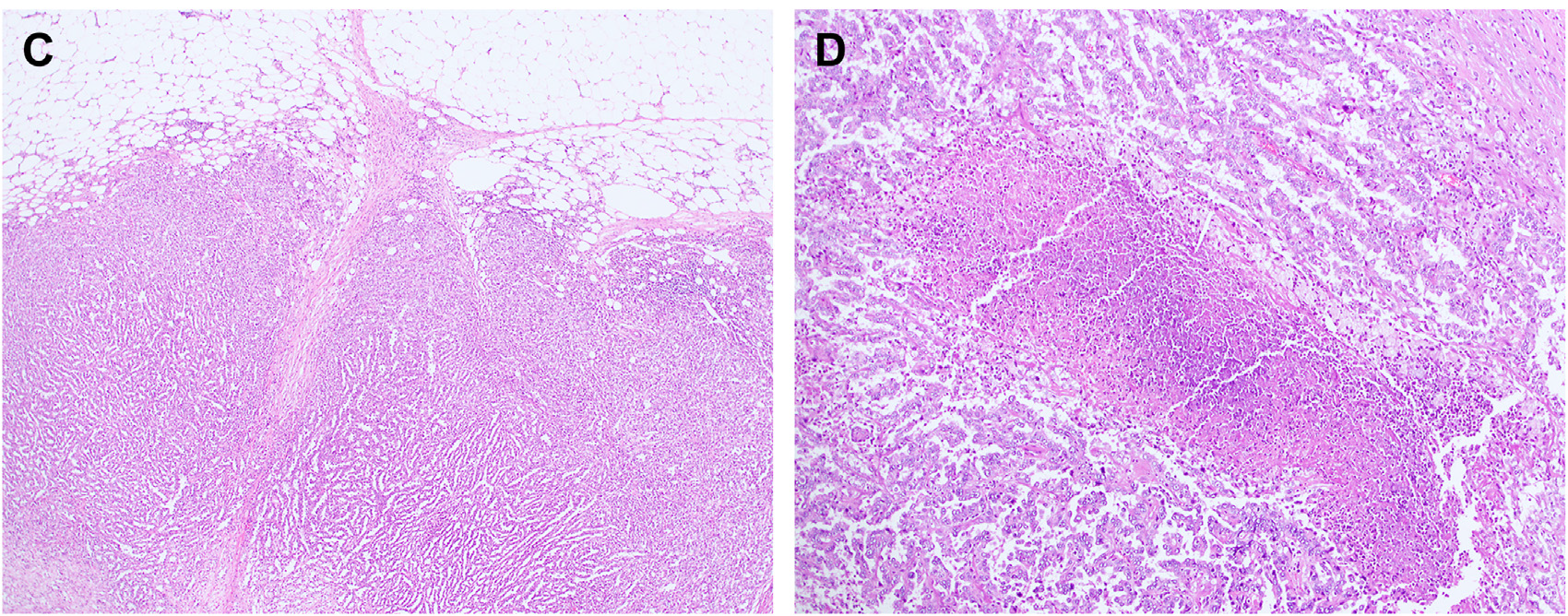 图10.高级别黏液管状及梭形细胞癌,伴肾周脂肪浸润,可见乳头状结构及坏死。
图10.高级别黏液管状及梭形细胞癌,伴肾周脂肪浸润,可见乳头状结构及坏死。
关于黏液管状及梭形细胞癌和乳头状肾细胞癌形态学重叠时辅助检测的研究文献较多,但高级别转化情况下的研究较少,尤其分期高/转移性肿瘤时。低级别肿瘤的特征性拷贝数改变有1、4、6、8、9、13、14、15、22号染色体的缺失,而高级别肿瘤则有报道称存在其他拷贝数改变,如CDKN2A/B的杂合性缺失、1q的获得、3/3p和21号染色体的缺失。
梭形细胞为主的黏液管状及梭形细胞癌中只有少数(<5%)上皮成分时,可以解释为取材所致;此时根据免疫组化PAX8和CK的阳性,可以很容易的鉴别血管平滑肌脂肪瘤、平滑肌瘤。此外,肉瘤样肾细胞癌的排除则是根据无细胞学非典型和坏死。相反,与存在显著形态学重叠的乳头状肾细胞癌鉴别,则难度较大。伴高级别转化的肿瘤常误判为乳头状肾细胞癌、或非特殊类型的肾细胞癌,即使某些病例中加做了分子检测也是如此,因为所用分子检测方案中可能并不包括染色体拷贝数分析。因此,在做出高分期/高级别的非特殊类型肾细胞癌诊断前,建议进行恰当的分子检测以排除黏液管状及梭形细胞癌。
“低级别”的FH缺陷型肾细胞癌(类似SDH缺陷型肾细胞癌表型)
延胡索酸水合酶(fumarate hydratase,FH)缺陷型肾细胞癌可见于散发型、也可见于FH基因致病性改变所致的FH肿瘤易感综合征/遗传性平滑肌瘤病和肾细胞癌(hereditary leiomyomatosis and renal cell carcinoma,HLRCC)情况下。当代临床实践中,必须准确识别出这类肿瘤,这不仅是因其预后不良,更因为它可能与遗传性平滑肌瘤病和肾细胞癌综合征存在关联,确诊后者将推动对受累家族成员进行胚系基因检测,并纳入旨在早期发现肾肿瘤的筛查计划。
基于免疫组化的有效筛查方案推广应用,已使病理医生能够越来越多地识别出FH缺陷型肾细胞癌,即常见FH不表达、且有S-(2-琥珀酰)-半胱氨酸(S-(2-succino)-cysteine,2SC)的异常过表达;罕见情况下FH仍有表达(可能功能异常)、且2SC异常过表达。这些基于免疫组化的检测使得我们能够识别出FH缺陷型肾细胞癌的多种形态学模式,常见结构模式如乳头状、管状囊性(伴较高级别/去分化区域)、筛状等,且有显著的大核仁。
文献中已有该组肿瘤的罕见形态报道,比如无上述特征性表现,此时则可能给鉴别诊断带来重要陷阱。具体来说,部分FH缺陷型肾细胞癌的形态学特征会类似琥珀酸脱氢酶(succinate dehydrogenase,SDH)缺陷型肾细胞癌,即结构呈巢状,细胞的胞质嗜酸性、空泡状,核仁相对不明显。文献中报道的病例SDHB仍有表达,免疫组化和/或分子特点符合FH缺陷型肾细胞癌。
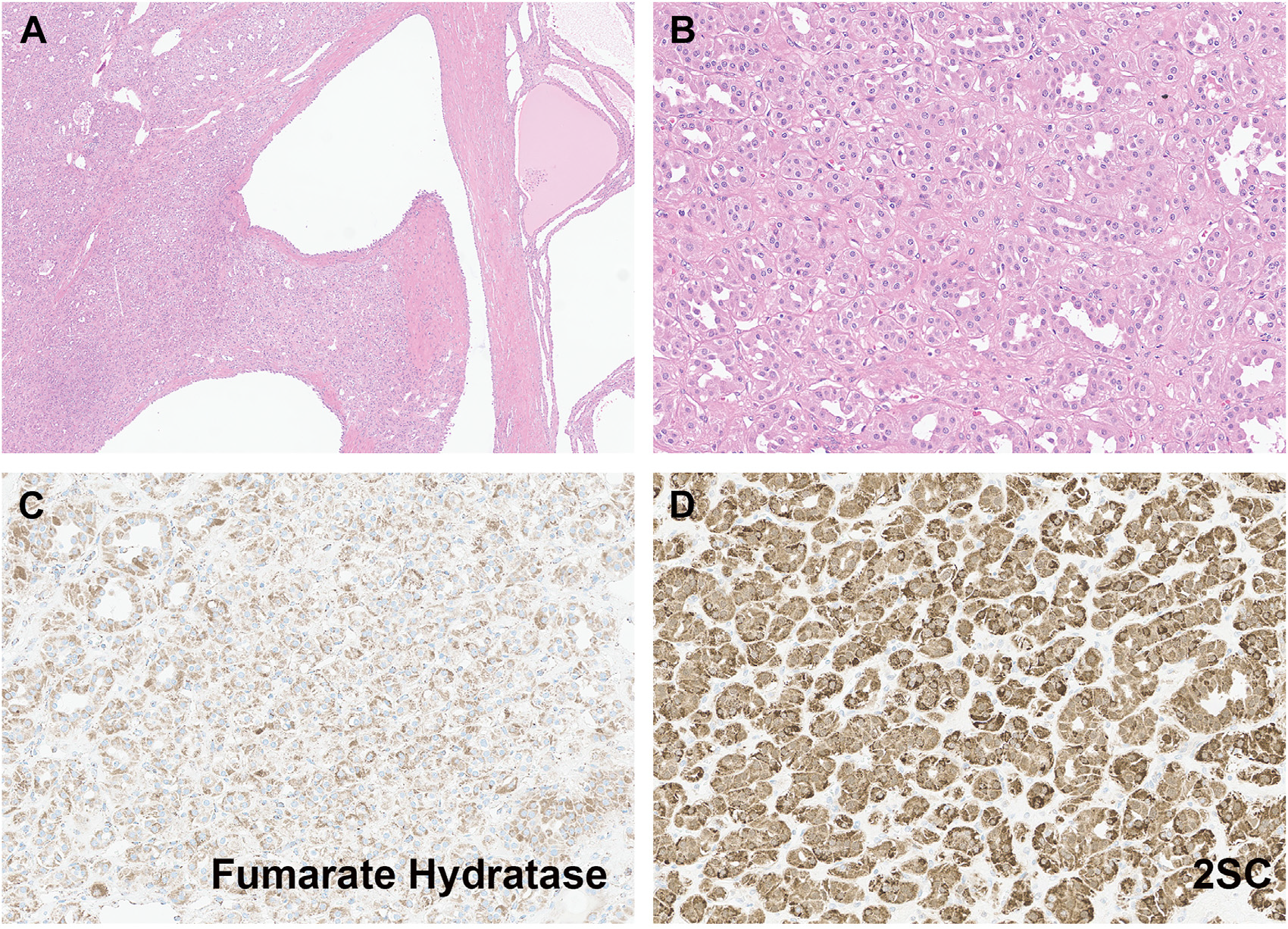 图11.低级别FH缺陷型肾细胞癌形态学表现,可见管状囊性区域;免疫组化该肿瘤仍有FH的表达(C),但2SC有异常过表达(D)。本例经二代测序证实有FH基因的致病性改变。
图11.低级别FH缺陷型肾细胞癌形态学表现,可见管状囊性区域;免疫组化该肿瘤仍有FH的表达(C),但2SC有异常过表达(D)。本例经二代测序证实有FH基因的致病性改变。
目前来说,具有上述形态特征的病例在英文文献中仅有少数报道,且如何对其准确命名仍有争议。很多研究形容这类肿瘤为“低级别”嗜酸性FH缺陷型肾细胞癌,因为这类肿瘤无高级别成分时并无不良预后。不过,也有人认为肿瘤分级应体现其生物学潜能而非仅依据形态学特征;鉴于至少有一例“低级别”嗜酸细胞型FH缺陷型肾细胞癌患者出现转移并死于该疾病,且该类肿瘤可与具有转移行为的非“低级别”FH缺陷型肾细胞癌成分同时或异时发生,加之当前报道病例数有限且临床随访资料不足,所以采用前述“低级别”的命名方案可能为时过早。总之,尚需更多具有充分临床随访的研究以明确“低级别”嗜酸细胞型FH缺陷型肾细胞癌患者的自然病程。此外,未来的诊疗指南在确定此类肿瘤的恰当命名时,应当充分纳入这些临床数据。
囊性TFE3重排肾细胞癌
TFE3重排的肾脏肿瘤包括PAX8阳性肾细胞癌和PAX8阴性的“TFE3重排PEComa样肿瘤”。虽然TFE3重排肾细胞癌的形态学谱系宽泛,但还是有些共同之处的,比如乳头状结构、肿瘤细胞的胞质丰富且相对透明、砂砾体样钙化。
目前已报道了大量TFE3重排时的配体基因,且有研究提出,根据TFE3融合的配体不同,存在特异的基因型-表型相关性和预后相关性。就基因型-表型相关性来说,文献中报道过NONO::TFE3重排的肾细胞癌多表现为存在“核下空泡”从而导致细胞核“在基底膜上方形成栅栏状”。
最近还报道了TFE3重排肾细胞癌的一种少见形态学表现,即存在囊性特征、且形态学与低度恶性潜能多房囊性肾肿瘤(multilocular cystic renal neoplasm of low malignant potential,MCN-LMP)存在重叠。需要注意的是,文献中报道的MED15::TFE3重排肾细胞癌病例几乎都存在有分隔的囊性成分,衬覆细胞胞质透明、核仁不明显,且散在砂砾体样钙化灶。虽然这些肿瘤都与低度恶性潜能多房囊性肾肿瘤存在形态学的重叠,但却有特征性免疫组化特点,比如CA9细胞膜阳性、程度不等的表达TFE3/Melan A/cathepsin K。
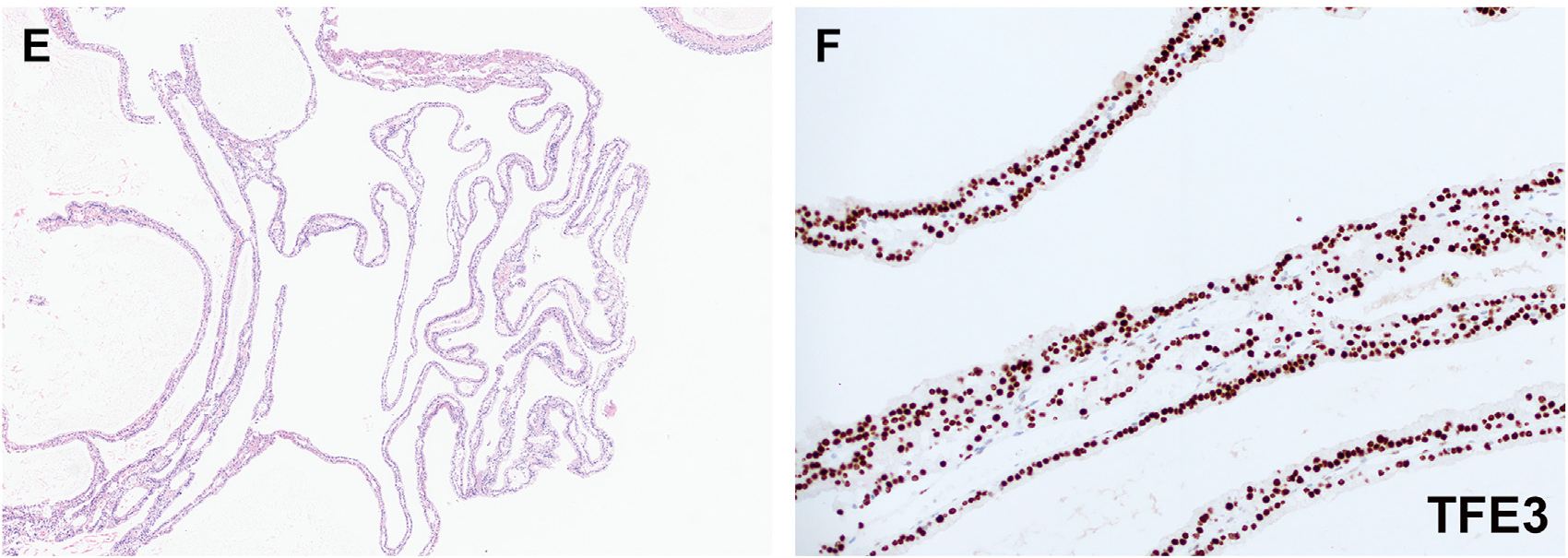 图12.与低度恶性潜能多房囊性肾肿瘤存在显著形态学重叠的TFE3重排肾细胞癌;本例经二代测序证实有TFE3基因重排。
图12.与低度恶性潜能多房囊性肾肿瘤存在显著形态学重叠的TFE3重排肾细胞癌;本例经二代测序证实有TFE3基因重排。
目前为止,文献中报道的MED15::TFE3重排肾细胞癌患者大部分预后很好,仅有1例患者在15年后出现了肺转移。鉴于存在转移的罕见情况,因此对具有低度恶性潜能多房囊性肾肿瘤形态学特征的肿瘤要进行恰当的免疫组化评估,且相应指标至少应包含CA9,以避免这一重大的诊断陷阱。
全文完
往期回顾:
其他罕见亚型肾细胞癌及少见临床表现(一)
其他罕见亚型肾细胞癌及少见临床表现(二)
其他罕见亚型肾细胞癌及少见临床表现(三)

















共0条评论