[导读] 编译整理:强子
鼻腔鼻窦未分化癌
鼻腔鼻窦未分化癌是一种少见且有侵袭性的上皮性恶性肿瘤,在所有鼻腔鼻窦癌中占比约为3%至5%。由于该肿瘤生长迅速,且容易累及眶周组织和中枢神经系统,因此确诊时一般为局部进展期。患者年龄分布宽泛,20-80岁均有报道,平均年龄58岁,男性多见。临床表现为鼻塞、鼻出血、眼球突出、脑神经麻痹、视力障碍、头痛及面部疼痛;症状持续时间较短,数周至数月不等。
世界卫生组织头颈部肿瘤分类中,对鼻腔鼻窦未分化癌的定义是无可辨识分化方向(如鳞状、腺样、神经内分泌分化)的恶性上皮性肿瘤,且属于排除性诊断。鼻腔鼻窦未分化癌常被视为表达CK但未分化、且无法分类病变的“垃圾筐”诊断。近些年已明确,此前被认为是鼻腔鼻窦未分化癌的肿瘤实际是包括了多种以遗传学特征为定义的异质性病种,后者具体如NUT癌、SWI/SNF复合体缺陷型癌,这些都排除了之后才能诊断“真正的鼻腔鼻窦未分化癌”。
此前对真正的鼻腔鼻窦未分化癌分子机制一直没有什么了解,直至2017年才有两位研究者独立发现了IDH1/2突变,这会改变三羧酸循环中异柠檬酸脱氢酶的酶结构、从而引发干扰DNA修复的级联反应、最终导致癌性增生。这类突变大部分局限于三个热点区,即IDH2 R172x、IDH2 R140x、IDH1 R132x。有多项报道称这类突变可见于约50-80%的鼻腔鼻窦未分化癌。
鼻腔鼻窦未分化癌一般较大(>4cm),侵及骨组织。组织学上,具体为膨胀性的片状、巢状、分叶状、宽大梁状,细胞为未分化的原始表现细胞,胞质嗜酸性,较少或中等量,并无合体样特征。细胞核圆形至卵圆形,染色质空泡状至深染,伴显著核仁。核分裂、坏死、血管/神经侵犯等容易查见。尽管有高级别特征,但瘤细胞并无多形性,细胞核一般为圆形,大小相当规则。文献中也有在被覆上皮出现Paget样浸润的报道。组织学上无鳞状、腺样、神经内分泌分化的特征。IDH1/2突变的鼻腔鼻窦未分化癌组织学特征与野生型者并无区别。
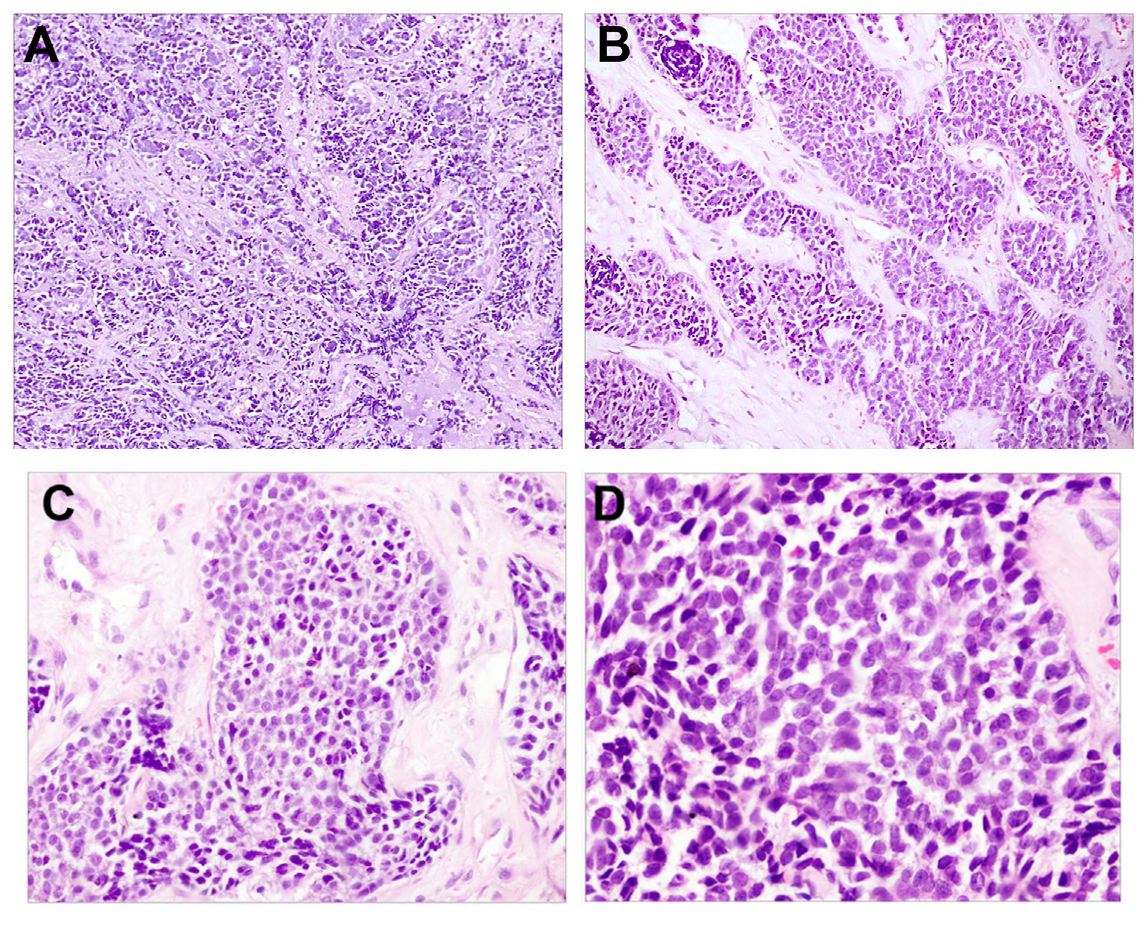 图16.鼻腔鼻窦未分化癌,图示片状(A)、巢状、梁状(B),细胞为原始表现,胞质稀少至中等量,肾上腺(C),细胞核圆形至卵圆形,形态相对单一(D)。
图16.鼻腔鼻窦未分化癌,图示片状(A)、巢状、梁状(B),细胞为原始表现,胞质稀少至中等量,肾上腺(C),细胞核圆形至卵圆形,形态相对单一(D)。
免疫组化方面,鼻腔鼻窦未分化癌的瘤细胞表达CKpan和EMA,也可能会表达CK7。鳞状上皮标记和神经内分泌标记一般为阴性,但可有p63和Syn的散在阳性。NUT阴性,SMARCB1/INI1和SMARCA4(BRG1)有表达,p16可为阳性,但与HPV无关。IDH1/2突变特异性抗体可用于IDH1/2突变型肿瘤的检测,具体为中至强阳性的颗粒状胞质着色,但敏感性和特异性不一,且不能确定出所有描述过的亚型,因此限制了其诊断中的应用。虽然目前并未推荐IDH突变检测用于诊断、预后判断和治疗方案的确定,但一旦正在进行的IDH1抑制剂临床实验得出结论、未来相关药物的应用可能需要这么做。具体可通过测序、靶向二代测序、定量PCR等方法进行检测。
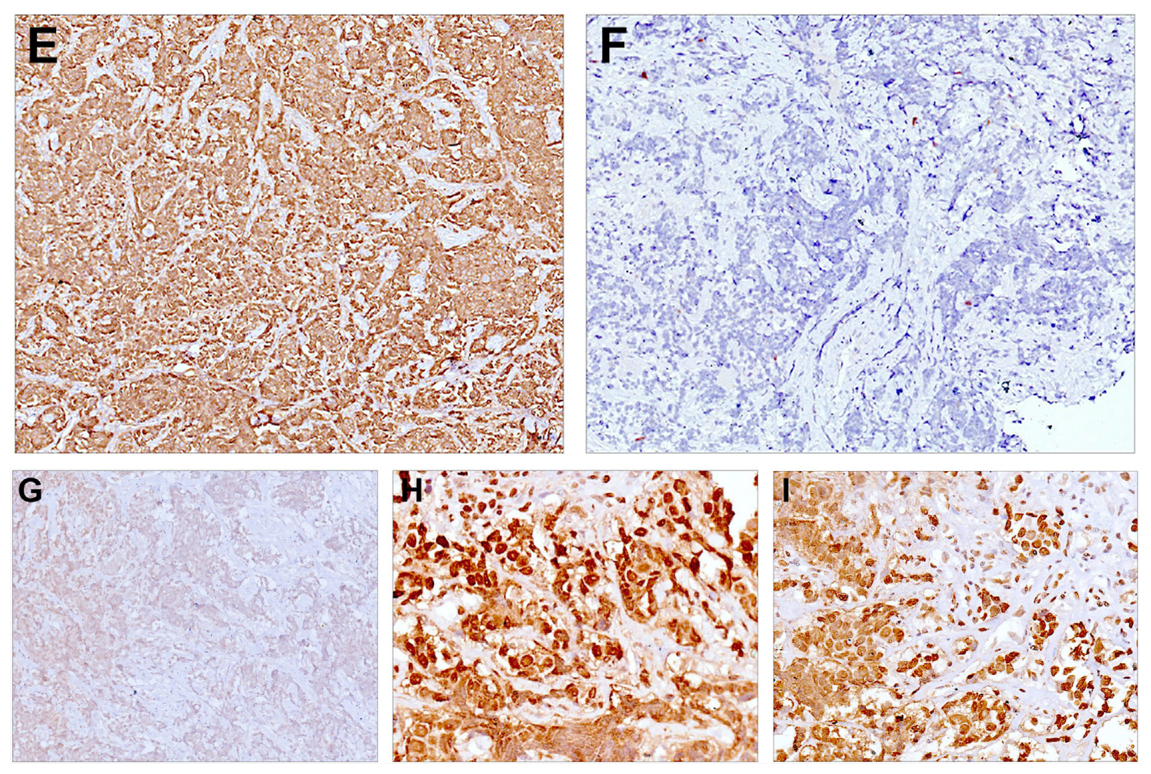 图17.鼻腔鼻窦未分化癌免疫组化。(左上)CK弥漫阳性,(右上)p40阴性,(左下)Syn非特异性弱阳性;INI1(中下)和BRG1(右下)仍有表达。
图17.鼻腔鼻窦未分化癌免疫组化。(左上)CK弥漫阳性,(右上)p40阴性,(左下)Syn非特异性弱阳性;INI1(中下)和BRG1(右下)仍有表达。
鼻腔鼻窦未分化癌总是预后较差。SEER数据分析表明,总时长时间的中位数为22.1个月,3年、5年、10年的生存率分别为44%、35%、31%。手术及放疗的多学科治疗已证实可以改善预后。多学科治疗后的死亡可能是因为局部复发、远处转移、持续的局部病变。IDH1/2突变型鼻腔鼻窦未分化癌的疾病特异性生存较好,但还需更多证据才能将其单独区分为分子定义病种。
需要指出的是,有些低分化肿瘤并无特定谱系分化、仅因为CK阳性就被归为了鼻腔鼻窦未分化癌,这一方面模糊了这一独立病种的特性,也引发了相关争论:鼻腔鼻窦未分化癌到底是一组基因异质性病变的总和,还是的确为独立病种。有研究提出,鼻腔鼻窦未分化癌似乎具有独特临床病理特征,且遗传学一般为IDH突变所致。不过,目前还不确定这一概念是否会被下一版的世界卫生组织分类方案所采纳,可能需要对IDH野生型鼻腔鼻窦未分化癌进行更精准的特征界定之后才能实现相关病种的独立分类。
鼻腔鼻窦淋巴上皮样癌
鼻腔鼻窦淋巴上皮样癌在组织学上类似未分化的鼻咽癌,只是后者局限于鼻咽部而已。具体来说,鼻腔鼻窦淋巴上皮样癌表现为分叶状、巢状、合体状的体积较大肿瘤细胞,伴致密的淋巴细胞和浆细胞浸润。瘤细胞多边形,胞质中等量、分界不清,细胞核增大、空泡状,伴显著核仁。核分裂多见。浸润的淋巴细胞可非常致密,以至于掩盖肿瘤性的上皮细胞从而类似淋巴瘤。不过,免疫组化CKpan、CK5/6、p63、p40可以显示出肿瘤细胞。其中的淋巴细胞为B细胞和T细胞混杂。该肿瘤与EB病毒感染相关,可以通过EB病毒编码的RNA原位杂交而确定。
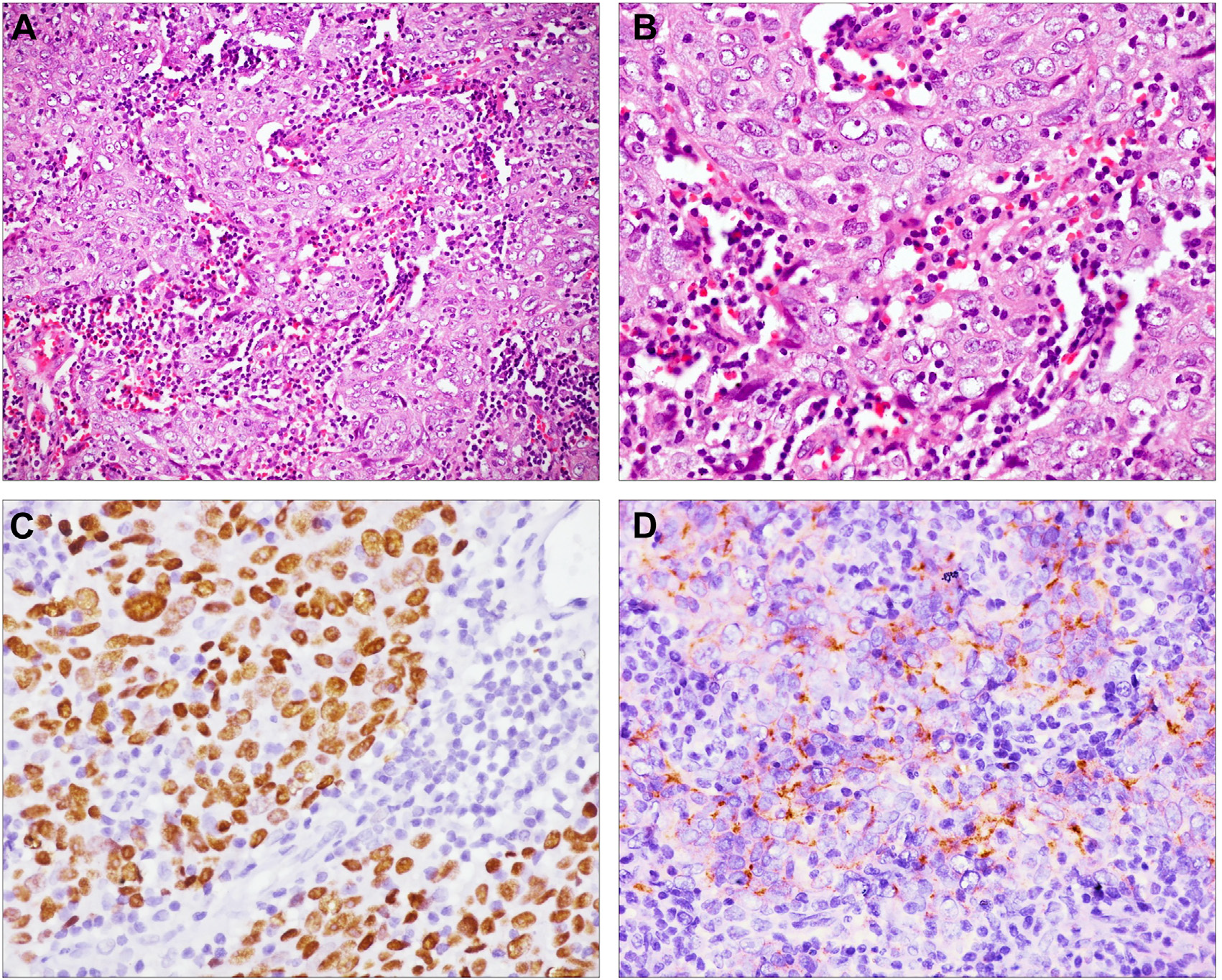 图18.淋巴上皮样癌,具体为体积大的肿瘤细胞呈合体状结构,间质内伴淋巴浆细胞浸润(A);瘤细胞胞质中等量,细胞核增大、空泡状,伴显著核仁(B)。免疫组化检测,瘤细胞阳性表达p40(C),EV病毒潜伏膜蛋白-1(EBV-LMP1)阳性(D)。
图18.淋巴上皮样癌,具体为体积大的肿瘤细胞呈合体状结构,间质内伴淋巴浆细胞浸润(A);瘤细胞胞质中等量,细胞核增大、空泡状,伴显著核仁(B)。免疫组化检测,瘤细胞阳性表达p40(C),EV病毒潜伏膜蛋白-1(EBV-LMP1)阳性(D)。
鼻腔鼻窦处淋巴上皮癌的淋巴结转移几率(15%)似乎低于鼻咽癌,且远处转移的情况也极为罕见。关于该肿瘤生存方面的数据极少,有研究称中位时间48个月的随访中,2例死亡,但8例无病健在。
实性型腺样囊性癌
腺样囊性癌也多见于鼻腔鼻窦区域,由于存在典型的筛状及管状结构,因此一般容易识别出来。不过,实性型腺样囊性癌为片状的基底样细胞、且核分裂增加、常见坏死,因此类似鼻腔鼻窦未分化/低分化癌的表现。关键的鉴别点在于实性型腺样囊性癌中极为致密的巢状结构会形成类似“炮弹”样表现,且至少会局灶存在真正的筛状生长。
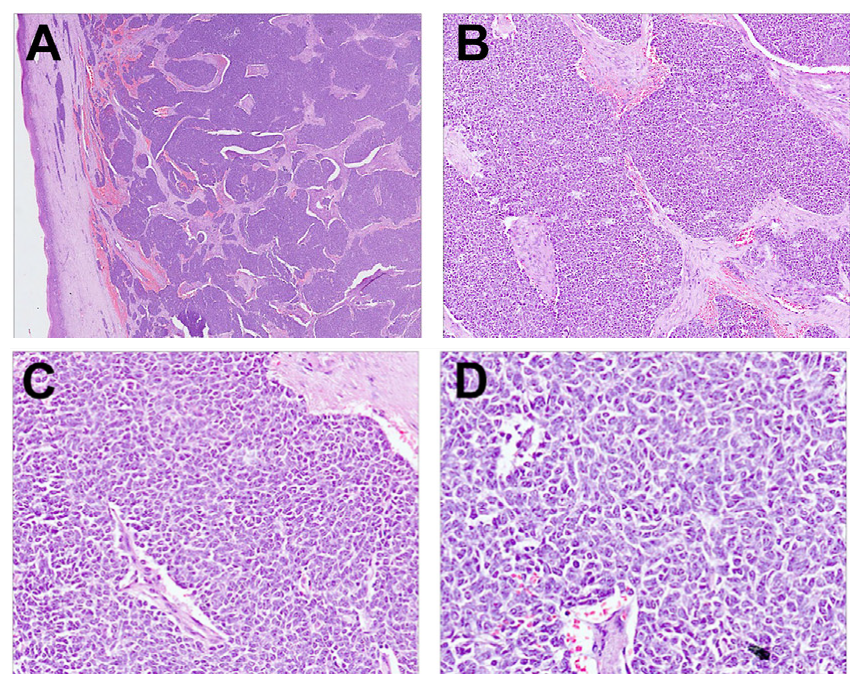 图19.本例腺样囊性癌,位于上皮下,具体为实性岛状、片状、梁状结构,瘤细胞基底样,胞质稀少,细胞核深染、成角。
图19.本例腺样囊性癌,位于上皮下,具体为实性岛状、片状、梁状结构,瘤细胞基底样,胞质稀少,细胞核深染、成角。
免疫组化可以很容易的区分出腺样囊性癌,因为其细胞为双相型,也就是管腔细胞表达CK7、CEA、EMA和CD117,而周围细胞表达p63/p40、S100、SOX10、SMA。MYB免疫组化及分子检测MYB/MYBL1重排可证实诊断。
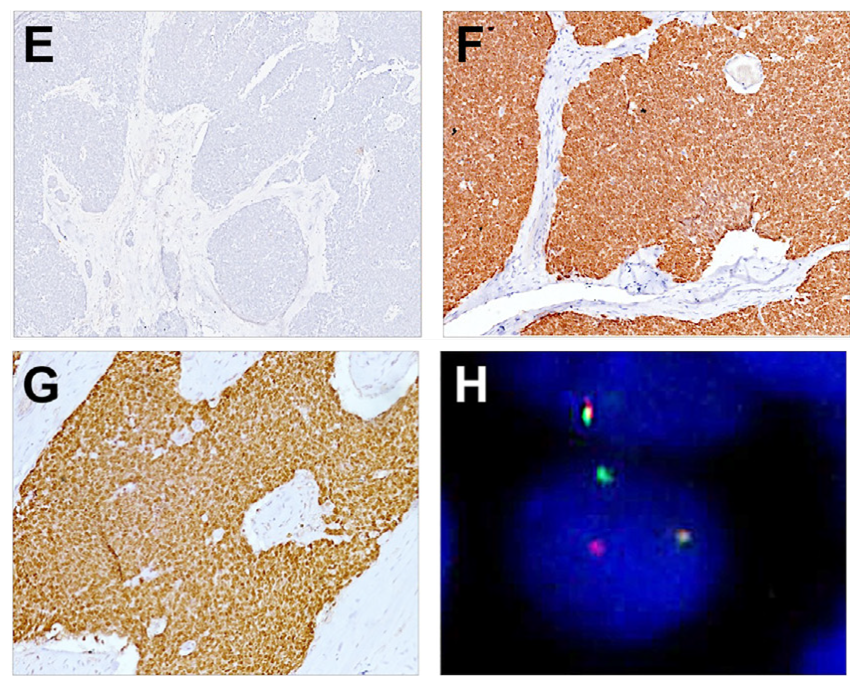 图20.腺样囊性癌免疫组化:瘤细胞p40阴性(左上),但SOX10(右上)和MYB(左下)弥漫阳性。此外,MYB断裂探针FISH检测可见分离信号,提示MYB重排,符合腺样囊性癌(右下)。
图20.腺样囊性癌免疫组化:瘤细胞p40阴性(左上),但SOX10(右上)和MYB(左下)弥漫阳性。此外,MYB断裂探针FISH检测可见分离信号,提示MYB重排,符合腺样囊性癌(右下)。
——未完待续——
往期回顾:
小部位,大问题-鼻腔鼻窦处病理集中学--鼻腔鼻窦处未分化及低分化癌(一)
小部位,大问题-鼻腔鼻窦处病理集中学--鼻腔鼻窦处未分化及低分化癌(二)
小部位,大问题-鼻腔鼻窦处病理集中学--鼻腔鼻窦处未分化及低分化癌(三)


















共0条评论