[导读] 编译整理:强子
施万细胞瘤
施万细胞瘤为源于外周神经鞘中施万细胞的良性肿瘤。高达45%的施万细胞瘤发生于头颈部。该肿瘤一般起源于脑神经或自主神经的分支,但鼻腔鼻窦处神经鞘瘤是较为罕见的亚型。施万细胞瘤可见于任何年龄,一般为散发性;罕见情况下可发生于遗传易感综合征,如神经纤维瘤病1型、神经纤维瘤病2型、施万细胞瘤病、Carney综合征。其发生机制与NF2基因产物肿瘤抑制因子merlin缺失有关。
MRI中,施万细胞瘤境界清楚,T1加权相有增强。大体检查境界清楚,圆形至纺锤形,质实。切面淡褐色,质地不均,局部有黄色及出血区域。偶可见肿瘤自起源神经延伸的迹象。
组织学上,施万细胞瘤为伴双相型表现的梭形细胞病变。部分区域富于细胞、细胞核呈栅栏状,形成Verocay小体,又称为Antoni A区。Antoni A区的细胞呈梭形,胞质中等量,嗜酸性,细胞分界不清,细胞核拉长。Antoni B区为细胞稀疏、形态温和区域,背景为疏松蜂窝状,伴大量吞噬脂质的组织细胞。有些区域可能存在显著非典型,但无核仁、和/或核分裂,因此称为老化改变/退行性变。常见厚壁的玻璃样变血管,部分区域有血栓,血管壁可有纤维素样坏死而导致部分病例呈梗死样坏死。也常见表现为含铁血黄素沉着、含铁血黄素颗粒的陈旧性出血及被膜下或病变周围淋巴细胞浸润。细胞性施万细胞瘤为主要由Antoni A区构成、但无Verocay小体成分的亚型。部分病例中的细胞可有核深染、核分裂、坏死等,从而使人担心是否为恶性外周神经鞘肿瘤。免疫组化广泛表达S100/SOX10及IV型胶原(意味着施万细胞周围大量基底膜),H3K27Me3完整表达,加之相应组织学特征(如细胞性施万细胞瘤的被膜下有淋巴细胞浸润),有助于明确为细胞性施万细胞瘤的诊断。偶见神经鞘瘤作为混合性神经鞘肿瘤的组成部分出现,这种病例是指组织学特征具有一种以上良性神经鞘来源肿瘤的情况,最常见为神经鞘瘤/神经束膜瘤的组合或神经纤维瘤/神经鞘瘤的组合,尤其与遗传综合征相关时更是如此。
该肿瘤的诊断是基于组织形态学特征。免疫组化方面,瘤细胞弥漫阳性表达S100、SOX10、IV型胶原。GFAP和EMA一般为阴性。综合征相关的施万细胞瘤中可能会有INI1的局灶表达缺失。对于无明确病史但表现为多发性神经鞘肿瘤的患者,应充分重视这一相关性。施万细胞瘤与神经纤维瘤的鉴别在于后者有CD34阳性间质细胞。NF可用于评估陷入的轴突:神经纤维瘤中一般有大量轴突,而施万细胞瘤中轴突仅局限于周边区域,这是因为施万细胞瘤膨胀性生长所致。
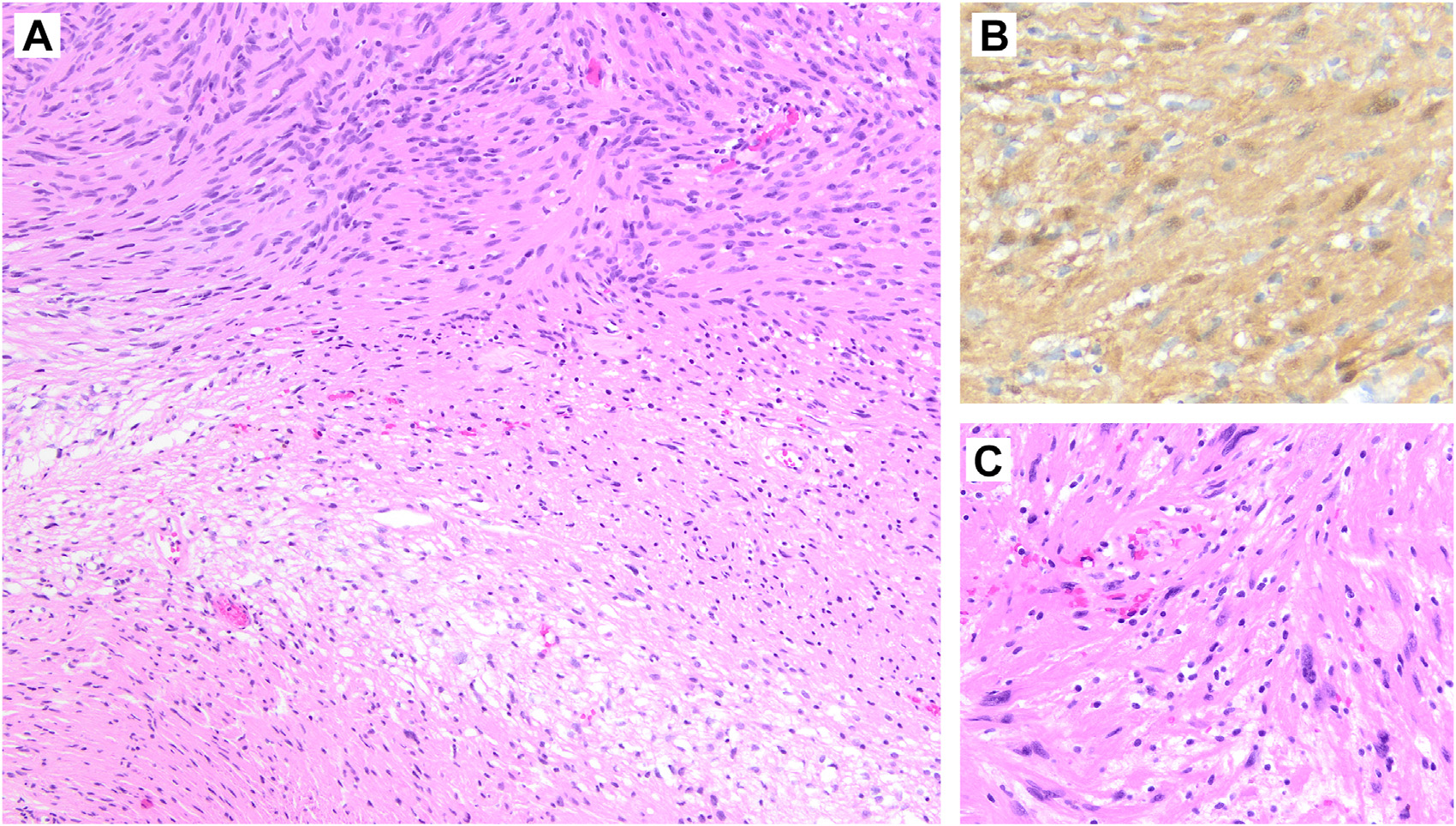 图7.施万细胞瘤,形态学可见Antoni A区和Antoni B区的双相型结构,免疫组化S100强阳性(B);局灶可见细胞核有退行性变所致的非典型/老化改变(C)。
图7.施万细胞瘤,形态学可见Antoni A区和Antoni B区的双相型结构,免疫组化S100强阳性(B);局灶可见细胞核有退行性变所致的非典型/老化改变(C)。
施万细胞瘤为良性肿瘤,WHO分级为1级,预后极好。一般手术切除可治愈。
脑膜瘤
脑膜瘤一般是位于硬脑膜的肿瘤,也是中枢神经系统最常见的原发肿瘤,人群发生率高达1%。颅底的颅内肿瘤也可通过直接侵犯、或罕见情况下转移而累及头颈部结构。颅内脑膜瘤侵犯颅外时,最常见受累部位是眼眶。罕见情况下,头颈部可以发生颅外原发脑膜瘤,文献中曾报道于耳部、鼻腔、鼻旁窦、下颌骨、腮腺、喉部、皮肤。推测这类肿瘤来源于发育过程中中线融合时陷入的脑膜细胞、或颅神经覆盖时被包裹的脑膜细胞、或源于其他未分化间叶细胞的化生。脑膜瘤的发生风险随着年龄增加而增加,且女性多见。临床表现取决于肿瘤大小及所在部位,但常见症状有头痛、视觉改变、乏力、癫痫发作。
MRI中,脑膜瘤一般表现为硬膜内、轴外占位性病变,且在T1加权像上呈现均匀的显著强化。可能会有硬膜尾征,尤其位于硬脑膜的肿瘤。大体检查,肿瘤界清,质实,白色,结节状至漩涡状。伴砂粒体(板层状营养不良性钙化)或不规则营养不良性钙化的肿瘤可呈砂砾样。相邻骨结构常见反应性骨肥厚(hyperostosis,指骨皮质增厚伴髓腔狭窄的形态学改变)。
组织学上,脑膜瘤一般为形态温和、胞质合体样细胞构成,结构呈漩涡状;但也有多种不同亚型会有独特表现。可以说脑膜瘤可能是人体内组织学形态最多样的肿瘤之一。瘤细胞的细胞核圆形至卵圆形,常见核内假包涵体、核透明、核沟、胞质内假包涵体。砂粒体型钙化表现不一,但如果有的话,是一个有助于诊断的特征。
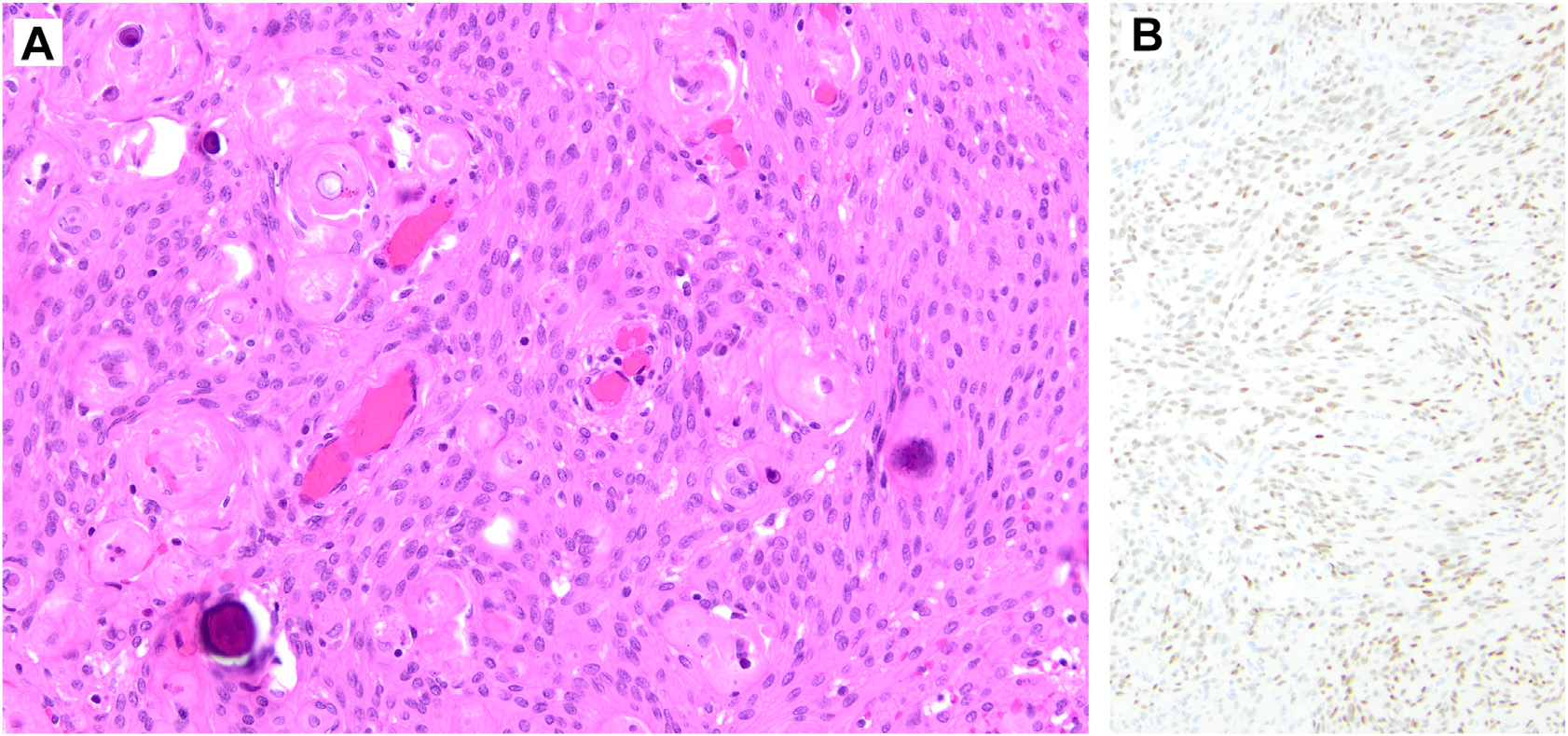 图8.脑膜瘤,形态学为合体样细胞、呈漩涡状结构,有核内假包涵体、核透亮、核沟、砂粒体;免疫组化,该肿瘤阳性表达PR。
图8.脑膜瘤,形态学为合体样细胞、呈漩涡状结构,有核内假包涵体、核透亮、核沟、砂粒体;免疫组化,该肿瘤阳性表达PR。
脑膜瘤的亚型包括脑膜皮样、纤维性、移行性、砂粒体样、血管型、微囊性、分泌型、富于淋巴浆细胞型、化生性、脊索样、透明细胞型、横纹肌样、乳头状、非典型、间变性。其中脊索样、透明细胞型脑膜瘤的预后更差,因此被归为WHO分级2级、而并不按照常规分级标准进行分级;但最新研究数据对脊索样脑膜瘤是否应归类为高级别亚型提出了质疑。
免疫组化方面,脑膜瘤的细胞一般EMA胞质阳性,SSTR2A细胞核阳性;后者也是这类肿瘤dotatate PET显像的理论依据。该肿瘤表达PR,且与分级呈负相关。免疫组化也可以鉴别脑膜瘤与其他梭形细胞肿瘤,如孤立性纤维性肿瘤会有STAT6的细胞核表达、神经纤维瘤及施万细胞瘤会有SOX10/S100的表达。
核分裂是脑膜瘤分级的重要特征,小于4个/10HPF(1.6mm2)对应1级,4-19个/10HPF对应2级、非典型脑膜瘤、大于等于20个/10HPF对应3级间变性脑膜瘤。对于颅内脑膜瘤,若出现脑实质浸润(需满足肿瘤细胞岛深入脑实质内,而非仅呈推挤性边界或沿Virchow-Robin间隙浸润),可进一步升级为2级。GFAP有助于证实脑实质侵犯。肿瘤出现5条非典型特征中的3条或以上,可升级为2级,具体为:小细胞改变(即出现致密的细胞丰富区域、伴核浆比高),片状(片状生长、无典型漩涡状或束状结构),自发坏死,显著核仁,细胞丰富。骨或软组织侵犯虽然会增加手术切除难度,但不会改变肿瘤分级。除核分裂外,具有明确的间变特征(如黑色素瘤样、癌样或肉瘤样组织学表现)可将肿瘤升级为3级。
脑膜瘤中最常见的分子改变为包括NF2基因在内的染色体22q缺失。基因改变与肿瘤部位有关,颅底脑膜瘤出现22q缺失的几率小,更多见为AKT1、TRAF7、SMO、PIK3CA的突变。级别较高的脑膜瘤染色体改变更为复杂,可有1p、6p、10q、14q的缺失。已证实两种基因变异可独立提示预后不良,即TERT启动子突变、CDKN2A/B纯合型缺失,因此可以作为将肿瘤升级为3级的分子标准。最近的数据表明,即使CDKN2A/B为杂合性缺失,也意味着预后欠佳。NF2患者可有多发性脑膜瘤、发病年龄更轻、发生于少见部位。
大部分脑膜瘤为缓慢生长的肿瘤,约80-90%为1级,10-20%为2级,1-3%为3级。对于有症状的病例来说,治疗方案为手术切除。切除的范围是复发和总生存的主要预测指标,累及鼻腔鼻窦的肿瘤一般因为解剖复杂、累及骨及软组织而难以完整切除。切除不完整者、或级别较高者可进行辅助放疗。预后及复发的情况取决于肿瘤级别。最近的研究表明,甲基化谱系也可能有预后意义。由于颅外原发脑膜瘤非常罕见,因此目前还不清楚颅内肿瘤分级标准在预后判断中的适用性如何、细胞遗传学和甲基化谱系分析的意义。
——未完待续——
往期回顾
小部位,大问题-鼻腔鼻窦处病理集中学--累及鼻腔鼻窦的神经性病变(一)
小部位,大问题-鼻腔鼻窦处病理集中学--累及鼻腔鼻窦的神经性病变(二)
小部位,大问题-鼻腔鼻窦处病理集中学--累及鼻腔鼻窦的神经性病变(三)















共0条评论