[导读] 编译整理:强子
鳞状细胞癌组织学亚型中的HPV
鼻腔鼻窦其他癌中的高危型HPV
鼻腔鼻窦非鳞状细胞癌中HPV的相关数据很少,但也是很有意义的。就具体病种进行学习之前,需要明确几个基本要点:虽然p16表达一般是具有转录活性HPV的较好替代性标记,但在鼻腔鼻窦肿瘤中不能仅凭这一检测做出判断;按照前述建议提出的“70%细胞的细胞核和胞质着色、且至少为中等程度”作为p16阳性判断标准的话,也还是有很多肿瘤、尤其很多非鳞状细胞癌的癌种结果为阳性。
就头颈部来说,高危型HPV的DNA曾报道见于部分涎腺型癌(如黏液表皮样癌),但这一观点已被其他通过p16加HPV DNA原位杂交、或PCR等多种方法检测具有转录活性高危型HPV的研究团队基本否定。相关研究中p16弥漫阳性且分子检测阳性的病例在形态学上为高级别(实性型),形态学上非常类似腺样囊性癌,但后续确定是一种新型且极具临床意义的肿瘤实体,即HPV相关的多表型癌,从而开辟了头颈病理学中最引人入胜的研究方向之一。
鼻腔鼻窦的未分化癌大部分都没有HPV DNA,但也曾有阳性的罕见病例报道。不过,鼻腔鼻窦未分化癌(即某些其他类型的癌,如小细胞癌、腺样囊性癌)也曾有即使不伴转录活性的HPV、但p16广泛阳性表达的报道。小细胞(高级别神经内分泌)癌也是少见类型的癌,很多会有免疫组化p16的过表达但并无HPV的参与。鼻腔鼻窦处很多非鳞状细胞癌的肿瘤中也已证实并无转录活性的高危型HPV,具体如DEK-AFF2融合的非角化型鳞状细胞癌、SWI/SNIT改变的癌、NUT癌、釉质瘤样尤文肉瘤(adamantinoma-like Ewing sarcoma)、肠型和非肠型的腺癌。
文献中有些病例的确不是真正的腺样囊性癌,但形态学却非常类似腺样囊性癌,具体表现为:基底样细胞,呈实性和/或筛状分叶结构,周边有栅栏状表现,并伴僵硬、圆形的微囊腔,内有类似糖胺聚糖的嗜碱性物质,且局灶有导管形成;文献中的8个病例中,6例具有表面的鳞状上皮异型增生。所有病例免疫组化检测显示均有局灶、但明确的肌上皮分化,且所有病例弥漫阳性表达p16、DNA原位杂交和/或PCR检测中高危型HPV(33型或35型)结果阳性。这与经典腺样囊性癌中p16的表达是不同的,后者一般是较为随机、散在的分布。作者最初将这类肿瘤命名为“腺样囊性样的癌”,并提出可能是一种新型的、独特的瘤种。其实回顾此前的文献,可能那些“实性腺样囊性癌”病例也是这一病种。
一项针对49例该组肿瘤的大型随访研究中,作者发现大部分(57%)肿瘤都局限于鼻腔,虽有少数(37%)存在局部复发,但并无淋巴结转移,远处转移罕见。总体生存数据很好,即使局部进展期病变也是如此。这49个病例中,仅2例出现了远处转移,其临床行为不同于鼻腔鼻窦的腺样囊性癌。目前,这一病种已被最新的第五版世界卫生组织肿瘤分类著作中纳入为单独病种,即鼻腔鼻窦HPV相关的多表型癌。
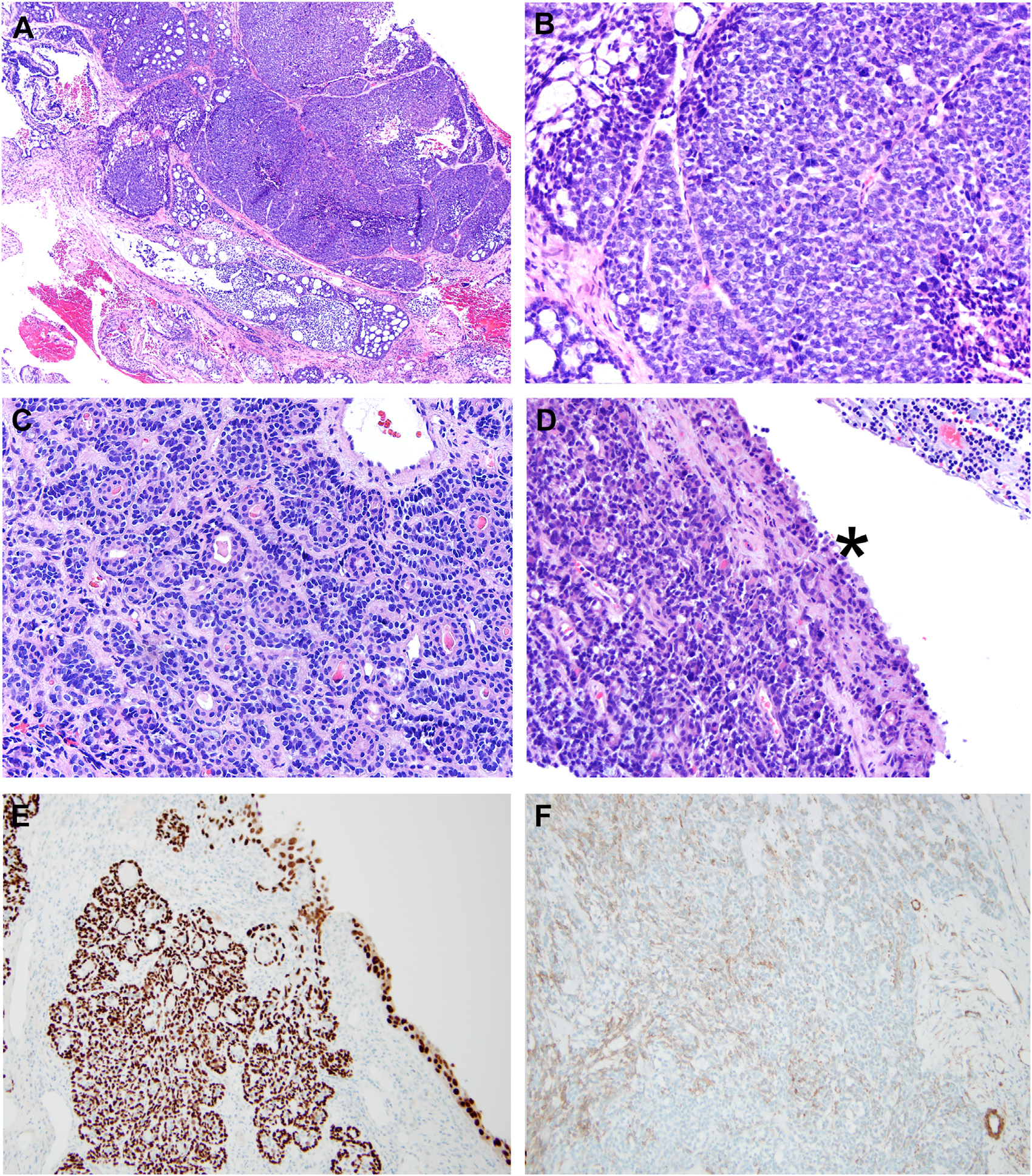 图5.鼻腔鼻窦HPV相关的多表型癌。(A)低倍镜下为基底样表现的癌,有实性的大细胞巢,混杂有致密、筛状结构的细胞巢;(B)中倍镜下的实性细胞巢,细胞呈基底样,细胞核有显著多形性;相邻可见筛状结构;(C)中倍镜下的真正导管区域及肌上皮分化区域;(D)基底样癌的高倍观,呈条索样,相邻表面上皮可见一定的鳞状上皮异型增生表现(星号所示)。(E)免疫组化p40,表面有强阳性着色,也证实具有异型增生的上皮为鳞状表型;导管形成区域的管腔有强阳性着色;(F)免疫组化SMA,肌上皮有显著阳性着色,显示病变为双相型。
图5.鼻腔鼻窦HPV相关的多表型癌。(A)低倍镜下为基底样表现的癌,有实性的大细胞巢,混杂有致密、筛状结构的细胞巢;(B)中倍镜下的实性细胞巢,细胞呈基底样,细胞核有显著多形性;相邻可见筛状结构;(C)中倍镜下的真正导管区域及肌上皮分化区域;(D)基底样癌的高倍观,呈条索样,相邻表面上皮可见一定的鳞状上皮异型增生表现(星号所示)。(E)免疫组化p40,表面有强阳性着色,也证实具有异型增生的上皮为鳞状表型;导管形成区域的管腔有强阳性着色;(F)免疫组化SMA,肌上皮有显著阳性着色,显示病变为双相型。
Tips:鼻腔鼻窦HPV相关的多表型癌病理要点
主要见于鼻腔,可为息肉样;
基底样癌;
常伴表面鳞状上皮异型增生;
免疫组化p16弥漫、强阳性;
高危型HPV阳性(一般为33型);
局部复发几率中等;
淋巴结转移和远处转移的几率低;
预后极好。
——未完待续——
往期回顾:
小部位,大问题-鼻腔鼻窦处病理集中学--鼻腔鼻窦肿瘤中的HPV(一)
小部位,大问题-鼻腔鼻窦处病理集中学--鼻腔鼻窦肿瘤中的HPV(二)
小部位,大问题-鼻腔鼻窦处病理集中学--鼻腔鼻窦肿瘤中的HPV(三)














共0条评论