[导读] 责任编辑:王强
肾脏上皮性肿瘤免疫组化详解(一)
肾脏上皮性肿瘤免疫组化详解(二)
肾脏上皮性肿瘤免疫组化详解(三)
肾脏上皮性肿瘤免疫组化详解(四)
肾脏上皮性肿瘤免疫组化详解(五)
肾脏上皮性肿瘤免疫组化详解(六)
肾髓质癌、集合管癌、其他侵袭性/浸润性肿瘤
主要位于髓质的罕见高级别侵袭性肿瘤从形态学来说和远端肾单位有关,具体如肾髓质癌、集合管癌、以及极少数其他肾原发肿瘤,详见表4。该组肾肿瘤PAX8总是阳性,但一定要牢记:诊断该组肿瘤之前一定要考虑尿路上皮癌或其他癌转移的可能,尤其尿路上皮癌还可表达PAX8,因此要注意联合其他尿路上皮标记一起应用,如GATA3、p63。
表4. 累及肾脏的高级别浸润性肿瘤免疫组化。
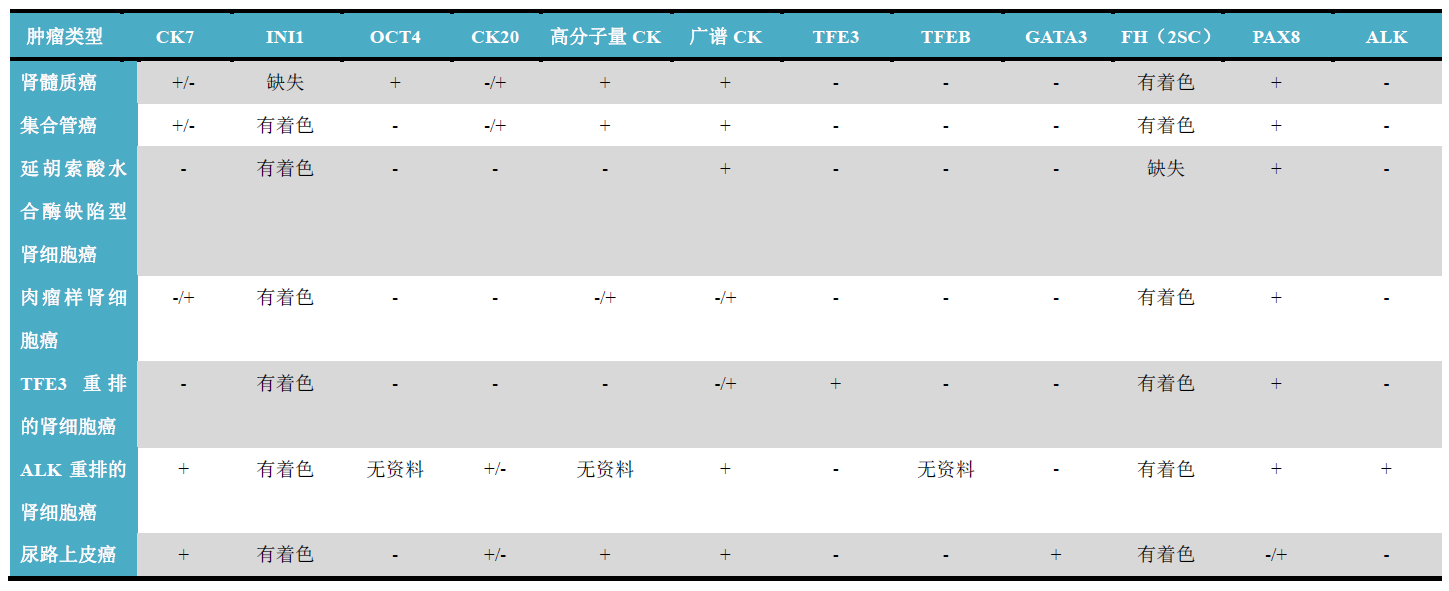
备注:
1. 肾髓质癌的诊断需要证实有镰状血红蛋白病,否则建议诊断为“伴髓样特征的未分类肾细胞癌”;
2. 集合管癌的诊断是排除性诊断,没有哪项标记有助于该诊断;
3. 考虑转移性肿瘤的时候,要注意结合临床病史。
镰状血红蛋白病是诊断肾髓质癌的必备条件,最近已发现有形态学类似、但并无镰状血红蛋白病的罕见病例,对于后者有人提出可称之为“伴髓样表型的未分类肾细胞癌(RCC unclassified with medullary phenotype)”。
肾髓质癌呈浸润性生长,常有融合的管状结构,肿瘤细胞为高级别表现,显著浸润良性肾实质,常伴肾小管的急性炎症。肾髓质癌中常见SMARCB1基因(也称之为INI1基因)的易位,导致几乎所有该肿瘤的免疫组化中SMARCB1/INI1表达缺失。常用于生殖细胞肿瘤诊断的OCT4(也称之为OCT3/4)在很多肾髓质癌中也是阳性。CK7和CK20可共表达。
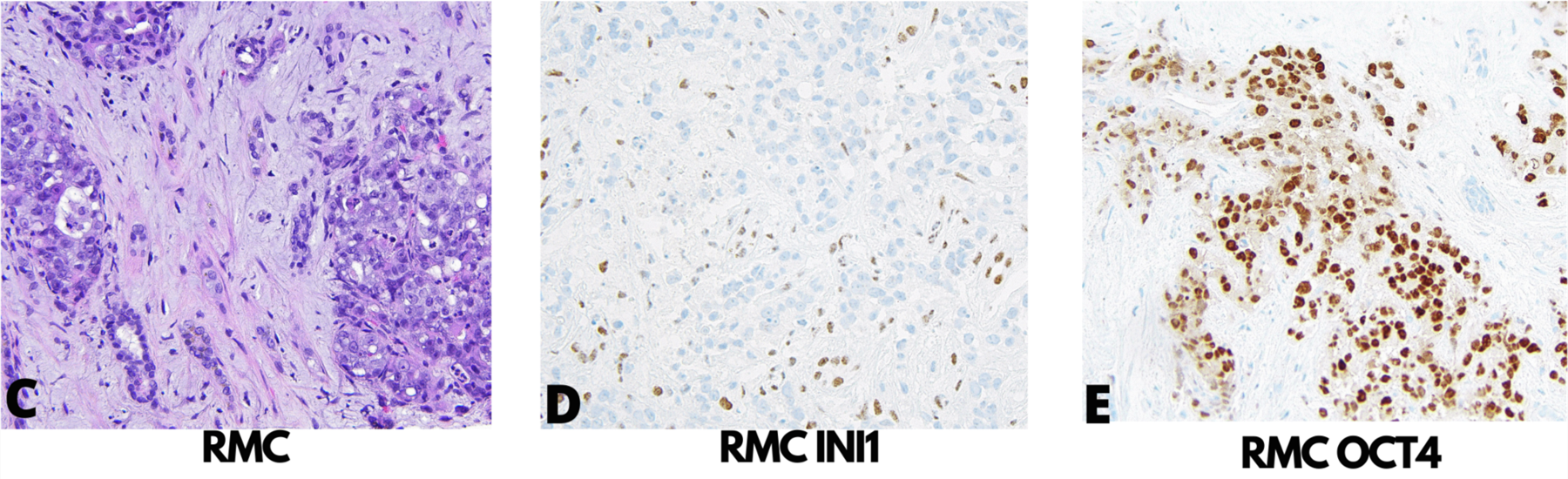
图1. 肾髓质癌的形态学及免疫组化:(左)形态学表现为高级别的细胞,一般胞质嗜双色性,伴急性炎症表现;免疫组化INI1表达缺失(中),OCT4细胞核阳性(右)。
一旦排除了肾髓质癌(以及前述伴髓质表型的未分类肾细胞癌)、尿路上皮癌、延胡索酸水合酶缺陷型肾细胞癌、其他器官转移癌之后,其实属于该组的其他肾原发肿瘤诊断就是排除性诊断了。比如,集合管癌没有可靠的生物学标记,只能是根据几项非特异性组织学表现来诊断,具体如显著管状结构、促纤维结缔组织增生、浸润性生长,且要排除其他原发和继发肿瘤。有作者报告集合管癌中p63阳性;但本文原作者认为对此需要慎重解读,因为这种情况下多为尿路上皮癌。延胡索酸水合酶缺陷型肾细胞癌可以表现为具有显著浸润性的管状结构,但免疫组化FH/2SC可以鉴别开来。
该组肿瘤中还有一类是最近才得以认识的瘤种,即ALK重排的肾细胞癌。ALK重排的肾细胞癌形态学表现具有异质性,常呈横纹肌样形态、背景为黏液样。也有非常类似后肾腺瘤、但却具有ALK重排的罕见肿瘤报道,具体意义还不清楚。ALK重排肾细胞癌一般可通过免疫组化ALK检测诊断出来,且这一诊断具有重要治疗意义:可选择相应靶向治疗。
其余以浸润性为特征的原发肾细胞癌,如果没有前述治疗类型的特征性表现,可诊断为未分类的肾细胞癌。
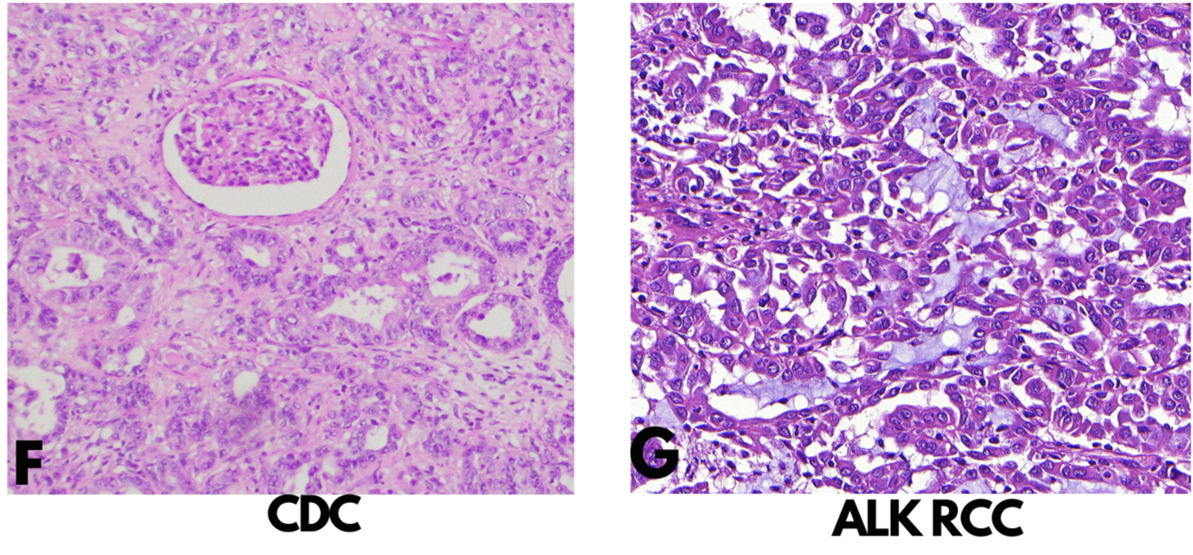
图2. (左)集合管癌,形态学为高级别的细胞、呈浸润性管状结构,有促纤维结缔组织增生表现。(右)ALK重排的肾细胞癌,细胞核显著高级别,背景为黏液样。
小结
很多肾肿瘤的病例,仅凭形态学就可以做出准确分类。但,有些病例需要在两种或多种类型肾细胞癌之间做出鉴别,此时一般几项免疫组化就可以缩小鉴别诊断的范围。
这些年来,肾肿瘤诊断中的免疫组化指标研究有很多,但大部分诊断困难的病例中,少数几项就可以有助于诊断。对于证实为肾来源来说,PAX8是最佳指标,但要了解其某些局限性。
肾肿瘤诊断中的其他指标还有CA-IX(用于透明细胞型肾细胞癌的诊断)、AMACR(用于乳头状肾细胞癌的诊断)、CD117(用于嫌色细胞肾细胞癌和嗜酸细胞腺瘤的诊断)、CK7(用于乳头状、透明细胞乳头状、嫌色细胞肾细胞癌的诊断)、vimentin(嗜酸细胞腺瘤、嫌色细胞癌中不表达)。
SDHB、FH、SMARCB1则有助于相应具有分子遗传学特点和肾髓质癌的诊断和鉴别。
全文完
参考文献
Akgul M, Williamson SR. Immunohistochemistry for the diagnosis of renal epithelial neoplasms. Semin Diagn Pathol. 2022;39(1):1-16.
doi:10.1053/j.semdp.2021.11.001
















共0条评论