编译整理:强子
肺癌免疫组化解惑答疑(1)
肺癌免疫组化解惑答疑(2)
肺癌免疫组化解惑答疑(4)
肺癌免疫组化解惑答疑(5)
肺癌免疫组化解惑答疑(6)
6.神经内分泌肿瘤与其他类型非小细胞癌鉴别时,最佳抗体组合如何选?哪种抗体最可靠?
简答:用于神经内分泌肿瘤的最佳免疫组化抗体组合为CgA、Syn、CD56。每种抗体在不同标本类型、不同组织学分型、阳性程度及阳性范围方面,均有所差异。
详解:2015年世界卫生组织分类建议应用CgA、Syn、CD56三种免疫组化抗体来进行神经内分泌分化标记。免疫组化指标应结合形态学特点、标本类型(细胞、活检、切除)及阳性的范围来解读。
CgA、Syn的抗原表位为神经内分泌颗粒或突触泡的一部分,因此它们是真正的神经内分泌分化标记。相比大细胞神经内分泌癌或小细胞肺癌来说,类癌中CgA阳性更多见;类癌中CgA一般为胞质弥漫、强阳性,相反,小细胞癌中部分(而非全部)细胞可出现CgA的阳性。Syn也有类似情况。当然,部分小细胞癌和大细胞神经内分泌癌可能会出现多种神经内分泌标记的弥漫、强阳性,这并不妨碍最终诊断。
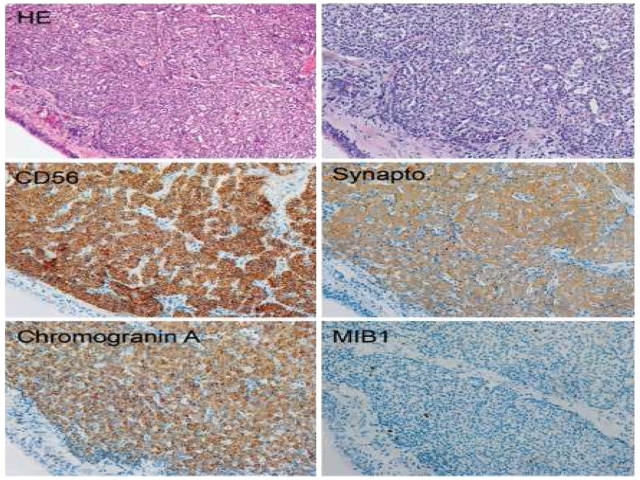
图9. 类癌一例,三项神经内分泌标记均一、强阳性,但MIB-1标记的增殖指数低。
CD56是肺小细胞癌诊断中最敏感的标记,不过约5-10%的肺小细胞癌上述三种神经内分泌标记均阴性。对于神经内分泌分化来说,CD56并不特异,该蛋白还可表达于神经元、神经胶质、造血细胞(NK细胞、γδ-T细胞、活化的CD8+T细胞、树状突细胞)、骨骼肌。因此,将其视为“神经内分泌”标记时应注意结合HE染色中的神经内分泌形态学特征来解读。大部分小细胞肺癌中,CD56为所有肿瘤细胞均为强的膜阳性。TTF-1阴性而可疑小细胞肺癌或大细胞神经内分泌癌的病例中,应加做p40以排除基底细胞样鳞状细胞癌。
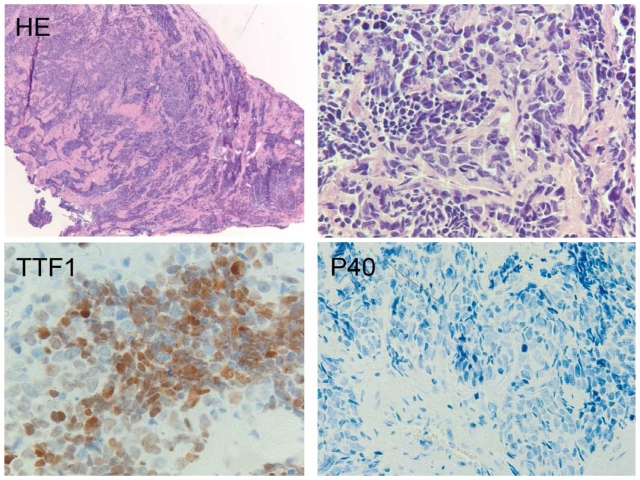
图10. 形态学符合小细胞癌,但免疫组化TTF-1阳性、p40阴性。
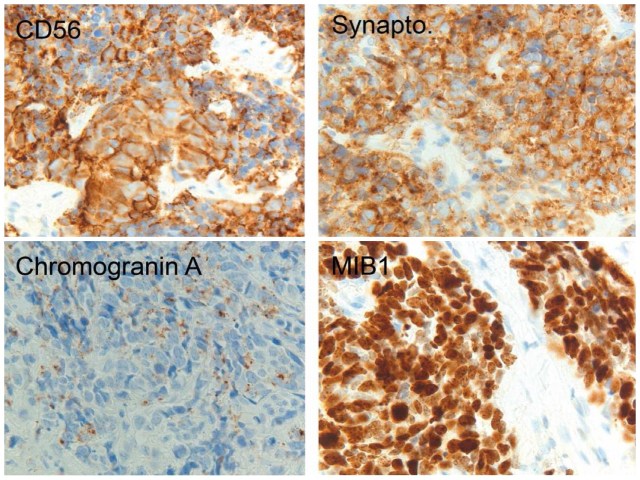
图11. 图10病例,两项免疫组化指标强阳性,CgA呈逗点样阳性,但MIB-1标记的增殖指数高。
神经内分泌形态学特征、加之上述神经内分泌标记任一阳性,则提示神经内分泌肿瘤的诊断。目前对神经内分泌标记的数量(比如一种、还是两种或三种)尚无一致意见。需要指出的是,约10-20%的非小细胞肺癌会表达一种神经内分泌标记,因此对于无神经内分泌形态学表达的低分化、非小细胞癌来说,并不建议常规进行神经内分泌的免疫组化标记,因为即使阳性也并无临床意义。
除上述三项指标外,也有其他神经内分泌标记,如hASH1、Leu7/CD57、多克隆的NSE、INSM1等,但由于敏感性、特异性等问题或抗体较新、应用经验尚需进一步完善等,目前并不常规推荐。除前述三项神经内分泌免疫组化指标CgA、Syn、CD56外,大部分大细胞神经内分泌癌、小细胞肺癌中会还会有其他神经内分泌相关指标的阳性;但具体什么程度的着色才可视为阳性,也并无相关共识。本文中专家组一般认为只要有神经内分泌的形态学特点,则任何程度的着色均可视为阳性。HE形态学评估的基础上结合免疫组化,提高了病理医师之间、以及最终诊断的一致性。
7.诊断中何时应用增生相关指标?
简答:肺癌中Ki-67已明确的主要意义在于协助区分类癌和高级别神经内分泌癌(大细胞神经内分泌癌、小细胞癌),尤其在小活检标本或挤压的活检/细胞学标本中。Ki-67鉴别典型和非典型类癌的意义尚未明确,需进一步研究。
详解:可用于石蜡包埋切片的Ki-67抗体有几种,其中克隆号为MIB-1者可能是抗原修复介入后应用最广泛的。Ki-67的表达可在热点区人工计数500-2000个细胞后计算阳性细胞比例而达到半定量评分,也可计算2mm2区域、或目测,但肺癌中尚无公认的标准评分方案。
肺神经内分泌肿瘤中,Ki-67的主要诊断意义在于对受挤压的小活检中协助鉴别类癌和高级别小细胞癌、大细胞神经内分泌癌。鉴别非典型类癌和典型类癌方面,尚无明确的阈值;有研究表明Ki-67增殖指数在典型类癌中为2.3-4.15%,在非典型类癌为9-17.8%。非典型类癌与高级别肿瘤的鉴别阈值实际也并未得到公认,非典型类癌和大细胞神经内分泌癌之间的鉴别阈值范围则认为是2.5%至30%之间。2015年版世界卫生组织分类中,非典型类癌Ki-67增殖指数的上限规定为20%,大细胞神经内分泌癌和小细胞癌Ki-67增殖指数的下限则规定为40-50%;因此如何更好的应用Ki-67来鉴别非典型类癌和高级别神经内分泌癌,还需进一步研究确定。
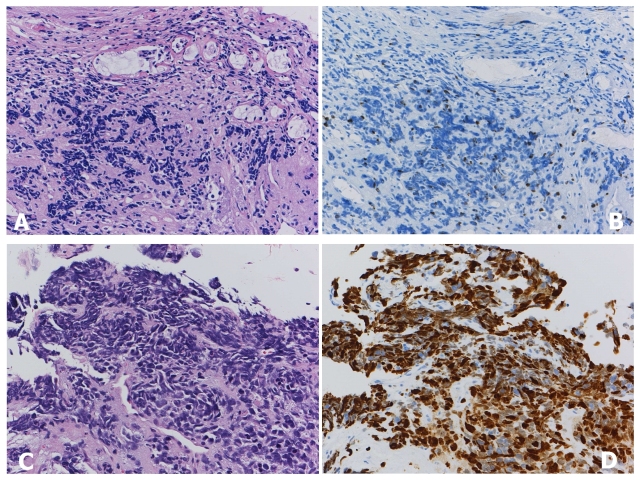
图12. 活检标本,瘤细胞挤压显著(左上、左下);此时如有细胞学标本,也可用于诊断。Ki-67免疫组化(右侧)可协助鉴别类癌(上)和小细胞癌(下)。
目前不再推荐将Ki-67用于非小细胞肺癌的诊断或管理。一般说来,Ki-67高并不意味着预后不良,但低分化肿瘤中的确Ki-67增殖指数增高。不同组织学类型间,Ki-67的预后意义可能有所不同:Ki-67增殖指数高与腺癌预后差有关,但可能与鳞癌无关。
新型标志物PHH3可视为核分裂特异性标记,且已在多种癌中进行了研究,但肺癌中还缺乏大规模研究。
未完待续
点击下载英文文献
参考文献
YatabeY,DacicS,BorczukAC,etal.Best Practices Recommendations for Diagnostic Immunohistochemistry in Lung Cancer[J].Journal of thoracic oncology,2018.
DOI:10.1016/j.jtho.2018.12.005

















共0条评论