[导读] 译者:慧海拾穗
往期回顾:
从发育的角度看儿童泌尿生殖系统肿瘤(1)
(2)儿童囊性肾瘤
儿童囊性肾瘤(Pediatric Cystic Nephroma,PCN)是一种罕见的良性肾脏肿瘤,其特征是多房囊肿,主要发生在2岁以下的幼儿中,90%的病例与DICER1综合征有关。PCN通常表现为在常规检查中偶然发现的无症状腹部肿块,或在患有胸膜肺母细胞瘤和/或胚系DICER1突变的儿童筛查中发现的。
组织病理学特征:PCN通常是一个边界清晰、多房的肿块,由大小不等的囊肿组成,囊肿内充满透明或出血性液体。肿块通常局限于肾脏,没有侵入周围组织的证据。显微镜下观察,囊肿内衬扁平、立方或鞋钉状上皮(On microscopic examination, the cysts are lined by flattened, cuboidal, or hobnail epithelium)。没有异型性或明显的核分裂象。隔膜薄、细胞少,有细胞聚集区和分化良好的小管,但没有胚芽组织(图2A-F)。囊胚的存在是“囊性部分分化肾母细胞瘤”(cystic partially differentiated nephroblastoma,CPDN)的诊断标准,ER表达缺失有助于区分PCN和成人囊性肾瘤。
分子诊断:PCN与DICER1的胚系突变有关,DICER1现在被认为是DICER1肿瘤易感综合征的特征。PCN的诊断应立即检测DICER1的体细胞和胚系改变。DICER1中的胚系突变以常染色体显性模式遗传。DICER1是microRNA加工途径的一部分,与DICER1相关的肿瘤具有不寻常的进化模式。它们不是获得第二个DICER1体细胞功能丧失突变,而是获得RNase IIIb结构域中的体细胞错义突变。在DICER1肿瘤易感性综合征的背景下,可能会出现各种其他肿瘤,包括胸膜肺母细胞瘤、子宫颈胚胎性横纹肌肉瘤(ERMS)、Sertoli-间质细胞瘤、甲状腺结节(良性和恶性)和松果体瘤等。
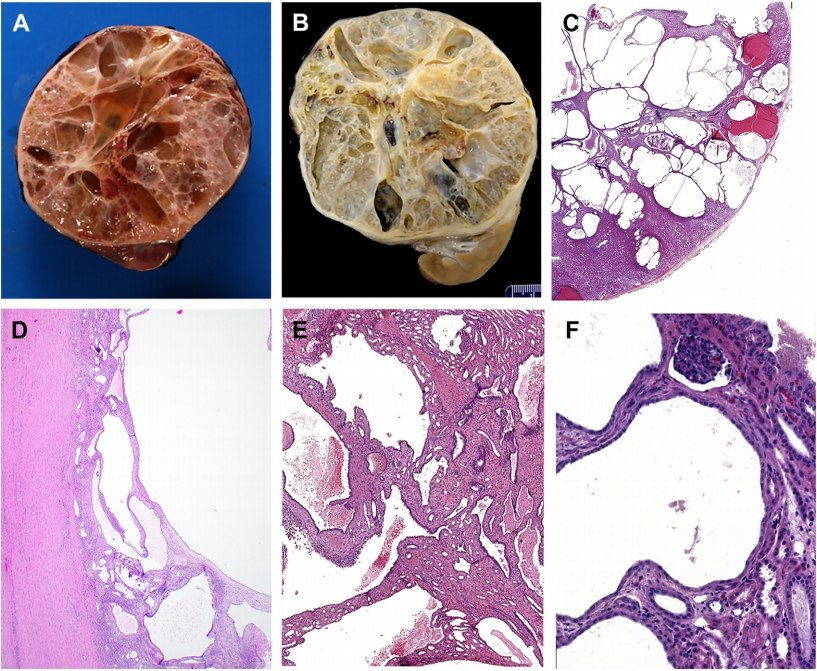 图2 儿童囊性肾瘤:(A,B)边界清晰的囊性肾瘤切面,具有典型的多囊外观,隔膜细小,无明显出血或坏死。(C-F)囊肿与中间基质的代表性图像。囊肿被覆低立方形上皮(E)。
图2 儿童囊性肾瘤:(A,B)边界清晰的囊性肾瘤切面,具有典型的多囊外观,隔膜细小,无明显出血或坏死。(C-F)囊肿与中间基质的代表性图像。囊肿被覆低立方形上皮(E)。
治疗与预后:手术切除,通常是通过肾移植手术或部分肾切除术,是首选的治疗方法。完全切除通常预后良好,复发风险低。已经描述了非常罕见的PCN转化为DICER1肉瘤的病例。
(3)先天性中胚层肾瘤
Robert Bolande于1967年描述,先天性中胚层肾瘤(CMN)是最常见的先天性肾肿瘤,主要发生于婴儿,通常在出生后的前6个月内。通过适当的手术治疗,预后良好。MN通常表现为新生儿或婴儿可触及的腹部肿块。
组织病理学特征:从大体上看,肿瘤边界清晰,呈灰黄色至棕褐色,呈旋涡状(whorled)。大多数位于肾门附近。显微镜下可见肾实质和肾周脂肪浸润。出血和坏死区域通常不存在。组织学上,CMN分为:经典型、细胞型、混合型(经典型和细胞型成分均存在)。经典型CMN(约占25%的病例)由温和、细长的梭形细胞组成,这些细胞呈长而交叉的束状,并伴有细小的细胞间嗜酸性胶原基质。核分裂象比较少见。可见肿瘤细胞内可见内陷的肾小管和肾小球。没有包膜将肿瘤与未受累的肾实质隔开。细胞型CMN由紧密排列的肥大梭形细胞组成,细胞核较大,类似于婴儿型纤维肉瘤。肿瘤显示核分裂象增加,倾向于浸润肾盂或肾周组织,并可能出现出血和坏死区域。极少数病例可存在间变[1]。
免疫表型:梭形细胞表达平滑肌肌动蛋白(SMA)、结蛋白(desmin)偶尔阳性,但通常不表达CD34和S100。pan-TRK的核表达支持NTRK基因融合的细胞型CMN的诊断。肿瘤细胞可弥漫表达Cyclin D1和WT1,SMA和BCOR阴性表达,并保留了核INI-1表达。间变区域p53呈弥漫强阳性。肿瘤细胞可表达EGFR,但不是诊断CMN存在EGFR ITD的有用标志物[2]。p-Mek1/2和p-Erk1/2免疫反应可能是EGFR ITD的有用标志物。因此,MEK1/2抑制剂有可能用作具有EGFR ITD的CMN的靶向治疗[2]。
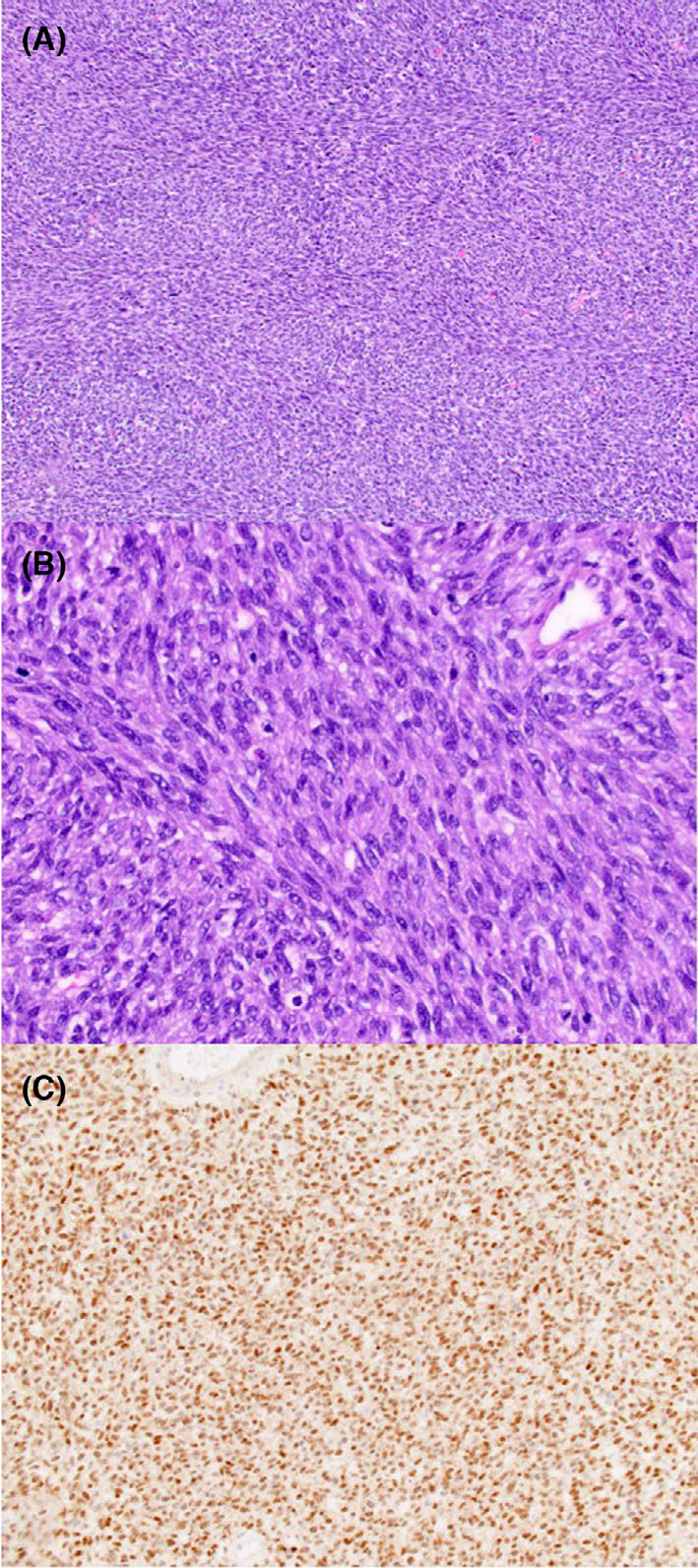
图3 组织学特征:大多数病变区域具有细胞型先天性中胚层肾瘤的典型特征(A)和(B),免疫组织化学染色显示panTRK的核阳性(C)。
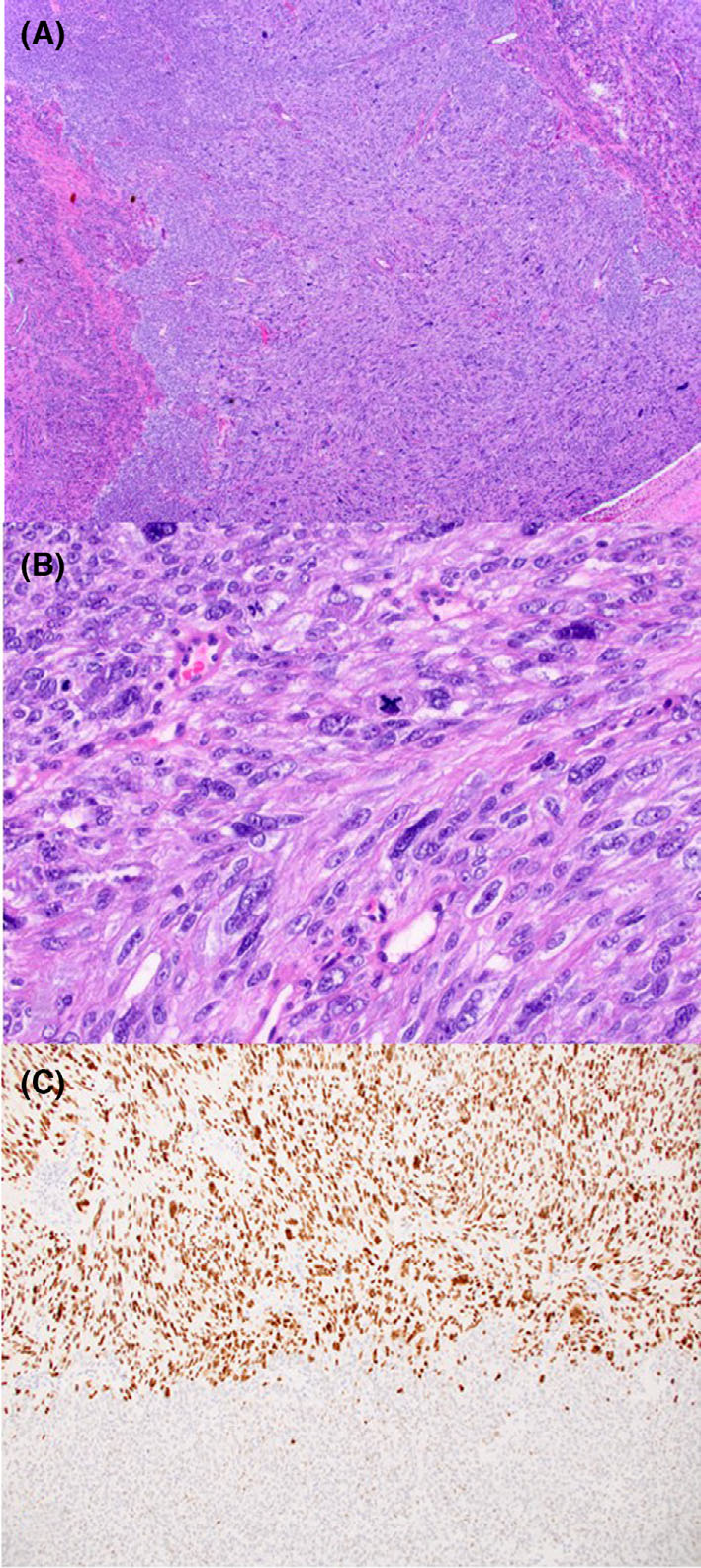
图4 组织学特征:发现了一个间变性区域(A)具有多极有丝分裂(B)。与其余肿瘤中的野生型染色相比(底部),p53的免疫组织化学染色在间变性区域(顶部)呈强阳性和弥漫性阳性(C)。
分子诊断:在CMN中发现的最常见的遗传改变(约70%的病例中可见)是t(12,15;p13;q25)染色体易位,导致ETV6与NTRK3融合,与婴儿型纤维肉瘤的经典易位相同。这种易位与细胞型CMN形态有关。此外,在经典型CMN和一些混合型CMN病例中可以看到EGFR内部串联重复(ITD)。虽然大多数病例只能通过切除治疗,但NTRK重排的存在为TRK抑制剂的靶向治疗提供了可能性。这在不可切除或转移性疾病的情况下可能尤为重要。pan-TRK免疫组织化学是NTRK重排病例的敏感筛查工具;然而,使用荧光原位杂交(FISH)或下一代测序(NGS)进行确认是必要的。EGFR ITD的鉴定需要先进的技术和生物信息学分析,如NGS或全转录组测序等[2]。
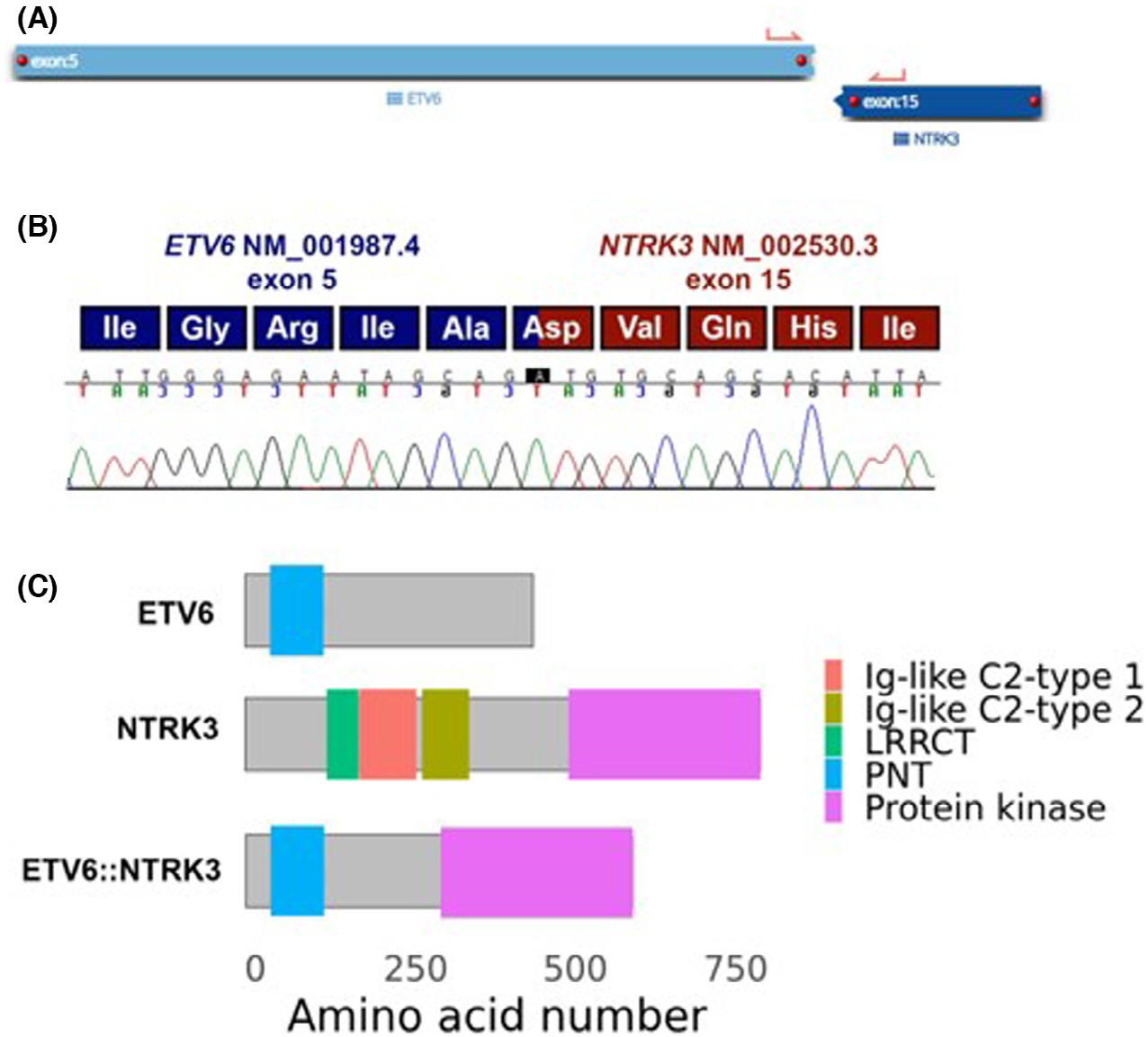
图5.ETV6::NTRK3基因融合的分子特征。
治疗与预后:采用边界清晰的肾切除术治疗的CMN预后良好,不需要常规化疗。据报道,局部复发和/或转移都与细胞型CMN有关,并且在手术后12个月内发生。局部复发与不完全手术切除有关,完全切除仍然是最好的治愈方法。TRK抑制剂似乎是一种潜在的治疗方法,尽管现在评估它将如何影响CMN的治疗还为时过早。最近有文献报道伴有TPM3::NTRK1融合的先天性中胚层肾瘤预后不良[3]。p-Mek1/2和p-Erk1/2免疫反应可能是EGFR ITD的有用标志物。因此,MEK1/2抑制剂有可能用作具有EGFR ITD的CMN的靶向治疗[2]。
参考文献
[1] Rubrecht A, Shah N, Aldrink JH, et al. Cellular congenital mesoblastic nephroma with focal anaplasia, report of a case. Histopathology. 2024,85(5):826-829.
[2]Hamada H, Kohashi K, Iwasaki T, et al. Adjunctive diagnostic tool for histopathological classification of congenital mesoblastic nephroma based in molecular genetic findings. J Cancer Res Clin Oncol. 2025,151(2):69.
[3]Sun M, Chen J, Xue Y, Deng Y, et al. Poor outcome in congenital mesoblastic nephroma with TPM3::NTRK1 fusion: a case report from multi-disciplinary treatment to molecular tumor board. Transl Pediatr. 2024,13(6):976-986.

















共0条评论