[导读] 译者:慧海拾穗
【摘要】与成人相比,儿童肿瘤相对少见。儿童常见的是淋巴造血系统肿瘤和中枢神经系统肿瘤。在颅外实体肿瘤中,泌尿生殖系统肿瘤相对比较常见,其中肾母细胞瘤是最常见的,其他肿瘤相对少见,给诊断带来一定的挑战。本文【Pediatric Genitourinary Tumors: The Developmental Angle. Surg Pathol Clin. 2025 Mar;18(1):191-207.】综述了利用组织病理学、免疫表型和分子信息来诊断常见的儿童泌尿生殖系统肿瘤的最重要信息。
【概述】儿童泌尿生殖系统肿瘤包括各种各样的良性和恶性病变。它们相对罕见,但代表了儿科人群中遇到的肿瘤的一个重要部分,约占所有儿童肿瘤的7%至10%。其中一些肿瘤几乎只发生在儿童人群中,和/或可能具有与成人不同的临床表现、行为和遗传学背景。儿童泌尿生殖系统肿瘤的早期准确诊断对于有效治疗至关重要,必须基于详细的组织病理学和遗传/分子检测。作者在这里回顾了目前关于最常见的儿科泌尿生殖系统肿瘤的诊断和病理分类的知识,强调了它们的精确诊断如何影响这些具有挑战性的疾病的管理。
(1)肾母细胞瘤 (Wilms瘤)
肾母细胞瘤,由Max Wilms于1899年描述,通常被称为“Wilms瘤(WT),是最常见的儿童原发性肾脏恶性肿瘤,患病率为万分之一。它主要发生于5岁以下的儿童,约占儿童肾癌的90%,但也很少发生在成年人身上。WT在非洲和非洲裔美国人中更常见,在东亚人群中不太常见。与其他儿童肿瘤类似,它通常表现为腹部肿块或腹围增大、血尿、高血压、体重减轻或厌食症。父母最常见的第一句话是他们在给孩子洗澡时触诊肿块。
肿瘤起源于胚胎肾脏发育前体组织,称为肾源性残余组织,其分化和增殖异常。WT的遗传变化是复杂的,在基因和染色体水平上都有变化,其中许多变化具有预后和/或临床意义。WT1基因位于11p13,编码一种DNA结合转录因子,是第一个与WT发展有关的基因。虽然WT1中的突变可以在WT中看到,但也可以看到胚系改变,并可能导致几种增加肾母细胞瘤风险的综合征。例如,WAGR综合征包括WT、虹膜缺失、泌尿生殖道异常和发育迟缓,是由11p13微缺失引起的。WT1中的胚系突变可导致其他综合征,如Denys-Drash和Frasier综合征。在11p15处发现了另一个WT基因位点,该位点的异常甲基化是肾母细胞瘤中最常见的遗传学改变。11p15处的各种胚系表观遗传和遗传学改变(如单亲二体)导致Beckwith-Wiedemann综合征(BWS)。BWS是一种过度生长综合征,也会增加肾母细胞瘤、肝母细胞瘤,横纹肌肉瘤和其他肿瘤的风险。体细胞突变也可以在许多其他基因中看到,包括TP53(与间变性WT相关,见下文)、CTNNB1、IGF2和MYCN(也与间变性相关)等。拷贝数改变在肾母细胞瘤中也很常见,包括2p24的获得(MYCN)和17p13的丢失(TP53),这两者都与间变性有关。1p和16q杂合性缺失以及1q获得被认为是WT预后不良的因素。
组织病理学特征:WT的特征是存在未成熟/原始的肾组织,其中未分化(胚芽)和部分分化的上皮和间叶谱系的百分比各不相同,这给出了一个典型的三相模式,由胚芽(blastema)、上皮和间叶成分组成。然而,仅由1或2个成分组成的肿瘤并不罕见。胚芽是分化程度最低的成分,由紧密排列的小细胞组成,细胞质稀少,核质比高,核分裂像较多。在大多数WT病例中,上皮成分表现出不同程度的肾上皮/肾小管分化。最原始的管状结构类似菊形团样结构。此外,还可以识别出具有更多分化元件的小管和乳头状结构,如肾小球结构,这些成分概括了正常肾脏发生的各个阶段。这些小管具有柱状上皮和高核分裂象。然而,一些肿瘤可能只有局灶管状成分,具有立方上皮和低核分裂象,类似于后肾腺瘤。间叶成分可以显示出不同的形态、细胞数量和分化。它主要由梭形细胞组成,可选择性分化为异源成分(横纹肌母细胞、脂肪组织、软骨)。应避免使用基于异源成分存在的描述性诊断术语,因为它们不是不同的实体或具有预后意义。
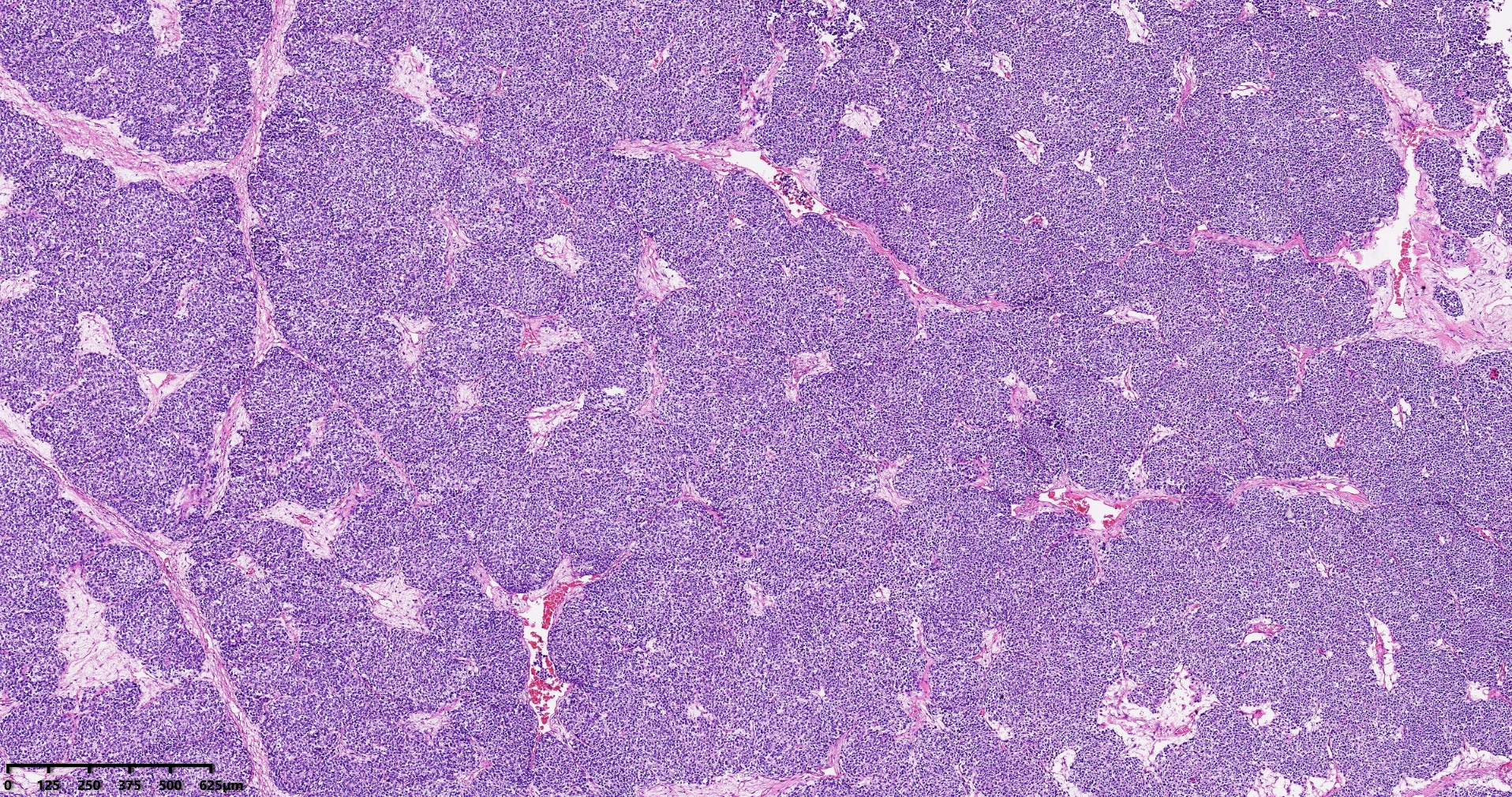
图1:胚芽为主型肾母细胞瘤组织形态学(40倍放大,图片来源作者)
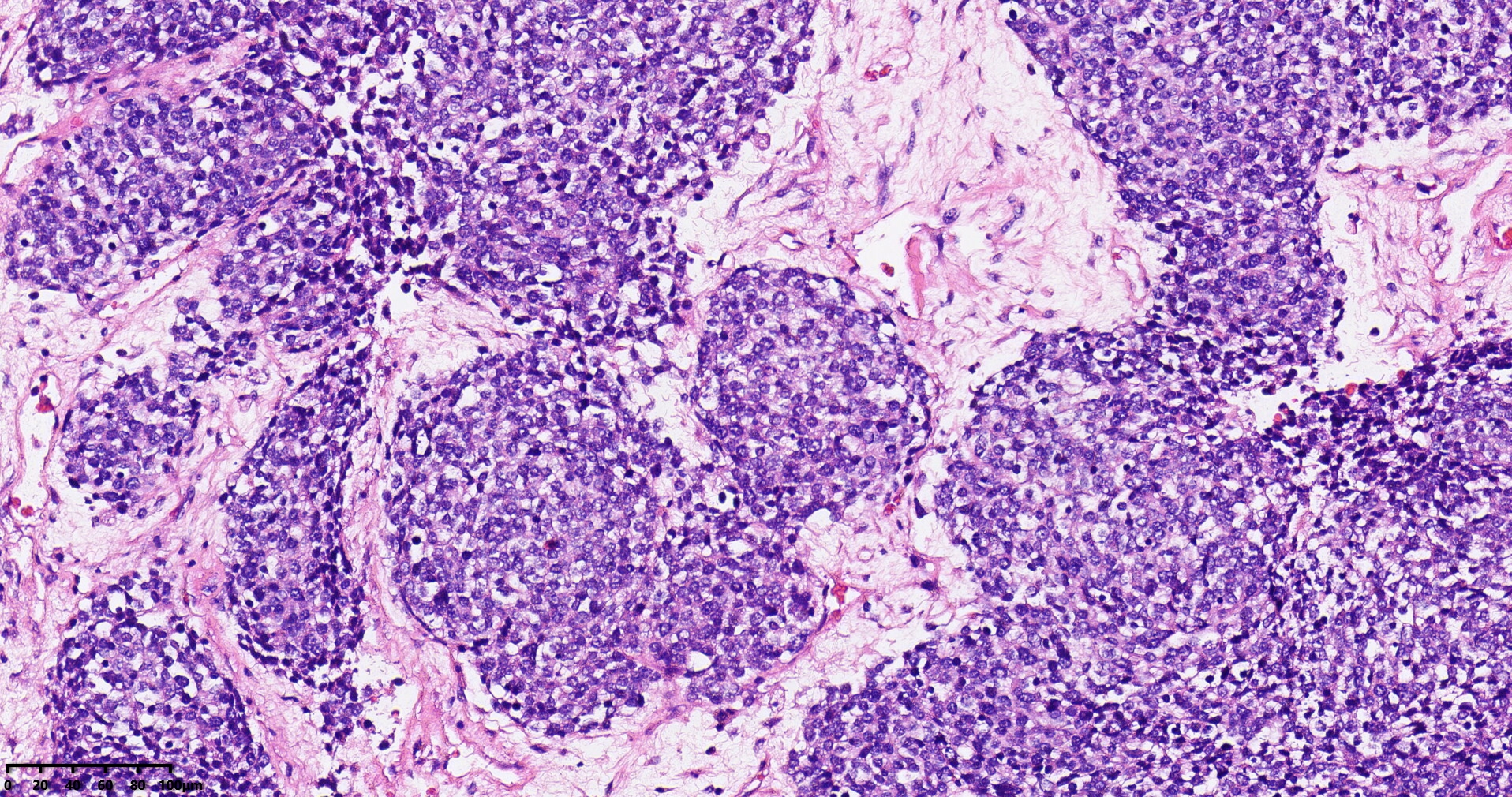
图2:来自图1的200倍放大(胚芽为主型肾母细胞瘤组织形态学,图片来源作者)
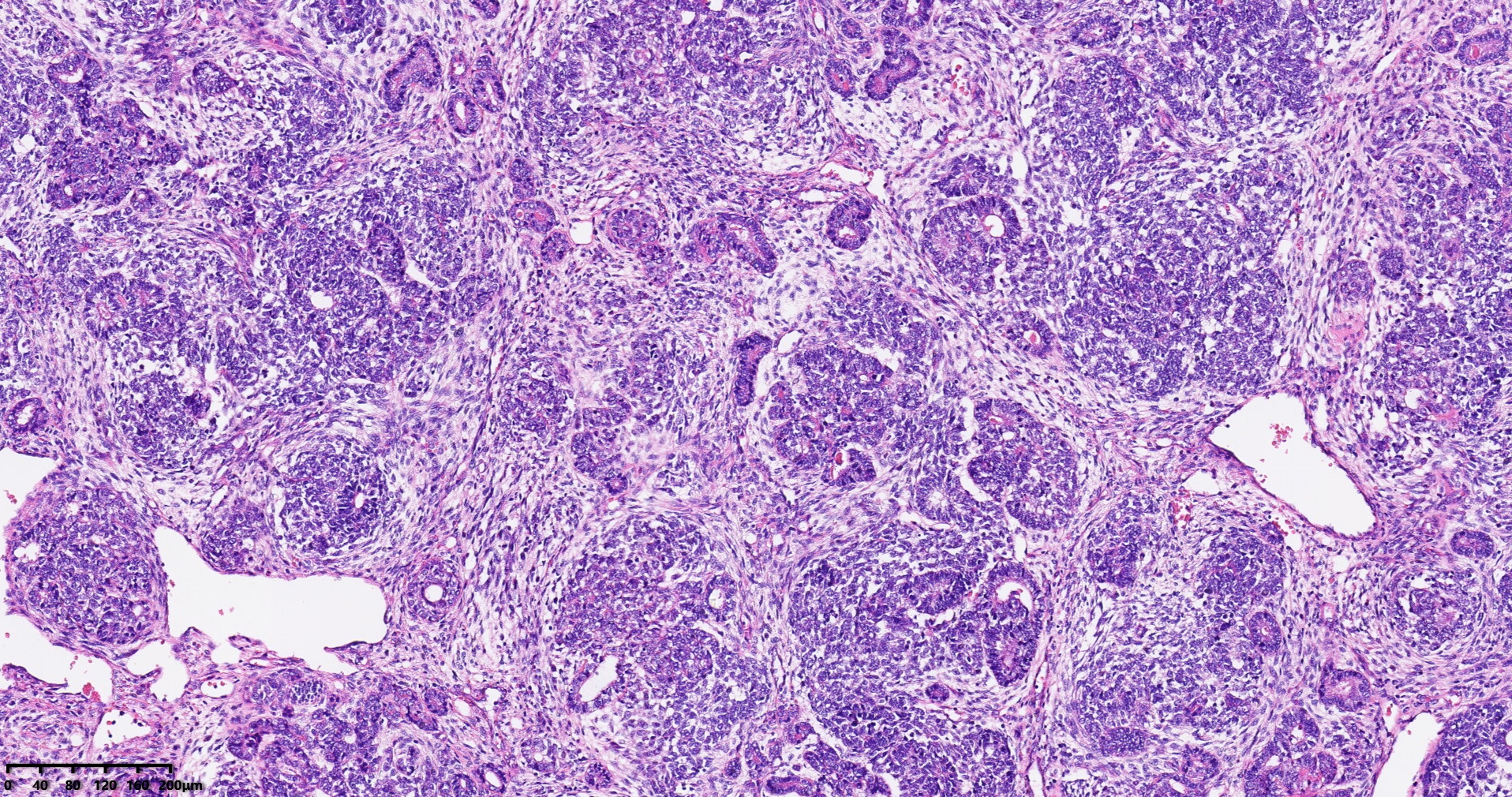
图3:混合型肾母细胞瘤组织形态学(100倍放大,图片来源作者)
WT中存在间变的病例占7%-10%,这是一个需要评估的重要组织学参数。它被定义为存在2个特定标准:(1)非典型、明显非整倍体、三极或多极核分裂象,以及(2)明显的核增大(即染色质过浓的肥大核,核比非间变性核大至少3倍)。这两种特征的存在是诊断WT间变所必需的。间变分为局灶性或弥漫性,对预后和治疗有重要影响。在儿童肿瘤学组(Children’s Oncology Group,COG)中,局灶性间变被定义为小于4个病灶,在国际儿科肿瘤学会(International Society of Pediatric Oncology,SIOP)中,被定义为2个或小于15mm的病灶。弥漫性间变被定义为:①非局灶间变;②肿瘤包膜外出现间变;③肾内、肾外血管、肾窦或远处部位出现间变;④或随机活检标本中出现间变。弥漫性间变通常见于大龄儿童和晚期患者。
在SIOP研究中,弥漫性间变WT的预后明显低于非间变WT,而局灶性间变与非间变WT的预后相似。WT家族中的一种组织学亚型是“囊性部分分化肾母细胞瘤”(cystic partially differentiated nephroblastoma,CPDN),其定义是在非常年幼的儿童中存在多房且仅囊性的肾肿瘤,含有肾母细胞成分。这种肿瘤不同于“儿童囊性肾瘤”(pediatric cystic nephroma,PCN),因为CPDN显示了PCN中不存在的胚芽成分。此外,CPDN缺乏PCN特有的DICER1改变。
WT在化疗后表现出许多变化,包括坏死、含铁血黄素沉积、泡沫巨噬细胞丰富的区域和纤维化。该治疗还可以诱导肿瘤成分的成熟,包括骨骼肌分化。SIOP标准将化疗的组织学反应纳入风险评估。完全坏死的肿瘤被认为风险较低,术后接受最小的治疗。具有丰富胚芽或化疗后间变的肿瘤预后较差,需要增加治疗。
免疫表型:WT具有经典的临床表现和病理学特征,不需要特殊的染色进行诊断。然而,免疫组织化学可能有助于单相型WT的病例,这些病例可能难以与其他肿瘤区分开来。WT1(针对WT1蛋白的C端和N端部分)是最敏感和最特异的标记。它通常在胚芽和上皮成分中显示核表达,但在基质成分中表现较弱或缺失(在实际工作中大约5-10%的病例存在WT1阴性或少量阳性的表达,此时需要结合形态学和其他免疫组化指标综合分析)。胚芽成分还显示PAX8和PAX2的弥漫表达,以及程度不一的细胞角蛋白、EMA和结蛋白染色。上皮成分显示细胞角蛋白、EMA的表达,PAX8的表达各不相同。笔者在实际工作中,发现细胞型先天性中胚层肾瘤也可弥漫表达WT1(如下图),在粗针穿刺标本时需要注意这个诊断陷阱。
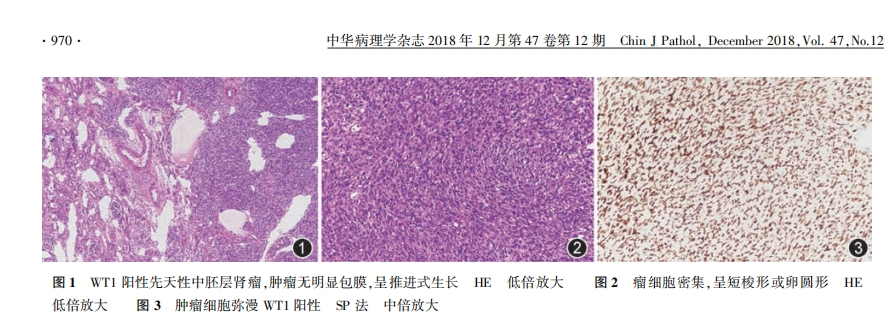
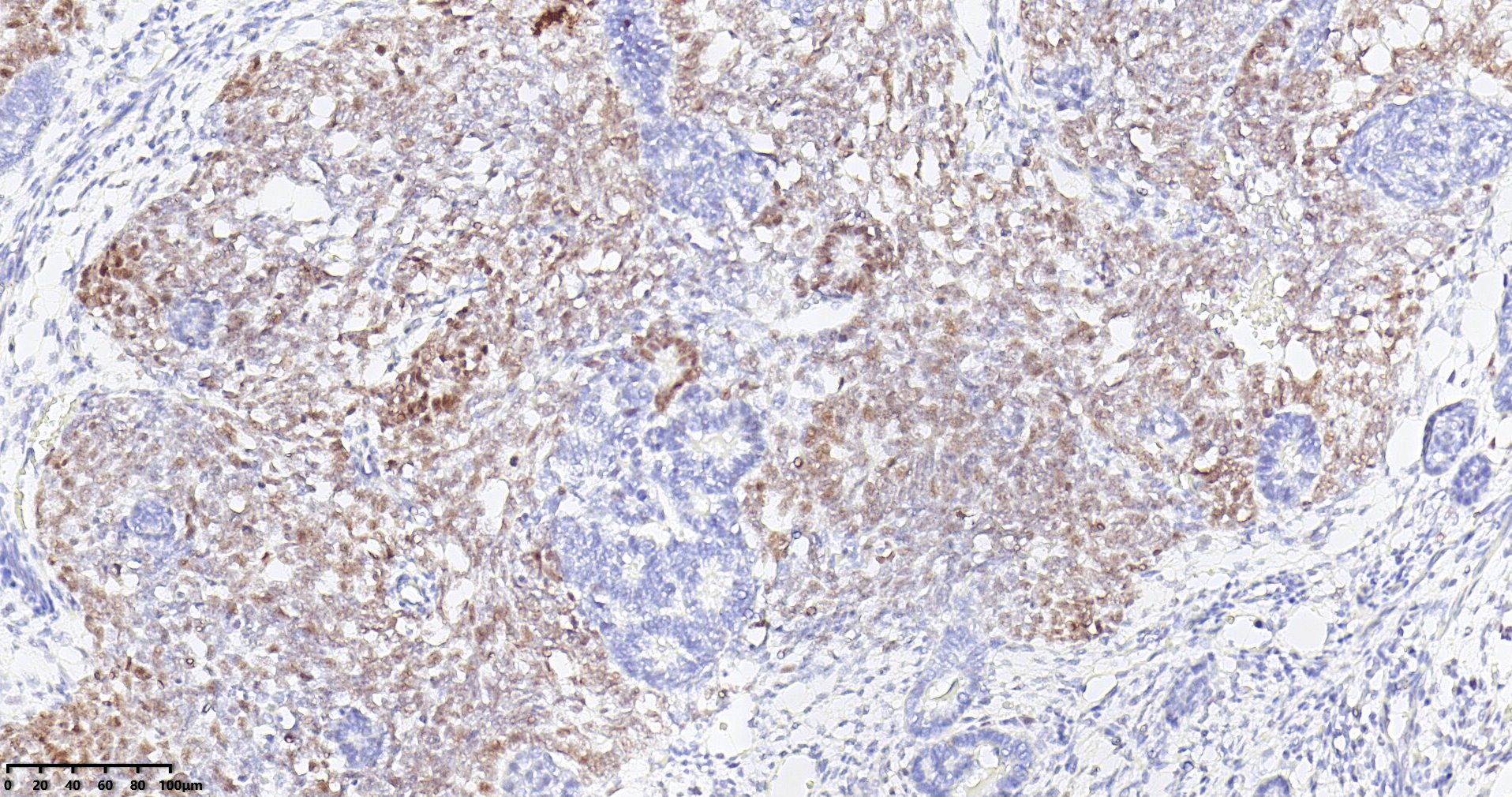
图4:肾母细胞瘤WT1在胚芽和少量上皮中细胞核阳性表达(图片来源作者)。
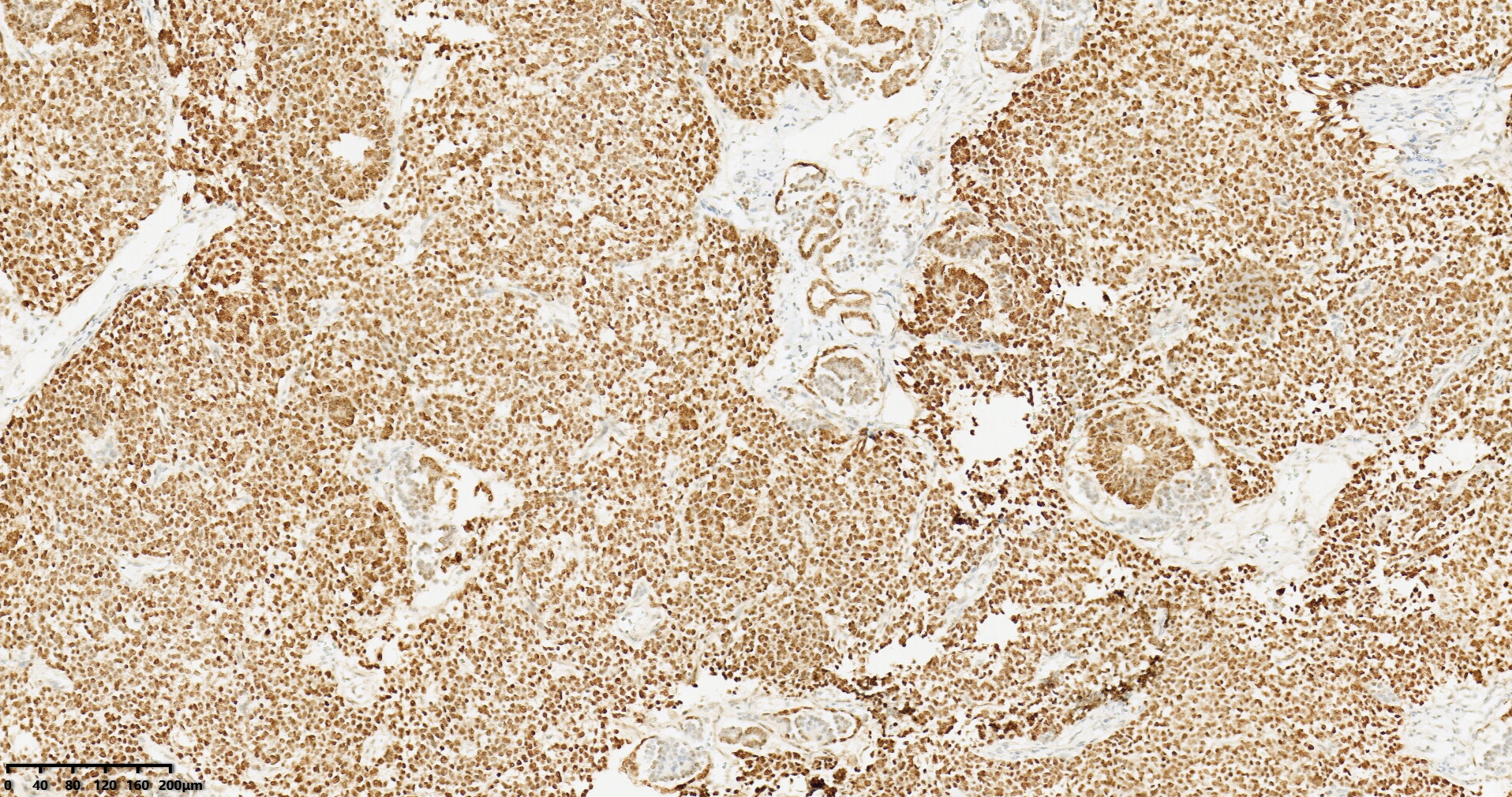
图5:肾母细胞瘤PAX2在胚芽和上皮中细胞核阳性表达(图片来源作者)。
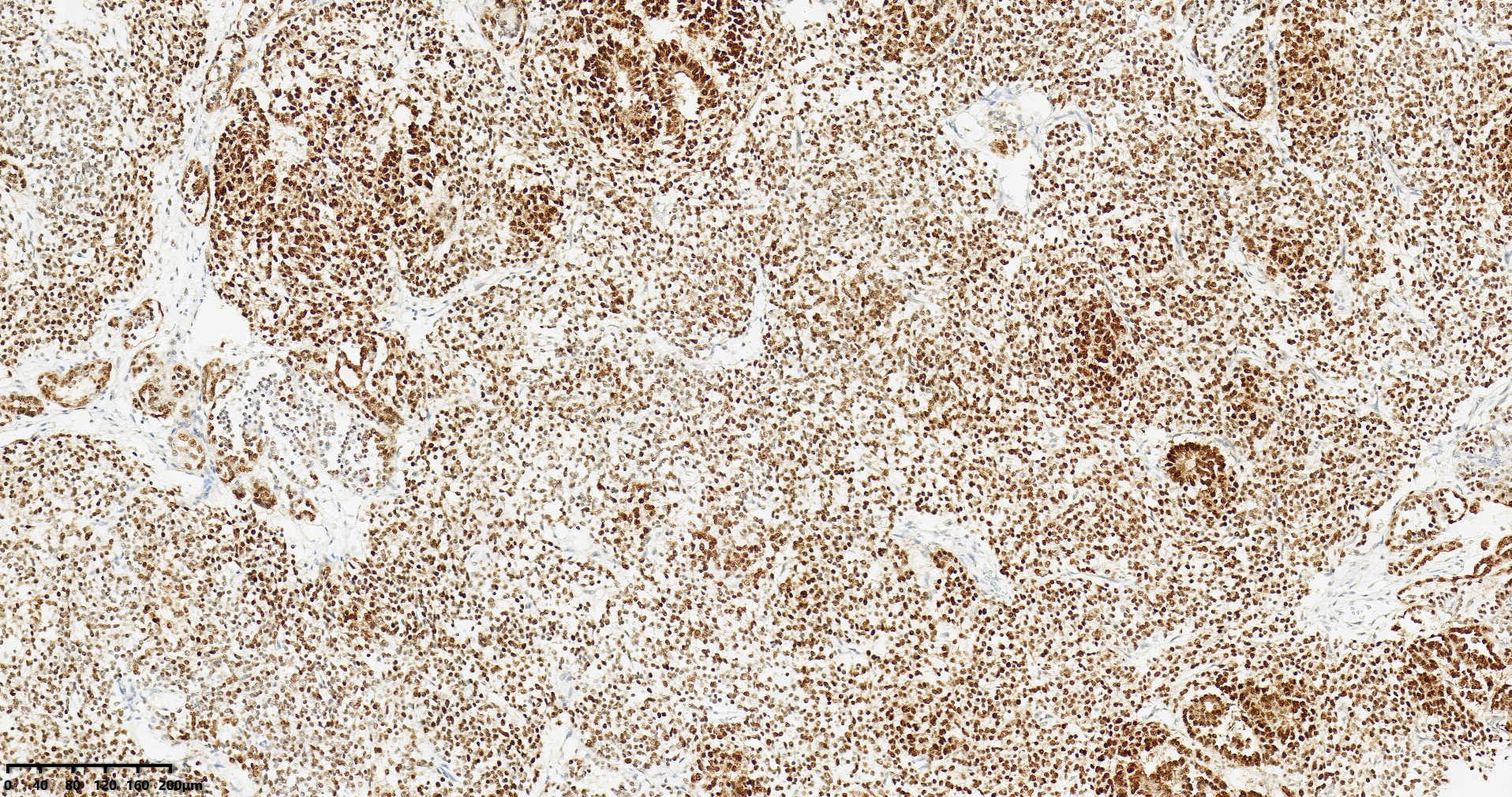
图6:肾母细胞瘤PAX8在胚芽和上皮中细胞核阳性表达(图片来源作者)。
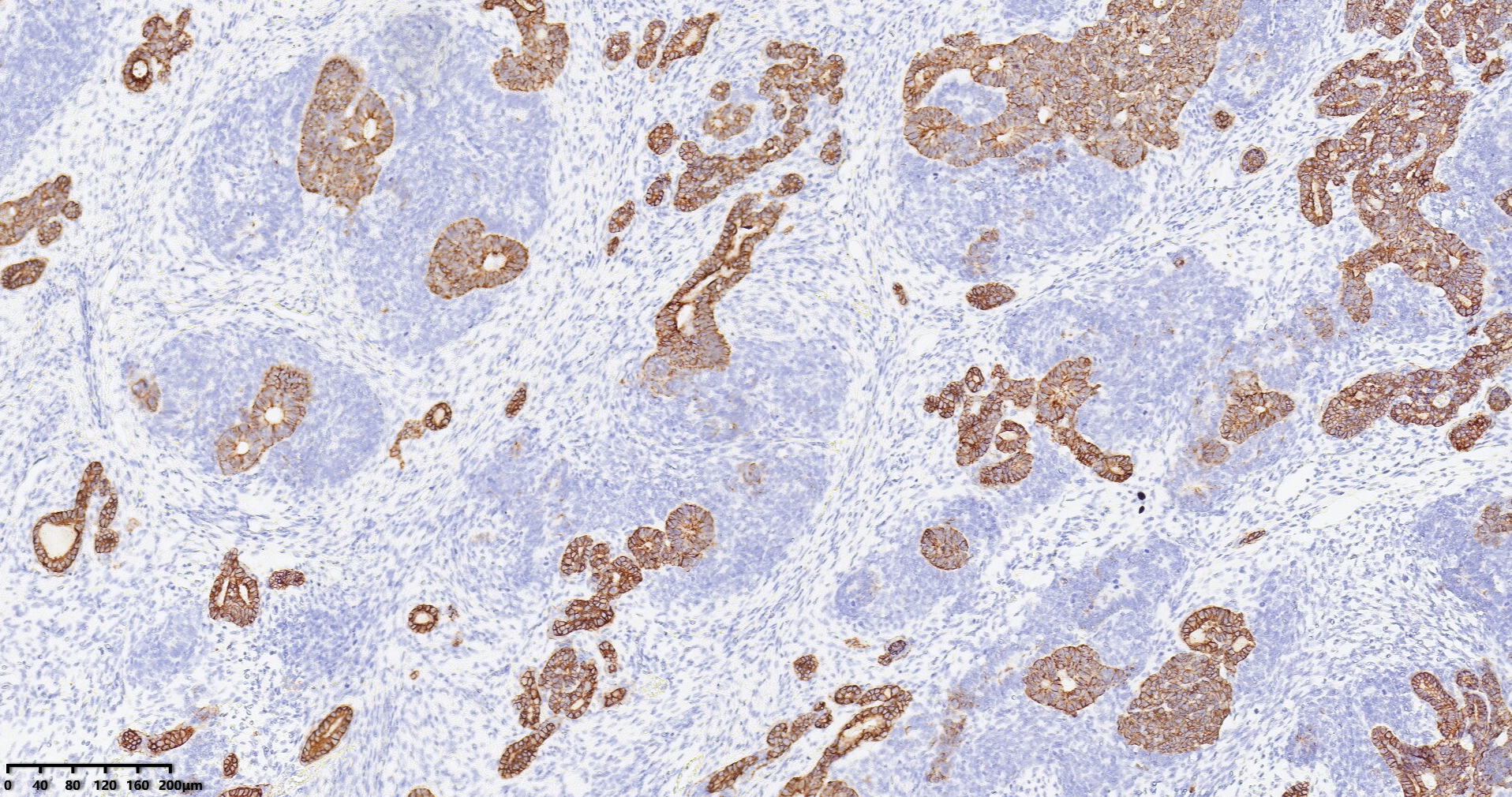
图7:广谱CK在肾母细胞瘤的上皮和少量胚芽中阳性表达(图片来源作者)。
分子病理学:WT没有特定的分子诊断标志物。然而,一些分子研究可以提供预后信息。拷贝数变化分析是风险评估的重要部分,因为1p和16q杂合性缺失以及1q获得被认为是预后不良的因素。此外,间变的存在与TP53突变有关,TP53突变分析可能有助于弥漫性间变性患者的风险分层。在儿童和成人WT中,已经描述了一组与BRAF p.V600 E突变相关的以上皮为主的WT。这些肿瘤显示出组织学上类似于后肾腺瘤的形态学。上皮型WT中的另一个亚群与TRIM28基因的胚系和体细胞突变有关。这种亚型通常发生在非常年幼的儿童中,预后良好。
治疗与预后:WT仍然是儿科肿瘤学成功治疗的典范,总体生存率约为90%。复发发生约15%,大多数在诊断后2年内复发。在COG和SIOP方案的两种主要治疗方法中,WT有几个预后因素不同。病理学/分子病理学评估肿瘤的作用至关重要,因为组织学和肿瘤分期是两组的重要预后因素。对肿瘤行为的遗传和分子理解的进展正在重新定义诊断和预后评估,从而实现更个性化的治疗方法。最近发表了对WT领域最重要的生物学发现的全面综述[1]。
参考文献
[1] Perotti D, Williams RD, Wegert J, et al. Hallmark discoveries in the biology of Wilms tumour. Nat Rev Urol. 2024 Mar;21(3):158-180.





















共0条评论