[导读] 作者:abin,崔艳梅
上期回顾
27岁女性,先做了左乳肿瘤粗针穿刺,后做了肿块切除术。
肿块最大径约1.3cm,有厚包膜的乳头状肿瘤,核异型性极显著,考虑包裹性乳头状癌(EPC)。但年轻女性的高级别EPC极罕见,所以签发了很保守的病理报告,开了免疫组化。
初步报告:(左侧乳腺)乳头状肿瘤,伴穿刺后改变。建议做免疫组化协助诊断:1#ER、PR、HER2、Ki67、calponin、SMA、p63、CK7、CK5/6、CD56。
接下来,需要解决几个重点问题:
1.识别浸润,形态学和肌上皮免疫染色相结合。
2.识别假浸润/穿刺后假象。
3.诊断命名与报告。
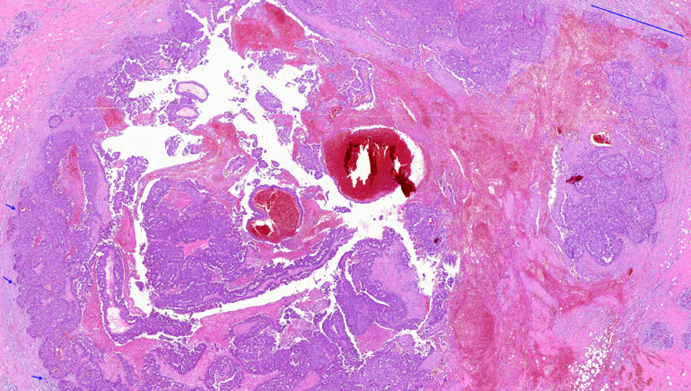
图1 免疫组化对照片,超低倍,示肿瘤主体。蓝色小箭头示肿瘤边缘可疑浸润,蓝色线段示穿刺边缘的假浸润(蓝色线段长约1.8mm)。
1. 识别浸润
《乳腺病理诊断难点》指出,识别间质浸润时,有4种情况可能成为诊断难题:微小浸润;假小叶结构;癌累及变形组织(如:组织假象,先前存在硬化性腺病等基础病变);以及膨胀性浸润。单个细胞或小簇细胞的微小浸润,常被遗漏;高分化癌成群或成巢团状浸润,伪装成小叶结构或腺病病灶;小团细胞浸润,非常类似被良性病变扭曲的腺体;大巢状浸润,很像被原位癌充盈膨胀的导管。
本例涉及微小浸润和膨胀性浸润。
1.1 微小浸润
识别微小浸润并没有特殊技巧,只能仔细观察。必要时加做CK和肌上皮免疫染色,一般能解决问题。
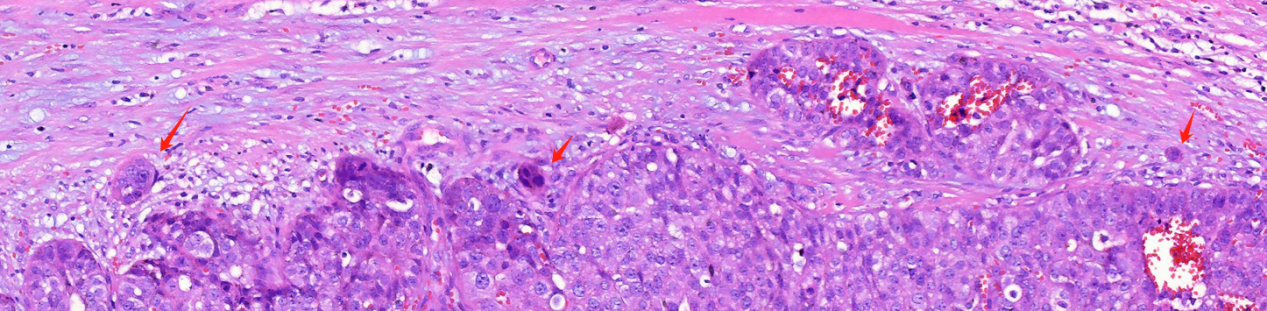 图2 低倍,红色箭头示肿瘤边缘可疑微小浸润
图2 低倍,红色箭头示肿瘤边缘可疑微小浸润
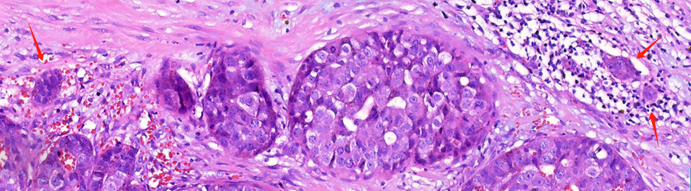
图3 中倍,红色箭头示肿瘤边缘可疑微小浸润
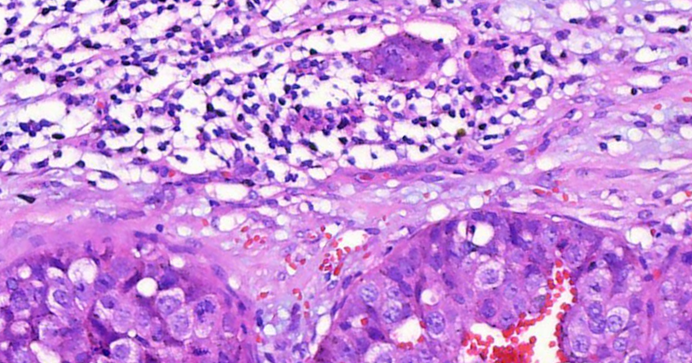
图4 高倍,示一处可疑微小浸润,周围有慢性炎症和水肿性间质反应。为了便于观察,图像已旋转至舒适状态。
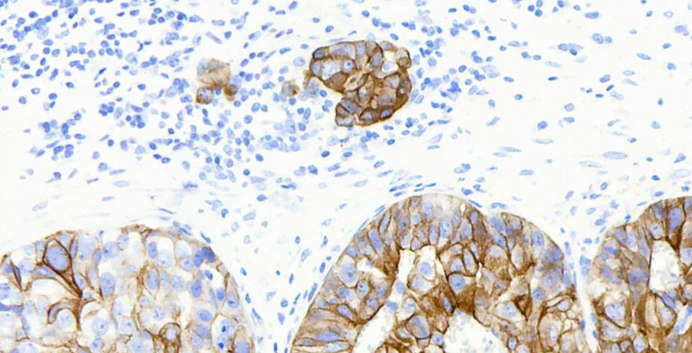
图5 借助CK7免疫染色,微小浸润显而易见。
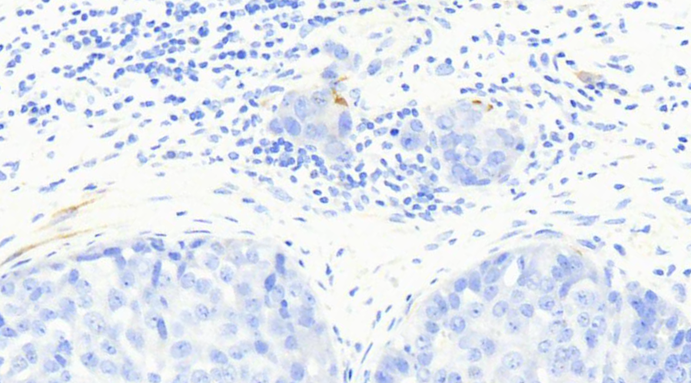
图6 calponin染色,微小浸润灶不伴肌上皮细胞。注意,除了染肌上皮外,肌纤维母细胞和平滑肌细胞也表达calponin,即,非特异性染色。真正的肌上皮染色应结合其本来位置,即,紧贴肿瘤边缘或正常导管腺上皮之外层,且有适当的染色强度,同时结合其他肌上皮标记物染色情况,综合判断。

图7 SMA特异性差,对肌上皮判读没有帮助。甚至癌细胞也表达SMA,这种现象并不少见,尤其是基底样亚型。
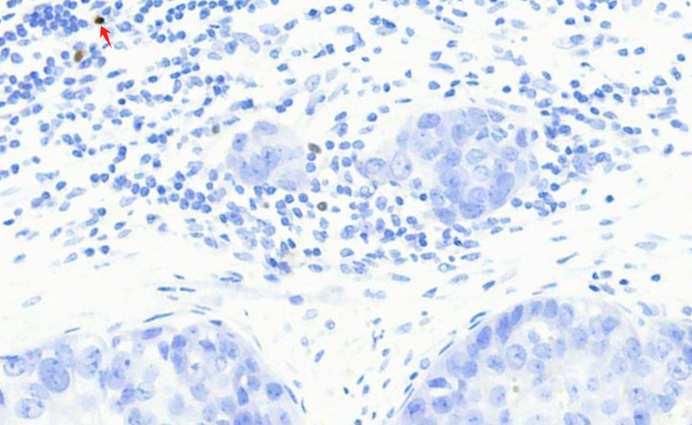
图8 P63未见肌上皮显色,注意炎症细胞的非特异性染色,
结论
肌上皮免疫染色证实了HE切片上观察到的肿瘤表面微小浸润。
1.2 膨胀性浸润/推挤性浸润
上面几图肌上皮染色同时观察到肿瘤边缘大部分区域肌上皮染色阴性,判断为推挤性浸润。
以下几图为仅有的几处calponin微弱显色,占比不到5%。再次强调,calponin显色不一定代表肌上皮,需结合阳性细胞的具体位置,排除纤维母细胞的干扰。
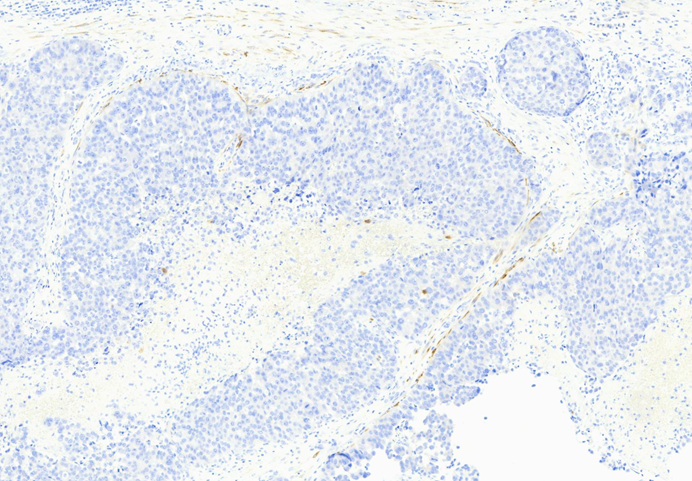
图9 此处calponin微弱显色。
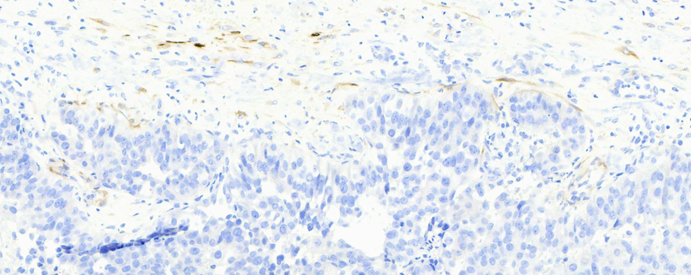
图10 此处calponin微弱显色。
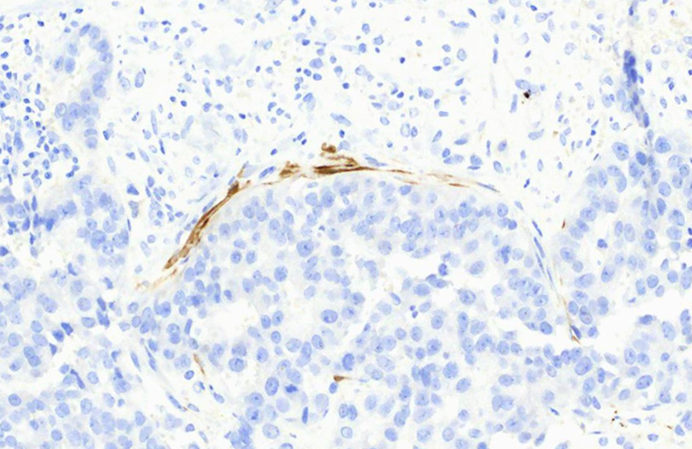
图11 此处calponin显色强度尚可,相当于内对照和外对照的染色强度。
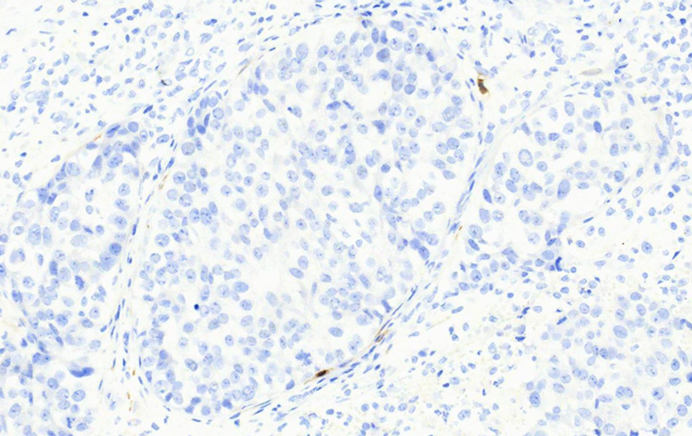
图11 此处calponin染色显示个别细胞阳性。根据位置判断,图下方中央是真正的肌上皮细胞。右上方另一个不是肌上皮细胞,可能是小血管。
1.3 传统型浸润
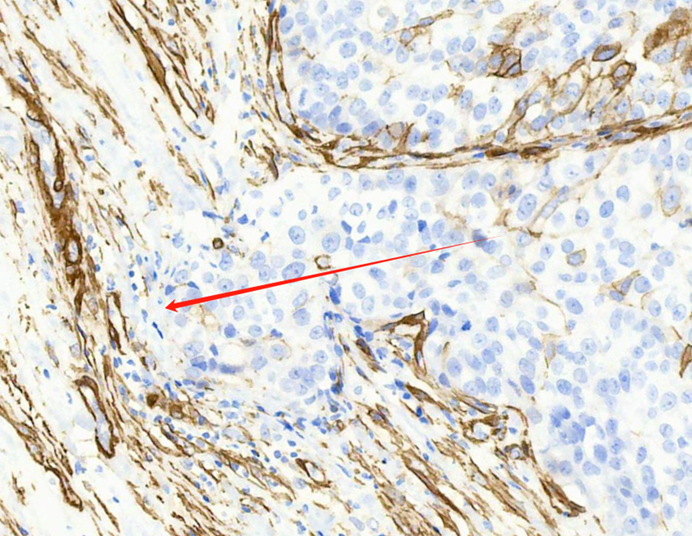
图12 传统型浸润是指明显的、破坏性浸润。上图为SMA染色,显示肿瘤细胞打断了纤维或肌纤维母细胞,形成传统型浸润灶。本例SMA特异性差和异常染色,对肌上皮识别没有帮助。但在这里有助于识别浸润。
小结
上述图文已证实数灶微小浸润、广泛膨胀性/推挤性浸润和小灶传统型浸润。
(未完待续)
往期回顾:
从粗针穿刺到切除活检:年轻女性高级别包裹性乳头状癌?(一)
从粗针穿刺到切除活检:年轻女性高级别包裹性乳头状癌?(二)


























共0条评论