[导读] 译者:慧海拾穗
往期回顾:
免疫组化在肾上皮性肿瘤诊断中的应用(一)
免疫组化在肾上皮性肿瘤诊断中的应用(二)
免疫组化在肾上皮性肿瘤诊断中的应用(三)
【透明细胞形态的肾肿瘤】
(5)嫌色肾细胞癌
一种相对常见的以透明细胞为主的肾细胞癌是嫌色肾细胞癌,这种细胞被认为是远端小管的润细胞(intercalated cell)。其经典型包含两种不同的细胞群,一种是具有突出细胞膜的大透明细胞,给人以植物细胞壁的印象,另一种是核周透亮的较小嗜酸性细胞(“空晕”=“halo”)(图7A)。这两种细胞类型都含有核膜不规则的细胞核。除了这些细胞学特征外,在大多数嫌色肾细胞癌中还存在一种实体生长模式,其透明血管系统由大多数大的透明细胞排列(图7A)。这种特征组合通常足以在没有免疫组化或分子研究的情况下进行诊断。然而,弥漫性CK7(图7B)和KIT(图7C)表达通常存在于嫌色肾细胞癌中,这在其他具有透明细胞的肿瘤类型中是非常不常见的。与透明细胞肾细胞癌相比,波形蛋白在嫌色性肾癌中始终呈阴性。较少使用的生物标志物是肾脏特异性钙粘蛋白(kidney specific cadherin)和小清蛋白(parvalbumin)。
【嗜酸细胞形态的肾肿瘤/Renal tumors with eosinophilic/oncocytic cytology】
(1)嗜酸细胞瘤和嫌色肾细胞癌
诊断具有嗜酸性细胞的肾肿瘤是泌尿生殖系统病理学中最具挑战性的领域之一。主要的鉴别诊断是嗜酸细胞瘤,它被认为是一种良性肿瘤,尽管它可能包含组织学上令人担忧的特征,如脂肪或血管受累。然而,嗜酸细胞瘤和几种恶性肿瘤之间存在形态学重叠,如嗜酸性嫌色肾细胞癌和琥珀酸脱氢酶缺陷型肾细胞癌。此外,到目前为止,单一的嗜酸性肿瘤的范围正在扩大,这些肿瘤基本上没有侵袭性,目前正在争论是否存在一个或多个不同的实体。一般来说,我们的方法是嗜酸细胞瘤应符合严格的形态学标准,包括温和的(bland)嗜酸性肿瘤细胞在水肿基质(edematous stroma)背景中形成大小不等巢(图7D),缺乏非典型特征,特别是核周空晕(perinuclear halo)或不规则核膜。核分裂象的确切阈值尚不确定;然而,大多数泌尿科病理学家会犹豫是否诊断出有1个以上易于识别的核分裂的嗜酸细胞瘤。阳性KIT标记(图7E),加上CK7的罕见、散在的肿瘤细胞标记(图7F)是嗜酸细胞瘤的特征,尽管包埋的良性小管也可能标记CK7。嗜酸性嫌色肾细胞癌(图7G)通常KIT呈阳性,并且通常显示CK7阳性数量大于嗜酸细胞瘤;然而,CK7阳性特定阈值尚未达成一致。这种模式通常在嫌色肾细胞癌的组织学变异型中持续存在,包括色素性微囊状和神经内分泌样嫌色肾细胞癌。波形蛋白除了在嗜酸细胞瘤的“中央瘢痕”区域染色外,在嗜酸细胞瘤和嫌色肾细胞癌中始终呈阴性。值得注意的是,CK7的标记在这些疤痕区域也通常增加。较少使用的标记包括HNF1β和S100A。这些在嗜酸细胞瘤中更常见阳性,而在嫌色肾细胞癌中HNF1β的标记较少,S100A1的标记很少。嗜酸细胞性乳头状肾细胞癌偶尔类似于嗜酸细胞瘤,但通常强表达AMACR,常阳性表达波形蛋白,CK7表达不一,缺乏KIT表达。
(2)琥珀酸脱氢酶缺陷型肾细胞癌
琥珀酸脱氢酶缺陷型肾细胞癌(SDH-RCC)可能是在细胞学上为温和的嗜酸性肾肿瘤中最具临床影响的鉴别诊断。它显示出特征性的嗜酸性细胞质,伴空泡和/或空泡状包涵体(vacuoles and/or bubbly inclusions),细胞核一致和细胞特征性形成实性片状或囊性生长模式。尽管这种温和的细胞形态和有被误诊为嗜酸细胞瘤的风险(图7H),SDH-RCC具有已知的转移潜力,并且它通常与胚系突变有关,胚系突变影响表达SDH酶亚基的基因之一(主要是SDHB,但也有SDHA和SDHC)。异常阴性的SDHB免疫组化(“丢失”)(图7I)似乎检测到大多数或所有缺陷性肿瘤,即使异常不在B亚基,由于酶复合物的不稳定。由于SDHB 免疫组化可能并非在所有实验室都可用,因此该诊断的其他免疫组化标记线索包括广谱角蛋白、CK7(甚至是散在的阳性细胞,通常阴性,与嗜酸细胞瘤相反)和KIT的常见阴性反应。值得注意的是,最近描述了罕见的低级别富马酸水合酶缺陷型肾细胞癌(FH-RCC),这可能是SDHB结果正常的类似SDH-RCC的肿瘤的考虑因素。
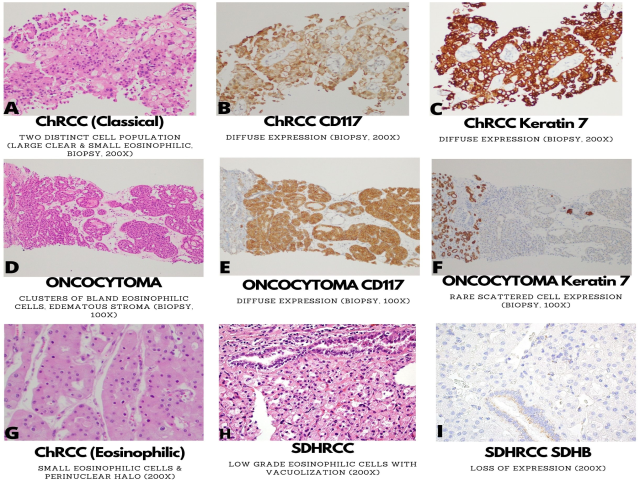
图7.嫌色肾细胞癌(ChRCC,经典型A-C;嗜酸细胞型G)、嗜酸细胞瘤(D-F)和琥珀酸脱氢酶缺陷型肾细胞癌的形态学和免疫表型特征(SDHRCC,H-I)。
【参考文献】
[1] Akgul M, Williamson S R.Immunohistochemistry for the diagnosis of renal epithelial neoplasms[J].Seminars in Diagnostic Pathology,2022.














共0条评论