[导读] 编译整理:强子
肺部神经内分泌肿瘤鉴别诊断
由于肺部神经内分泌肿瘤具有显著异质性,比如肿瘤内核分裂和坏死的分布不均一,因此其诊断难度较大,尤其活检标本中。实际上,肺部原发神经内分泌肿瘤在形态学方面会类似很多其他肿瘤,还要注意鉴别其他部位神经内分泌肿瘤的转移。虽然免疫组化有重要意义,但用于鉴别诊断的时候一定要仔细、谨慎,因为其他肿瘤也可能表达相关标记。
由于肺部神经内分泌癌临床表现为显著侵袭性、且一般难以手术切除,因此小标本(如小活检或细胞学)中准确诊断出来具有重要意义。这方面需要注意几种病种的鉴别诊断。
需要鉴别的病种之一是基底样鳞状细胞癌,其形态学可能和大细胞神经内分泌癌重叠,偶见与小细胞肺癌重叠。甚至罕见的情况下,这一肿瘤还会表达某些神经内分泌标记(尤其CD56);不过,弥漫、强阳性表达鳞状标记(p40、p63、高分子量CK-34βE12)还是支持基底样鳞状细胞癌的诊断。
另一个需要鉴别的病种是SMARCA4缺陷型未分化肿瘤,也会和大细胞神经内分泌癌存在某些形态学的重叠,且可能也会表达神经内分泌标记,尤其伴挤压假象的时候更是鉴别困难。这种情况下,免疫组化SMARCA4(BRG1)表达完全缺失则支持诊断;不过,一定要注意的是,约25%的SMARCA4缺陷型未分化肿瘤中这一标记是表达显著降低、而不是完全缺失。从临床来说,一定要区分出这一病种和神经内分泌癌,因为前者对于化疗高度耐药,但可能会对针对SWI/SNF复合体的靶向治疗有效。
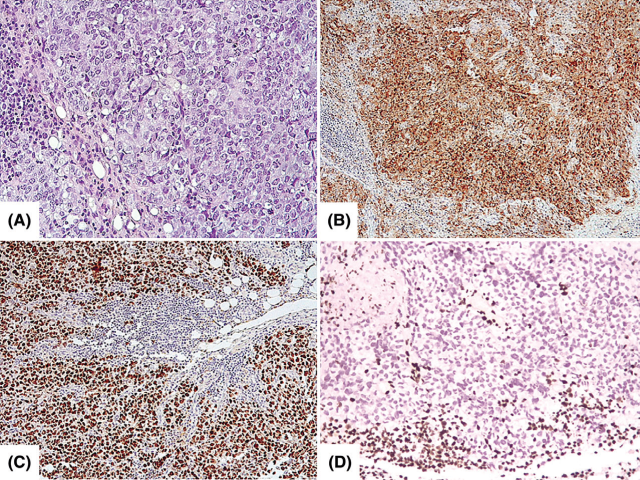
图6.SMARCA4缺陷型未分化肿瘤,在高级别神经内分泌癌鉴别诊断中可能是一个陷阱。这一肿瘤呈实性生长,细胞为中等至较大表现,细胞核形态相对单一,染色质空泡状,有显著核仁(A);与高级别神经内分泌癌一样,Syn可有明显表达(B);罕见情况下,还会有TTF1的表达(C)。SMARCA4(BRG1)细胞核表达完全缺失,是诊断这一病种的线索(D;肿瘤旁的小淋巴细胞着色作为阳性内对照)。本例免疫组化不表达CK(CK7、CK20、AE1/AE3),且SMARCA2(BRM)细胞核表达缺失,也支持为SMARCA4缺陷型未分化肿瘤。
小细胞肺癌的鉴别诊断中一定要注意NUT癌,即以存在NUTM1基因重排这一分子特征为定义的低分化癌。与小细胞肺癌一样,NUT癌一般为小细胞、呈巢状及片状生长,细胞形态单一,可有坏死。此外,可能会有CgA、Syn甚至TTF1的表达,更是使得鉴别诊断困难,尤其小活检标本中。细胞间距均匀、细胞核无铸型样特点、突然角化,都支持NUT癌。此外,NUT癌一般表达广谱CK、p63、p40和NUT抗体,这和小细胞肺癌是不同的。
形态学类似肺部神经内分泌癌的其他病种还有小圆细胞肉瘤、黑色素瘤、淋巴瘤、Merkel细胞癌,不过这些病种在免疫组化层面都比较容易的区分出来。肺部的类癌还要注意鉴别转移性神经内分泌肿瘤,尤其来源于胃肠胰腺部位者。某些形态学特征(如胃肠胰腺来源者更常见腺样结构)和某些免疫组化标记有助于鉴别。OTP(orthopedia homeobox protein)阳性提示倾向于肺来源;相反,CDX2或PAX8阳性分别倾向于肠嗜铬样细胞来源及胰腺来源。结合临床表现,还可以加做胃泌素或五羟色胺免疫组化:胃泌素阳性,支持在胃窦或十二指肠上段存在产胃泌素的神经内分泌肿瘤;五羟色胺一般表达于阑尾或空肠-回肠处的神经内分泌肿瘤,罕见情况下肺部神经内分泌肿瘤也有表达。
更重要的是,存在转移性(IV期)神经内分泌肿瘤的情况下确定原发部位是非常关键的。IV期的肺类癌少见情况下会类似胃肠胰腺处的神经内分泌肿瘤。为避免过诊断为神经内分泌癌,病理医师一定要了解:转移的情况下,肺类癌的核分裂计数、尤其是Ki-67增殖指数会显著高于原发灶,Ki-67增殖指数有时甚至超过30%。不过,IV期肺类癌中Ki-67增殖指数的精确预后意义和治疗意义还不完全清楚。因此,目前WHO建议对这种病变命名为“转移性类癌,非特指”,无需指出是典型类癌还是非典型类癌,但要报告Ki-67增殖指数及核分裂计数,报告有无坏死。
——全文完——
往期回顾:
肺部神经内分泌肿瘤病理-干货版(一)
肺部神经内分泌肿瘤病理-干货版(二)














共0条评论