[导读] 编译整理:强子
引言
病理的魅力在于“不讲理”。比如随着临床应用的增多,此前认为高度敏感和特异的相关免疫组化标记会逐渐发现也程度不等的表达于其他组织和病变。如果不了解这一知识点,可能会导致病理诊断中的误诊误判,尤其应用于转移性肿瘤原发部位判断的场景下。
2024年,美国MD Anderson癌症中心病理专家Donthi等人曾在《Cancer Cytopathol》杂志发表研究,提出此前认为乳腺特异性的免疫组化标记TRPS1可表达于多种非乳腺肿瘤。这一结果对于转移性肿瘤原发部位判断来说具有重要意义。为帮助大家更好的了解相关知识点并应用于临床实践,我们将该文要点编译介绍如下。
研究内容及结果
TRPS1为乳腺癌发生所必需的谱系特异性转录抑制因子,在肿瘤细胞存活和增殖过程中发挥重要作用。比如已有研究证实,TRPS1对于所有遗传学亚型乳腺来说,其敏感性为86%,且对于三阴型乳腺癌敏感性更高。
虽然文献中早已有原发非乳腺肿瘤可表达TRPS1的报道,但该标记在转移性乳腺癌与非乳腺癌鉴别中的表达情况还并不清楚。对于转移性肿瘤、多原发性肿瘤、或原发灶不明的患者来说,临床实践中常通过免疫组化确定原发灶,加之细胞学标本免疫组化检测有其独特优势,因此本文原作者利用细针穿刺抽吸和积液标本制作细胞块,评估了TRPS1在源自乳腺、苗勒管、肺、胃肠道及胰腺转移性肿瘤时的敏感性与特异性。
该研究共计纳入160例细胞学标本,其中细针穿刺抽吸127例,积液标本33例。细针穿刺标本中,原发部位为乳腺者35例,苗勒源性者25例,肺来源36例,胃肠道和胰腺来源31例。33例积液标本中,源自乳腺者18例,苗勒源性者12例,肺来源1例,胃肠道来源2例。关于病变部位及病种方面的更多细节,请移步原文。
TRPS1的表达方面,53例转移性乳腺肿瘤中阳性表达者有51例(96%):除两例经细针穿刺检测的ER阳性转移性乳腺癌病例外,其余所有乳腺肿瘤(包括9例三阴性转移性乳腺癌)的TRPS1检测结果均呈阳性。
107例其他部位来源的转移性肿瘤中TRPS1阳性表达者也有28例(26.2%)。其中最大一组为转移性苗勒源性肿瘤,37例标本中有20例(54%)结果为阳性,具体包括12例细针穿刺抽吸标本、8例积液标本。12例TRPS1阳性的细针穿刺抽吸标本中,转移性卵巢浆液性癌6例,转移性癌肉瘤1例,子宫的子宫内膜样腺癌2例,未分类的苗勒源性肿瘤3例。8例TRPS1阳性的积液标本中,转移性卵巢浆液性癌4例,子宫的子宫内膜样腺癌1例,未分类的苗勒源性癌3例。
TRPS1阳性的其他部位来源转移性肿瘤中,第二常见的一组为肺肿瘤,37例标本中7例(19%)阳性,其中6例为细针穿刺抽吸标本,1例为积液标本。细针穿刺抽吸标本中,5例为腺癌,1例为鳞癌;积液标本的1例为腺癌。
14例转移性胰腺肿瘤中,有1例(7%)TRPS1阳性;转移性胃肠道肿瘤中,未见TRPS1阳性表达。
图例赏析
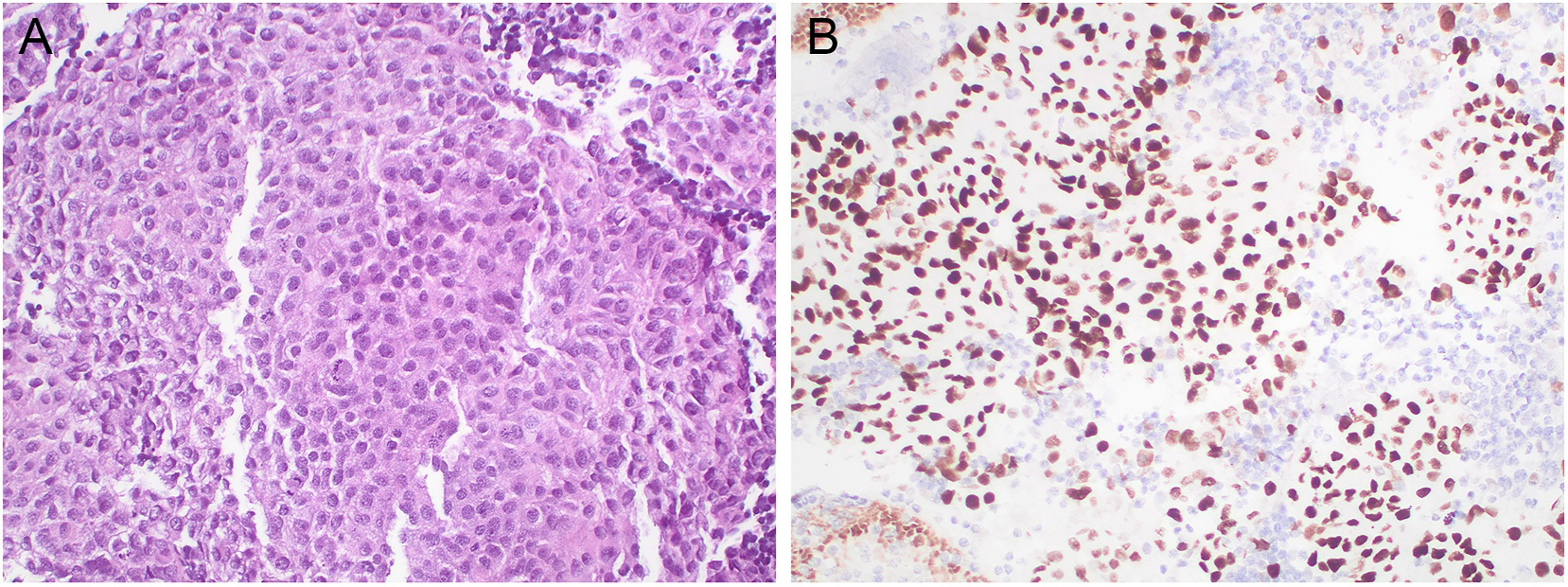 图1.转移性乳腺癌,右侧腋窝淋巴结细针穿刺抽吸标本细胞块,免疫组化TRPS1呈弥漫、强阳性表现。
图1.转移性乳腺癌,右侧腋窝淋巴结细针穿刺抽吸标本细胞块,免疫组化TRPS1呈弥漫、强阳性表现。
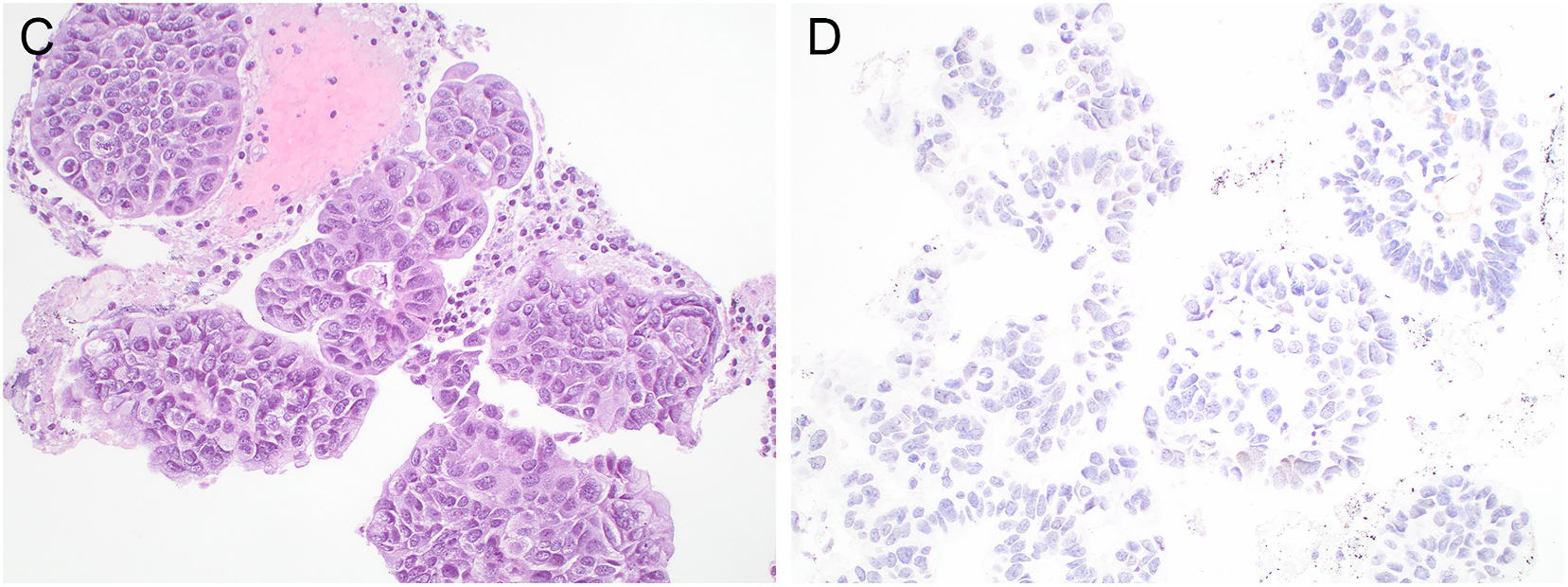 图2.转移性乳腺癌,左肺叶间淋巴结细针穿刺抽吸标本细胞块,免疫组化TRPS1为完全阴性。
图2.转移性乳腺癌,左肺叶间淋巴结细针穿刺抽吸标本细胞块,免疫组化TRPS1为完全阴性。
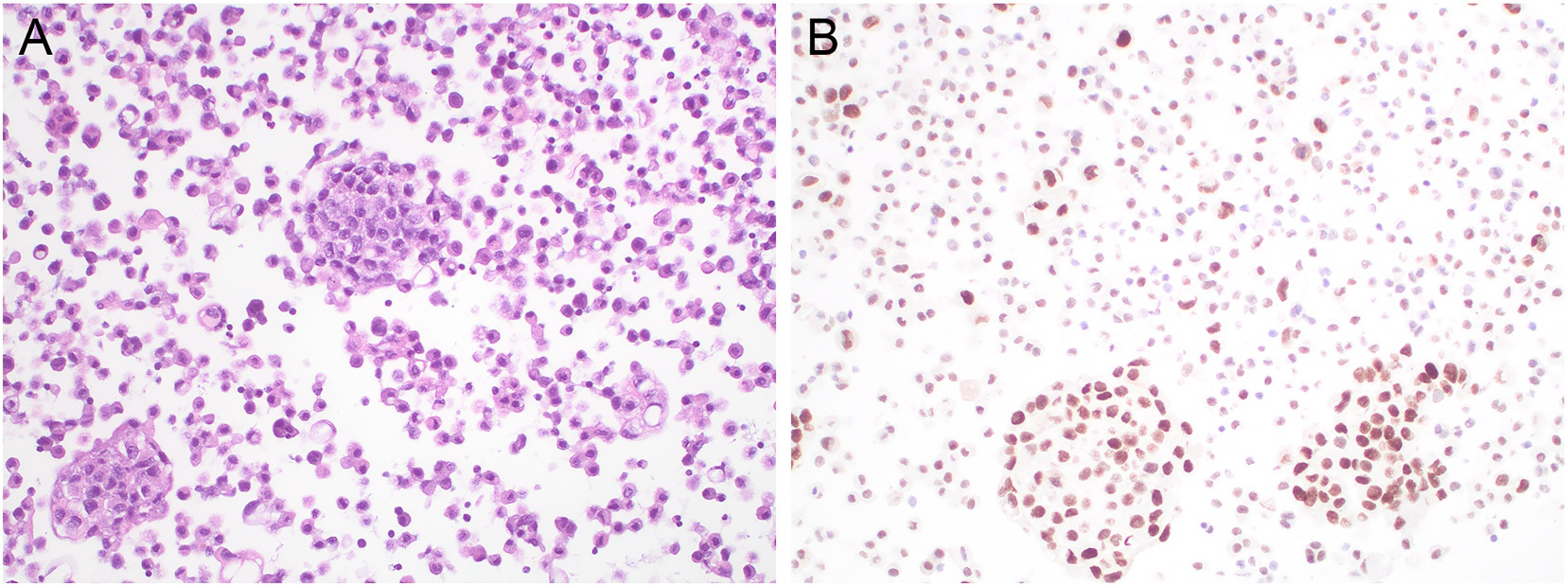 图3.转移性乳腺癌,胸腔积液标本细胞块,免疫组化TRPS1在肿瘤细胞为强阳性,但间皮细胞也有弱阳性着色。
图3.转移性乳腺癌,胸腔积液标本细胞块,免疫组化TRPS1在肿瘤细胞为强阳性,但间皮细胞也有弱阳性着色。
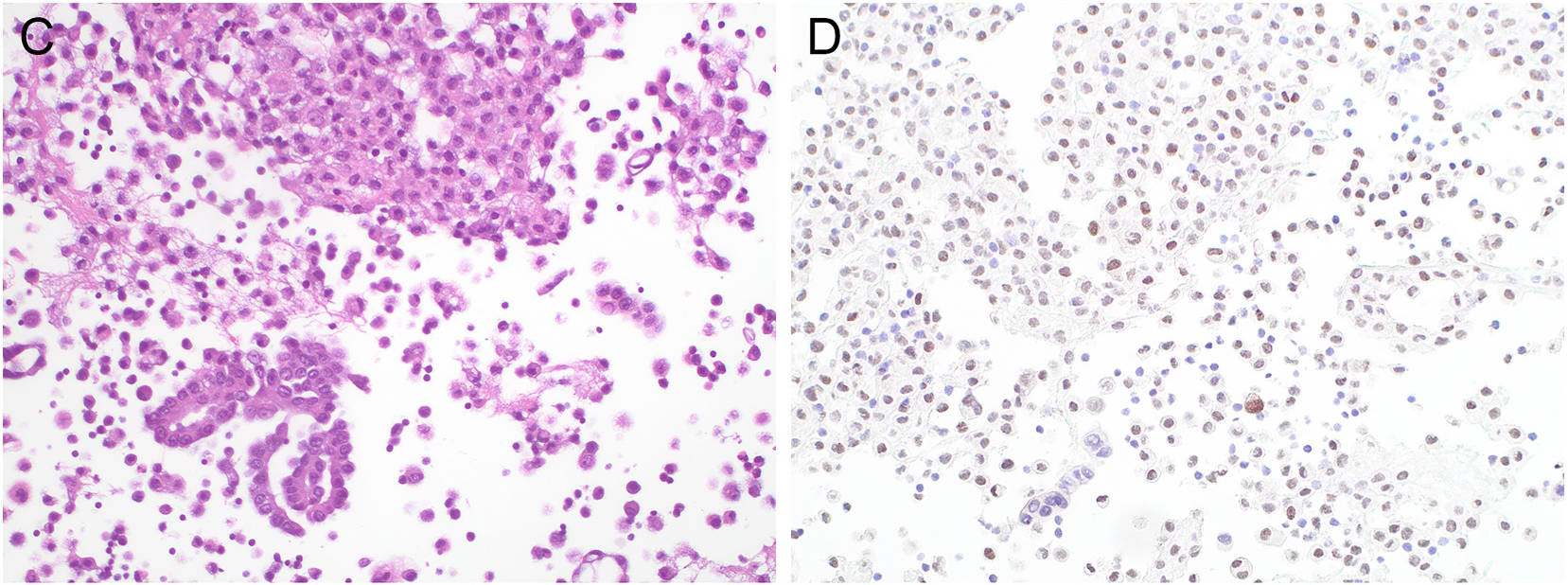 图4.转移性肺癌,胸腔积液标本细胞块,免疫组化TRPS1在肿瘤细胞为阴性,但间皮细胞有弱阳性着色。
图4.转移性肺癌,胸腔积液标本细胞块,免疫组化TRPS1在肿瘤细胞为阴性,但间皮细胞有弱阳性着色。
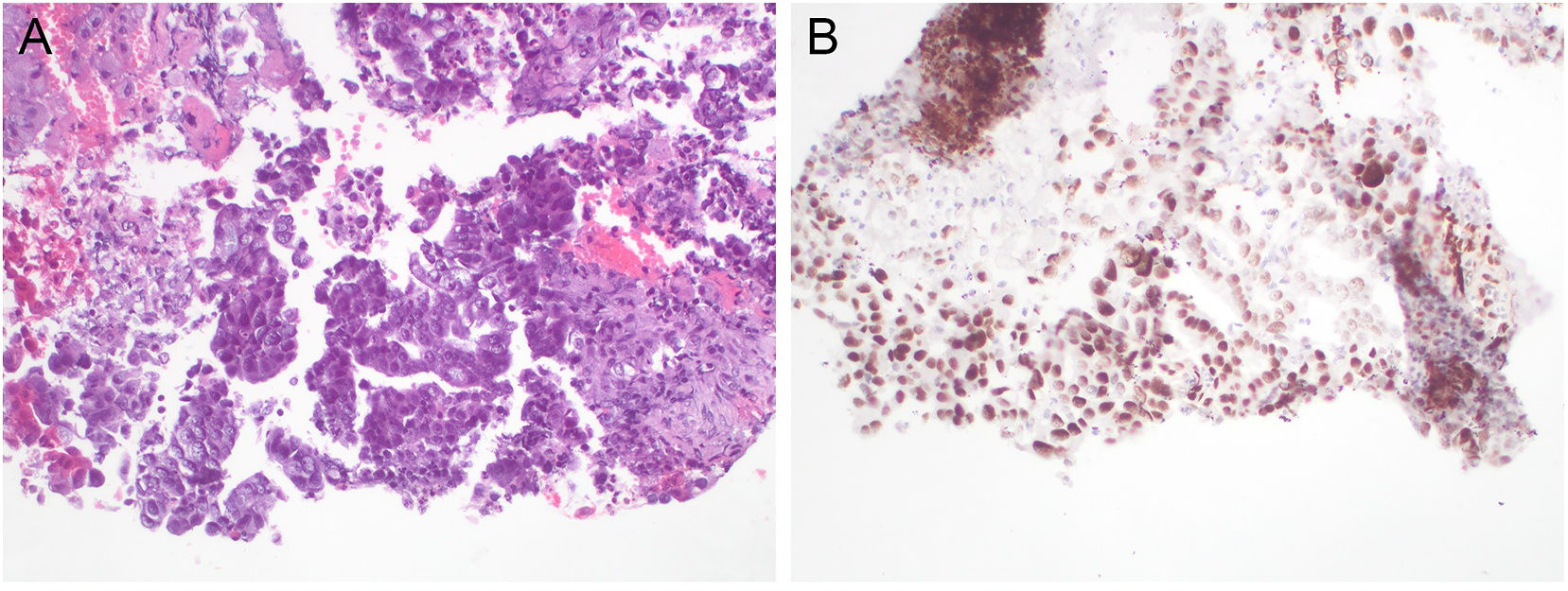 图5.转移性苗勒源性癌细针穿刺抽吸细胞块标本,免疫组化TRPS1,几乎所有肿瘤细胞都呈强阳性。
图5.转移性苗勒源性癌细针穿刺抽吸细胞块标本,免疫组化TRPS1,几乎所有肿瘤细胞都呈强阳性。
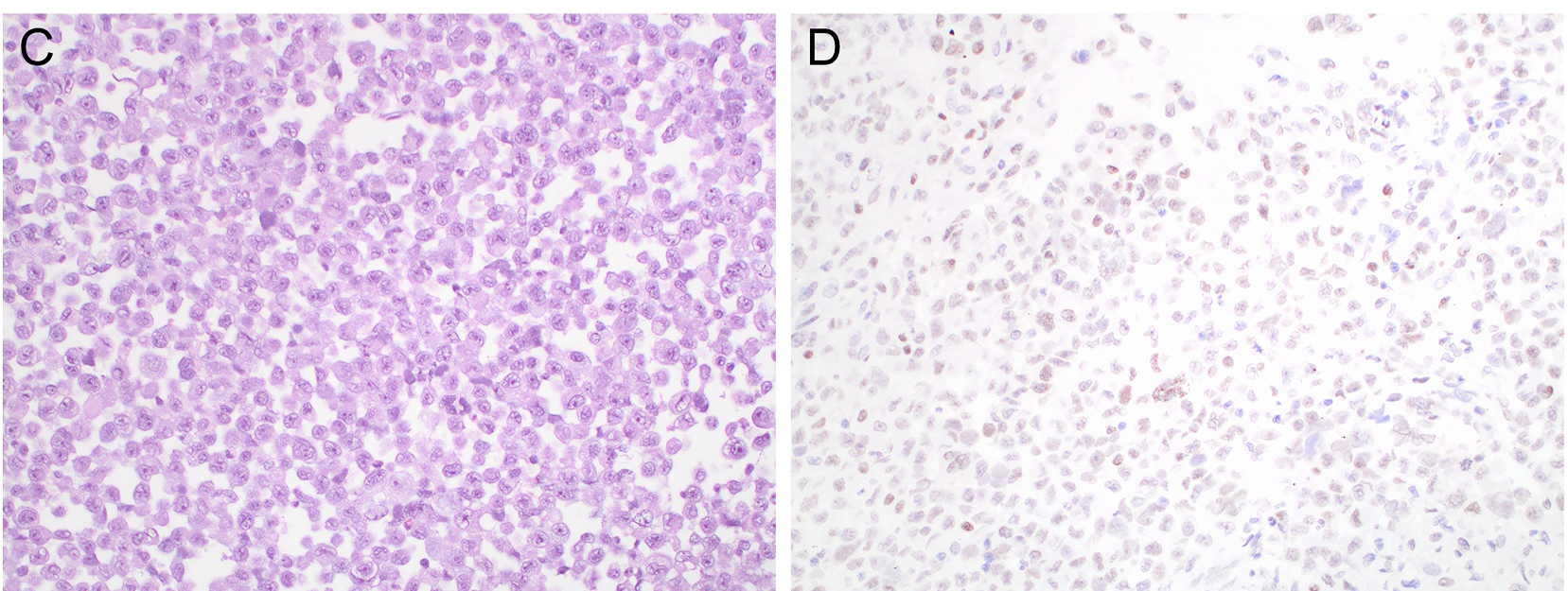 图6.转移性肺腺癌细针穿刺抽吸细胞块标本,免疫组化TRPS1,几乎所有肿瘤细胞都为弱至中等阳性。
图6.转移性肺腺癌细针穿刺抽吸细胞块标本,免疫组化TRPS1,几乎所有肿瘤细胞都为弱至中等阳性。
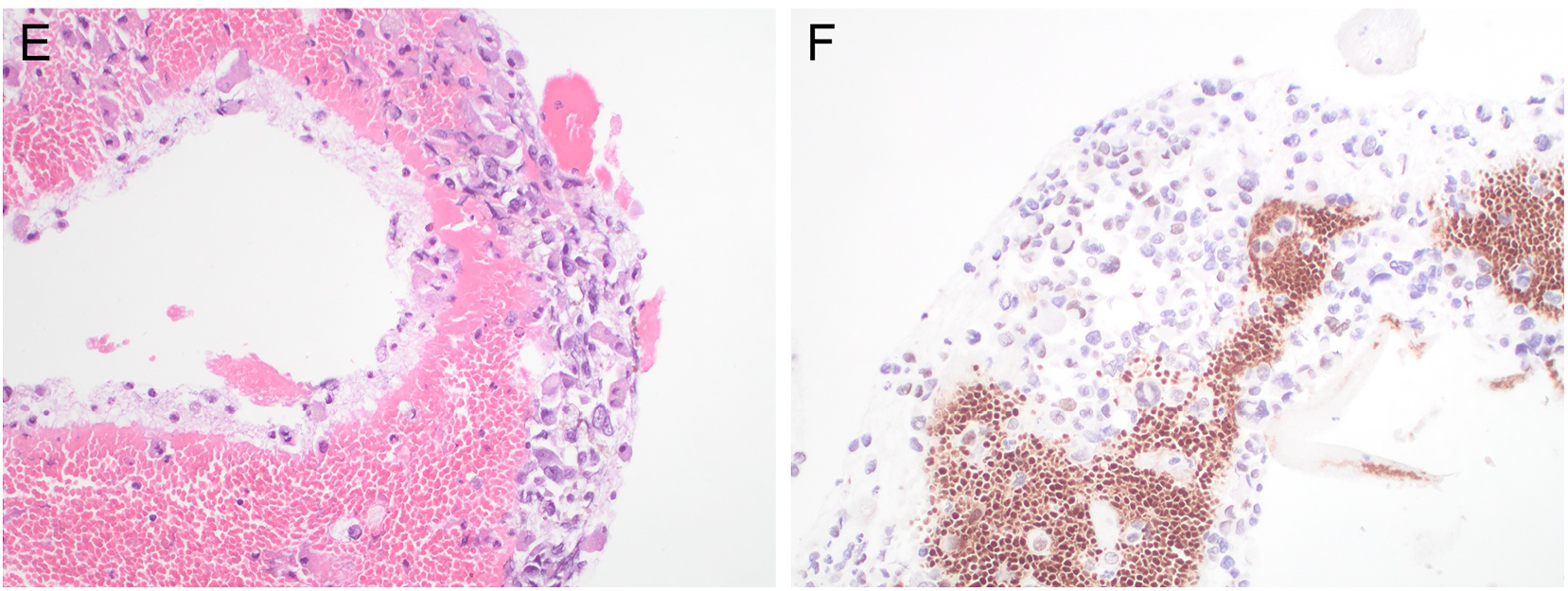 图7.转移性胰腺癌细针穿刺抽吸细胞块标本,免疫组化TRPS1,部分肿瘤细胞呈强阳性。
图7.转移性胰腺癌细针穿刺抽吸细胞块标本,免疫组化TRPS1,部分肿瘤细胞呈强阳性。
小结
作为乳腺来源判断依据的免疫组化指标TRPS1总体敏感性较高,但由于在非乳腺肿瘤中也有表达,因此其特异性较低。必须充分认识TRPS1在转移性乳腺肿瘤与非乳腺肿瘤中的表达范围,以避免错误判断转移性肿瘤的组织起源。
全文完
点此下载原文献
参考文献
Donthi D, Gan Q, Ding QQ, Krishnamurthy S. Trichorhinophalangeal syndrome 1 expression in breast and nonbreast metastases from Müllerian, lung, gastrointestinal tract, and pancreatic primary tumors by immunohistochemistry with cytology cell block specimens. Cancer Cytopathol. 2024;132(12):799-808.
doi:10.1002/cncy.22901




















共0条评论