[导读] 作者:尤明月
透明性肾细胞癌,也叫肾透明细胞癌(Clear Cell Renal Cell Carcinoma, ccRCC),是肾脏最常见的一种恶性肿瘤,占所有肾癌的70%–80%。近年来,它在全球的发病率还在逐渐上升,每年新发病例超过40万。
ccRCC起源于肾近曲小管的上皮细胞,特点是血管特别丰富,也很容易发生转移。所谓“透明细胞”,指的就是在显微镜下这些癌细胞的胞质显得透亮。下面我们结合两个实际病例来看一下。
病例1 男 44岁
肉眼所见:灰白灰红色结节样物一枚,大小3*2.5*2cm,包膜完整,上覆部分肾组织,面积2*1.3cm,切面灰白灰黄色,质稍韧
镜下所见:
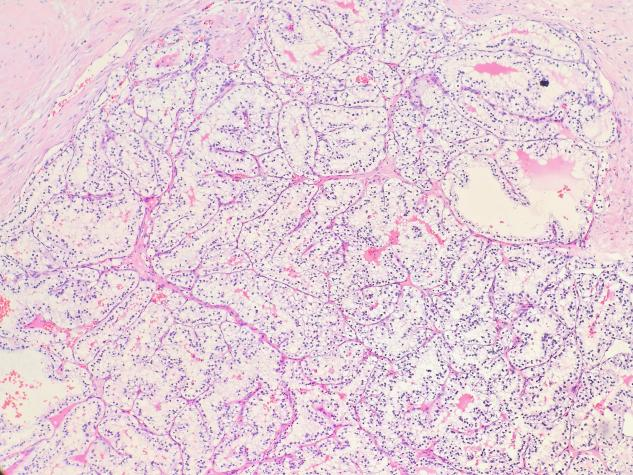
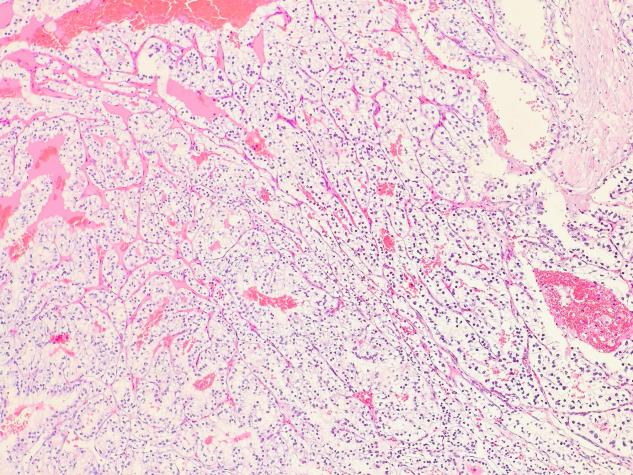
低倍镜(×40)下,可见肿瘤细胞呈巢团样分布,腔隙间有纤细的毛细血管网分割,肿瘤细胞成分较一致,胞质透明。
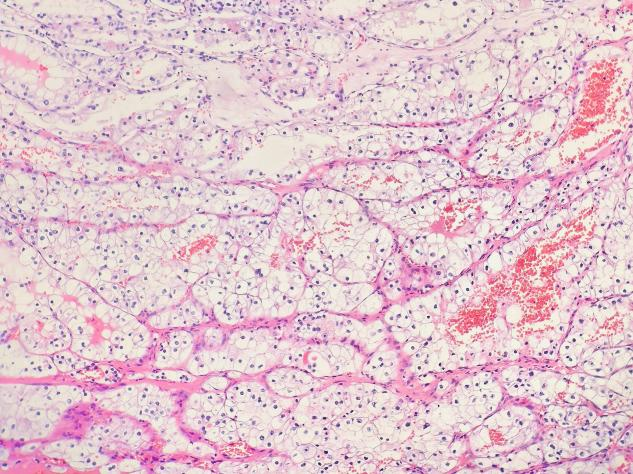
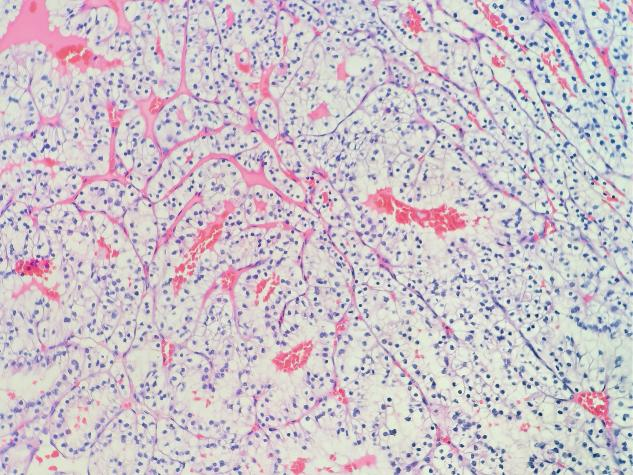
中倍镜(×100)下能更清楚看到,细胞体积大、核小,胞质透明,细胞核呈圆形或卵圆形,挺一致的,也看不到明显核仁。
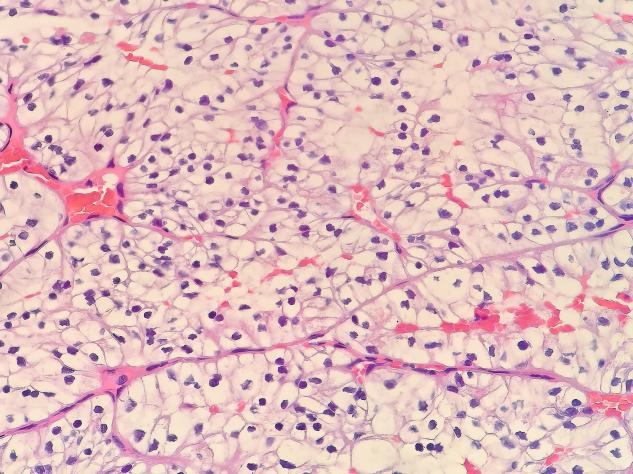
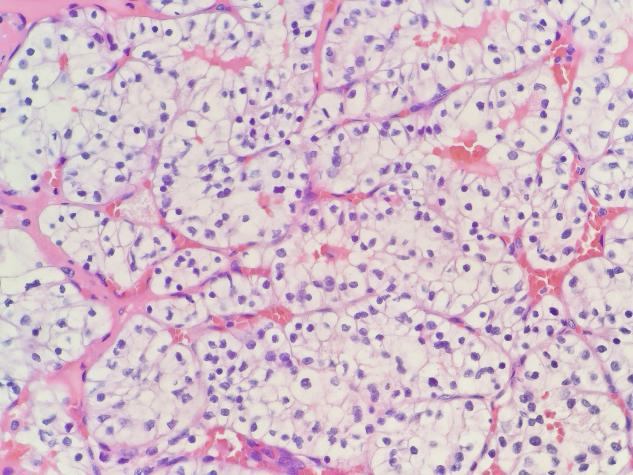
高倍镜(×400)下,依然能看到巢团状排列和纤细的血管网。细胞核大小和红细胞差不多,核仁不明显。
按照国际泌尿病理学会(ISUP)的分级标准,这个病例在400倍下核仁不明显,我们把它分为1级。
病理诊断:
右肾透明细胞癌,ISUP核分级1级,肿瘤未侵出肾被膜,断面阴性
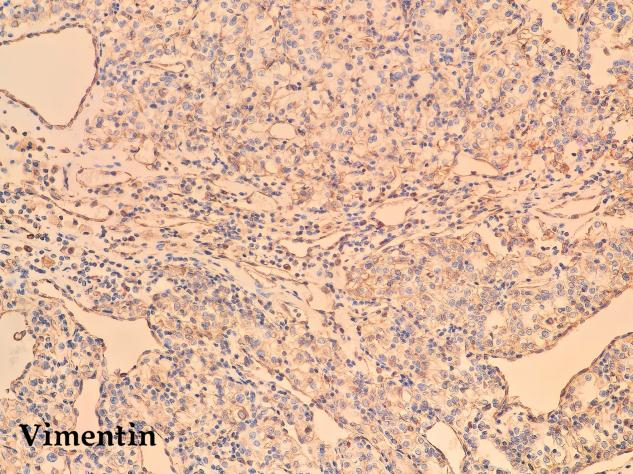
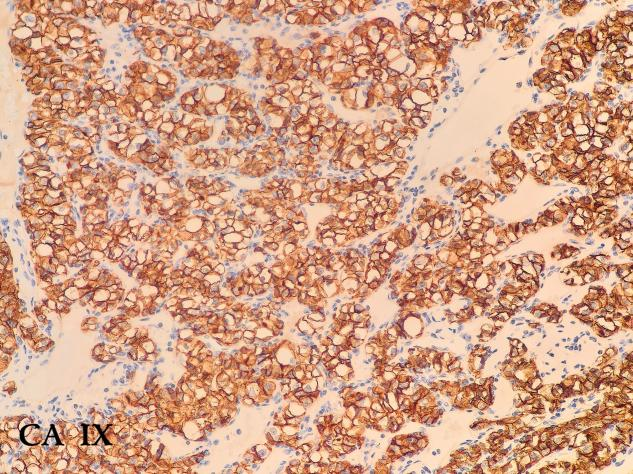
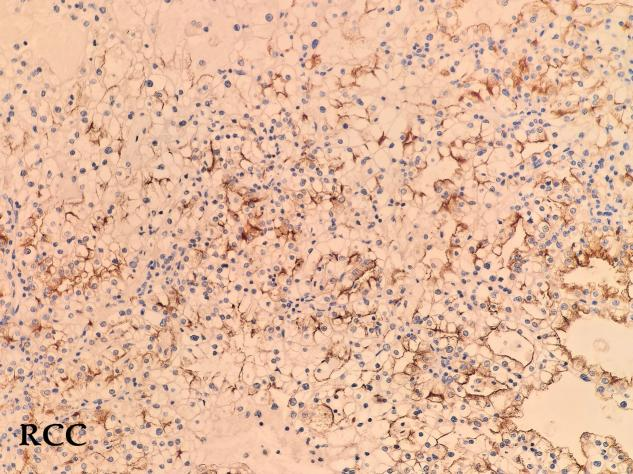
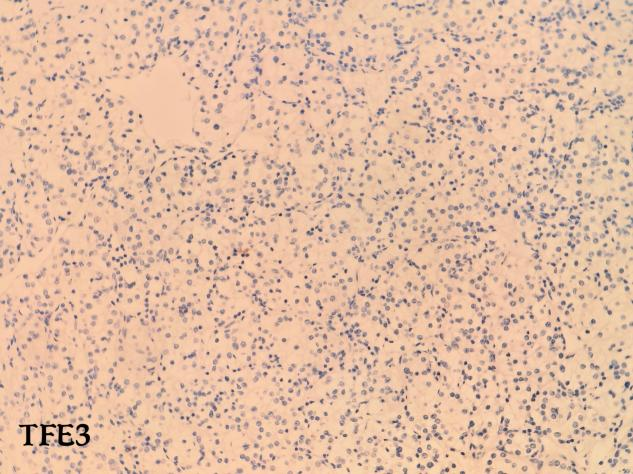
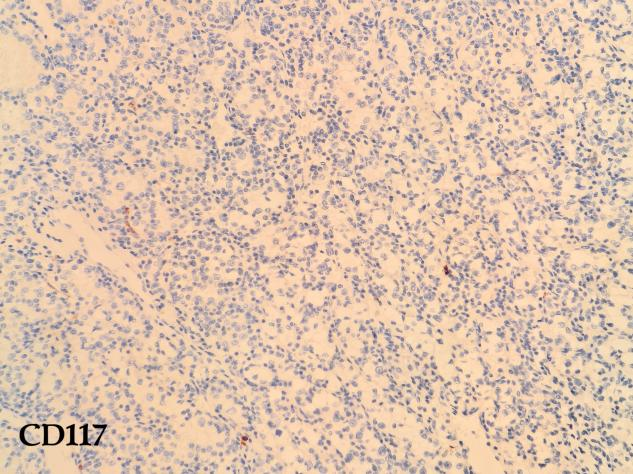
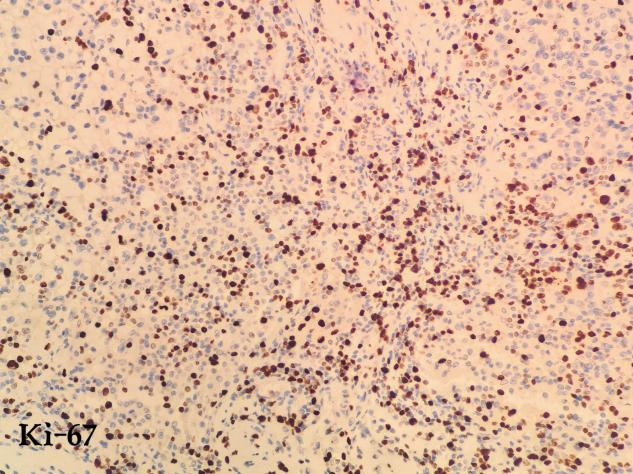
免疫组化结果:CD10(+)、CA IX(+)、HNF1β(+)、Pax-8(+)、Vimentin(+)、p504s(+)、CD117(-)、TFE3(-)、RCC(部分+)、Ki-67(+10%)
病例2 男 53岁
肉眼所见:肾脏及周围脂肪组织,大小为14*7.5*4.5cm,其中肾脏大小12*7*4.5cm,输尿管长7cm,最大直径0.5cm,切开肾脏下极紧邻被膜见一灰黄色肿块,大小为5.5*4*3.3cm,切面灰黄灰褐色,局部有出血,质地软,界清;余肾红棕色,皮髓质分界清,质地中,肾周脂肪组织内未触及明显淋巴结。
镜下所见:
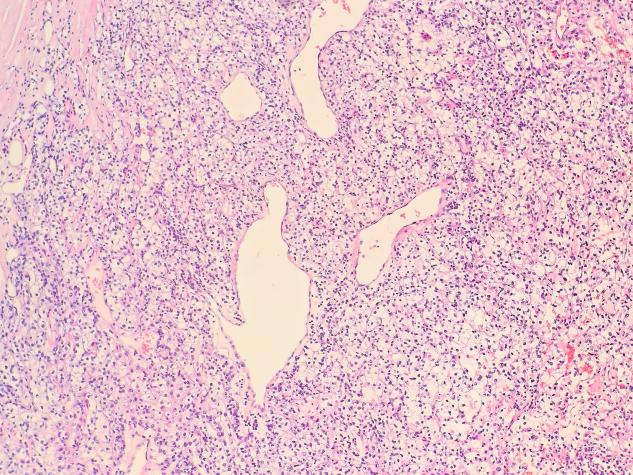
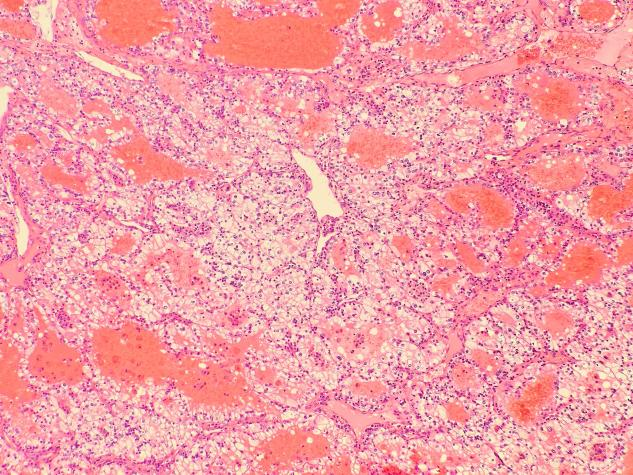
低倍(×40)下,部分区域肿瘤细胞排列得比较密,呈实性片状,还伴有不少出血。
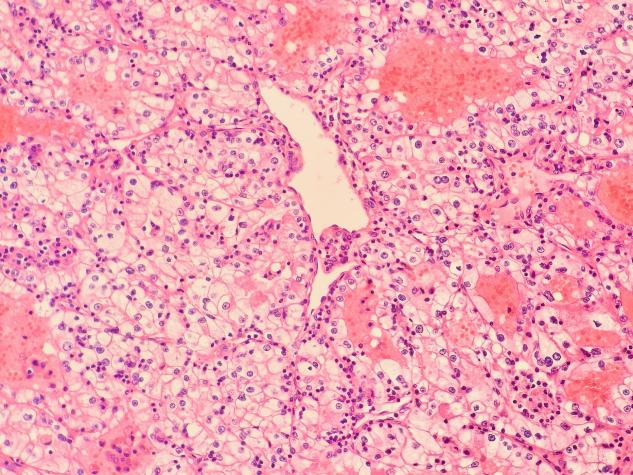
中倍镜(×100)下,细胞核稍增大,细胞胞质透明,细胞核呈圆形或卵圆形,核仁若隐若现
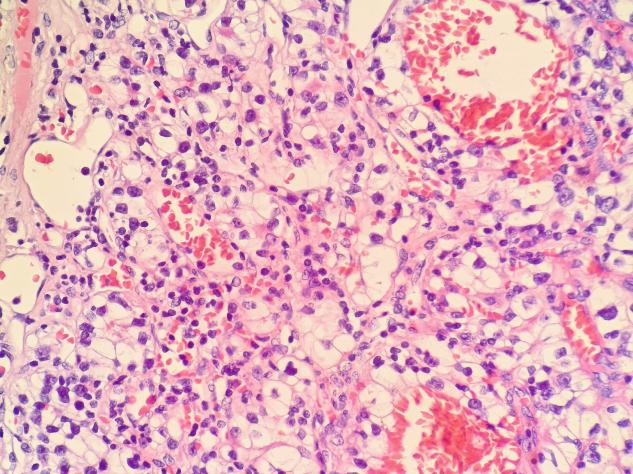
高倍镜(×400)下,肿瘤细胞核稍增大,细胞核大小不一,部分细胞核大小差不多是红细胞的2-3倍,未见明显的嗜酸性核仁。
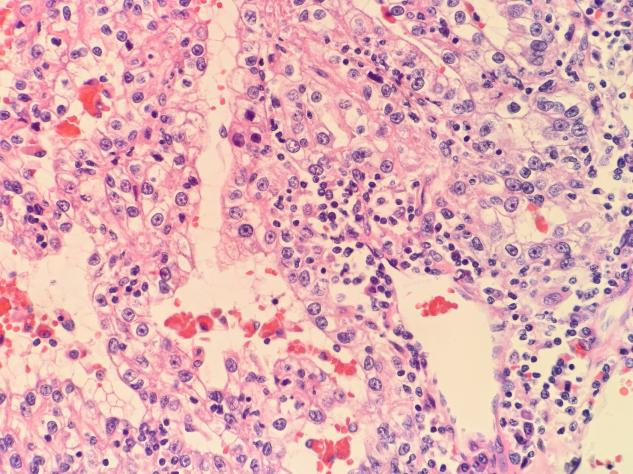
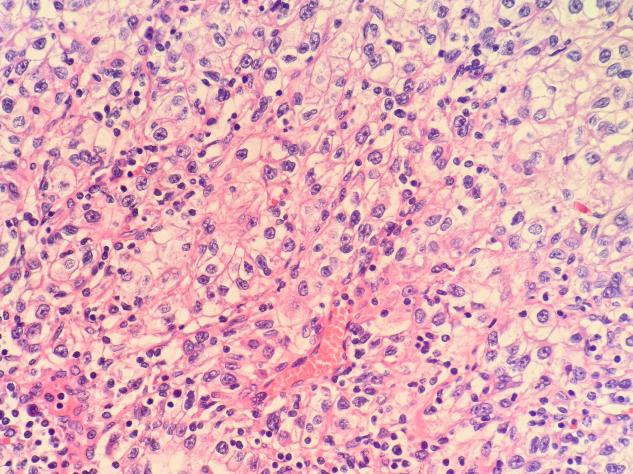
高倍镜(×400)下,肿瘤细胞核变大了,圆形或卵圆形,胞浆有些嗜酸性。细胞核大小差不多是红细胞的3–4倍,能看到明显的嗜酸性核仁。
这个病例在400倍下核仁非常明显,符合ISUP 3级。
病理诊断:
肾透明细胞癌,ISUP核分级3级,肿瘤未侵犯肾窦脂肪及肾盂黏膜,未侵犯肾周脂肪。
神经侵犯(-),脉管癌栓(-)。
输尿管切端和脉管切端均(-)。
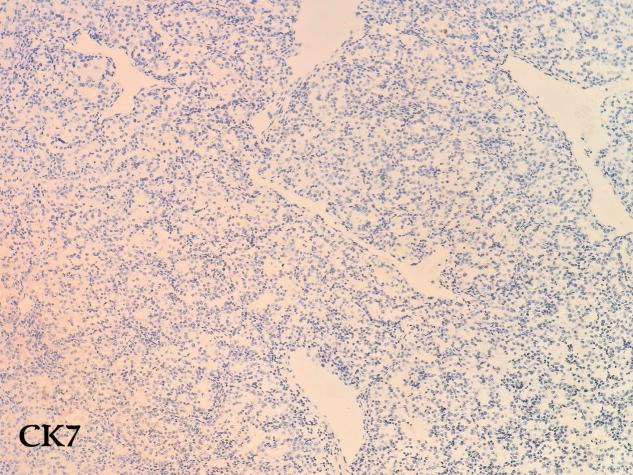
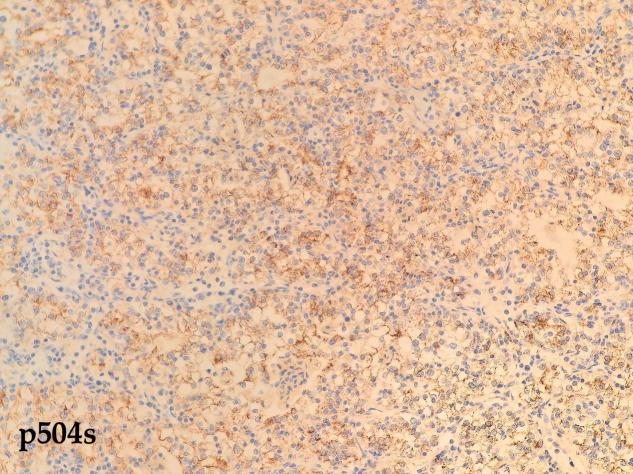
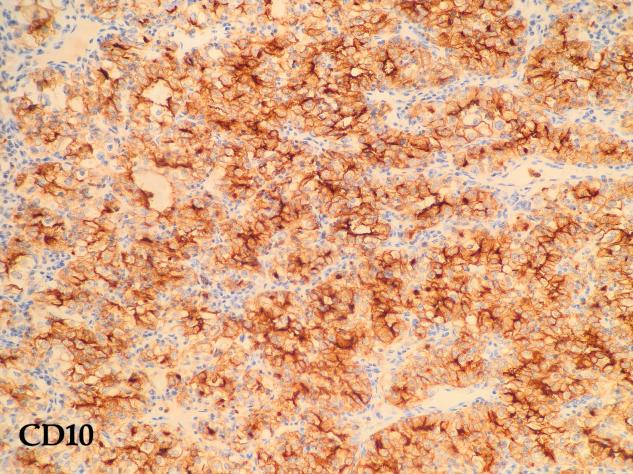
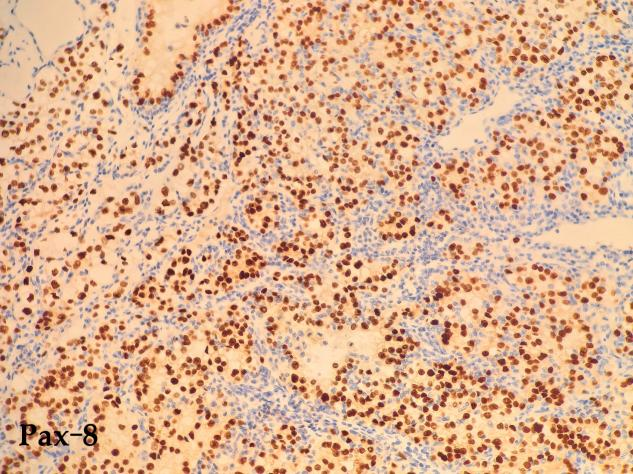
免疫组化结果:CD10(+)、CA IX(+)、CK7(-)、HNF1β(+)、Pax-8(+)、Vimentin(+)、p504s(+)、CD117(-)、TFE3(-)、RCC(部分+)、Ki-67(+60%)
讨论
一、发病机制:VHL基因是关键
ccRCC的发生和一个叫VHL的抑癌基因关系密切。如果VHL基因失活了(比如突变、缺失或者被甲基化“沉默”了),就会导致缺氧诱导因子HIF-α堆积。接下来,它就会激活VEGF、PDGF这些促血管生成的因子,还有GLUT1这类代谢相关基因——结果就是肿瘤疯狂长血管、拼命用糖酵解供能。
大约90%的散发性ccRCC都存在VHL基因异常。除此之外,3号染色体短臂上的其他基因,比如PBRM1、SETD2、BAP1等也常常发生突变,这些突变不仅和不同的分子亚型有关,还影响患者的预后。
ccRCC还有很多表观遗传层面的异常,比如全基因组低甲基化、某些基因启动子却高甲基化。组蛋白修饰相关基因突变也会改变染色质结构,促进癌变。在代谢方面,肿瘤细胞大量用糖、堆脂质和糖原,形成我们看到的“透明”胞质。
二、谁容易得?有什么表现?
ccRCC好发于中老年人,如果年纪比较轻就发病,要警惕是不是遗传性的癌症综合征,比如VHL综合征。男女发病率差别不大。
临床表现五花八门。大概一半多的患者是通过体检做影像学偶然发现肾脏有个肿块,自己没什么感觉。以前经典的“肾癌三联征”——血尿、腰痛、腹部包块——现在其实不多见了(不到10%),而且一旦出现,往往提示已经不是早期。
另外,20%–30%的患者可能伴有副肿瘤综合征,比如:
· 贫血
· 高血压
· 乏力或恶病质
· 高钙血症
· 肝功能异常
· 红细胞增多症
如果发生转移,可能会出现骨痛、咳嗽、气短这些症状。不幸的是,大概25%–30%的患者在第一次确诊时就已经发生了转移,最常见的转移部位是肺、骨、肝、脑和肾上腺。
三、病理长啥样?
3.1 肉眼观
肿瘤往往是肾内一个孤立的、边界清楚的团块,切面金黄色、多彩斑斓(因为含脂质和糖原多),常伴有出血、坏死或囊性变。大的肿瘤可能会侵犯肾周脂肪、肾上腺或者集合系统。
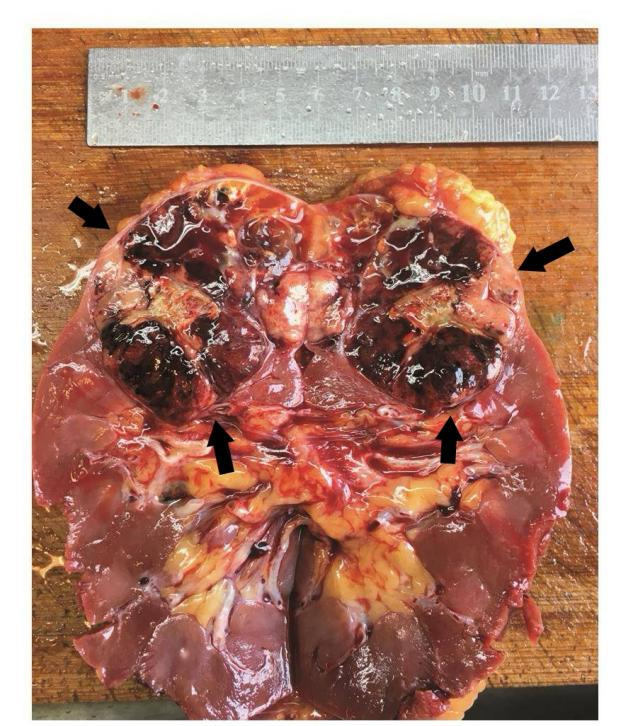
肿瘤起自肾皮质,界限清楚,切面呈五彩状(来源于临床病理诊断与鉴别诊断---泌尿及男性生殖系统疾病)
很多肿瘤周围还有一层纤维假包膜,说明它长得比较慢。大约5%–10%的病例可以是多中心或双侧发生,这类要多考虑遗传背景。
3.2 组织学特点
经典的ccRCC由一片透明细胞组成,细胞边界清楚,胞质透亮或略带嗜酸性,细胞核圆圆的、核仁不明显。肿瘤细胞排成巢状、腺泡状或者实性片状,之间是丰富的薄壁血管网。
3.3 免疫组化有啥用?
免疫组化在鉴别诊断中特别有用:
· 阳性标记:CA-IX(碳酸酐酶IX)是最特异的,几乎90%以上的病例都是弥漫强阳性。PAX8、CD10、RCC marker、Vimentin也常阳性。
· 阴性标记:通常不表达CK7(可和嫌色细胞癌、乳头状癌区分)、CD117(鉴别嫌色细胞癌)、TFE3(鉴别Xp11易位癌)。
· 还有些新的标志物像HIF-α、GLUT1、BNC1等也逐渐在用。
3.4 如何分级?
现在普遍用的是ISUP/WHO核分级系统(2016),根据核的形态从1到4级:
· 1级:核小、圆,核仁不明显(400倍下看不见)
· 2级:核稍大、稍不规则,核仁能看见但不突出(400倍下可见)
· 3级:核中等大小,异型性明显,核仁清晰(100倍就能看见)
· 4级:核极度异型,出现多形性、巨核,甚至肉瘤样或横纹肌样分化
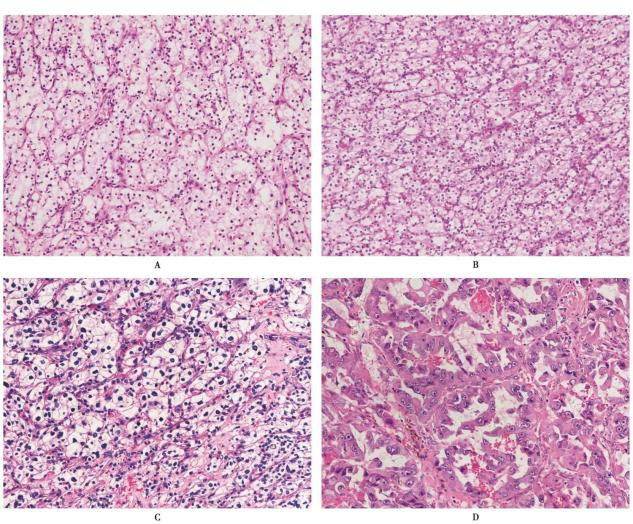
透明细胞癌WHO/ISUP核分级1级至4级形态学特征
A.WHO/ISUP 1级肿瘤细胞核浆比小,核圆,胞质透明,400倍下瘤细胞无核仁或核仁不明显;B.WHO/ISUP 2级肿瘤细胞核浆比小,核圆或卵圆,核仁不明显;C.WHO/ISUP 3级肿瘤细胞核浆比大,核大小不一,100倍下可见核仁;D.WHO/ISUP 4级肿瘤细胞胞质嗜酸,瘤细胞显示明显多形性的核、瘤巨细胞,伴横纹肌样分化(来源于临床病理诊断与鉴别诊断---泌尿及男性生殖系统疾病)
注意,分级要看最差的那片区域,哪怕只占肿瘤的一小部分。核级别越高,越容易转移和复发。
约5%的ccRCC会出现肉瘤样或横纹肌样分化,一旦出现,往往提示预后差——即使只有一小灶,也建议按高级别肿瘤对待。
五、分期、风险分层与治疗选择
5.1 TNM分期(AJCC第8版)
· T1:肿瘤局限于肾脏,最大径≤7cm(T1a≤4cm;T1b>4cm且≤7cm)
· T2:肿瘤局限于肾脏,最大径>7cm(T2a>7cm且≤10cm;T2b>10cm)
· T3:肿瘤侵犯主要静脉、肾周脂肪或肾窦脂肪,但未超过Gerota筋膜
· T4:肿瘤侵透Gerota筋膜或侵犯同侧肾上腺
除了TNM分期,临床上还会综合评估组织学分级、有无肿瘤坏死、肉瘤样分化、微血管侵犯等因素,进行危险分层,常分为低危、中危、高危三类,用于指导后续治疗策略。
5.2 治疗原则概要
· 局部肿瘤(I-III期):手术是根治的主要手段。根据肿瘤大小、位置和患者情况,可选择肾部分切除术(保留肾单位)或根治性肾切除术。
· 晚期/转移性肿瘤(IV期):已经以全身治疗为主。传统化疗放疗效果不佳,目前主要采用靶向治疗(如舒尼替尼、帕唑帕尼等TKI药物)和免疫治疗(如PD-1/PD-L1抑制剂),或两者联合。部分符合条件的患者也可能从减瘤性肾切除术中获益。
六、预后、随访与患者管理
6.1 预后因素
ccRCC的预后与多种因素相关:
· 病理因素:分期、分级、肉瘤样变、肿瘤坏死、微血管侵犯
· 临床因素:体能状态、症状、贫血、血小板增多、中性粒细胞/淋巴细胞比
· 分子标志物:BAP1突变(与不良预后相关)、PBRM1突变(与较好预后相关)
6.2 随访建议
治疗后的定期随访至关重要,目的在于监测复发、转移和处理治疗相关副作用。一般建议:
· 术后前2-3年:每3-6个月进行一次病史询问、体格检查、肾脏区域和胸部影像学检查(如CT)及实验室检查。
· 术后第3-5年:每6-12个月复查一次。
· 5年后:每年复查一次。
当然,具体随访计划和内容必须根据患者的具体情况(如病理分期、分级、治疗方式等)进行个体化调整。
总之,肾透明细胞癌虽然常见,但通过细致的病理检查、分级分期以及合理的辅助检测,我们能够更准确地判断患者的预后,并制定个体化的治疗和随访方案。





































共0条评论