[导读] 编译整理:强子
引言
新冠病毒的流行,凸显了传染病防控的重要意义。近些年,麻疹、梅毒、艾滋病再度成为紧迫的全球公共卫生问题,且因为它们会累及淋巴结、脾脏、骨髓等重要免疫器官结构,因此病理医师在临床实践中能准确识别出这些感染性疾病具有重要意义。
美国病理专家Auerbach等人曾在《Histopathology》杂志发表综述,介绍了这三种感染性疾病的临床与病理特征,尤其介绍了对淋巴系统的特异性影响、重点介绍了淋巴结的组织病理学改变,以提高这类病种的病理诊断准确性。为帮助大家更好的了解相关知识点并将其应用于临床实践,我们将该文要点编译介绍如下。
人免疫缺陷病毒
导致获得性免疫缺陷综合征(Acquired Immunodeficiency Syndrome,AIDS,简称艾滋病)的病原体为人免疫缺陷病毒(human immunodeficiency virus,HIV,可简称为艾滋病病毒)。其实1981年就认识了艾滋病,但1984年才分离出了HIV,也才有了后续相关治疗、以及疫苗的相关研究。当然,后续三十余年都没有研制出疫苗,主要问题在于这一病毒突变几率高、且有遗传多样性。不过,抗逆转录病毒疗法已将这一疾病转变为一种可控制的慢性疾病。干细胞移植也已经可以达到长期的低病毒载量、甚至测不出的水平。不过,这些方法都无法清除潜伏的艾滋病病毒,长期疗效有限。
HIV感染的情况下,病毒复制和储存的主要部位就是淋巴结,尤其淋巴结中的生发中心内。也正是因为如此,所以HIV感染患者的常见表现就是长期持续的淋巴结肿大。HIV感染的是CD4阳性T细胞、尤其生发中心中的T滤泡辅助细胞,导致CD4阳性T细胞死亡。HIV还会被捕获于滤泡树突细胞(follicular dendritic cells,FDC)膜上的周期蛋白内体(cyclin endosomes)中,但不会感染FDC。HIV被细胞膜的捕获可以同免疫组化P24检出。抗逆转录病毒治疗的停止,必然导致病毒反弹。
初次感染HIV的淋巴结形态学有三个分期,也有作者将滤泡溶解(follicle lysis,FL)作为单独一个分期、并有多个不同的描述性名称。具体来说,第一期为急性期,特征为滤泡旺炽性增生、伴或不伴滤泡溶解;具体为大而不规则的滤泡,套区变薄,边缘区增生(为单核样B细胞),且滤泡间有轻度出血。滤泡溶解是小淋巴细胞侵入生发中心、导致滤泡中心碎片化的过程。
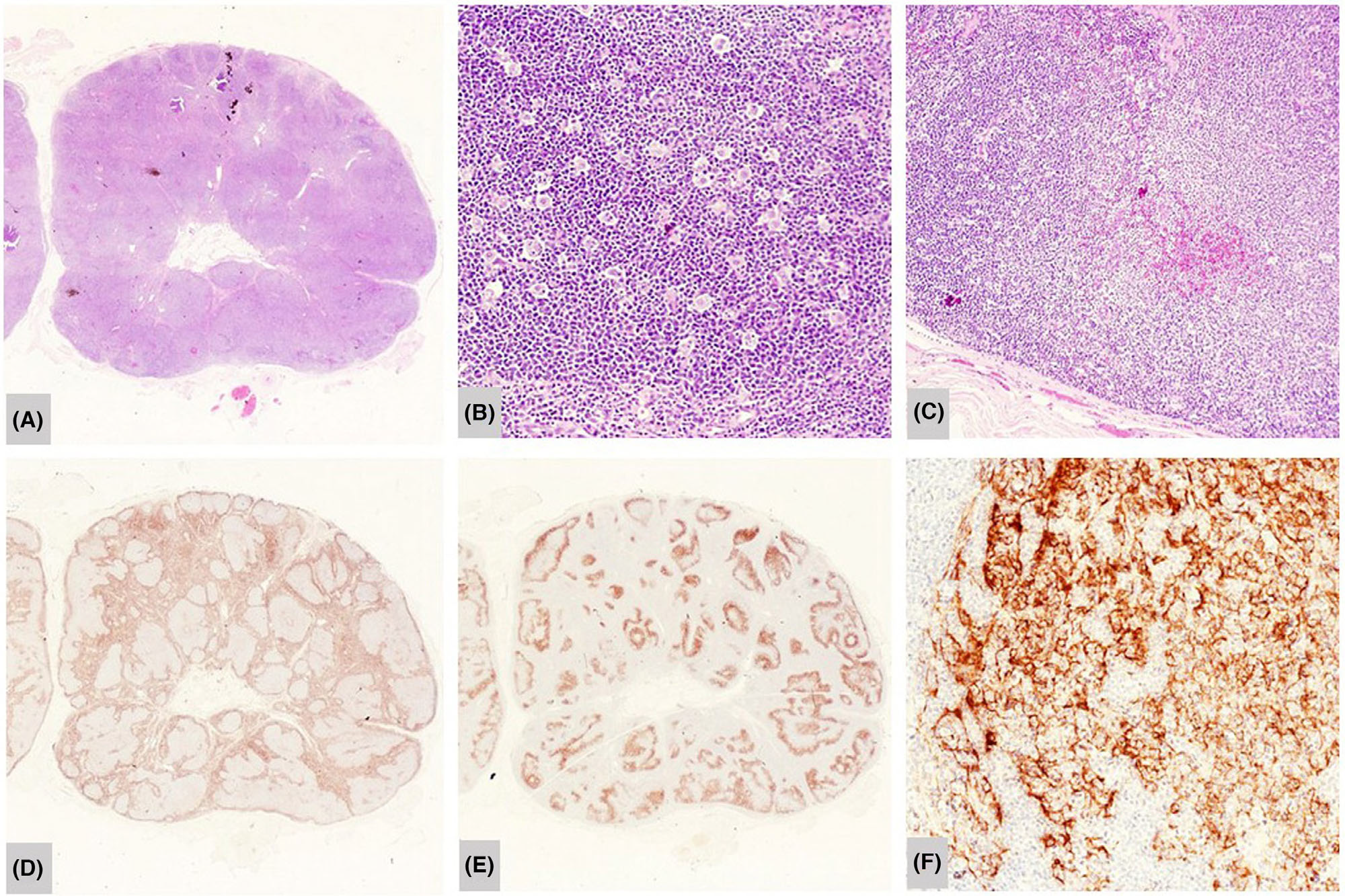 图1.淋巴结感染HIV的急性期。(A)低倍镜下,滤泡旺炽性增生;(B)生发中心有可染体巨噬细胞,B细胞的套区萎缩;(C)边缘区增生;(D)BCL2免疫组化,生发中心阴性,套区萎缩;(E)P24免疫组化,滤泡树突细胞网着色;(F)P24免疫组化高倍。
图1.淋巴结感染HIV的急性期。(A)低倍镜下,滤泡旺炽性增生;(B)生发中心有可染体巨噬细胞,B细胞的套区萎缩;(C)边缘区增生;(D)BCL2免疫组化,生发中心阴性,套区萎缩;(E)P24免疫组化,滤泡树突细胞网着色;(F)P24免疫组化高倍。
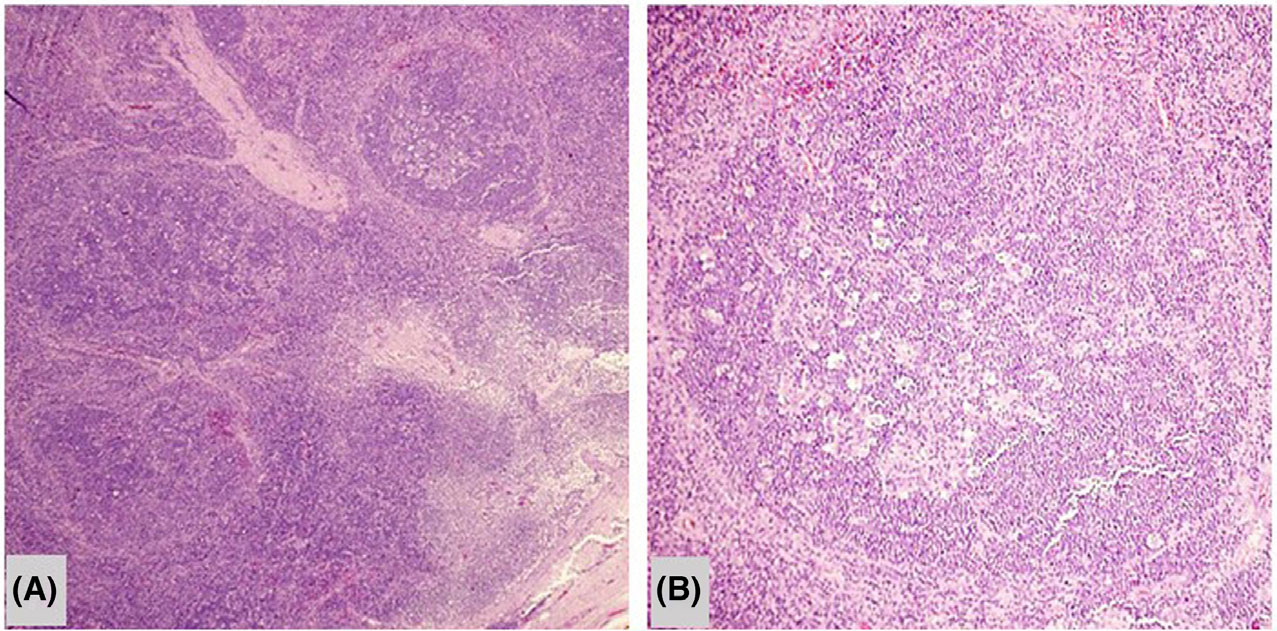 图2.淋巴结中的滤泡溶解:低倍镜及高倍镜,生发中心呈碎片状。
图2.淋巴结中的滤泡溶解:低倍镜及高倍镜,生发中心呈碎片状。
HIV感染中常见滤泡溶解,但这并非HIV感染所特有的形态学表现,因为也常见于其他情况。滤泡溶解是淋巴滤泡的碎片化,始自滤泡的明区,是对病毒抗原的直接免疫攻击。有滤泡树突网的破坏,且CD8阳性T细胞侵入生发中心;但有作者描述也会有套区B细胞的内陷。生发中心标记物HGAL在滤泡溶解的生发中心碎片中为阳性,但BCL6和CD10结果不一。与滤泡溶解不同,生发中心进行性转化表现为小B细胞和CD4阳性T细胞的浸润,其中很多为CD57阳性。生发中心进行性转化时,整个滤泡都扩张,且细胞混杂在一起,因此整个滤泡呈均质表现、而非滤泡溶解时的碎片状表现。滤泡间区可有浆细胞、免疫母细胞、淋巴细胞、组织细胞。对麻疹更有特异性的Warthin-Finkeldey细胞偶尔可见于HIV患者的淋巴结滤泡中。
HIV感染的初期,免疫组化可以显示出CD20阳性的滤泡,混杂的小T细胞则表达CD3。生发中心BCL2阴性,但这一标记也可用于显示滤泡溶解、并鉴别滤泡溶解和生发中心进行性转化。HIV感染早期,EBV一般是阴性的。κ和λ免疫组化显示B细胞为多克隆,且有浆细胞。生发中心滤泡树突细胞中P24可能为阳性,提示HIV感染。过去对P24免疫组化检测的应用一直存在争议,主要是医疗工作者对HIV诊断和检测知情同意的顾虑,所以病理医师应注意这些敏感问题、并了解所在单位相应的指导原则。
HIV感染第二个时期的特征为滤泡萎缩/退化。此期滤泡被破坏,浆细胞数量增多,皮质旁区域增生、有穿透滤泡的血管。此期还可能会有Castleman样改变,也可能会有纤维化。
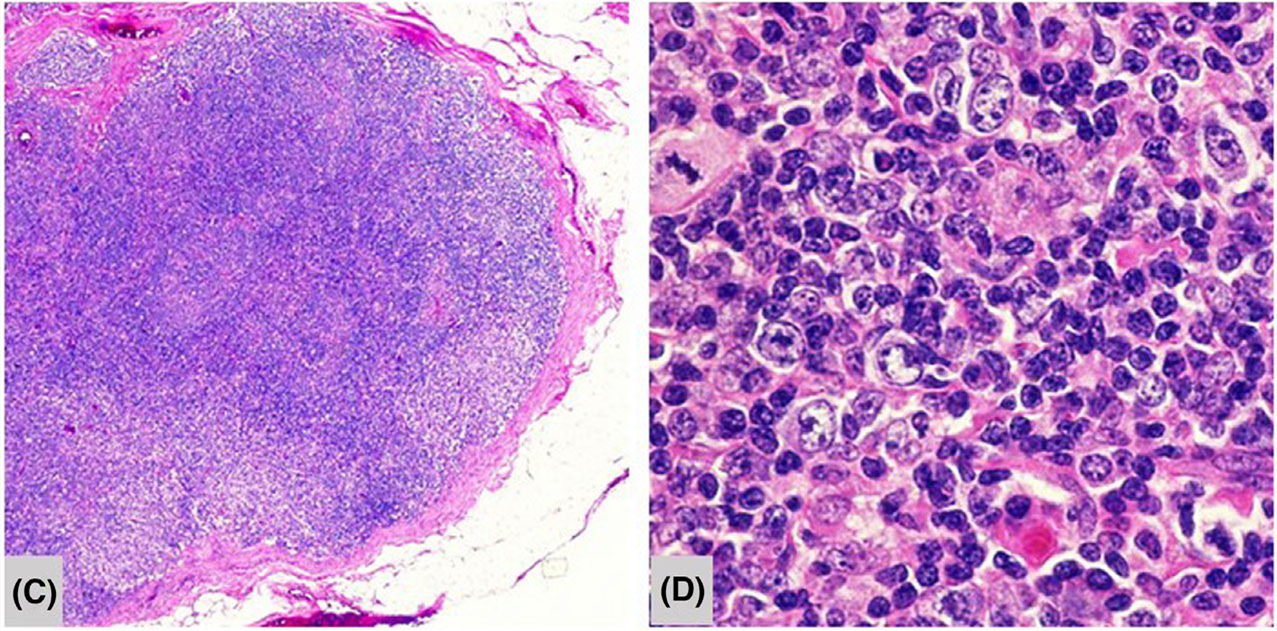 图3.HIV感染时,淋巴结的滤泡萎缩/退化期,低倍镜下滤泡已难以识别,高倍镜下萎缩/退化的滤泡中有残余的中心母细胞和中心细胞。
图3.HIV感染时,淋巴结的滤泡萎缩/退化期,低倍镜下滤泡已难以识别,高倍镜下萎缩/退化的滤泡中有残余的中心母细胞和中心细胞。
HIV感染的第三个时期为进展期,形态学为滤泡/淋巴细胞的耗竭。淋巴结呈燃尽(burnt-out)样表现,滤泡不明显。可有无定型的PAS阳性物质,甚至有显著纤维化。长期HIV感染时,皮质旁可有胶原纤维化,可能是由于慢性炎症所致。
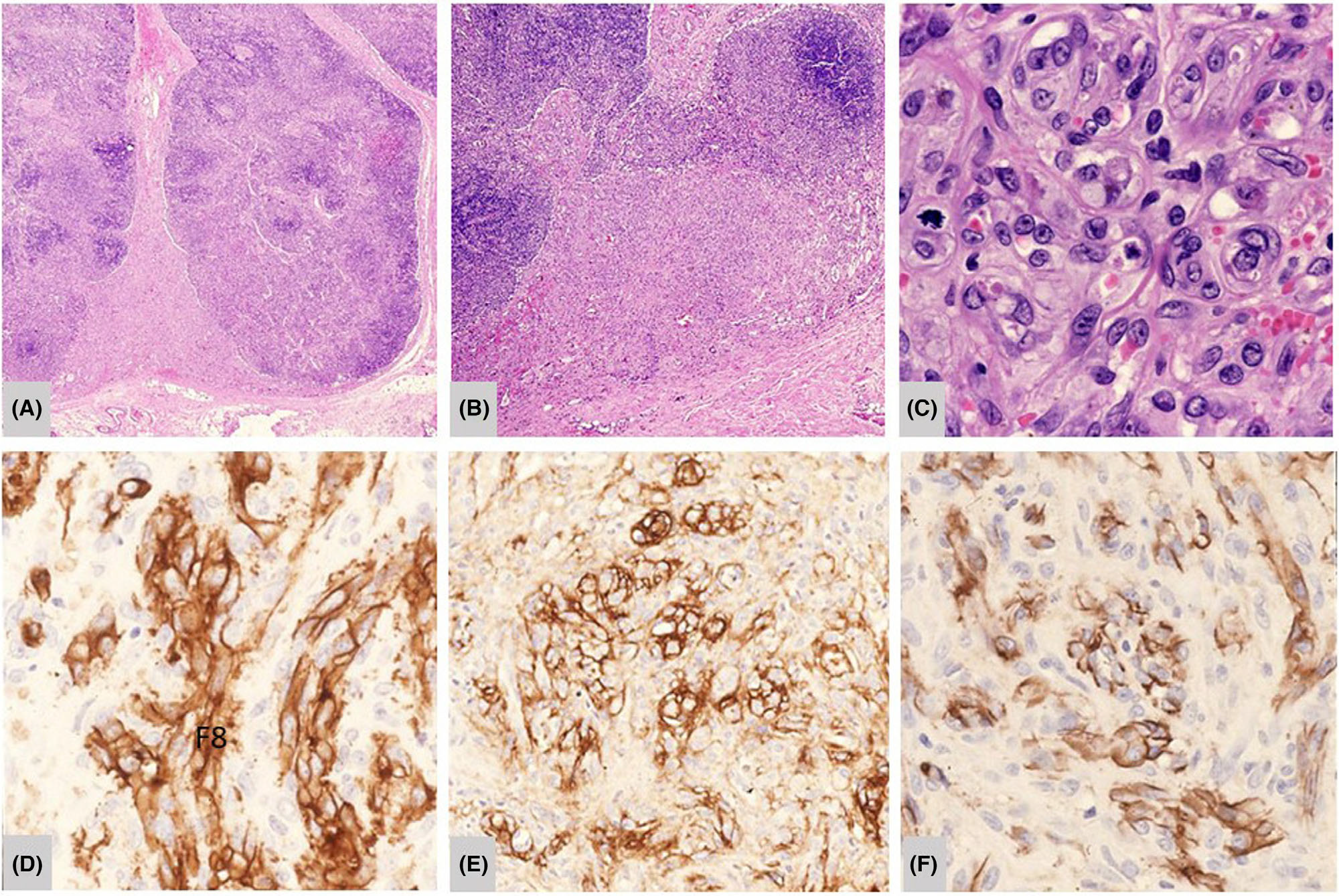 图4.HIV感染时,具有淋巴细胞耗竭及Kaposi肉瘤的淋巴结。(A)低倍镜下,淋巴细胞耗竭,局灶有血管增生;(B)图示淋巴结被膜内的血管增生;(C)高倍镜下,Kaposi肉瘤中的非典型血管增生;免疫组化检测,内皮细胞VIII因子阳性(D)、CD31阳性(E)、CD34阳性(F)。
图4.HIV感染时,具有淋巴细胞耗竭及Kaposi肉瘤的淋巴结。(A)低倍镜下,淋巴细胞耗竭,局灶有血管增生;(B)图示淋巴结被膜内的血管增生;(C)高倍镜下,Kaposi肉瘤中的非典型血管增生;免疫组化检测,内皮细胞VIII因子阳性(D)、CD31阳性(E)、CD34阳性(F)。
呈2期或3期改变的淋巴结需要鉴别淋巴瘤、Kaposi肉瘤、感染。上述三期的类似改变也可见于其他淋巴组织,如扁桃体、脾脏、胃肠道(即胃肠道相关淋巴组织),甚至可见于涎腺淋巴组织。
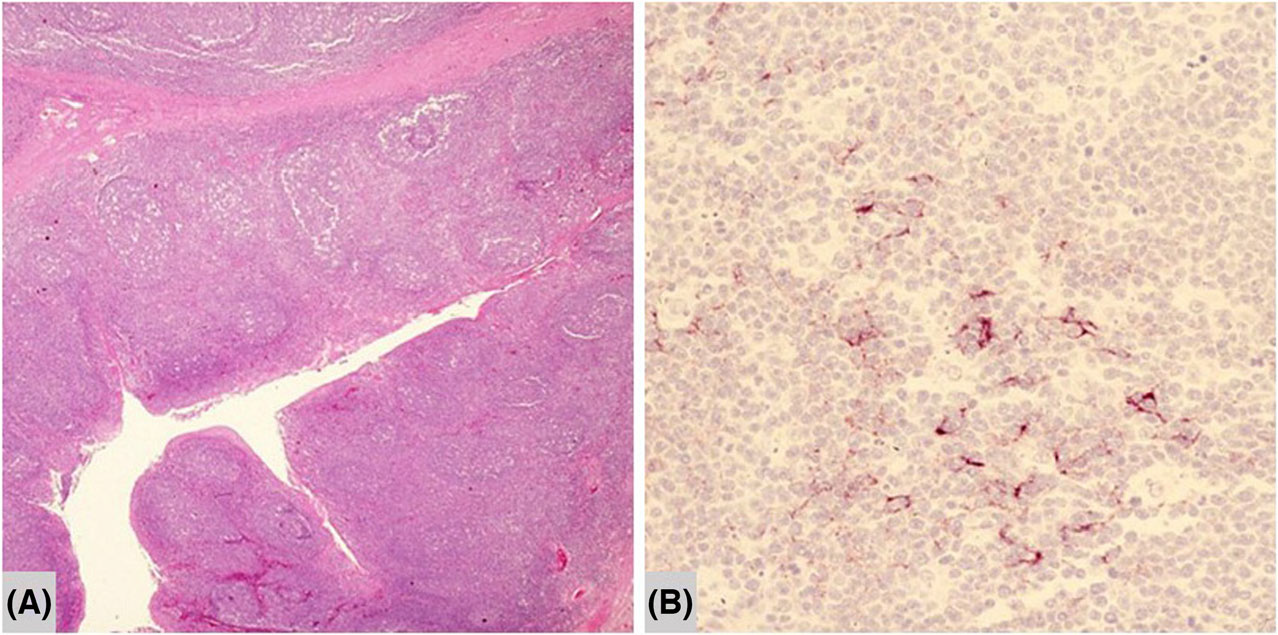 图5.一例HIV感染患者的扁桃体标本,低倍镜下可见旺炽性滤泡增生,免疫组化P24滤泡树突细胞阳性。
图5.一例HIV感染患者的扁桃体标本,低倍镜下可见旺炽性滤泡增生,免疫组化P24滤泡树突细胞阳性。
HIV首次感染后期的免疫组化中,可见CD20斑片状阳性,小淋巴细胞表达CD3。CD21和CD23有助于显示残余滤泡树突细胞网,提示有滤泡的存在、因此还有正常淋巴结结构。滤泡树突细胞中免疫组化P24可仍为阳性。如果有非典型血管增生,HHV8免疫组化有助于排除Kaposi肉瘤。显微镜下可见的Kaposi肉瘤病灶可见于淋巴结的被膜下位置,这样的轻微受累时诊断难度更大。还要做感染性病原体的相关检测,EBV免疫组化可为阳性。
未完待续
点击此处下载原文献
参考文献
Auerbach A, Schmieg JJ, Klassen M, Nelson A, Aguilera NS. HIV, measles, and syphilis: histopathologic characteristics of lymphatic system involvement of three reemerging infectious diseases. Histopathology. 2025;87(1):18-34.
doi:10.1111/his.15408


















共0条评论