[导读] 作者:甘肃省人民医院病理科 陈旭
临床概要
54岁男性患者,职业为装修工人,半年前无意中发现右侧腋窝肿物,直径约为4cm,伴轻微疼痛,行传统中医治疗,疼痛缓解。后腋窝肿物渐行性增大,直径约为9.5cm,伴疼痛7天,无发热、乏力等全身症状。于我院就诊,行CT检查提示,右侧腋窝淋巴结多发、融合性增大,边界不清。遂行手术切除右侧腋窝肿物。
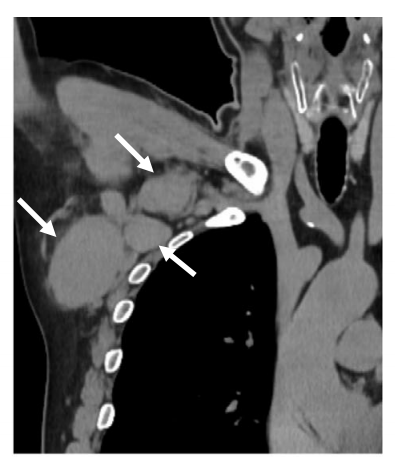
图1.CT检查提示,患者右侧腋窝淋巴结多发、融合性肿大,皮质髓质界限不清。
大体观察
(右侧腋窝)灰白不整形带皮肤组织一块,大小13×10×3cm,皮肤13×6.5cm,组织切面灰白灰黄实性质中,局部切面呈多结节状及出血坏死。
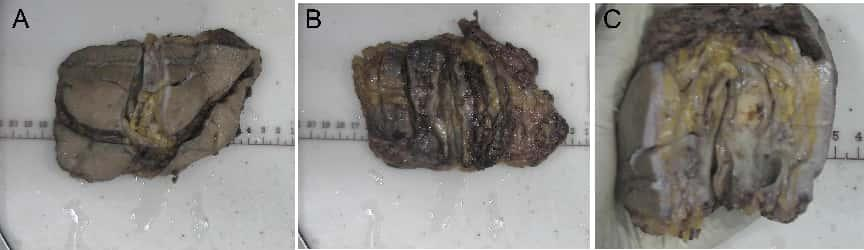 图2.大体观察。(A)带皮肤肿物;(B)切面灰白灰黄实性质中;(C)局部切面呈多结节状及出血坏死。
图2.大体观察。(A)带皮肤肿物;(B)切面灰白灰黄实性质中;(C)局部切面呈多结节状及出血坏死。
组织学特点
低倍镜下,淋巴结结构消失,肿瘤细胞位于真皮内,肿瘤细胞黏附性差,排列密集,呈弥漫浸润性生长,侵入周围骨骼肌、脂肪组织及胶原纤维。高倍镜下,肿瘤细胞以大细胞为主,胞质丰富,部分胞质显著嗜酸性,细胞异型性明显,部分核偏位,呈印戒样、横纹肌样,细胞双核、多核或奇异形核,细胞核仁不明显。
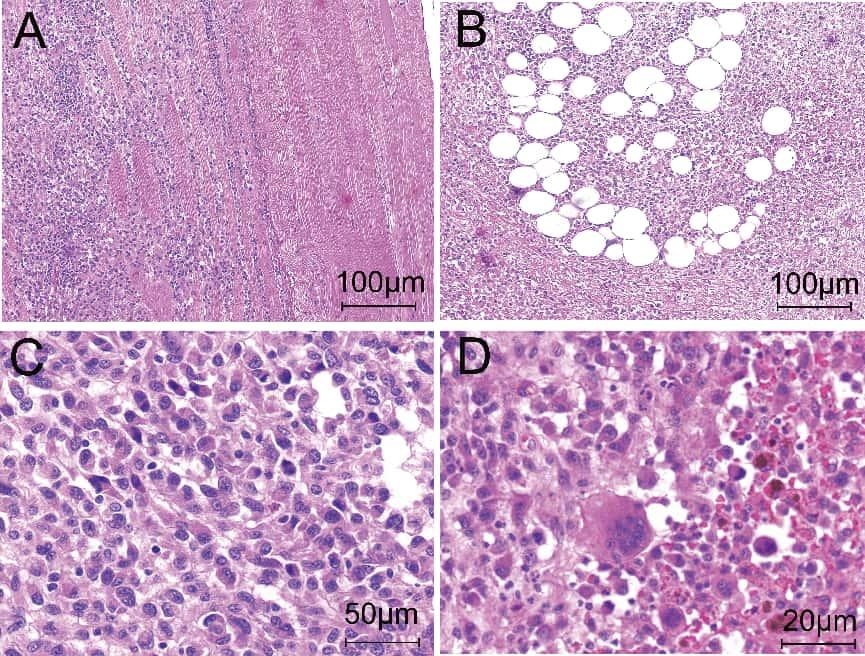 图3.组织学特点(A)低倍镜下,瘤细胞弥漫分布,侵犯周围骨骼肌及周围纤维组织;(B)瘤细胞黏附性差,侵犯周围脂肪组织;(C)高倍镜下,瘤细胞体积较大,胞质丰富,部分胞质显著嗜酸,异型明显;(D)部分区域瘤细胞可见双核、多核或奇异形核。
图3.组织学特点(A)低倍镜下,瘤细胞弥漫分布,侵犯周围骨骼肌及周围纤维组织;(B)瘤细胞黏附性差,侵犯周围脂肪组织;(C)高倍镜下,瘤细胞体积较大,胞质丰富,部分胞质显著嗜酸,异型明显;(D)部分区域瘤细胞可见双核、多核或奇异形核。
免疫组化特点
CKP(-)、Vimentin(-),CD45RO(-),CD21(-),CD1a(-),MPO(-),S-100(-),HMB45(-),Melan-A(-),MyoD1(-),CD30(-),ALK(-),EMA(-),CD68(+),CD163(+),Ki-67(增殖指数约为60%)。
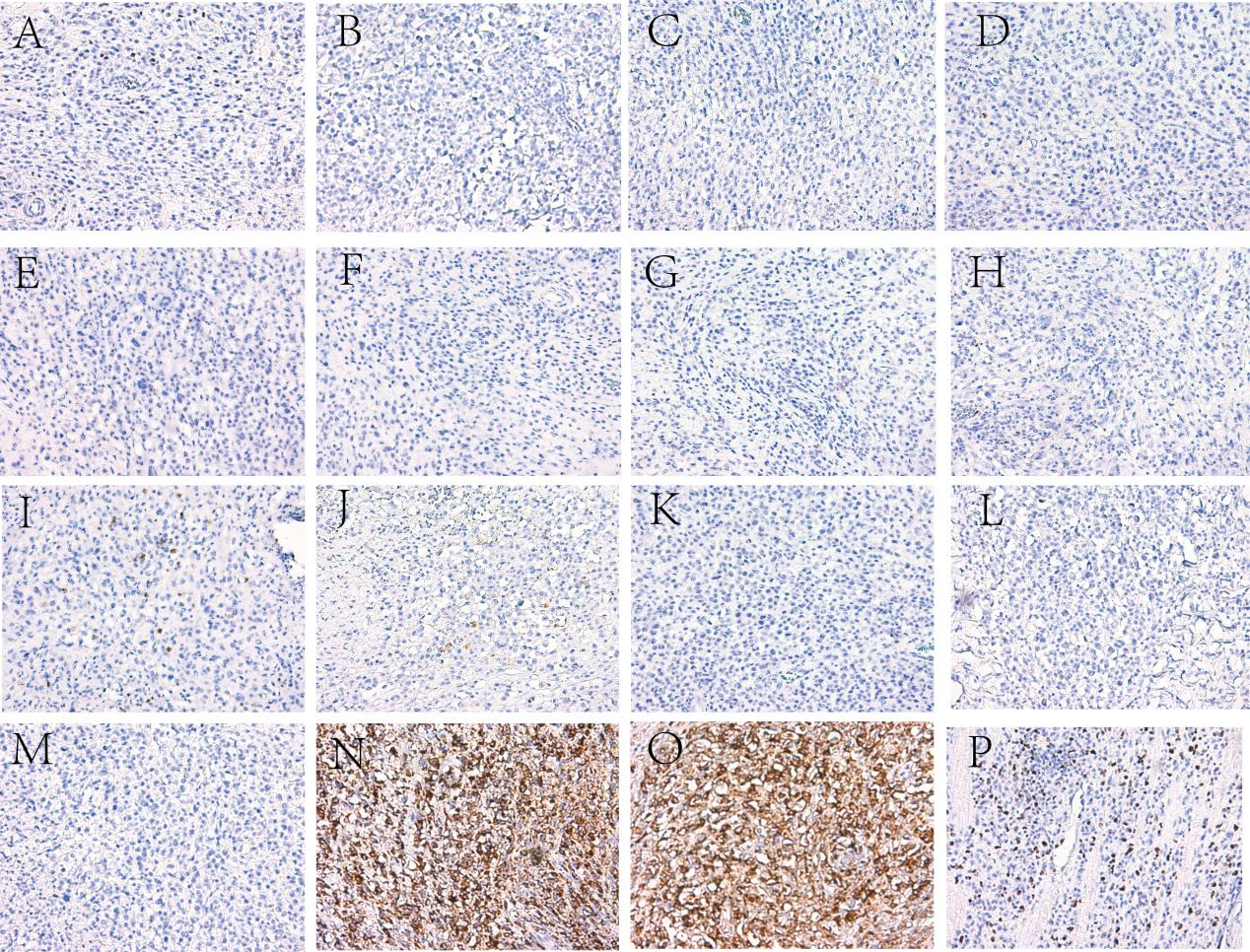 图4.免疫组化染色(×20)(A)CKP;(B)Vimentin;(C)CD45RO;(D)CD21;(E)CD1a;(F)MPO;(G)S-100;(H)HMB45;(I)Melan-A;(J)MyoD1;(K)CD30;(L)ALK;(M)EMA;(N)CD68;(O)CD163;(P)Ki-67
图4.免疫组化染色(×20)(A)CKP;(B)Vimentin;(C)CD45RO;(D)CD21;(E)CD1a;(F)MPO;(G)S-100;(H)HMB45;(I)Melan-A;(J)MyoD1;(K)CD30;(L)ALK;(M)EMA;(N)CD68;(O)CD163;(P)Ki-67
分子检测结果
ARMS技术检测发现BRAF V600E基因突变,突变形式为第15外显子的第1799位核苷酸上T突变为A,导致其编码的谷氨酸由缬氨酸取代。
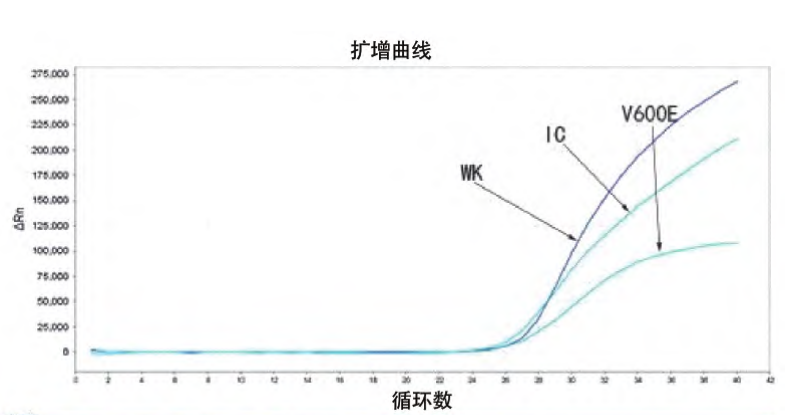 图5.BRAF V600E基因突变阳性
图5.BRAF V600E基因突变阳性
最终诊断
(右侧腋窝)组织细胞肉瘤。
随访
患者术后拒绝新辅助治疗及后续进一步检查,遂出院。3月后伴全身乏力7天,可见胸部皮疹,再次入我院就诊。PEC-CT检查提示多发高代谢转移灶。骨髓穿刺涂片可见大量多形性未成熟的肿瘤细胞,这些细胞具有不规则的细胞核。皮疹组织活检提示组织细胞肉瘤。患者遂行CHOP+维罗非尼方案化疗,随访26个月,患者死亡。
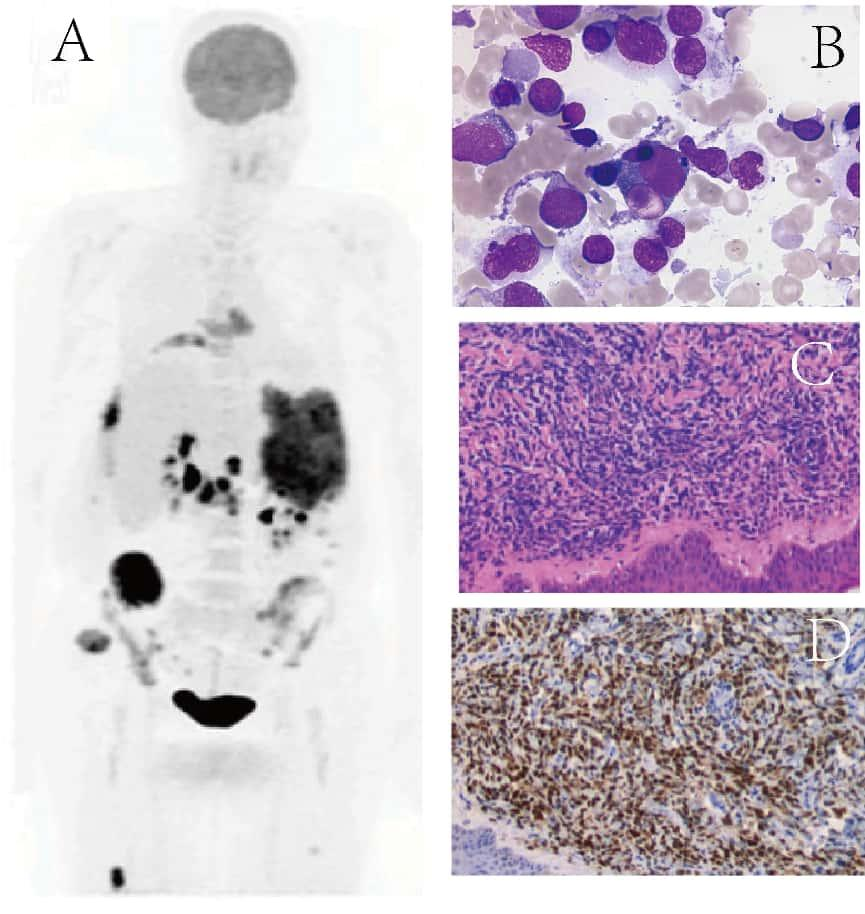 图6.再次检查结果。(A)PET-CT提示多发高代谢转移灶,集中于胰腺及左侧腹部;(B)骨髓穿刺图片显示大量多形性未成熟的肿瘤细胞,细胞核形态不规则,胞质呈蓝灰色且含量丰富(Giemsa染色,×100)。(C)皮疹活检,肿瘤细胞位于真皮内,与表皮之间有一个无细胞区域带,肿瘤细胞圆形,弥漫分别;(D)CD163免疫组化染色阳性。
图6.再次检查结果。(A)PET-CT提示多发高代谢转移灶,集中于胰腺及左侧腹部;(B)骨髓穿刺图片显示大量多形性未成熟的肿瘤细胞,细胞核形态不规则,胞质呈蓝灰色且含量丰富(Giemsa染色,×100)。(C)皮疹活检,肿瘤细胞位于真皮内,与表皮之间有一个无细胞区域带,肿瘤细胞圆形,弥漫分别;(D)CD163免疫组化染色阳性。
疾病概述
组织细胞肉瘤(HS)是一类来源于单核/巨噬细胞的恶性侵袭性肿瘤,WHO造血和淋巴组织肿瘤分类,定义该肿瘤是一种形态和免疫表型均与成熟组织细胞相似的组织细胞恶性增生,表达1种或1种以上组织细胞标记物,但不表达树突细胞标记物,并且不伴有急性单核细胞白血病。
发病原因
HS的病因学及发病机制尚不清楚,可能与EB病毒感染、毒物接触、环境污染、长期使用免疫抑制剂等很多因素相关。Sheryl等报道NLRX1可以抑制肿瘤的发生,并且通过NF-kB信号通路的负调节影响组织细胞肉瘤的发生。Shimono等发现BRAF V600E突变与HS的发生相关。
流行病学
在所报道的文献中,HS在各年龄段均可发病,但以成年人多见,发病年龄最小者为7月龄,最大者89岁,中位年龄52岁,男女发病率大致相等。
临床表现
HS病变部位主要为淋巴结、皮肤或结外组织。结外组织又以胃肠道最为常见,中枢神经系统、脾脏、肝脏、骨、甲状腺、乳腺、胸膜、肺、胆管、卵巢等均有报道。HS的临床表现缺乏特异性,多为单个肿物或多个肿物融合。不同部位的肿瘤临床表现不一,与系统症状相关。皮肤病变早期多表现为无特异性红斑,逐渐形成孤立性肿块,继而发展为躯干及四肢多发性病变。神经系统患者以头痛、发热、下肢无力、步态障碍多见,部分患者出现视力障碍、记忆力下降等。累及消化系统者常出现腹部胀痛,晚期患者往往出现高热、消瘦,同时伴有腹泻、血便、呕吐等不适,仅少数患者伴有肠梗阻表现;累及骨者以疼痛最为常见,部分患者伴有溶骨性表现;累及骨髓、脾脏的患者常以发热、无力为首发症状,多伴有血细胞减少,因肿瘤进展迅速,明确诊断时常伴有多系统累及。
病理学特点
镜下肿瘤细胞呈弥漫性分布,细胞形态多样,部分可为梭形细胞肉瘤样形态; 细胞核圆形或卵圆形,可多核,泡状核,核仁明显,病理性核分裂象多见,偶见瘤细胞吞噬细胞碎片、淋巴细胞和血细胞现象,但无特异性。肿瘤细胞周围还可见淋巴细胞、浆细胞、嗜酸性粒细胞和良性的组织细胞等。免疫标记 CD68、CD163、Lysozyme、抗胰蛋白酶、CD4、CD11C和CD14常表达阳性,Ki-67增殖指数为10%-90%。
分子遗传学特点
部分HS来自于以前B细胞性淋巴瘤的转分化,伴有IgH-BCL2融合和CyclinD1-IgH融合等分子改变。20%的HS存在BRAF基因突变。2022年修订的《造血与淋巴组织肿瘤 WHO分类》中提出HS可缺乏IgH和TCR基因的重排。
鉴别诊断
①急性(原)单核细胞白血病引起的皮肤及淋巴结病变
骨髓检查以单核系增殖为特征,骨髓活检见细胞弥漫成片分布,细胞核轮廓较不规则或有分叶倾向,分子检测不伴BRAF基因突变。HS骨髓活检常见外来分类不明细胞增生且成堆分布,组织形态学及分子检测有助于鉴别诊断。
②间变性大细胞淋巴瘤
肿瘤细胞形态单一,瘤细胞表达CD30,T细胞相关抗原阳性,CD68和CD163常阴性。
③髓系肉瘤
常与急性髓系白血病、慢性髓系增生性肿瘤和骨髓增生异常综合征相关,瘤细胞表达MPO、CD99、CD68、CD43及CD117等。
④树突细胞肉瘤
肿瘤细胞通常为梭形,漩涡状排列,少数呈上皮样亚型,瘤细胞表达CD21、CD23和CD35。
⑤恶性黑色素瘤
胞质内见黑色素有助于诊断,瘤细胞表达S-100、HMB45和MelanA。
⑥低分化癌
表达上皮性标记物。
预后及治疗
HS恶性程度高,侵袭能力强,预后差,患者多在确诊后2年内死亡。HS预后可能与肿瘤部位、肿瘤大小和肿瘤分期等多种因素有关。目前治疗上尚无统一的诊疗指南,多种治疗方案疗效尚未确切。
对于局限性肿瘤,在患者病情允许情况下,手术切除是最可靠的治疗手段。但单纯手术切除,术后效果不佳。推荐肿瘤分期在T1-T2b期的患者早期行以手术为主的综合治疗,术后予以辅助性化疗或放疗。
最常用的化疗方案为CHOP方案(环磷酰胺+阿霉素+长春新碱+泼尼松),该与其他化疗方案相比,该方案费用少、疗效相似且毒性低,但仅有少数患者短期内有效,长期随访复发率高。对CHOP方案治疗无效的患者,可采用盐酸吉西他滨+顺铂+地塞米松的化疗方案(GDP方案),GDP方案为CHOP方案治疗无效的患者带来了希望,同时可能为该类患者行自体干细胞移植或其他治疗方案赢得准备时间。
近年来,一些新型治疗方式不断问世。新型靶向药物如伊马替尼、索拉非尼和贝伐珠单抗在肺癌、肾癌及消化道肿瘤中得到广泛应用。HS不同程度表达VEGFR、VEGFC、PDGFR等血管增生相关因子及其他免疫表型,根据不同的免疫表型,应用索拉非尼、贝伐珠单抗及阿伦珠单抗等靶向药物治疗,有助于抑制肿瘤进展。HS中有BRAF V600E基因突变,针对这一位点的靶向药物维罗非尼可使患者病情短期内改善。
参考文献
[1]Dalia S,Shao H,Sagatys E,et al.Dendritic cell and histiocytic neoplasms:biology,diagnosis and treatment[J].Cancer Control,2014,21(4):290-300.
[2]Swerdlow SH,Campo E,Harris NL.World Health Organization classification of tumours: WHO classification of tumours of haemaopoietic and lymphoid tissues [M].Lyon: IARC Press,2022.
[3]Huang YP,Qian X.Histiocytic sarcoma[J].Arch Pathol Lab Med,2019,144( 5) : 650-654.
[4]Dalia S,Shao H,Sagatys E,et al.Dendritic cell and histiocytic neoplasma: biology,diagnosis,and treatment[J].Cancer Control,2014,21(4):290-300.



















共0条评论