[导读] 作者:赵东晖
病史:
患者,女,42岁,发现左侧扁桃体肿物2年,进行性增大4月余,平素无不适,一直未予治疗。
影像检查:


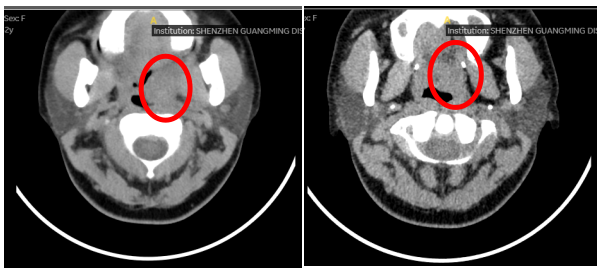
左侧扁桃体区见一不规则肿块影,大小约28mm×36mm×28mm,密度欠均匀, 边界欠清,内见低密度区。左侧咽旁间隙变窄、消失,口咽稍右偏移。诊断:左扁桃体区占位,性质待定。
病理检查:
大体:
组织一块,大小4.8×4×3.5cm,切面灰白、灰红,质韧、实性,挤压小块扁桃体组织上。
HE:
扁桃体组织内见瘤组织,排列呈巢片状、不规则状、梁状、少量筛状及小灶状,局部囊性变,细胞核卵圆形及皱缩,见个别核分裂象,胞质透明及淡红染,浸润性生长,伴间质明显玻璃样变及促结缔组织增生,黏液样变。
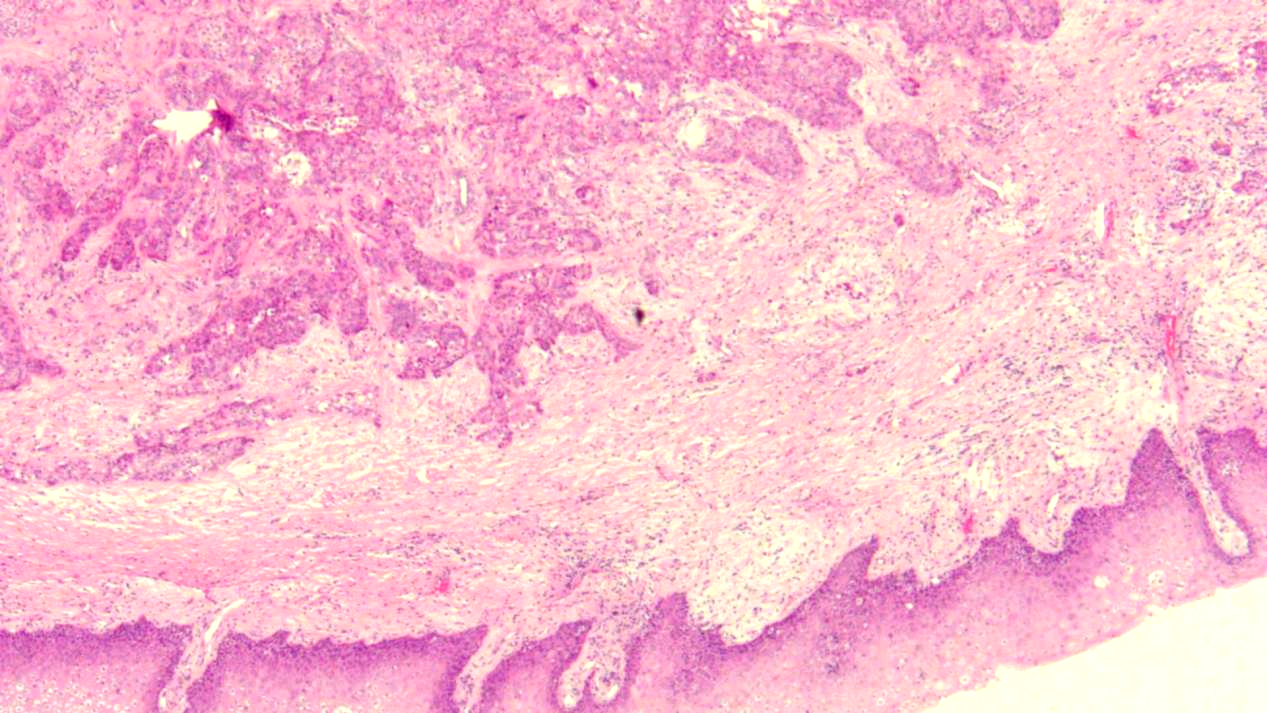
瘤组织在鳞状上皮下,浸润性生长

间质黏液变性,呈假筛状结构

细胞核圆形至卵圆形,“挖空样”及“皱缩感”
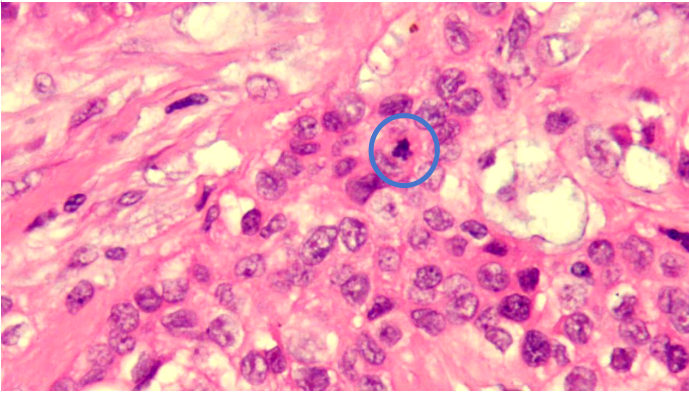
隐约可见小核仁,见核分裂象
IHC结果:
AE1/AE3、CK5/6、p40、p63、CK7、Vimentin(均弥漫强+),p16(斑驳+),EMA(弱+),p53(散在弱+,野生型表达),Calponin、SMA、S-100、CD117均(-),Ki67(约5%+)。
特殊染色结果:透明细胞PAS(+),AB及黏液卡红染色均(-)。

特殊染色:透明细胞PAS(+)
病理诊断:
(左侧扁桃体)符合玻璃样变透明细胞癌,建议加做FISH检测行EWSR1基因断裂情况进一步协助诊断。
讨论:
概述:
涎腺玻璃样变透明细胞癌(hyalinizing clear cell carcinoma,HCCC)是好发于口腔内小涎腺的少见肿瘤,最常见于腭、舌根、颊黏膜、口底,生物学低度恶性。
曾被命名为透明细胞腺癌、透明细胞癌(非特指性)和透明细胞癌。
2022年第5版WHO《头颈部肿瘤分类》又将其重新命名为HCCC。
该肿瘤以前被称为下列肿瘤的单形性变异型或与其混淆:即上皮-肌上皮癌、黏液蛋白缺失的黏液表皮样癌和肌上皮癌。因为缺乏明显的鳞状、黏液和肌上皮分化,该肿瘤成为独立的疾病实体。后来研究发现,该疾病最常见的遗传学改变是EWSR1-ATF1基因融合,而在其他任何类型的涎腺肿瘤中目前都没有发现这种分子改变,进一步支持其为独立的疾病实体。
该肿瘤典型形态学特点是:透明细胞增生伴显著玻璃样变性的间质反应。
由于罕见,该肿瘤不为病理科医师和临床医师所熟知,且许多其他类型原发和转移性涎腺肿瘤常见透明细胞成分,因而误诊时有发生。
临床特征:
1.流行病学:发病率低,约占唾液腺上皮性肿瘤的1%。患者年龄范围1-86岁,平均54岁,女性较多见,男女之比约为1:1.4。约90%的病例发生于小唾液腺,其中以舌根和腭部最多见。大唾液腺仅占10%,以腮腺多见,下颌下腺也可发生。
2.症状主要表现为无痛性肿块,可伴有黏膜溃疡较少出现疼痛、麻木等症状。病程1个月至15年不等肿瘤固定不活动。
3.治疗及预后 手术切除。约20%-25%的病例就诊时已发生淋巴结转移。术后一般无复发和转移,预后良好。
病理特征:
1.大体特征:肿瘤通常在3cm以下,界限不清,常无明显包膜,浸润性生长。剖面为实性,呈灰白色或灰褐色。
2.镜下特征:肿瘤浸润性生长,瘤细胞排列呈片状巢状、小梁状或条索状。瘤细胞主要为胞质透明的多边形细胞。细胞核圆形或多边形,核位于细胞中央或偏位,核仁常不明显。组织化学染色显示PAS染色阳性,可被淀粉酶消化,黏液卡红染色通常为阴性,证实肿瘤胞质内含有糖原。部分病例中少数细胞呈浅嗜伊红或嗜双色性胞质,多见于肿瘤周边。细胞异型性不明显,核分裂罕见,部分细胞有中等程度胞核异型性。有时肿瘤可出现明显的鳞状分化甚至黏液细胞分化。导管罕见或缺乏,可见囊性变。大多数病例肿瘤间质致密胶原化,有时出现黏液变性,部分病例间质表现为互相连接的纤细纤维间隔,内含薄壁血管,成纤维细胞丰富,胶原纤维疏松肿瘤无包膜,侵袭性较强,常浸润周围的黏膜、腺体和肌肉组织,可见神经周浸润,但一般无血管浸润。
免疫组化:
瘤细胞表达AE1/AE3、CK7、CK5、CK6、CK14、CK8/18、CK19等,CK20阴性,p63呈弥漫阳性,vimentin 常呈阴性,但部分病例可阳性。部分病例EMA阳性,肌上皮标记物如S-100、SMA、calponin 阴性。
有学者发现口咽部的涎腺HCCC P16阳性,阳性率为5%-80%,但RNA原位杂交结果显示高危型HPV均为阴性,病毒感染与否及其与肿瘤发生之间的关系仍有待进一步研究。
分子病理:
HCCC具有EWSR1基因相关易位,并进一步证实EWSR1和ATF1基因融合。有报道分别发生于舌根、肺和鼻咽的3例呈显著黏液分化的HCCC具有EWSR1-CREM基因融合。
鉴别诊断:
1.黏液表皮样癌:这是最容易与HCCC相混淆的肿瘤,特别当其仅由透明样细胞和表皮样细胞构成时,此时黏液表皮样癌中的中间型细胞与HCCC中的嗜酸性细胞很相似,而且高达50%的HCCC病例中会出现局灶性黏液分化,特别是在疑难病例或者小活检标本中,仅靠形态和免疫组织化学不易区分,需行EWSR1和(或)MAML2基因易位检测辅助诊断。
2.肌上皮癌:透明细胞型肌上皮癌与HCCC形态相似,仅凭形态鉴别较为困难,但免疫组织化学染色能够提供较大帮助,因为HCCC通常不表达S-100、Calponin、SMA等肌上皮相关标志物。
3.伴有透明细胞样特点的涎腺鳞状细胞癌:涎腺鳞状细胞癌罕见,多数情况下细胞异型性明显,细胞核大小不一、不规则,核分裂象易见,可见如角化、间桥等鳞癌特点,或鳞状上皮异型增生移行至鳞癌的形态改变。
4.转移性肾透明细胞癌:肾透明细胞癌转移到涎腺或头面部偶有发生。就形态而言,肾透明细胞癌的癌巢之间有丰富的充满红细胞的毛细血管网,这在涎腺HCCC几乎不可见。此外,肾透明细胞癌几乎不表达P63、CK5/6,其他肾癌标志物染色也有助于进一步确诊。
治疗与预后:
涎腺HCCC患者初诊时多为局限性病灶,部分发生局部淋巴结转移,极少数发生远处转移。患者5、10和20年疾病特异性生存率分别为81.3%、69.6%和55.3%。病变局限且仅行手术切除治疗的患者5、10年DSS可分别达96.4%和86.3%。单一手术治疗、手术联合放疗、单一放疗的10年DSS分别86.3%、57.6%和18.8%。
结果显示,女性患者、无淋巴结转移、无远处转移的患者预后较好,而手术切除可能也是目前最为合适的治疗方式。
要避免误诊,以防对患者造成不必要的过度治疗和加重心理负担。
患者的总体预后较好。
诊断体会:
1.本例罕见,最初考虑是黏液表皮样癌及鳞状细胞癌,标本全部取材,均未见黏液细胞及角化细胞,所以产生疑问,接下来是考虑鳞癌,但是表面鳞状上皮完好,并无与间质内肿瘤组织相延续,而且Ki-67很低,还是不支持。在诊断之际,临床医生曾电话我们加做P16免疫组化,我当时有些疑惑,他们的目的是为了研究清楚与HPV感染的关系?免疫结果出来,P16确实斑驳阳性表达,复片确实看到大量透明细胞,部分细胞似“挖空样”,加上间质玻璃样变明显,与同事反复讨论,最终确定该诊断。
2.查阅原发性肺涎腺型肿瘤(PSGTs),通常起源于气管、支气管腺黏膜下的上皮,典型表现为腔内病变,很少发生在外周肺实质。2021年WHO胸部肿瘤分类列出了6种PSGTs亚型,其中提到玻璃样透明细胞癌(HCCC),形态与本例完全一致,顺便深入对比学习。
3.遗憾的是患者经济条件一般,没有来得及加做分子病理检测,已经出院,但形态典型,诊断无异议。
参考文章及书籍:
1.张岩,王正,陈彤箴,等.涎腺玻璃样变透明细胞癌8例临床病理学特征分析[J].中国癌症杂志,2023,33(2):168-173.
2.临床病理诊断及鉴别诊断---口腔颌面部疾病,第1版,主编:李铁军,副主编:陈新明,陈小华,人民卫生出版社.




















共0条评论