[导读] 作者:abin
摘要
目的:描述罕见的貌似女性生殖器官浆液性癌的浸润性乳腺癌(浆液样乳腺癌,SLBC),研究其临床病理,免疫表型和遗传特征。
方法与结果:所有患者均为女性(n=15,中位年龄49岁),无女性生殖器官恶性肿瘤病史。SLBC组织学特征为成角的、分支的、有时吻合的腺体,伴微乳头状和/或假乳头状管腔内突起,位于促结缔组织增生性间质内。大多数SLBC为三阴性(TN,n=10)或HER2阳性(n=2),组织学分级为2级或3级,少数为ER低阳性/HER2阴性,低级别(n=3)。CK5/6阳性(10/10),与分级和受体状态无关。所有SLBC均表达GATA3(14/15)、TRPS1(7/7)和/或mammaglobin(MMG)(4/13)。SOX10在TN(9/10)和ER低阳性(3/3)肿瘤中均为阳性,而在HER2阳性肿瘤中为阴性。WT1普遍阴性,PAX8仅局灶表达于一例MMG阳性肿瘤。ER阴性的SLBC均为p53异常,9/11为p16异常,而ER阳性的SLBC中p53和p16均为野生型(3/3)。TP53是唯一频繁突变的基因,在所有ER阴性(10/10)肿瘤中发生改变,但在ER阳性肿瘤中无一改变(0/4)。临床表现多变。新辅助化疗仅1/6患者病理完全缓解。
结论:SLBC是浸润性乳腺癌的一种罕见的形态学模式,貌似转移性女性生殖器官浆液性癌,是一种潜在的诊断陷阱。SLBC在分级、激素受体状态和致癌驱动因素改变方面具有异质性,未发现特异性的遗传基础。需要进一步研究来评估这些肿瘤的临床行为。
关键词:乳腺癌,浸润性导管癌,二代测序,p16,p53,浆液性癌
介绍
我们曾遇到罕见的浸润性乳腺癌,其组织形态与女性生殖器官发生的浆液性癌非常相似,我们称之为浆液性样乳腺癌(serous-like breast carcinomas,SLBC)。我们注意到文献中以前关于所谓的管状乳头状癌的报道似乎显示类似的组织学特征,可能代表相同的肿瘤。目前尚不清楚这些肿瘤是否包括具有独特的共同遗传和分子基础和/或特征性临床行为的单独类型的乳腺癌,或者它们是否代表非特殊型浸润性乳腺癌(IBC-NST)的特殊形态模式。
本研究评估了15例SLBC的临床病理特征、免疫组化表达模式和基因改变,以及它们对新辅助化疗的反应。
结果
浆液性样乳腺癌的临床病理特征
所有患者均为女性,诊断年龄27~75岁,平均49岁。所有患者都没有已知的乳腺癌或女性生殖器官恶性肿瘤的致病性种系风险变异。
在三阴性SLBC患者中,75%(6/8)出现早期疾病。63%(5/8)的三阴性SLBC临床和/或病理分期为T2或T3期,腋窝淋巴结转移占38%(3/8)。三阴性SLBC的中位大小为3.3 cm(0.6~12 cm,包括新辅助治疗肿瘤的放射学预处理大小和未治疗肿瘤的病理大小)。ER阳性的SLBC病理分期为T1b或T1c,淋巴结阴性,中位体积较小,为1.2 cm(0.6~1.5 cm)。
表1 浆液性样乳腺癌的临床病理特征
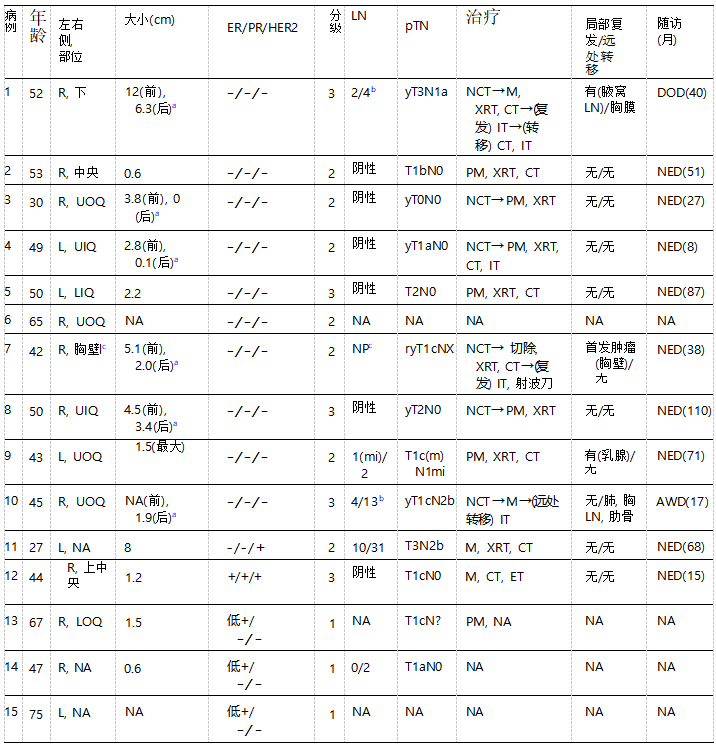
AWD,带病存活;CT,化疗;DOD,死于疾病;ET,内分泌治疗;IT,免疫治疗;L,左;LOQ,下内象限;LN,淋巴结;LOQ,下外象限;M,乳房切除术;NA,不可用;NP,未执行;mi,微转移;NCT,新辅助化疗;NED,无疾病迹象;PM,乳腺部分切除术;R,右;UIQ,上内象限;UOQ,上外象限;XRT,放射治疗。
a新辅助化疗前的肿瘤大小(前),新辅助化疗后病理大小(后)。
b新辅助化疗后。
C所评估的肿瘤在胸壁首次复发时切除(三阴性浸润性导管癌,经NCT和双侧乳腺切除术,病理完全缓解)。
浆液性样乳腺癌的组织学特征
组织学检查,所有的SLBC具有特征性形态学,均表现为完好的、成角的、分支的、有时吻合的腺体,伴微乳头状和/或原始假乳头状突起,突向开放的管腔内,背景为促结缔组织增生性至胶原化间质(图1和图2)。这种形态模式就像女性生殖器官发生的浆液性癌的典型特征,在低倍镜下容易识别,在所有病例中占据所评估肿瘤的大多数(至少70%)。小灶非浆液样区域类似于不形成腺体的IBC-NST,仅1例例外(浸润性乳头状特征伴中央坏死,病例10)。胞质呈不同速度的双染性到嗜酸性,常有合胞体外观,部分病例中含有大小不等的空泡(图1E,F)。少数病例的部分腺腔内有嗜酸性或黏液性分泌物(图1H)。
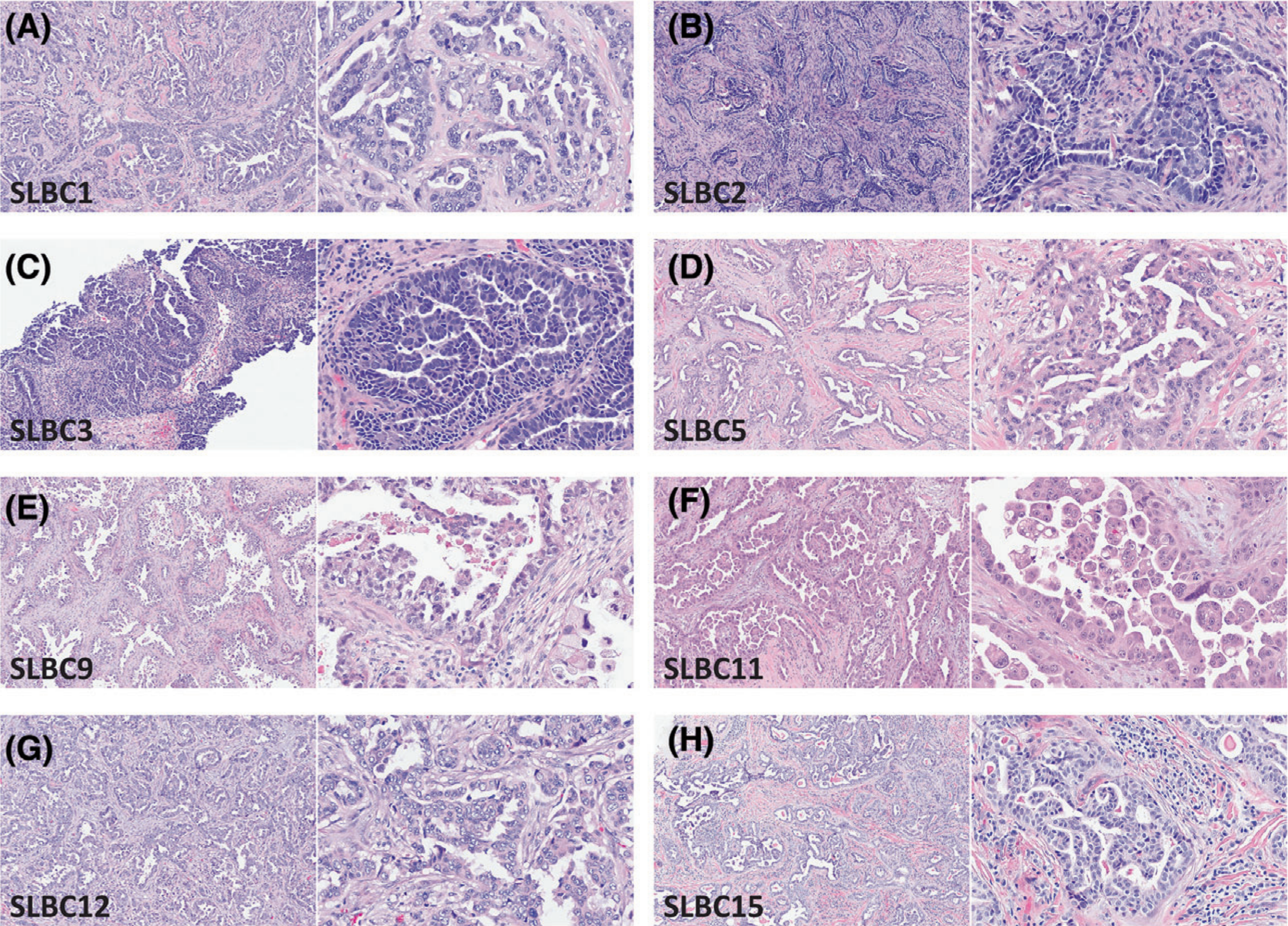
图1 浆液样乳腺癌的组织学特征。(A) SLBC1,三阴性。(B)SLBC2,三阴性。(C)SLBC3三阴性。(D)SLBC5,三阴性。(E)SLBC9,三阴性。(F)SLBC11,ER-/PR-/HER2+,(G)SLBC12,ER+/PR+/HER2+,(H)SLBC15,ER低+/PR-/HER2-。注意腺体的常用定义模式,即微乳头状和/或原始假乳头状突起进入开放的管腔,位于促结缔组织增生性间质中。
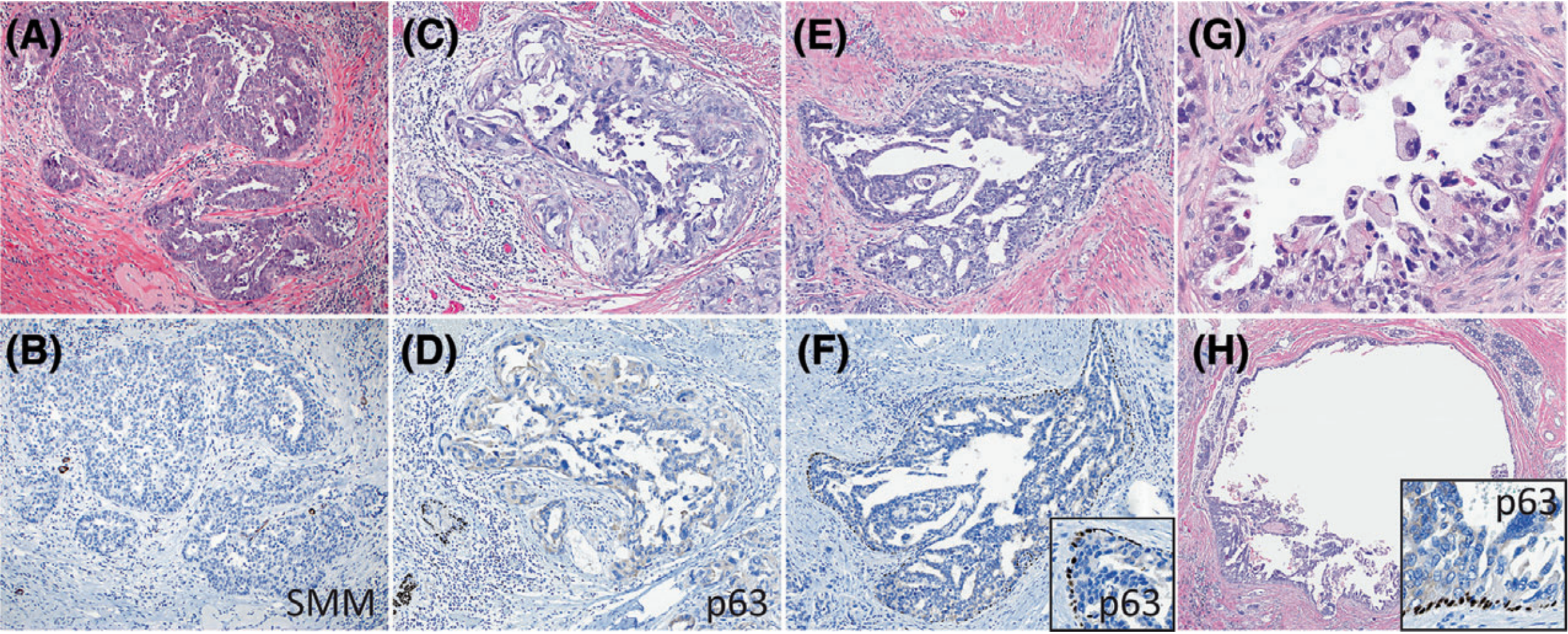
图2 浆液样乳腺癌(SLBC)的浸润成分貌似导管原位癌(DCIS),反之亦然。(A-D)
SLBC8(A,B)和SLBC1(C,D)的浸润性腺体貌似DCIS。肌上皮免疫组化染色有助于区分(B,SMM;D,p63)。(E,F)相反,具有微乳头状和/或乳头状生长模式的DCIS也可以貌似浸润性浆液样腺体(SLBC1)(F,p63)。(G) SLBC9的浸润性腺体貌似DCIS。(H) SLBC1扩张的大导管更容易识别为DCIS(插图p63)。
三阴性和HER2阳性SLBC(见下文)普遍具有高级别核,核圆形到不规则轮廓、深染到空泡状染色质,以及单个到多个、小到显著的核仁(图1A-G)。在所有三阴性和HER2阳性病例中,核分裂活性较高(诺丁汉分级至少2分)。然而,尽管核级较高且核分裂计数高,但大多数(58%,7/12)三阴性和HER2阳性的SLBC为诺丁汉2级,原因是腺体生长模式为主(诺丁汉分级1或2分)(表2)。
表2 从生物标志物状态看浆液样乳腺癌的组织学特征
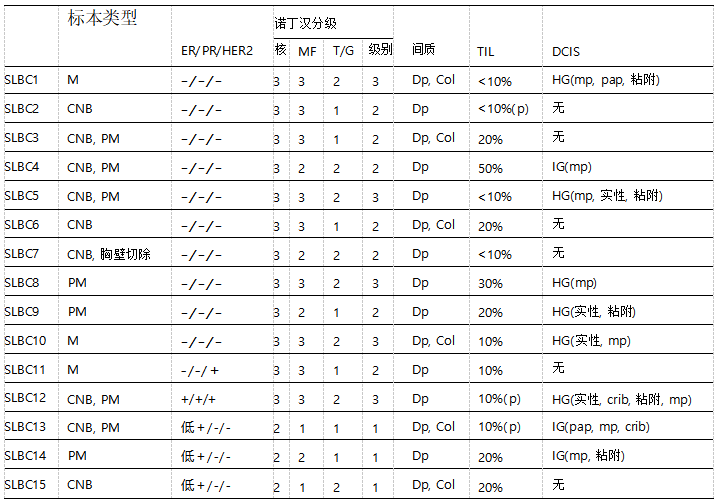
CNB,粗针穿刺活检;Col,胶原化;crib,筛状结构;DCIS,导管原位癌;Dp,促结缔组织增生;HG,高核级别;IG,中核级别;M,乳房切除术;MF,核分裂评分;mp,微乳头状;p,外周;pap,乳头状结构;PM,乳腺部分切除术;T/G,小管/腺体分化评分;TIL,肿瘤浸润性淋巴细胞。
就像高级别浆液性输卵管卵巢癌,高级别细胞学和高分化生长模式之间呈现明显的细胞和结构不一致,是这些病例的诊断性特征。另一方面,所有三例ER低阳性SLBC(见下文)均为诺丁汉1级,具有低至中等核级别和少量核分裂象(图1H)。
间质TIL在大多数肿瘤中较低(≤20%者占87%,13/15)(表2)。浸润性癌伴有导管原位癌(DCIS)的肿瘤占60%(9/15)。DCIS的核级别通常反映浸润性癌的核级别,DCIS通常为微乳头状或乳头状(表2)。
在评估单个肿瘤病灶时,浸润性SLBC和微乳头状/乳头状DCIS之间的区别有时具有挑战性。可以通过整体浸润性生长模式、间质结缔组织增生和借助肌上皮细胞免疫组化进行区分(图2)。在两例三阴性SLBC的浸润性成分和两例DCIS(共三例SLBC)中发现钙化。1例浸润性成分钙化为砂粒体样。
浆液样乳腺癌中生物标记物状态
SLBC在激素受体和HER2表达方面具有异质性(表1和表2,图3)。10例SLBC呈ER/PR表达阴性和HER2过表达阴性(三阴性),3例肿瘤呈ER低表达(1%~10%),HER2过表达阴性。FISH和/或免疫组化证实2例SLBC过表达HER2(1例ER-/PR-,另一例ER+/PR+)。这2例HER2阳性肿瘤均弥漫性表达AR,而HER2阴性肿瘤均为AR阴性(0/12)。Ki-67增殖指数在三阴性SLBC中平均为60%(范围为20%~90%),在两例ER阳性肿瘤中分别为~10%和~15%。
浆液样乳腺癌的免疫组化表达谱
SLBC的免疫组化结果如图3所示,代表性图像如图4和图5所示。所有SLBC均表达乳腺标志物GATA3、TRPS1和/或MMG。除1例外(93%,13/14)GATA3均呈阳性,9例(64%)呈强弥漫性染色,其余均呈斑片状染色(图4E和5E,M)。MMG阳性率为31%(4/13),包括单一GATA3阴性肿瘤,主要呈局灶性表达(3/4例)。TRPS1在7例肿瘤中均为阳性(6例为三阴性,1例为ER+/HER2+),其中6例呈中-强弥漫性染色,1例呈斑片状染色。SOX10是一种在TNBC中也经常表达的转录因子,在80%(12/15)的SLBC中呈弥漫性阳性,包括90%(9/10)的三阴性肿瘤(图4F)和所有三例ER低阳性肿瘤(图5F),而HER2阳性病例均为阴性(图5N)。所有SLBC对GCDFP-15均为阴性(0%,0/13)。WT1是一种在浆液性输卵管卵巢癌中表达的转录因子,在所有肿瘤中均为核染色阴性(0%,0/15),在某些情况下为非特异性细胞质染色(图4K)。1例MMG阳性,GATA3阴性。基底样角蛋白CK5/6在所有已检测病例中均呈阳性(100%,10/10),包括三阴性(n=7,图4G)、ER低阳性/HER2(n=2,图5D)和三阳性(n=1,图5L)肿瘤。
肿瘤抑制因子p53在ER阴性的SLBC(9/10三阴性,1例ER-/PR-/HER2+)中表达异常(91%(10/11),包括弥漫性强染色(7/10,图4I)、完全不染色(2/10)或胞质染色(1/10)。1例三阴性SLBC以p53阴性为主,局灶性弱染色为模棱两可;该肿瘤含有TP53突变(SLBC9,见下文)。相反,所有ER阳性SLBC(1例三阳,2例ER低阳性/HER2-)显示野生型p53免疫染色模式(图5G,O)。
细胞周期调节因子和肿瘤抑制因子p16在82%(9/11)的ER阴性SLBC中表达异常(8/10三阴性,1例ER-/PR-/HER2+),其中8例呈弥漫性强染色(图4J),1例三阴性肿瘤完全无染色。相反,ER阳性的SLBC(1例三阳,2例ER低阳性/HER2-)显示p16染色呈正常的斑片状染色(图5H,P)。
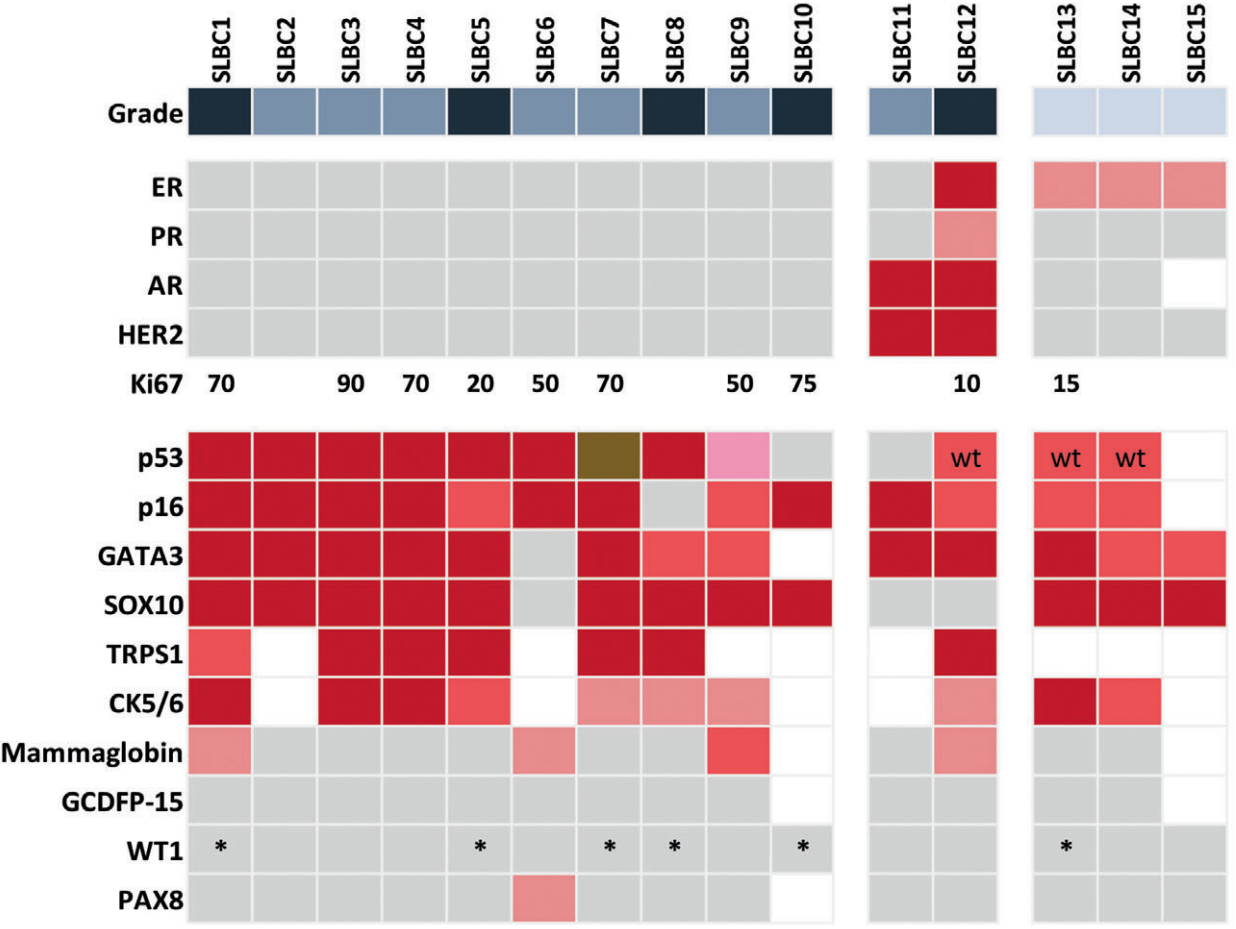

图3 浆液样乳腺癌的免疫组化研究。
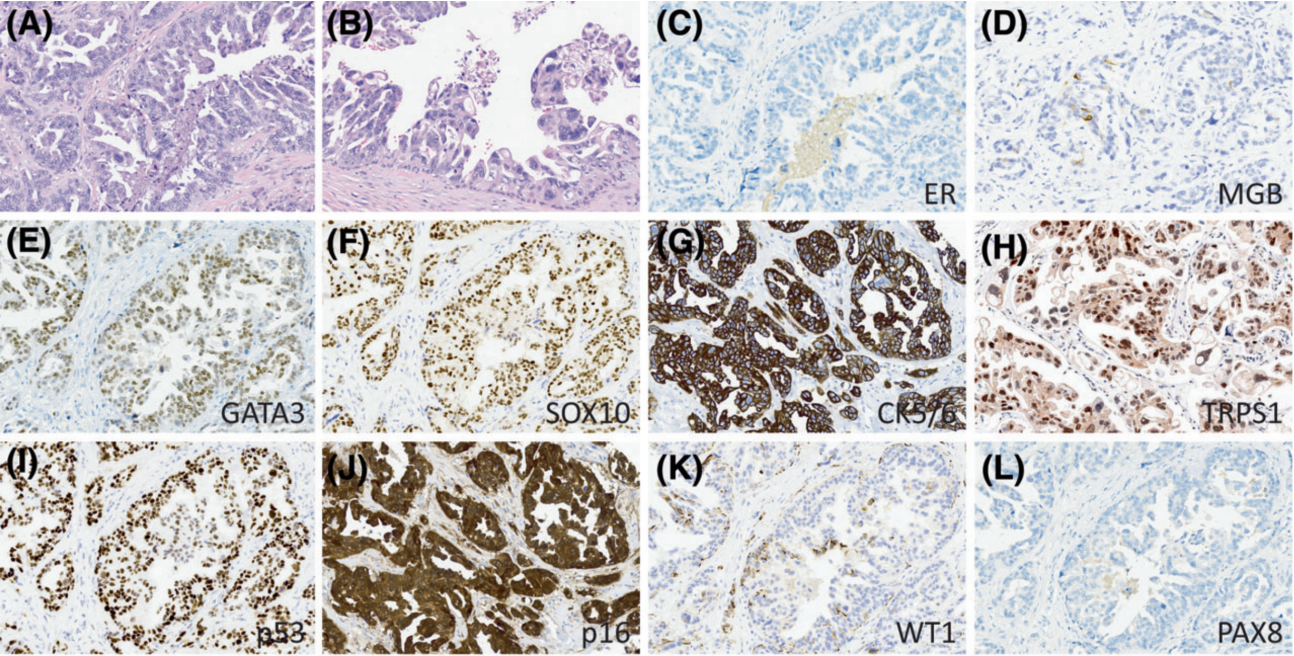
图4 三阴性浆液样乳腺癌的免疫免疫组化表达谱,SLBC1。(A)高倍镜下具有典型形态学并伴有导管原位癌(B),二者具有相似的细胞学特征。(C) ER为阳性。(D) MMG呈局灶性阳性。(E) GATA3、(F)SOX10和(G)CK5/6呈弥漫性阳性,(H)TRPS1呈斑片状阳性。(I)p53(过表达)和(J)p16(过表达)的异常表达。(K)浆液性癌标记物WT1和(L)苗勒管标记物PAX8均为阴性。
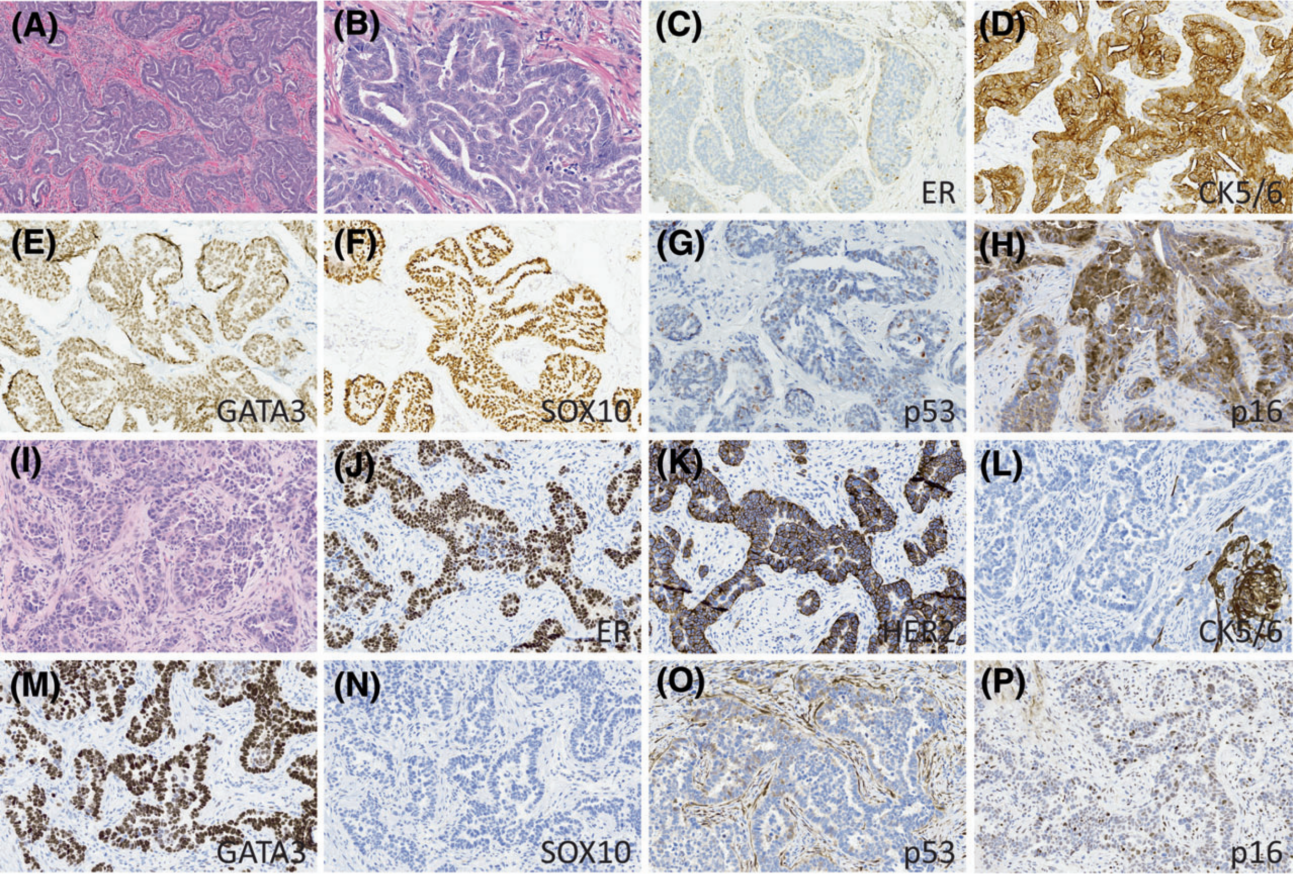
图5 非三阴性浆液样乳腺癌的免疫组化表达谱。
A-H为SLBC13。这例低级别肿瘤表现为(C)ER低阳性(<10%,弱)和(D)弥漫性CK5/6表达。与其他SLBC一样,(E)GATA3和(F)SOX10呈弥漫性阳性。(G) p53和(H)p16在ER阳性肿瘤中均为野生型表达。
I-P为SLBC12。这例高级别肿瘤显示(J)ER弥漫强阳性和(L)HER2过表达。(L)CK5/6呈局灶性阳性。(M) GATA3呈弥漫性阳性,而(N)SOX10在2例HER2阳性肿瘤中均呈阳性。(O) p53和(P)p16表达模式为野生型。
浆液样乳腺癌的遗传学
图6显示了NGS在SLBC中识别的致病性和可能的致病性基因改变,表S1中列出了所有突变的汇总。平均靶区覆盖率为每靶区间隔786±534个独特读数(范围410-2509)(表S2)。


图6 浆液样乳腺癌的致病/可能致病基因改变。
除1例(SLBC15,12.4/Mb)外,所有病例的肿瘤突变负荷均<10/Mb。拷贝数分析显示,除1例ER低阳性外,所有肿瘤中均有大量染色体获得和丢失,36%(5/14)具有复杂的非整倍体特征(图6)。
在所有ER阴性的SLBC(100%;9例三阴性,1例ER-/PR-/HER2+)中,TP53基因突变,而在所有ER阳性的SLBC(0/4)中,TP53基因突变。除1例TP53 p.R306*突变(SLBC9)的p53免疫染色模棱两可外,免疫组化显示TP53突变状态与p53表达模式相关。其他重现性改变出现频率较低(在两例肿瘤中,各占14%),包括CCNE1、PIK3CA、KRAS、ARID1A和DNMT3A。除了一例具有失活RB1突变的肿瘤外,免疫组化检测到的p16异常的高频率并不容易通过RB-CDKN2A/B-CDK轴的基因改变来解释。未发现致病基因重排。
临床随访和结局
对大多数三阴性或HER2阳性SLBC患者进行临床随访(92%,11/12,平均随访48个月;范围8-110个月),但ER低阳性/HER2阴性肿瘤患者均无临床随访(表1)。所有随访患者均接受化疗(11/11),其中6例行新辅助化疗。对新辅助化疗的反应不一致。只有1例患者获得病理完全缓解(pCR),其余患者的RCB指数分别为I(1例)、II(2例)和III(2例)(表S3)。手术治疗包括乳腺部分切除术58%(7/12),乳腺切除术33%(4/12),胸壁切除术1例。7例(7/7)行保守性手术,2/4行乳腺癌根治术,并接受乳腺放疗。3例(27%)发生局部复发(2/11)和/或远处转移(2/11)。大多数患者在本次研究时(82%,9/11)无病存活,1例(9%)死于疾病(术后40个月),1例(9%)在最后一次随访(17个月)时带病存活。
讨论
我们描述了一系列具有独特组织形态学的浸润性乳腺癌,它们与女性生殖器官的浆液性癌非常相似,我们称之为SLBC。根据已发表的乳腺管状乳头状癌(tubu-lopapillary carcinoma)的图像,我们注意到这些肿瘤似乎显示出与我们系列中的SLBC相似的组织学特征,并且大多数(如果不是全部)可能代表相同的实体。我们将这些肿瘤也称为SLBC,以强调与浆液性输卵管卵巢癌的形态学和分子相似性,并强调排除这些病例中转移的重要性。包括GATA3、SOX10、MMG、WT1和PAX8的免疫组化套餐可以区分SLBC与女性生殖器官浆液性癌,在乳腺中没有DCIS成分的情况下特别有用。
靶向NGS发现TP53是SLBC中唯一一个高频率反复突变的基因,在所有ER阴性的SLBC中发现突变。大多数肿瘤的基因组不稳定,拷贝数增加,常出现复杂的非整倍体。通过靶向测序分析的2例已发表的管状乳头状癌也含有TP53突变和PIK3CA扩增。这些结果总体上与高级别三阴性乳腺癌的遗传学一致,其中只有TP53和PIK3CA突变频率>10%,并且没有为SLBC作为一种基因独特的乳腺癌亚型提供先验支持。同样,TP53也是唯一在卵巢高级别浆液性癌中发现的高度复发突变基因,几乎在所有肿瘤中都有突变。
我们的结果确定p16是ER阴性SLBC中肿瘤发生的驱动因素,在大多数情况下观察到异常表达。除了一个具有RB1突变的肿瘤外,我们没有发现直接的遗传基础来解释ER阴性SLBC中p16异常免疫表达的高频率,我们推测p16异常表达可能与TP53突变有关,正如在其他恶性肿瘤中所描述的那样。p16在我们系列中大多数ER阴性SLBC中与SOX10共表达,并且我们注意到Carrasco Tenezaca等人在他们对两个管状乳头状癌的研究中也报告了这两种标记物的表达。事实上,p16和SOX10在非特殊类型的三阴性乳腺癌中普遍共表达,并且与高肿瘤分级和高分化相关。不良预后因素。
表3 已发表文献中诊断为管状乳头状癌的乳腺癌
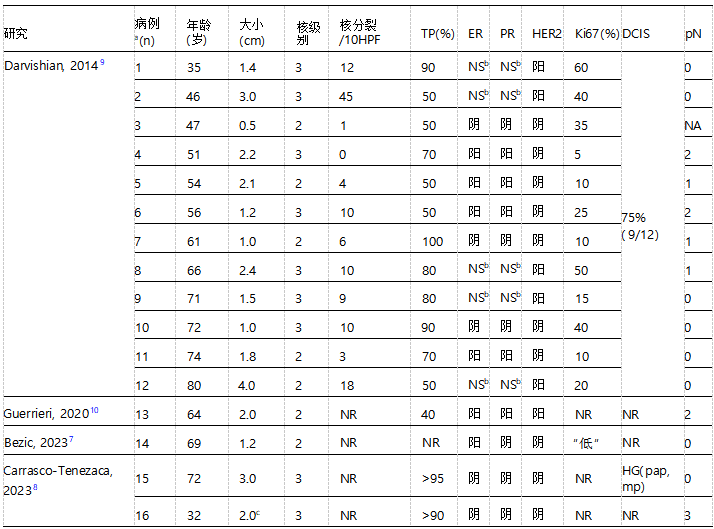
DCIS,导管原位癌;HG,高品位;Mp,微乳头状,NA,不可用;NR,未报告;NS,未指定;pN,节点级(AJCC);Pap,乳头状;TP,管状乳头状。
a在Darvishian等人的研究中,除一名男性外,所有患者均为女性
b在Darvishian等人的研究中,5例HER2+病例中,4例为激素受体阳性,1例为激素受体阳性,但未单独进一步明确。
c新辅助化疗前测量肿瘤大小。
结论
总之,SLBC是一种罕见的浸润性乳腺癌,其组织形态学与女性生殖器官来源的转移性浆液性癌相似。潜在的诊断陷阱可以通过免疫组化套餐来解决,包括乳腺标记物GATA3、SOX10和MMG,以及女性生殖器官标记物WT1和PAX8。尽管SLBC具有惊人的形态学相似性,但在分级、生物标志物和化疗反应方面,SLBC似乎是异质性的。大多数三阴性SLBC由致癌驱动因素p53和p16驱动,但具体的遗传基础尚未确定。总体而言,SLBC是IBC-NST的一种不寻常的形态学模式,而不是一种组织遗传学上不同的乳腺癌亚型。需要进一步评估这些特殊肿瘤的临床行为。
文献来源:
Krings G, Shamir ER, Laé M, Bean GR, Post MD, Schnitt SJ, Chen YY. Serous-like breast carcinomas: immunophenotypic, genetic, and clinicopathologic characterization of a morphologically distinct group of tumours. Histopathology. 2025 Apr;86(5):779-792. doi: 10.1111/his.15385. Epub 2024 Dec 9. PMID: 39654368.























共0条评论