[导读] 作者:罗遍野
1病史:女性,69岁,因“体检发现右肺肿物1周”入院。既往史:10年前甲状腺左叶手术史,术后诊断为“(左叶)甲状腺滤泡性性腺瘤”。
2辅查:
胸部CT增强+3D(图1):双肺散在结节状高密度影,部分为钙质密度影,较大位于左肺下叶,大小约10x9mm,增强扫描明显强化。右肺下叶背段见小片高密度影,边缘欠清。
3组织病理活检
3.1大体肉眼观(图2):右中肺:部分肺组织,35*15*10mm,距切缘6mm,紧邻胸膜见一结节,8*6*3mm,切面灰红,实性质软,与周围分界尚清。
3.2镜下观(图3-图10):
在既往的左叶甲状腺中,见一直径约21mm的结节,边界清,包膜不厚,镜下瘤组织由多量大小一致、排列拥挤的小滤泡构成,滤泡为单层扁平上皮,滤泡内含胶质,间质血管充血,肿瘤周围可见纤维组织包膜,诊断为甲状腺滤泡性腺瘤。
在本次肺结节中,低倍镜下,在肺组织的紧邻胸膜见一类圆形结节,边界清楚;中倍镜下,结节内为典型的甲状腺滤泡结构,未见明确包膜;高倍镜下,肿瘤大部分由弥漫分布、分化良好、大小不等的滤泡结构构成,细胞核呈圆形或卵圆形,异型性不明显,核分裂象罕见,缺乏 PTC 细胞核特征,均未观察到肿瘤性坏死;结节中央的部分甲状腺滤泡上皮细胞增生,核似毛玻璃样,但不见核构及核内假包涵体,核内可见小核仁,核分裂象罕见。
3.3免疫组化(图11-图14)及分子结果:免疫组化示肿瘤细胞TG(+),TTF1(+),CK19(+),Galectin-3(-),MC(-),TPO(+),CD56(-);
分子病理检测结果:BRAF-V600E(未检测出突变)。
病理诊断:(右中肺)转移性甲状腺肿瘤,结合既往甲状腺手术史、组织形态、免疫组化及分子病理检测结果考虑转移性甲状腺滤泡性癌。
讨论
1背景
甲状腺滤泡癌(follicular thyroid carcinoma,FTC)是发生于甲状腺的第二常见恶性肿瘤,占原发性甲状腺恶性肿瘤的10%~20%。虽然大多数 FTC 生物学行为表现为惰性,但其转移率可达1.2%~13%。一般情况下,FTC经血行转移至内脏和/或骨。相较于甲状腺乳头状癌(papillary thyroid carcinoma,PTC)来说,终末器官转移是FT独特的表现。
2. 转移性FTC的临床病理特征
2.1临床特点
转移性FTC患者,约42%以远处转移为首发表现,58%以甲状腺原发结节为首发表现。
2.2影像学特征
影像学上,肺转移病灶常为多发,境界清楚。
2.3病理学特征
肉眼观
大体观,肺转移性FTC常表现为肺实质内或胸膜下多发或单发结节,界清,结节大小不等,切面呈灰红,质地均一,类似甲状腺样切面。
镜下观:
镜下观,组织病理学上表现为典型的滤泡性肿瘤,肿瘤由弥漫分布、分化良好、大小不等的滤泡结构构成,细胞核呈圆形或卵圆形,异型性不明显,核分裂象罕见.缺乏PTC细胞核特征,常观察不到肿瘤性坏死。以远处转移为首发表现FTC 中的活检组织可见到甲状腺滤泡样结构,形态学类似于甲状腺滤泡性腺瘤,其主要成分包括4种常见形态学亚型:微滤泡型(胎儿型)、实性型(胚胎型)、正常滤泡型(单纯型)、大滤泡型(胶样型)。微滤泡型及实性型的病例中肿瘤由紧密排列的微小滤泡、小梁或实性片块组成,肿瘤细胞呈立方或矮柱状、含深染或浅染的圆形核,核仅为轻度异型,核仁不明显,核分裂少见。正常滤泡及大滤泡亚型的病例则滤泡分化良好且成熟,非常类似正常甲状腺组织或结节性甲状腺肿。在确诊滤泡癌的病理切片上,滤泡上皮细胞均未见明显异型性、坏死及较多的核分裂,亦未见明显核沟、核包涵体及毛玻璃样核等PTC的核特征。
免疫表型:免疫表型方面,转移性FTC均不同程度表达甲状腺球蛋白(TC)、MC、PAX-8、HBME-1、甲状腺转录因子1(TTF-1)及细胞角蛋白(CKpan或CK19),ki67增值指数在1%-10%之间。
分子遗传学:分子遗传学方面,大部分有RAS突变(NRAS或HRAS),TERT 启动子突变、 BRCA2突变、PTEN突变、PTEN突变、NFI 突变。
3.鉴别诊断:
肺转移性FTC诊断不难,结合临床病史、形态学、免疫组化及分子检测,诊断不难,主要应与以下肿瘤相鉴别:
(1)神经内分泌肿瘤(类癌):甲状腺滤泡癌转移至肺的形态学表现与肺类癌形态学需鉴别,后者较前者更为常见。另外,部分甲状腺滤泡癌可首先以转移灶的形式被发现,因此对此两种病变鉴别十分必要。典型甲状腺滤泡癌会形成滤泡状结构,滤泡腔内常见分泌的红染胶质,通过免疫组织化学对两者鉴别是必要的。与甲状腺源性肿瘤不同,类癌表达Syn、CgA及CD56等神经内分泌标志物,不表达TG。
(2)肺内甲状腺组织异位:异位甲状腺组织形态学最常表现为结节性甲状腺肿,其次为正常甲状腺组织形态。支气管异位的甲状腺组织中亦可出现原发的甲状腺滤泡性肿瘤,由于两者均起源于甲状腺滤泡上皮,因此通过组织形态及免疫组织化学有时对两者鉴别往往无法提供有效帮助,详细了解病史对两者的鉴别极为重要。如患者有甲状腺滤泡癌病史,应回顾既往病理切片如两者形态一致,应考虑转移性病变;如患者无既往病史,应对甲状腺行超声等辅助检查,如无可疑性病变,应考虑起源于支气管异位甲状腺组织的滤泡性肿瘤。
4.治疗及预后
在治疗上,通常对转移的FTC采用I131治疗。除此之外,还可行手术和外放射等治疗方法。
参考文献
[1]赵兵,石玉香,袁静萍. 甲状腺滤泡癌脑部转移1例[J]. 临床与实验病理学杂志,2012,28(12):1420-1421. DOI:10.3969/j.issn.1001-7399.2012.12.038.
[2]Cracolici V, Kadri S, Ritterhouse LL, Segal JP, Wanjari P, Cipriani NA. Clinicopathologic and Molecular Features of Metastatic Follicular Thyroid Carcinoma in Patients Presenting With a Thyroid Nodule Versus a Distant Metastasis. Am J Surg Pathol. 2019 Apr;43(4):514-522. doi: 10.1097/PAS.0000000000001208.
[3]户燕姣,孙玲玲,丁莉,等. 支气管转移性甲状腺滤泡癌一例[J]. 中华病理学杂志,2014(5):338-339. DOI:10.3760/cma.j.issn.0529-5807.2014.05.012.
[4]韩静,魏建国,高献争,等. 肺转移性甲状腺癌56例临床病理学特征及预后[J]. 中华病理学杂志,2021,50(5):505-507. DOI:10.3760/cma.j.cn112151-20210119-00052.
[5]吴江华,丁婷婷,潘毅,等. 以远处转移为首发表现的24例甲状腺滤泡癌临床病理特征分析[J]. 中国肿瘤临床,2016,43(13):552-556. DOI:10.3969/j.issn.1000-8179.2016.13.369.
[6]冉雯雯,刘艺璇,孔维懋,等. 转移性甲状腺滤泡癌22例临床病理和分子病理学特征[J]. 临床与实验病理学杂志,2023,39(12):1453-1459. DOI:10.13315/j.cnki.cjcep.2023.12.009.
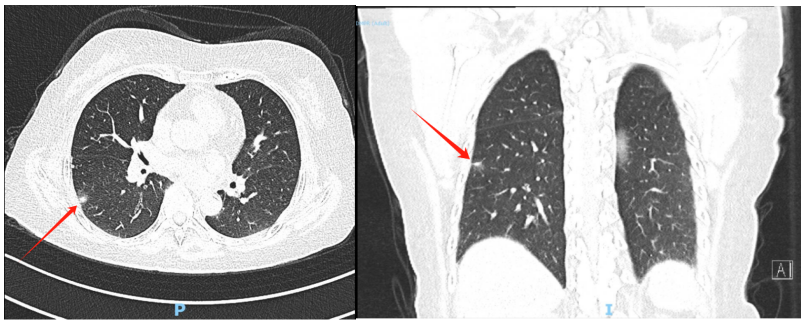

图1 胸部CT示右肺下叶背段见小片高密度影,边缘欠清。(左:横断面;右:冠状面)
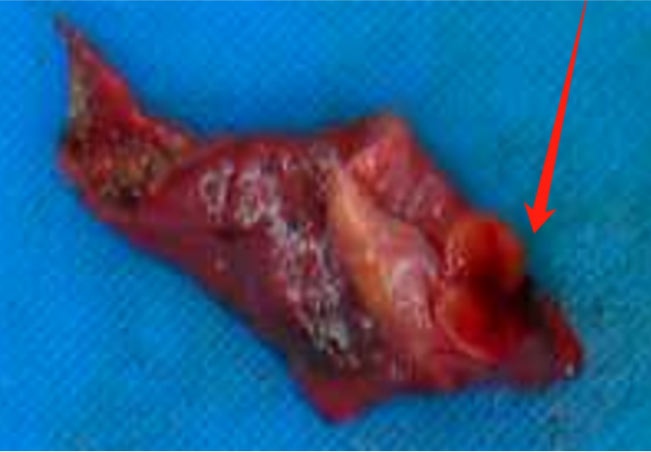
图2 肉眼观,肺胸膜表面见一灰红结节,与周围分界尚清.
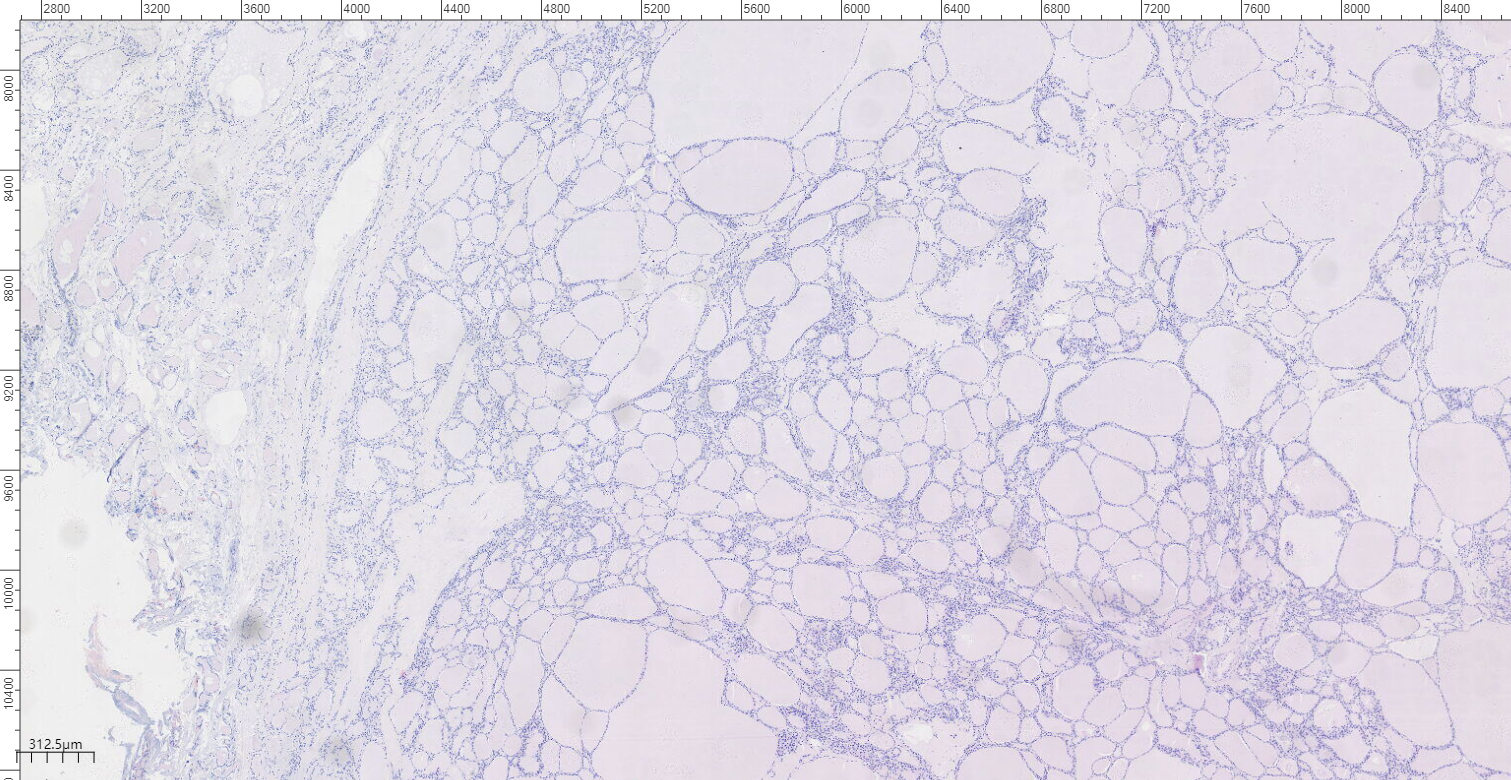
图3 中倍镜,甲状腺结节包膜不厚,甲状腺滤泡性腺瘤肿瘤细胞呈由多量大小一致、排列拥挤的小滤泡构成。
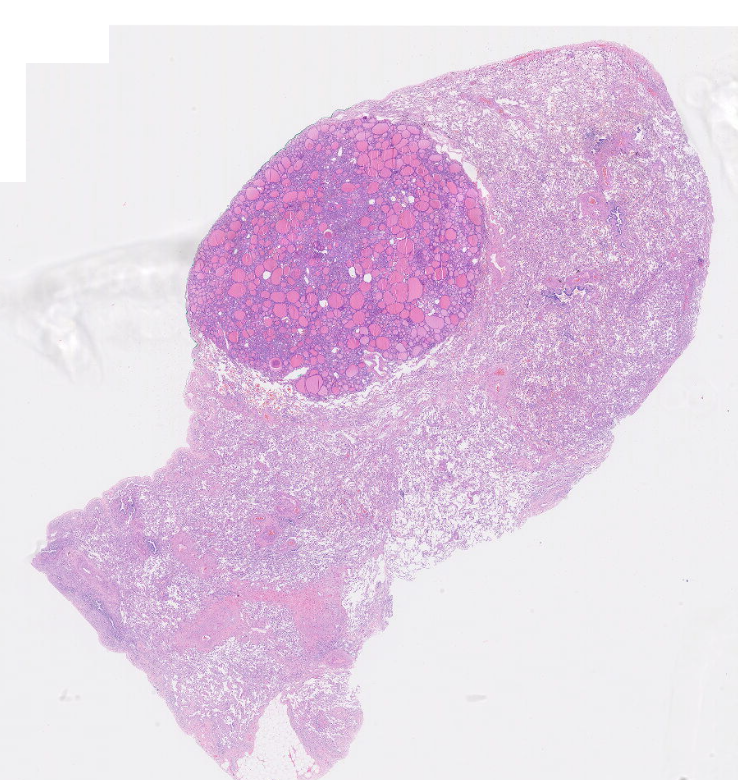
图4 肺结节中,低倍镜下在肺组织的紧邻胸膜见一类圆形结节,边界清楚
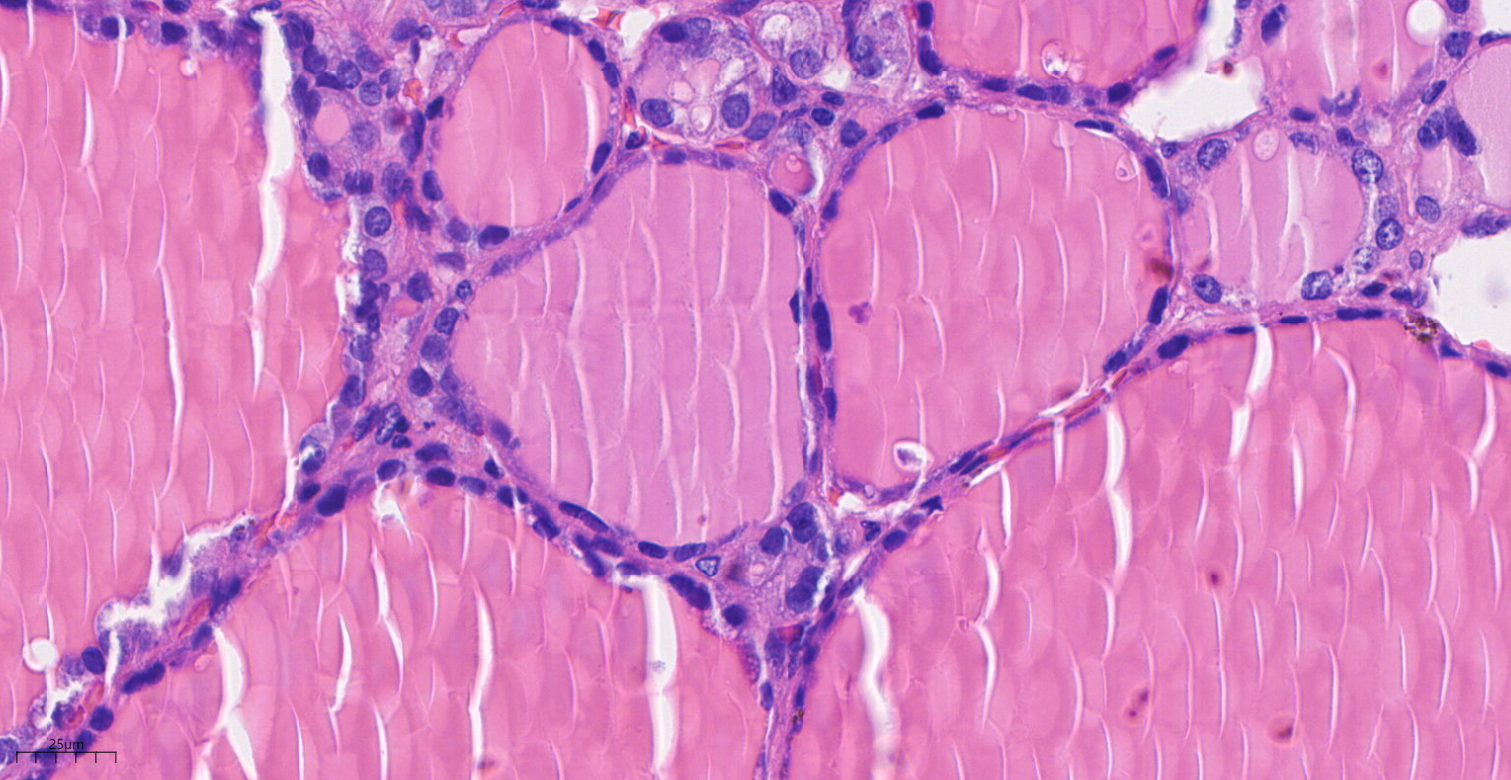
图5 高倍镜下见肺结节细胞核呈圆形或卵圆形,异型性不明显,核分裂象罕见,缺乏PTC细胞核特征
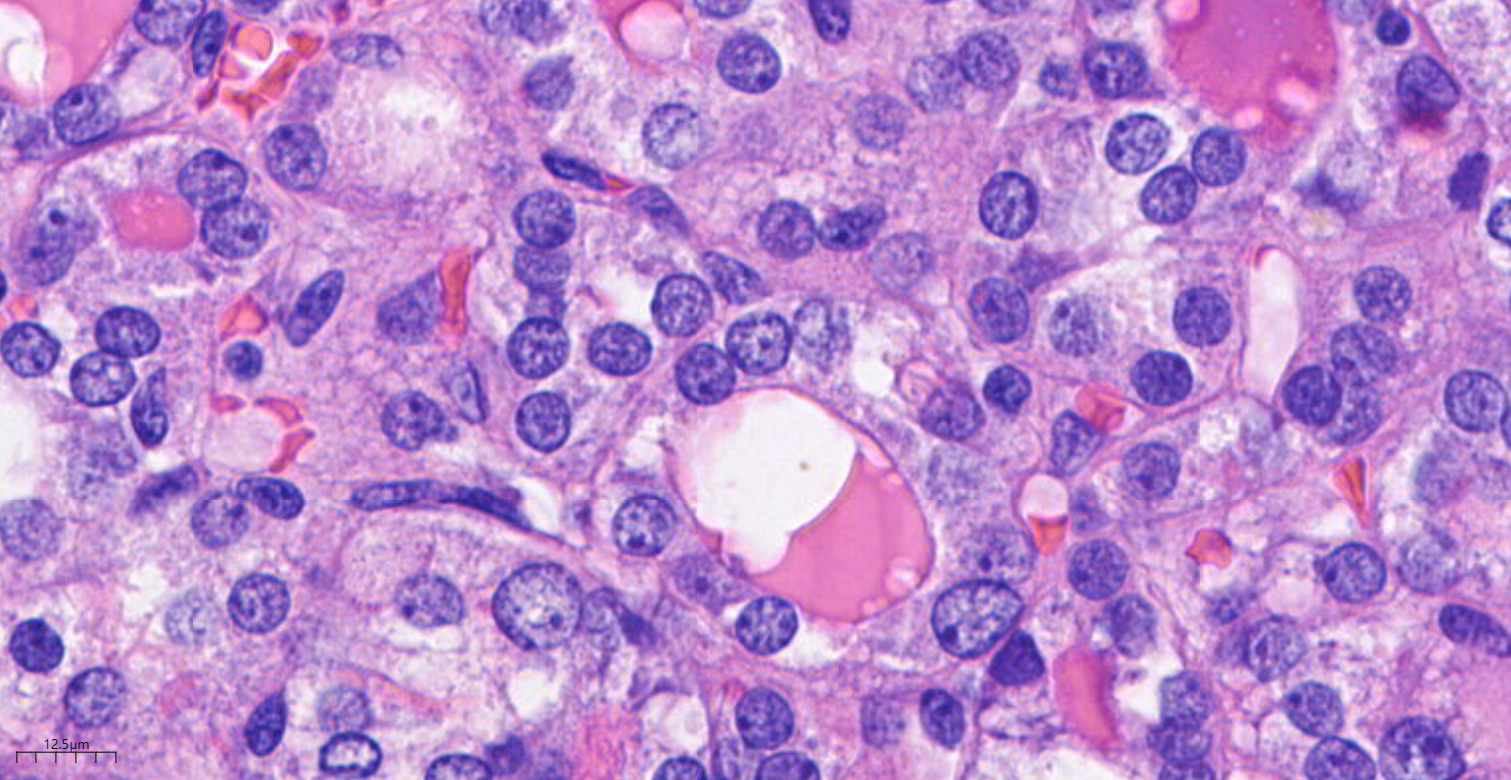
图6 高倍镜下,结节中央的部分增生甲状腺滤泡上皮细胞,核似毛玻璃样,核内可见小核仁,核分裂象罕见
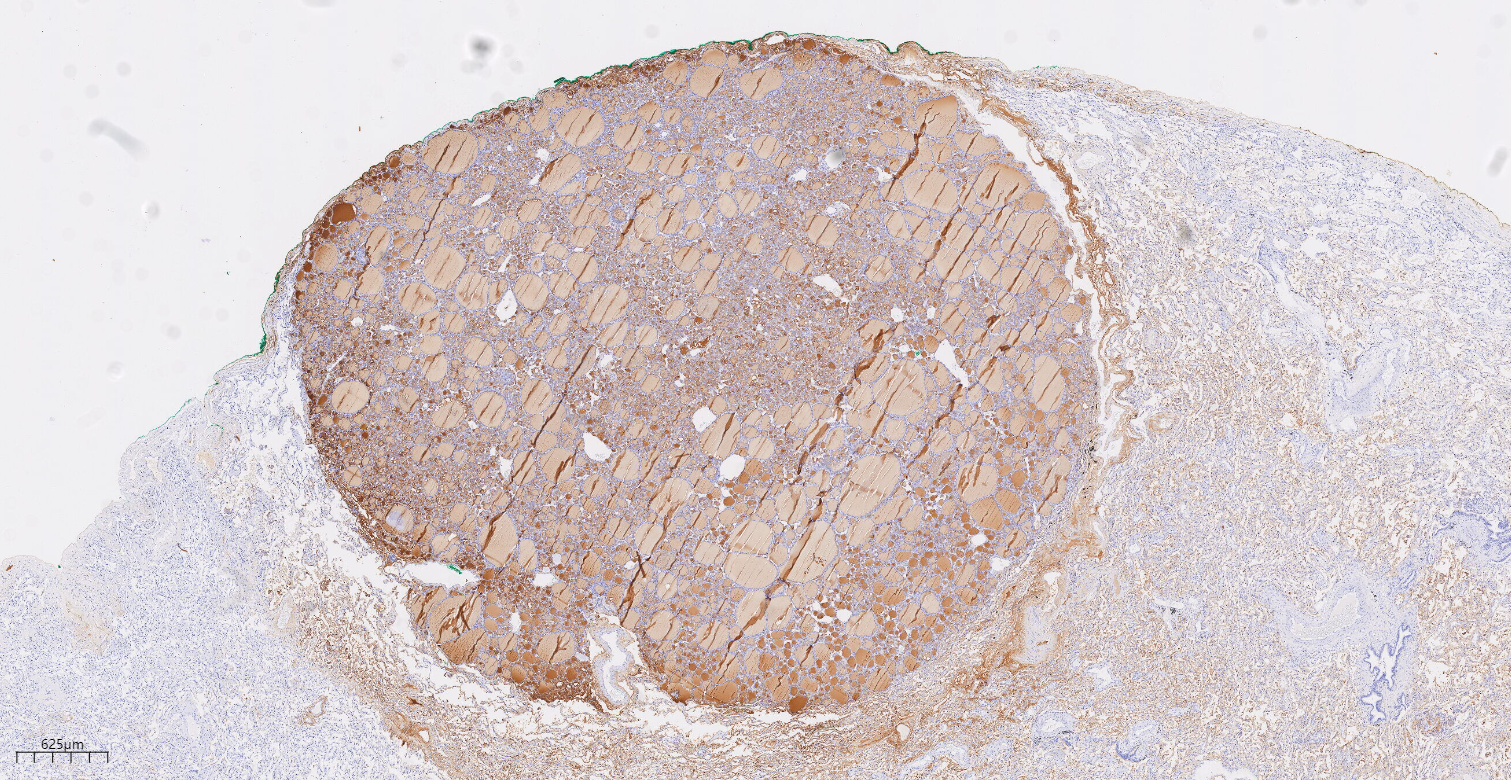
图7免疫组化示肿瘤细胞TG(+)
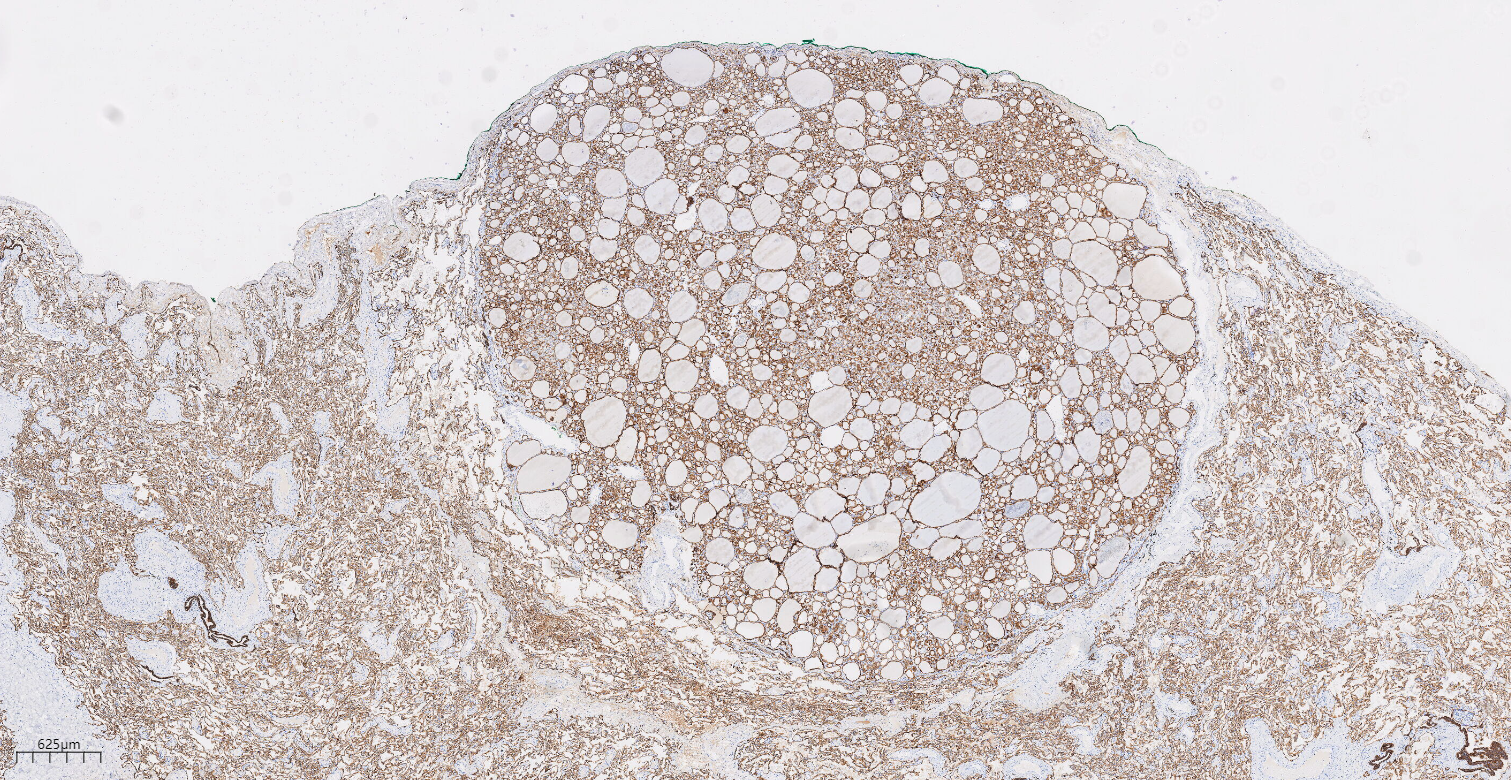
图8免疫组化示肿瘤细胞CK19(+)
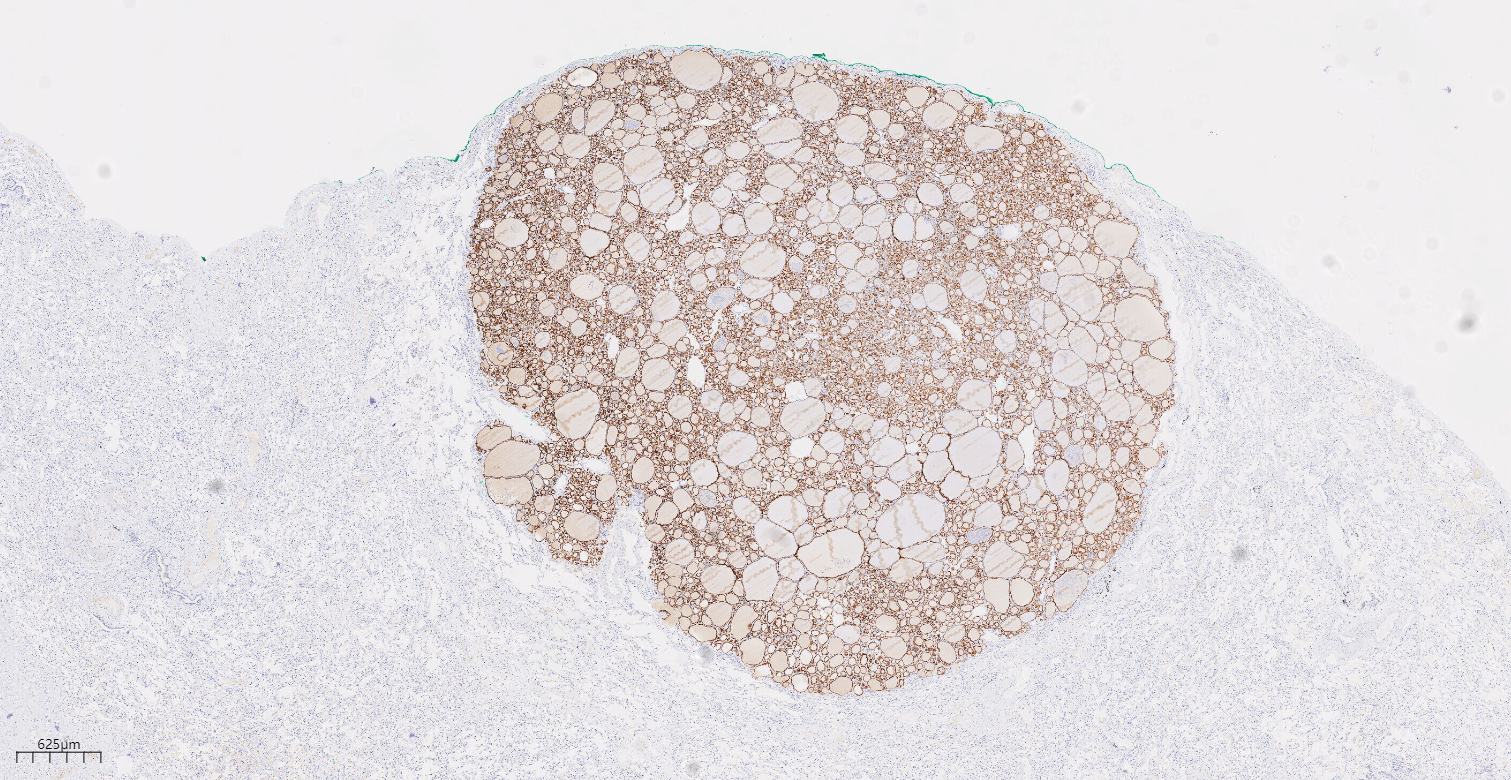
图9免疫组化示肿瘤细胞TPO(+)























共0条评论