[导读] 深圳市光明区人民医院 赵东晖 李庆军
病史:
患者,男,31岁,无明显诱因反复回吸涕中带血1年,左鼻塞,左眼肿胀,头痛、头晕。
影像检查:
鼻窦MR增强扫描示:左鼻腔-筛窦-额窦占位病变,侵犯左眼上斜肌,伴相应骨质破坏,考虑恶性肿瘤。
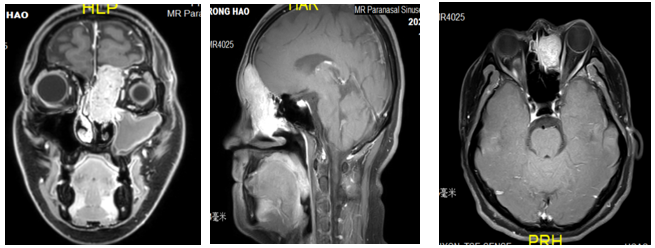
病理检查:
大体:
灰白碎组织一堆,直径约为1.2cm,全取。
镜下:
HE:
黏膜上皮下见癌组织大部分呈基底样排列,少数呈横纹肌样、浆样,核偏位、嗜酸性胞质、核仁明显,见核分裂象,并见横纹肌样细胞散在分布于基底样细胞之间,部分胞质内见空泡,伴坏死,间质纤维结缔组织增生。
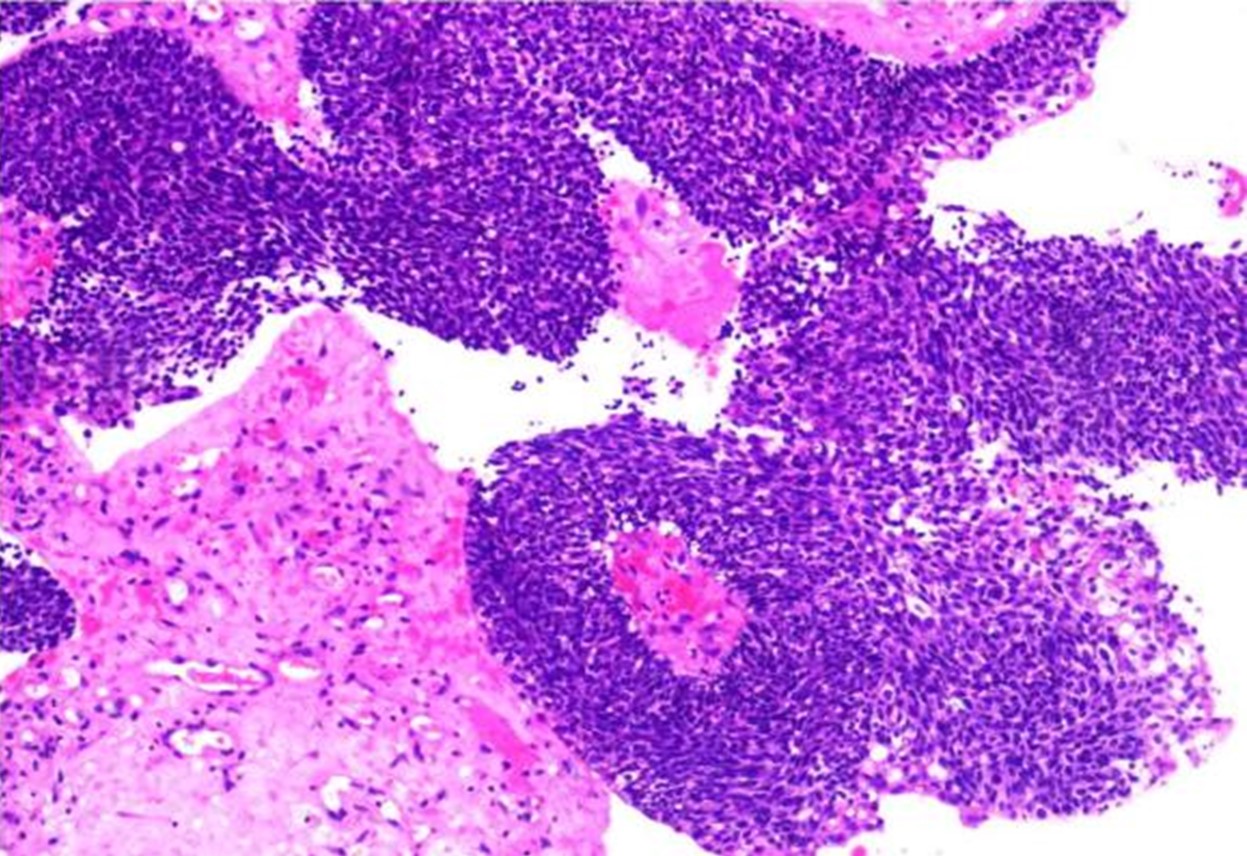 癌组织分化差,大部分呈基底样排列,未见明显的鳞状及腺样分化,浸润性生长,伴间质纤维组织增生
癌组织分化差,大部分呈基底样排列,未见明显的鳞状及腺样分化,浸润性生长,伴间质纤维组织增生
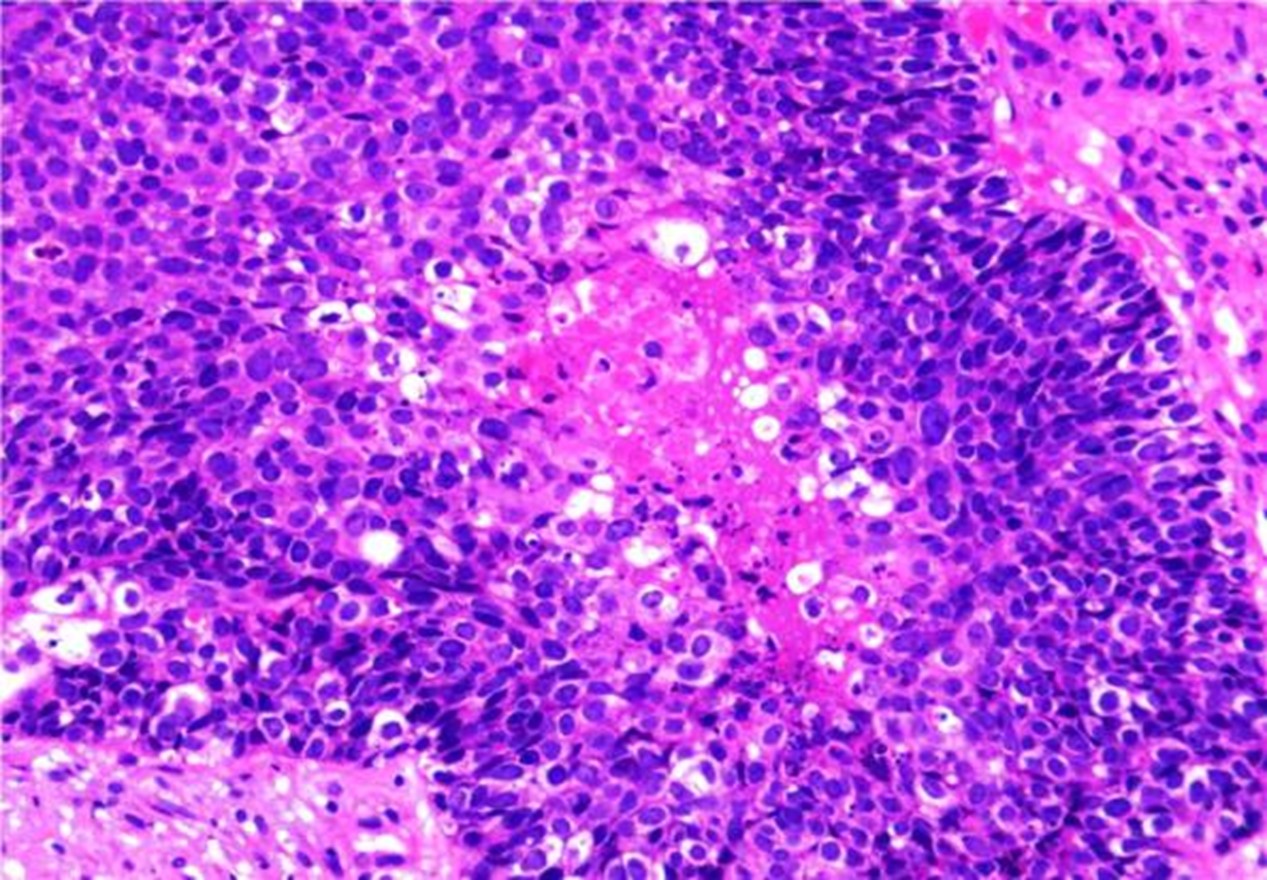 癌组织伴片状坏死,癌细胞呈横纹肌样、浆样,核偏位,胞质红染,部分透明
癌组织伴片状坏死,癌细胞呈横纹肌样、浆样,核偏位,胞质红染,部分透明
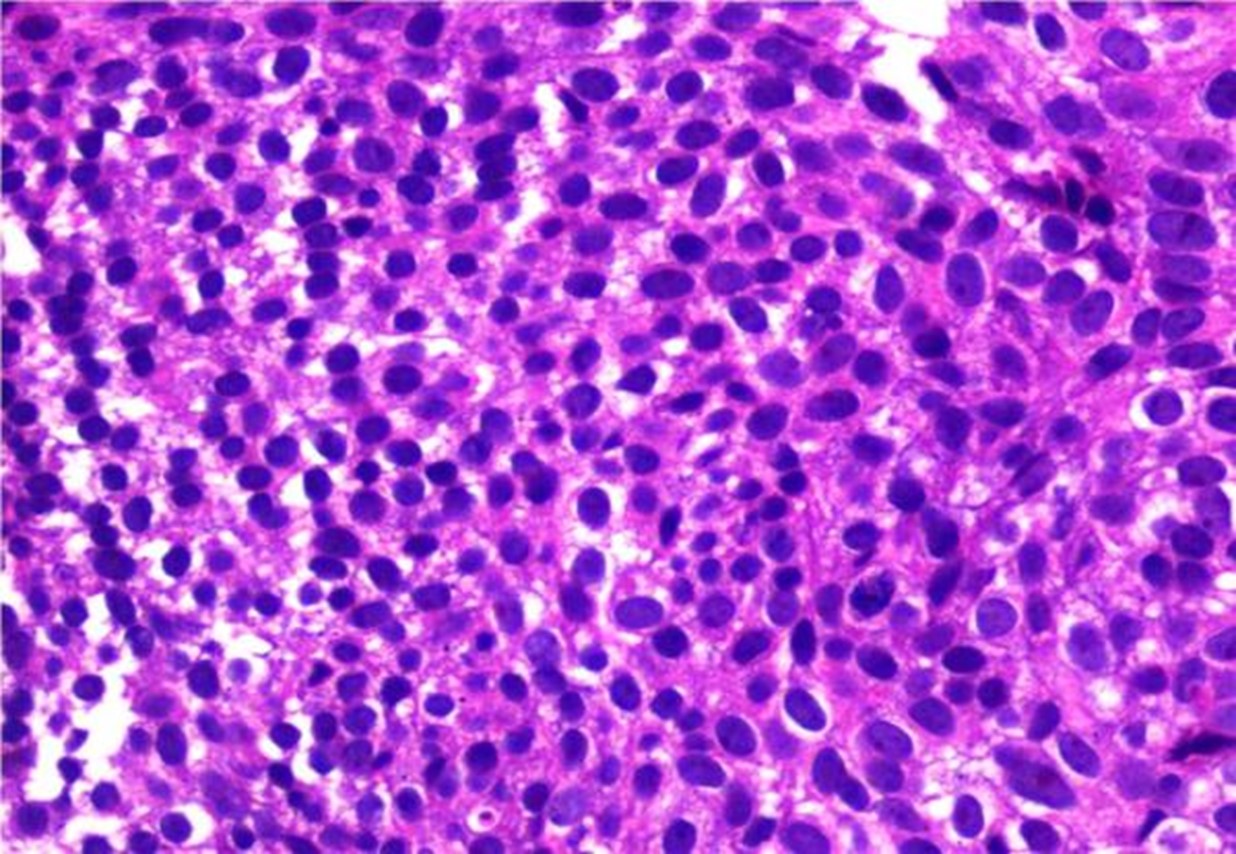
癌细胞核圆形,椭圆形,核增大,核浆比高,见核仁及核分裂象
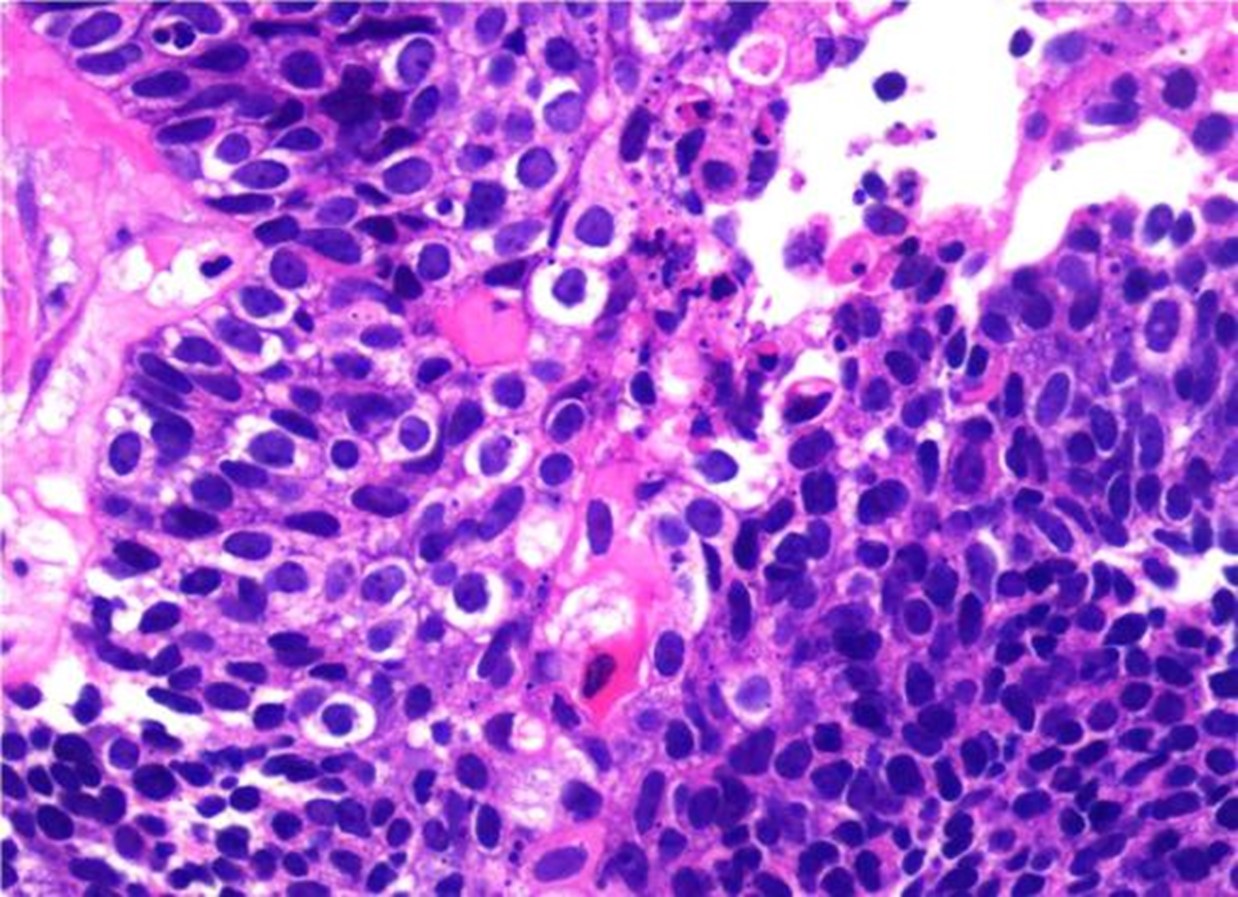 横纹肌样癌细胞散在于基底样细胞之间,胞质内见空泡
横纹肌样癌细胞散在于基底样细胞之间,胞质内见空泡
第一轮IHC:
1.AE1/AE3、Bcl-2、P53均(+);
2.CK5/6、P40、CD56均部分(+),Ki-67约40%(+);
3.其余:CgA、Syn、NSE、vimentin、S-100、Desmin、CD99、MelanA、HMB45均(-)。
第二轮IHC:
1.P16(部分+)、NUT(-)、SMARCB1(-);
2.EBER原位杂交(-)。
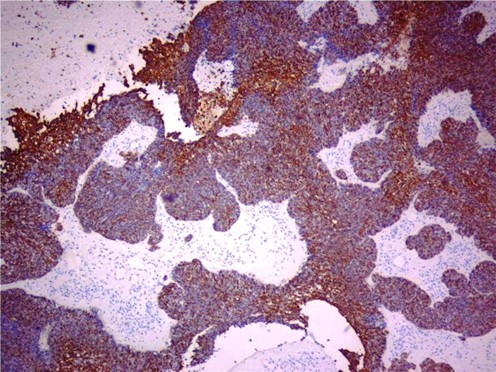
AE1/AE3(+)
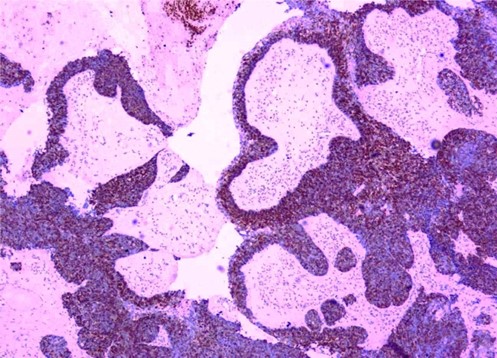
CK5/6部分(+)
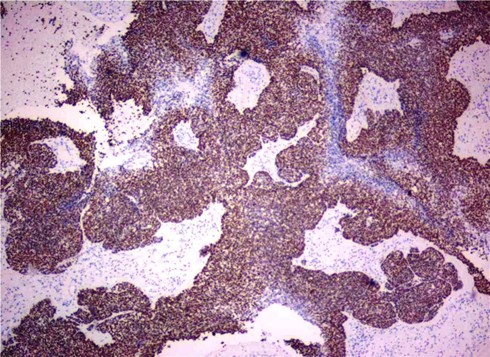
P40(多量+)
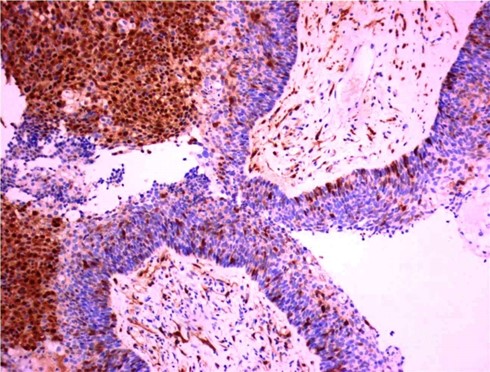
P16(部分+)
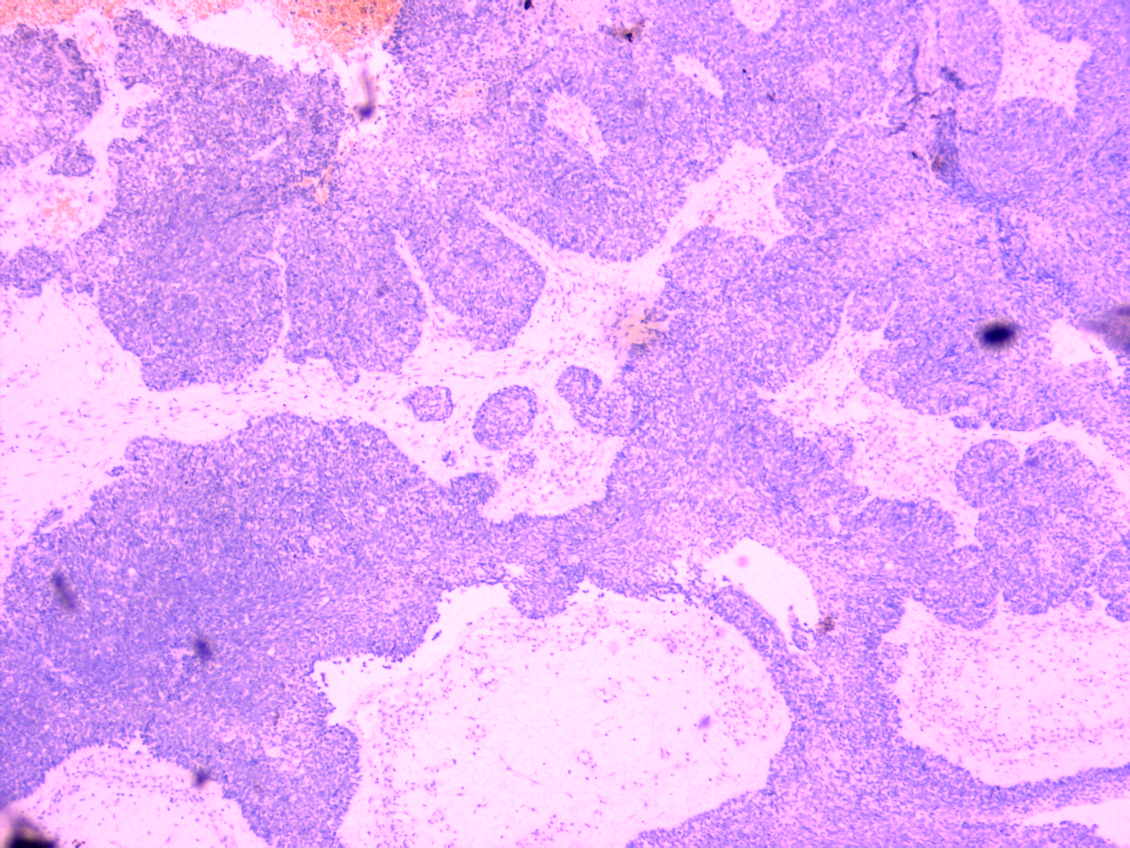 SMARCB1/INI1(-)
SMARCB1/INI1(-)
病理诊断:(左鼻腔)SMARCB1/INI1缺陷型鼻腔鼻窦癌。
讨论:
概念和发病机制:
鼻腔鼻窦SMARCB1缺失癌[SMARCB1(INI-1)-deficient carcinomas of the sinonasal tract]形态上表现为鼻腔鼻窦未分化癌或非角化性癌,但SMARCB1(INI-1)阴性的鼻腔鼻窦上皮性恶性肿瘤。
SMARCB1/INI1是SWI/SNF复合体中的核心亚基,位于染色体22q11.2,是高度保守的肿瘤抑制因子,普遍表达于正常人体细胞的核中。SWI/SNF复合物是一种多亚基的染色质重塑复合物,该复合物和转录因子相互作用,在DNA复制、修复、转录激活、调节细胞的生长、分裂和分化、器官发育中发挥着重要作用,通过这些过程,起到肿瘤抑制的作用,这些亚基包括SMARCA4 (ERG1) 、SMARCA2(BRM)、SMARCB1 (INI1)等。
临床特征:
SMARCB1缺陷是很多肿瘤性病变的定义性特征,也是诊断依据,大多数病例为进展期(cT4)。鼻腔鼻窦INI1缺失癌的发病年龄在28-78岁,中位年龄54岁,性别无明显差距,筛窦区多见,可累及鼻腔和上颌窦等,表现为鼻塞、局部疼痛和眼部症状。鼻内镜检查为鼻道红色肿块,表面尚光滑,有充血和少量分泌物,影像学显示鼻腔软组织占位,累及筛窦和上颌窦伴相应的骨组织破坏。
病理变化:
肉眼观:
肿瘤呈棕红色至黄白色,质地中等,可出现坏死。
镜下观:
黏膜上皮下癌组织呈巢状、团块状生长伴明显坏死,部分区可见不规则的囊样结构,肿瘤细胞大部分呈基底样,少数可呈浆样、横纹肌样(偏心性核、嗜酸性胞质、明显的核仁),部分胞质较丰富,核仁明显,可见核分裂象,横纹肌样细胞可多少不等散在于基底样细胞之间,肿瘤胞质内常见较明显的非特异性空泡,肿瘤细胞可以Paget样方式扩散至上皮层内,肿瘤常伴间质纤维结缔组织增生,肿瘤侵及周围组织及骨组织。
免疫组织:
1.SMARCB1/INI1表达缺失,而间质淋巴细胞和间质细胞可以显示为核阳性,可做为对照;
2.广谱细胞角蛋白(CKpan)、细胞角蛋白(CK)8/18均阳性,CK7、CK5/6、p40、p63、突触素、CD56及p16可不同比例的阳性;
3.基底样细胞常呈CK5/6、p63、p40阳性,波形蛋白阴性;
4.横纹肌样细胞常呈CK5/6、p63、p40阴性,波形蛋白阳性;
5.NUT阴性;
6.HPV及EB病毒检测结果阴性;
7.荧光原位杂交(FISH)检测结果均可见INI1基因缺失,可为纯合性缺失或杂合性缺失,HPV进行原位杂交和PCR检测均阴性。
鉴别诊断:
无INI1缺失的差分化肿瘤(形态学特点,但免疫组织化学染色INI1均为阳性):
1.鼻腔鼻窦非角化性鳞状细胞癌;癌细胞分化或高或低,偶有鳞化,除了表达上皮性标记外,同时表达SMARCB1/INI-1;
2.鼻腔鼻窦未分化癌;共同点都是分化差,有相似的镜下形态特点,鳞状分化的标志物CK5/6及p40通常阴性,而INI1缺失癌可有不同程度的表达;
3.NUT癌;有较明显的特征,即团巢状的癌细胞边缘区瘤细胞分化差,中心区域有突然出现的鳞化及角化灶,免疫组化染色肿瘤细胞表达NUT或NUT-1等;
4.HPV相关性癌:虽然少数的SMARCB1(INI-1)缺失的鼻腔鼻窦癌也可表达P16,但是与HPV相关性癌不同,FISH或PCR检测HPV是阴性,预后也更加差;
5.其他如淋巴上皮癌等也要进行鉴别。
伴有INI1缺失的肿瘤:
如与横纹肌样脑膜瘤、横纹肌样瘤、非典型畸胎样/横纹肌样肿瘤(AT/RT)等肿瘤进行鉴别;
拓展:
SMARCB1/INI1缺陷型鼻腔鼻窦腺癌:
罕见亚型,存在明确的腺癌典型特征改变和腺样分化,如局灶卵黄囊瘤样,最多见为裂隙样网状-微囊状表现、分泌性子宫内膜样表现、肠样腺体表现。一般CK7弥漫阳性,p40少见阳性,斑片状着色,常程度不等的表达卵黄囊瘤型标记,如glypican-3、SALL4、Hepatocyte、PLAP、AFP。
SMARCA4缺陷型鼻腔鼻窦癌:
非常类似鼻腔鼻窦未分化癌,见成片大而间变上皮样细胞,形成不规则、相互连续的巢状及小叶状或梁状,背景为散在至显著的反应性水肿或促纤维增生性间质,见高级别的细胞核特征,大量核分裂,显著凝固性坏死灶。
治疗预后和随访:
临床行为具有高度侵袭性,超过一半患者在2年内死亡,死因主要为局部进展、无法切除的肿瘤,尽管铂类化疗药有效。
随访本例患者,术后中西医结合治疗,目前情况基本稳定。
诊断小结:
本例诊断后,我的最大体会:首先一定要想到是SMARCB1/INI1缺陷型这一类肿瘤的可能,再者,这一类肿瘤既有上皮来源,又有间叶来源,结合临床病史,把握组织结构和细胞形态,辅以免疫组化及分子病理,最后确定诊断。
参考书籍:
1.《临床病理诊断与鉴别诊断》---眼耳鼻咽喉疾病分册,主编:刘红刚,P35-37,人民卫生出版社。
2.分子时代学病理-SWI/SNF缺陷型鼻腔鼻窦癌(二),原创:魏建国、王强,华夏病理网(微信公众号)
3.刘红刚.重视对头颈部几种新命名癌的观察和研究[J],中华病理学杂志, 2021,50(11): 1219-1221DOI: 10.3760/cma.j.cn112151-20210708-00492























共0条评论