[导读] 深圳市光明区人民医院 赵东晖 李庆军
病史资料:
患者,女,30岁,半年前无诱因出现左侧乳房2处肿物,约4×3cm,局部红肿流脓,烧灼痛,诊断为非哺乳期乳腺炎,伴脓肿形成,行乳腺脓肿引流术及对症治疗,好转,现双乳导管内多发实性结节,扩张,BI-RADS 4a类,行双侧乳腺肿物切除术。
影像检查:
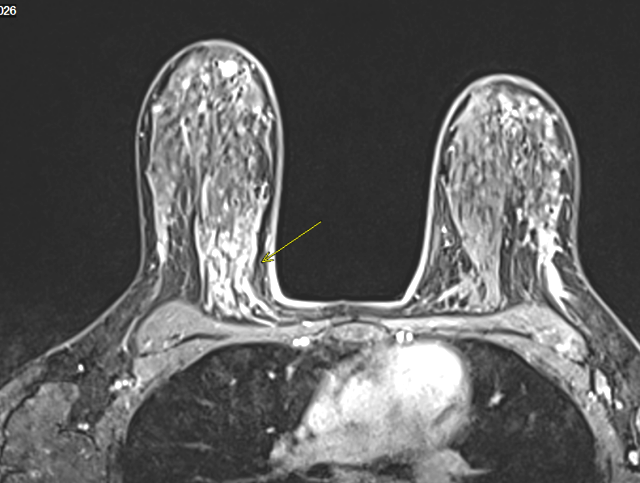
图1 增强MR扫描:肉芽肿性小叶性乳腺炎
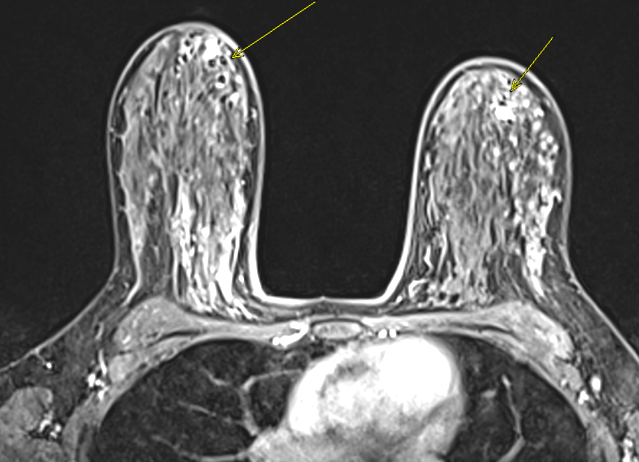
图2 增强MR扫描:乳腺导管扩张
病理检查:
大体:左乳1点、7点、9点及右乳4个部位组织:灰白、灰黄大小不等组织多块,大小分布在大小3×1×0.5---5.5×5×1cm之间,每个部位均全取。
镜下:以乳腺小叶为中心的肉芽肿性炎及融合性病变为主,伴有明显的淋巴细胞、浆细胞、中性粒细胞浸润或脓肿形成,其中巨噬细胞衍生的上皮样组织细胞和朗汉斯巨细胞是肉芽肿的特征细胞;并见圆形张力性囊状空泡(脂质吸收空泡)为中心的肉芽肿结构;局部伴乳腺导管扩张。
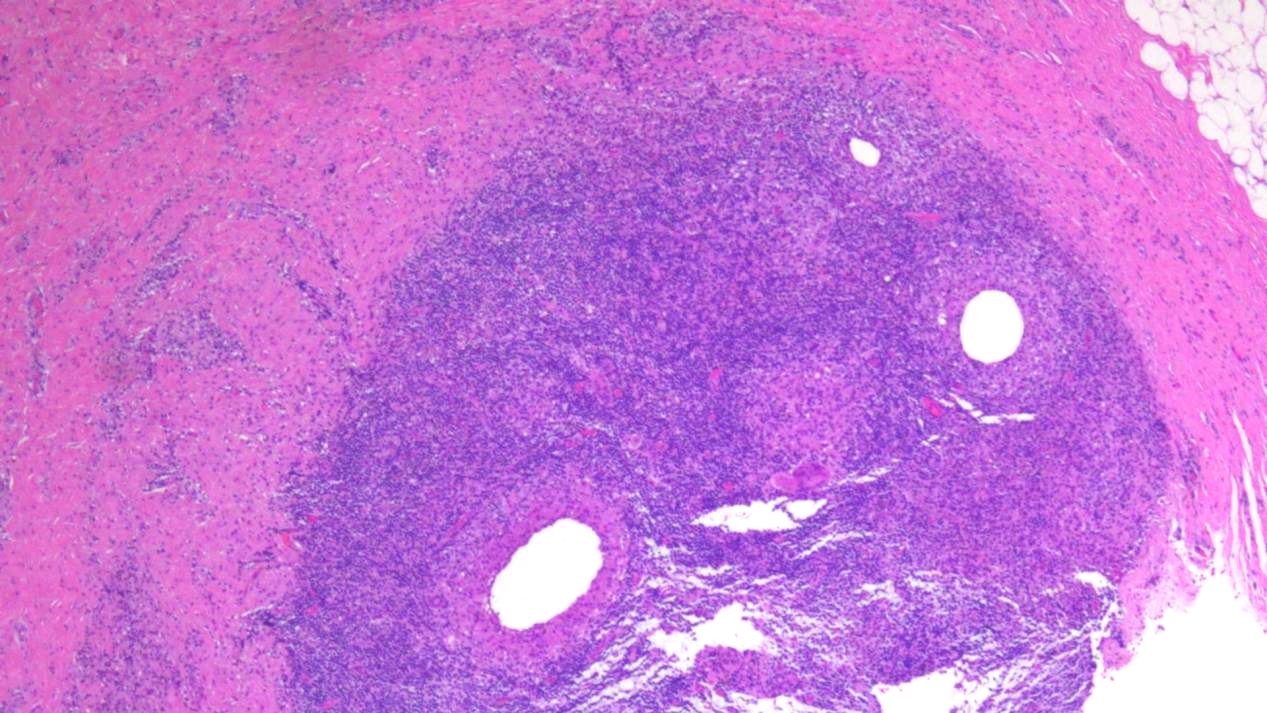 图3 以终末导管小叶单位为中心的肉芽肿性炎(低倍)
图3 以终末导管小叶单位为中心的肉芽肿性炎(低倍)
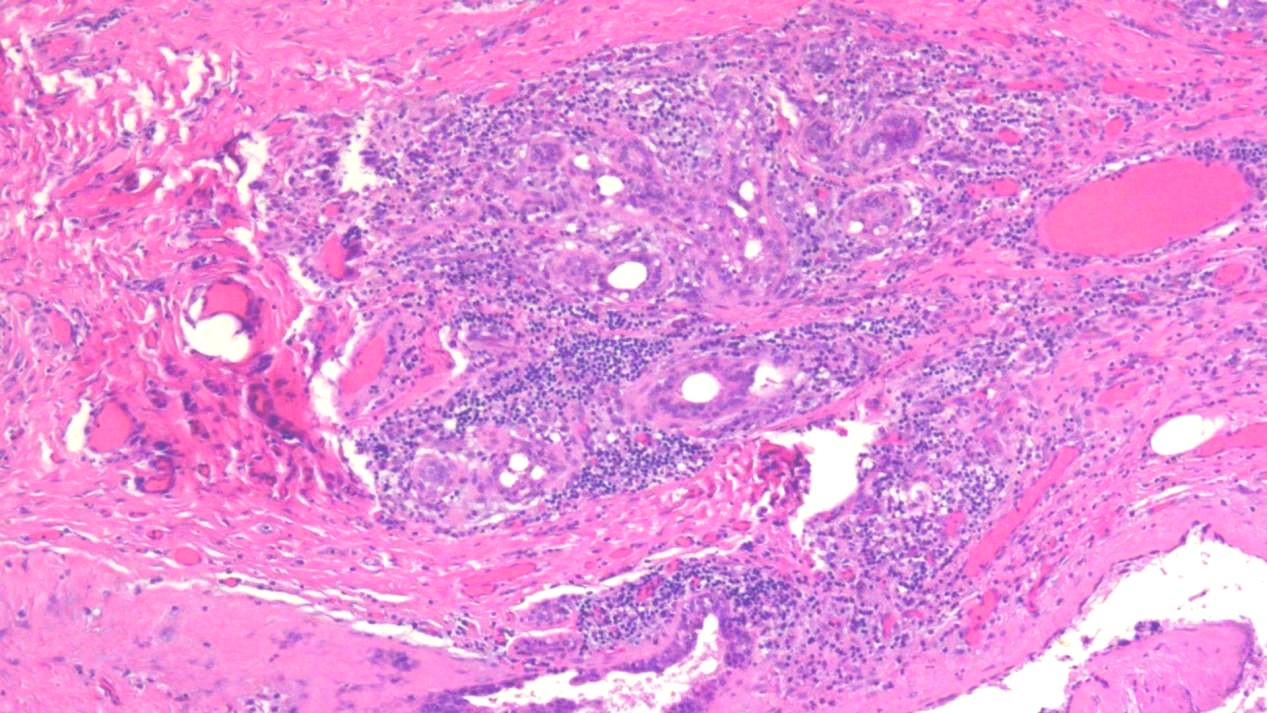 图4 以终末导管小叶单位为中心的肉芽肿性炎(中倍)
图4 以终末导管小叶单位为中心的肉芽肿性炎(中倍)
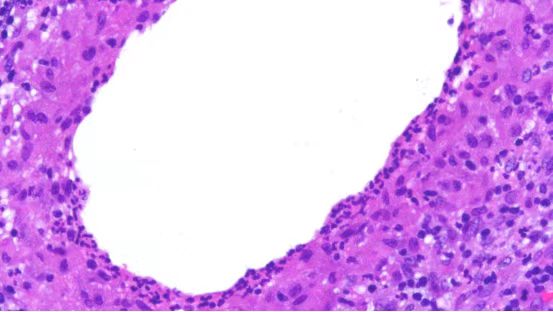
图5 肉芽肿内常见典型实性结节结构,中央可见圆形张力性囊状空泡(脂质吸收空泡),空泡周围由中性粒细胞和/或上皮样组织细胞环绕,常混杂有朗汉斯巨细胞和淋巴细胞等
病理诊断:(左乳1点、7点、9点及右乳肿物)均为肉芽肿性小叶性乳腺炎,伴乳腺导管扩张。
讨论:
定义和名称:肉芽肿性小叶性乳腺炎(granulomatous lobular mastitis,GLM)是一种描述性诊断名称,以乳腺小叶中心性肉芽肿性炎及融合性病变为主要特征,伴明显的淋巴浆细胞、中性粒细胞浸润(或脓肿形成)。肉芽肿的特征细胞为巨噬细胞衍生的上皮样组织细胞和朗汉斯巨细胞。1972年Kessler和Wolloch首次报道,文献中使用了很多名称,包括:肉芽肿性小叶性乳腺炎、特发性肉芽肿性炎、特发性肉芽肿性小叶性乳腺炎、囊性中性粒细胞肉芽肿性乳腺炎(cystic neutrophilic granulomatous mastitis,CNGM)、肉芽肿性小叶炎,等。CNGM出现圆形张力性囊状空泡(脂质吸收空泡)为中心的肉芽肿结构,一般认为是GLM的一种形式。
病因:目前认为棒状杆菌感染、泌乳素水平升高和自身免疫功能失调是GLM的主要致病因素。另外,其他相关因素包括α-1抗胰蛋白酶缺乏症、口服避孕药、吸烟及创伤等。
GLM临床及影像学改变:GLM多见于育龄期女性,少见于孕妇和哺乳期女性。早期,乳房区疼痛,继而出现肿块,皮肤无变化。病变通常从乳房周围区向乳晕区蔓延,随着进展,可迅速增大,伴有红肿热痛等,形成皮下或深部脓肿。后期主要表现为皮肤破溃流脓,形成溃疡、瘘管或窦道。病程反复不愈。伴有同侧或双侧腋窝淋巴结肿大,容易过诊断为乳腺癌。也可在确诊自身免疫性疾病较长时间后出现乳房症状。影像学检查无特异性。
组织学改变(包括病变切取/切除组织、粗针穿刺组织及细针穿刺细胞学标本):较独特,是一种以终末导管小叶单位为中心的肉芽肿性炎,包括:
1.肉芽肿沿小叶分布,即小叶中心性。也可通过“管状延伸”连通肉芽肿病灶结节,或破坏小叶结构,形成大片融合性病灶;
2.肉芽肿多为典型的实性结节状结构;部分肉芽肿结构中央可见大小不等的圆形张力性囊状空泡(脂质吸收空泡),空泡周围由中性粒细胞和/或上皮样组织细胞环绕,常混杂有朗汉斯巨细胞和淋巴细胞等;
3.部分肉芽肿结构内无脂质吸收空泡,可见大小不等的微脓肿;
4.肉芽肿内无干酪样坏死(与结核等感染性肉芽肿鉴别),无Schaumann小体或星状小体(与结节病性肉芽肿鉴别);
5.肉芽肿内、外可见显著的淋巴细胞(多数为T淋巴细胞)、浆细胞(IgG4阳性的浆细胞可增多)及中性粒细胞浸润,通常混杂少量嗜酸性粒细胞;
6.邻近的小叶内可见淋巴细胞及浆细胞浸润;
7.融合性病变内常有较大的脓肿形成,脓肿内通常可见大小不等脂质吸收空泡,经革兰染色,部分病例高倍镜下空泡内可见数量不等的淡染的棒状杆菌(多数呈革兰染色阳性,少数呈阴性);
8.间质小血管周围常有淋巴细胞浸润(血管周围炎),肌性血管的肉芽肿性炎罕见。
GLM可伴发:乳腺导管扩张症、输乳管鳞状化生、隆乳相关乳腺炎、脂肪坏死、导管/小叶增生或浸润癌。
细胞学诊断线索:
1.细胞量丰富,细胞类型多样,以上皮样组织细胞为主,可见朗汉斯巨细胞;
2.上皮样组织细胞聚集成巢团状,形成肉芽肿结节;
3.可见大小不等的脂质吸收空泡;
4.背景的炎性细胞以淋巴细胞、中性粒细胞为主,可见脓肿成分。
GLM分类:
1.感染相关GLM:亲脂性棒状杆菌是导致GLM的主要病原学因素。加做特殊染色,病原体培养或分子检测。表现为广泛的融合性病变,常形成大的脓肿,脂质吸收空泡更多、更大,空泡内偶可见数量不等的革兰阳性棒状杆菌。
2.高泌乳素相关GLM:肉芽肿性炎症病变往往融合成片、弥漫分布,小血管扩张、血管内皮肿胀及血管周围淋巴细胞密集围绕现象较明显;病变周围乳腺导管上皮损伤脱落,腔内泡沫样组织细胞聚集,甚至可形成腔内肉芽肿结构。该型脂质吸收空泡结构较明显,伴随不同程度的脂肪坏死。临床检出高泌乳素血症:高于1.14 nmol/L(25μg/L),可诊断为高泌乳素相关GLM。
3.自身免疫相关GLM:部分患者伴有自身免疫性疾病,包括结节病、干燥综合征等,对糖皮质激素治疗有效。肉芽肿常局限于多个乳腺小叶内,大范围融合性病变较少见,脓肿罕见。常见小血管炎改变,出现血管周及血管壁淋巴细胞浸润。
4.多种病因相关GLM:复合因素共同促进GLM进展。形态学上具有诊断GLM典型或较为典型的特征,患者存在2种及多种可能的致病因素。
5.病因未明的GLM:缺乏明确的相关病因。组织学符合GLM,建议进一步结合病原学、血清学检查和临床信息综合判断。
6.其他病变合并GLM:乳腺导管扩张症、输乳管鳞状化生等的患者标本中,有时亦可见到典型的GLM组织形态学改变。原因不明。以GLM与导管扩张症共存为例,诊断为“GLM合并导管扩张症”或“导管扩张症合并GLM”。
病理报告参考格式:
(左侧乳腺)粗针穿刺组织:病变表现为以乳腺小叶为中心的肉芽肿性炎,伴有明显的淋巴细胞、浆细胞及中性粒细胞浸润,有/无脓肿形成和/或脂质吸收空泡结构,组织病理学形态符合/提示肉芽肿性小叶性乳腺炎[GLM,详见注释:GLM是一组病因复杂、组织病理学形态相似的乳腺慢性炎症性疾病。常见病因包括细菌感染、高泌乳素血症(生理、病理及药物因素引起)及自身免疫失调等]。
小结:
随着对GLM病因和发病机制的深入研究,发现GLM并非如以往认为的是乳腺少见疾病,其发病率呈持续上升趋势。之前在工作过程中见到的基本上都是穿刺标本,而本例是做的双乳多位点乳腺组织切除术,观看全面、直观,典型形态集中于一张片子内,诊断明确,印象深刻,结合肉芽肿性小叶性乳腺炎病理诊断中国专家共识(2024版)内容,进行梳理学习,总结成文。
参考资料:
1.肉芽肿性小叶性乳腺炎病理诊断中国专家共识(2024版)


















共0条评论