WHO女生5ed第16章 女性生殖道的遗传性肿瘤综合征
第16章 女性生殖道的遗传性肿瘤综合征
01. BRCA1/2相关遗传性乳腺和卵巢癌症综合征
定义
BRCA1/2相关遗传性乳腺和卵巢癌症综合征是一种常染色体显性遗传的癌症易感性综合征,由BRCA1和BRCA2基因的种系突变引起,乳腺和卵巢癌症及其他癌症类型的风险增加。
MIM编号
604370乳腺-卵巢癌症,家族性,易感,1;BROVCA1
612555乳腺-卵巢癌症,家族性,易感,2;BROVCA2
ICD-11编码
2C65遗传性乳腺和卵巢癌症综合征
相关命名
可接受:遗传性乳腺和卵巢癌症综合征
亚型
无
部位
BRCA1/2相关遗传性乳腺癌和卵巢癌癌症综合征与乳腺、卵巢、输卵管癌和腹膜的癌相关。患者还可能发生前列腺、胰腺、子宫内膜的癌以及其他类型的癌症
临床特征
临床特征与特定部位的疾病有关。
流行病学
大约10%的卵巢癌症与BRCA1或BRCA2基因的遗传性种系突变有关。已知BRCA1和BRCA2的种系突变会导致乳腺和卵巢癌症以及对侧乳腺癌症的终生高风险。携带致病性BRCA1和BRCA2突变的女性人数估计为每300-500人中有1人。BRCA1突变显著增加卵巢/输卵管癌症风险(40-60%),诊断时患者平均年龄为50-53岁。BRCA2突变个体患卵巢/输卵管癌症的风险较低(11-35%),诊断年龄略高(55-58岁)。根据BRCA1/2变异个体研究者联合会(CIMBA)的数据,乳腺癌和卵巢癌的风险因BRCA1/2突变的类型和位置而异。乳腺癌症的发病率为46%(BRCA1)和52%(BRCA2),卵巢癌症的发病率分别为12%(BRCA1)和6%(BRCA2)。同一患者中两种癌症的发病率分别为5%(BRCA1)和2%(BRCA2)。
BRCA1/2突变的流行率在地理区域、种族/民族、突变类型和频率方面存在很大差异。如,德系犹太人的突变率(2.5%)明显高于普通人群(0.1%)。世界各地的其他地理位置,如挪威、荷兰和冰岛,特定有害BRCA/2突变的流行率也较高(1.8%)。在美国,特定有害的BRCA1/2突变的流行率也可能因种族和民族而异,包括非裔美国人、西班牙裔、亚裔美国人和非西班牙裔白人。
病因
种系突变导致BRCA1/2基因失活,进而导致同源重组修复途径缺陷,该途径负责使用姐妹染色单体作为模板,准确修复DNA断裂。
发病机制
BRCA1位于染色体17q21,包含23个编码外显子。它编码1863个氨基酸的核蛋白。N末端的RING指结构域介导与其他蛋白质的相互作用。BRCA1通常在三个结构域中发生突变:RING指结构域、外显子11-13和BRCA1 C末端结构域。BRCA2定位于染色体13q13.1,包含27个编码外显子。BRCA2蛋白包含3418个氨基酸。BRCA2中心部分(卵巢簇区域)的突变与卵巢癌的可能性增加之间存在关联。BRCA1和BRCA2蛋白与任何其他蛋白没有结构同源性。
BRCA1/2蛋白通过促进无错误的DNA修复,在维持基因组稳定性方面发挥着关键作用。BRCA1在细胞周期检查点控制中起作用,并通过与参与DNA损伤修复的蛋白质(如RAD51)结合而发挥作用。BRCA2调节RAD51介导的重组功能。功能性BRCA蛋白是肿瘤抑制因子,通过同源重组修复双链断裂、细胞分裂控制和细胞生长调节来维持基因组稳定性。种系BRCA1/2突变使个体易发生二次打击双等位基因失活,首先涉及一个BRCA等位基因的遗传致病性突变,然后是第二个野生型等位基因的体细胞性失活加上体细胞突变,这表明同源重组存在功能缺陷。DNA双链断裂,如果不进行修复,可能导致基因组重排和细胞死亡。
大体检查
无临床相关性
组织病理学
女性生殖道最重要的肿瘤是卵巢/输卵管/腹膜的高级别浆液性癌(HGSC)。癌肉瘤也与之相关。据报道,BRCA突变携带者中也有其他组织学肿瘤类型(如子宫内膜样癌、透明细胞癌和未分化癌),但与双等位基因失活的关系尚未得到证实。如果使用SEE-FIM(伞端切开并广泛检查)方案检查输卵管,在5-10%的预防性输卵管卵巢切除术标本中发现输卵管远端局部浆液性输卵管上皮内癌(STIC)(或STIC伴有限的浸润或扩散)。一些与BRCA1相关的HGSC更频繁地具有SET(实性、子宫内膜样、移行细胞癌样)结构模式、核分裂象计数高、肿瘤浸润淋巴细胞和地图样坏死或粉刺样坏死(见原书第45页的高级卵巢浆液性癌)。BRCA2相关的HGSC往往具有与BRCA1相关病例相似的结构模式,但肿瘤浸润淋巴细胞和坏死不太明显。
细胞学
无临床相关性
诊断分子病理学
存在种系BRCA1/2突变。
诊断标准
必要标准:种系BRCA1/2突变。
分期
无临床相关性
预后和预测
携带者HGSC的10年生存率与非携带者相当。5年后的存活率下降,接近非携带者的存活率。此外,突变携带者对铂类化疗的初始敏感性更高。靶向DNA损伤修复的聚ADP核糖聚合酶(PARP)抑制剂可提高BRCA1/2突变患者的生存率。
02. 林奇综合征
定义
林奇综合征(Lynch syndrome, LS)是一种常染色体显性遗传性疾病,病因是种系致病性改变(几乎总是突变),影响DNA错配修复基因MLH1、MSH2、MSH6和PMS2。
MIM编号
120435 Lynch综合征I(结直肠癌症,遗传性非息肉病,1型;HNPCC 1)
609310结直肠癌症,遗传性非息肉病,2型;HNPCC 2
614350结直肠癌症,遗传性非息肉病,5型;HNPCC 5
614337结直肠癌症,遗传性非息肉病,4型;HNPCC 4
613244结直肠癌症,遗传性非息肉病,8型;HNPCC 8
ICD-11编码
无
相关命名
不推荐:遗传性非息肉病性结直肠癌症
亚型
Muri-Torre综合征;种系(constitutional)错配修复缺陷综合征;双等位基因错配修复基因突变引起的等位基因疾病
(译注:constitutional=germline,故简单译为“种系”)
部位
根据涉及的基因,LS中发生的癌症可能发生在子宫内膜、卵巢、结直肠、胃、小肠、胆囊、肝胆道、胰腺、肾盂和/或输尿管、膀胱、肾脏、大脑或前列腺。
临床特征
LS的特点是易患多种癌症。在这种情况下发生的子宫内膜癌和卵巢癌可以在任何年龄发生,但通常发生在年轻女性。一些LS女性患多种肿瘤;另一些根本没有肿瘤。患有LS的女性的子宫内膜癌症是指标癌症,略高于50%。仅根据家族史的预测值很低(无论是阳性预测值还是阴性预测值)。从头发生的种系突变引起的LS病例得到了充分的研究。散发性癌症也可能发生在LS患者中。Muir-Torre综合征是指皮脂腺皮肤肿瘤(即皮脂腺腺瘤、皮脂腺瘤、皮脂腺癌或角化棘皮瘤)与任何内脏癌共存。癌症风险因突变类型而异。
流行病学
子宫内膜癌症的系统测试表明,以LS为病因的子宫内膜癌或卵巢癌约占26%。在许多人群中发现了导致LS的创始突变(founder mutation),在几个人群中的发生率各不相同。此外,一些突变相对更常见。
病因
错配修复基因的种系突变是最常见的。
发病机制
当错配修复基因的两个等位基因都失活时,细胞会失去错配修复功能。LS女性在相应的正常错配修复等位基因中获得躯体性打击(somatic hit,译者理解为非遗传学因素导致的体细胞突变),并发展为错配修复缺陷(dMMR)肿瘤。dMMR肿瘤摆脱了凋亡的正常控制,获得了相对的生长优势,尽管这可能取决于其他基因的后续突变。错配修复缺陷也会导致点突变率的增加,尤其是在被称为微卫星的重复DNA片段中;这表现为微卫星不稳定性(MSI)。错配修复缺陷通常会导致错配修复蛋白表达异常,这可以通过免疫组化来识别。
很大一部分(25-30%)非LS子宫内膜癌存在错配修复缺陷。大多数是由于MLH1基因启动子的零星体细胞双等位基因超甲基化。与结直肠癌不同,这些肿瘤不会获得特定的BRAF癌基因突变(BRAFp. Val600Glu突变)。在一些散发性癌症中,错配修复缺陷是由于两个体细胞错配修复基因突变或一个体细胞突变导致另一个等位基因杂合性缺失。“LS样综合征”一词用于一些有强烈dMMR肿瘤家族史的患者,这些患者中没有发现种系突变。
MLH1启动子的种系超甲基化也会导致LS。这通常是散发性的,不可遗传的,但在某些情况下,可遗传的染色体重排会导致MLH1启动子甲基化。
大体检查
大体表现与肿瘤类型有关,没有特殊。发生在子宫下段的子宫内膜癌在普通人群中很罕见,在LS患者中较多见。
组织病理学
与结直肠癌不同,具有DNA错配修复缺陷的子宫内膜癌的组织学特征无特异性,包括子宫内膜样和非子宫内膜样亚型,如透明细胞癌;混合性子宫内膜样和透明、未分化和去分化癌;以及癌肉瘤。卵巢癌往往是子宫内膜样癌、未分化癌或透明细胞癌。子宫内膜癌和卵巢癌都可有肿瘤浸润性淋巴细胞,但这种特征也出现在没有错配修复缺陷的散发性癌症。
由于LS相关的子宫内膜癌症的组织学特征无特异性,许多专业组织建议对子宫内膜癌症患者进行遗传学检测。用免疫组化或分子检测作为结直肠癌癌症的首选检测存在分歧,但免疫组化是子宫内膜癌的首选检测(单独或联合MSI检测),因为微卫星稳定(MSS)的子宫内膜癌携带MSH6突变的频率较高。随后检测超甲基化和(在没有种系突变的情况下)体细胞突变,进一步评估这些患者随后的患癌风险。与结直肠癌不同,在子宫内膜和卵巢癌症中,BRAF突变分析不是MLH1超甲基化检测的替代方法.
免疫组化,所有四种错配修复蛋白的表达都表明存在MSS。任何蛋白质的核染色缺失都表明MSI,并表明最有可能涉及的基因和需要额外的检测。MSH2和MSH6的缺失表明MSH2发生了突变。同样,MLH1和PMS2的缺失表明MLH1存在潜在的突变或甲基化。偶尔,MLH1单独缺失,这通常表明存在潜在的甲基化。MSH2和MSH6(或MLH1和PMS2)的同时缺失反映了错配修复复合物中MSH2与MSH6的异二聚体结合(或MLH1/PMS2),因此第一个伴侣的缺失会导致第二个伴侣的相对不稳定和缺失。典型的正常表达模式包括肿瘤细胞核和许多良性细胞核的弥漫性染色,包括上皮细胞、间质细胞和淋巴细胞。
错配修复蛋白免疫组化的解读通常很简单,但应始终有充分的内部对照。可能出现一些陷阱和不寻常的表达模式,知道这些就会防止错误解读。有多种染色模式不代表错配修复缺陷。由于肿瘤内异质性超甲基化,MLH1和PMS2的局灶性缺失可能发生。偶尔,MSH6和/或MSH2表达的局灶性缺失可能是由于MSH6编码单核苷酸束中的继发性(非种系)突变或POLE中的突变。大约5%的具有错配修复缺陷和MSI的LS肿瘤,免疫组化检测没有异常。
细胞学
无临床相关性
诊断分子病理学
LS是由四种DNA错配修复基因之一的种系突变的常染色体显性遗传引起的:MSH2(2p21)、MLH1(3p22.2)、MSH6(2p16.3,距离MSH2仅300kb)和PMS2(7p22.1)。在某些情况下,延伸到MSH2的EPCAM 3'(末端)末端的缺失导致表型与MSH2突变引起的病例无法区分。
有缺陷的错配修复阻止了对DNA复制过程中重复DNA序列中自然发生的插入或缺失的识别和修复。这就可以检测到MSI,其定义为与同一个体的正常DNA(来自正常组织或血液)相比,微卫星上的碱基缺失或插入。微卫星表现出不稳定性的倾向各不相同,因此同一微卫星在不同肿瘤类型中受到影响的频率也不同。在单核苷酸重复处比在二核苷酸重复处更容易观察到不稳定性。目前用于结直肠癌MSI诊断的标记物对于检测子宫内膜癌MSI并不敏感,尤其是在MSH6突变的女性中。因此,当使用这些标记物时,这些LS相关肿瘤可能看起来没有MSI(尽管它们可能被异常的错配修复免疫组化识别)。重要的是要注意,dMMR肿瘤并不总是具有异常的免疫组化或MSI检测阳性。
当这些移码发生在基因的蛋白质编码区时,它们会导致刺激免疫系统的新型抗原肽的表达。此类肿瘤中的局部免疫抑制使其存活;因此,打消这种抑制的免疫检查点抑制剂(如PD1/PD-L1阻断剂)可能对dMMR肿瘤更有效。
DNA错配修复缺陷具有特异性基因突变谱,这最终可能取代MSI检测。尽管组合基因测试不需要等待免疫组化筛查的待检基因目标,但免疫组化在提供表型数据以解释遗传变异(如意义不确定的变异)方面仍然至关重要。
诊断标准
必要标准:错配修复基因(MLH1、MSH2、MSH6、PMS2)或EPCAM中的种系突变;少见的分子异常,请参见上文讨论。
分期
无临床相关性
预后和预测
无临床相关性
03. Cowden综合征
定义
Cowden综合征,也称为PTEN错构瘤肿瘤综合征,是一组常染色体显性遗传的异质性疾病,由PTEN基因的种系突变所致,其特征是多发性错构瘤和易患癌症。
MIM编号
158350 Cowden综合征1;CWS 1
ICD-11编码
LD2D.Y其他特定的瘢痣病(phakomatoses)或错构瘤综合征—Cowden综合征
相关命名
可接受:PTEN错构瘤肿瘤综合征
亚型
Bannayan-Riley-Ruvalcaba综合征;变形综合征;变形样综合征
部位
Cowden综合征影响各种器官,包括子宫、皮肤、乳房、胃肠道、大脑、甲状腺、肾脏和软组织。
临床特征
Cowden综合征的临床特征变化多端,难以识别,详见简表16.01。受累个体常有大头、皮肤毛根鞘瘤和乳头状丘疹。妇科表现包括子宫内膜癌和子宫平滑肌瘤。符合部分而不是全部诊断标准的病例称为Cowden样综合征。
流行病学
流行率约为每二十万人一例。受累个体通常在二十多岁发病。从头发生的PTEN突变的频率估计在10%至48%之间。Cowden综合征患者发生子宫内膜癌的终生风险约为13-19%(而普通人群为2.5%)。子宫内膜癌患者通常为30-50岁,但有时<20岁。在明显的散发性癌症患者中,Cowden综合征的发病率非常低;在一项研究中,381例连续病例中只有1例发现了一种致病性PTEN种系突变。
病因
Cowden综合征和Cowden样综合征是由PTEN(85%的Cowden综合征病例)或其他基因(SDH基因、PIK3CA、AKT1或SEC23B)的种系突变或种系KLLN启动子超甲基化引起的。
发病机制
PTEN是一种几乎普遍表达的肿瘤抑制因子,是一种双特异性脂质和蛋白质磷酸酶,通过Pl3K/AKT通路抑制AKT来调节细胞增殖、细胞迁徙和凋亡。基因第二拷贝的失活使得AKT通路失调。
大体检查
大体没有特异性。
组织病理学
子宫癌通常为低级别子宫内膜样类型,但偶尔也可能发生浆液性子宫内膜癌。子宫平滑肌瘤无特殊。
细胞学
无临床相关性
诊断分子病理学
Cowden综合征主要由种系PTEN突变引起。其他基因很少涉及:SDH基因、PIK3CA、AKT1、SEC23B和KLLN。
诊断标准
国际Cowden联盟(ICC)制定的操作性诊断标准列于简表16.01中。
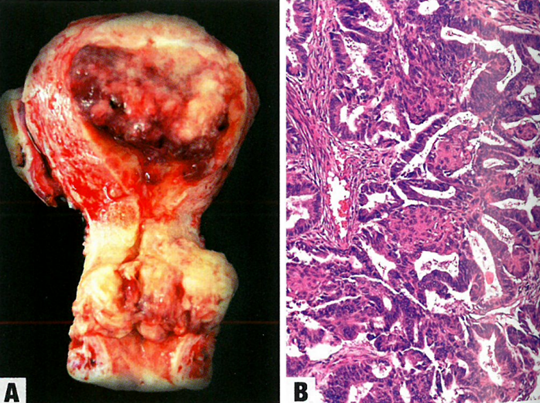
图16.01 Cowden综合征。A Cowden综合征患者子宫内膜癌的大体表现。B Cowden综合征患者低级别子宫内膜样子宫内膜癌。
分期
无临床相关性
预后和预测
对于子宫内膜癌和其他恶性肿瘤,预后取决于组织学类型、分级和分期。子宫平滑肌瘤是良性的。
简表16.01国际Cowden联盟(ICC)操作性诊断标准

a这里只是ICC标准的规定。
b这里只是2010年国家综合癌症网络(NCCN)标准的定义。
04. Li-Fraumeni综合征
定义
TP53相关的Li-Fraumeni综合征(LFS)是一种由TP53基因种系突变引起的常染色体显性遗传癌症易感性综合征。
MIM编号
151623Li-Fraaumeni综合征;LFS
ICD-11编码
无
相关命名
不推荐:Li和Fraumeni肉瘤家族综合征
亚型
无
部位
TP53相关LFS与乳腺软组织、骨、脑、肾上腺和女性生殖道的癌症相关。
临床特征
LFS的特点是早期发生广泛的癌症,终身癌症风险高。乳腺癌和肾上腺皮质癌、脑肿瘤(特别是脉络丛癌)、白血病以及软组织和骨肉瘤被认为是轴心肿瘤,约占LFS相关肿瘤的70%。女性生殖器官的癌症,特别是卵巢癌和子宫内膜癌,很少发生。扩大的临床定义允许更广泛地识别患有LFS的个人和家庭(见简表16.02)。
流行病学
妇科肿瘤罕见,占IARC TP53数据库R19版本(2018年8月)病例的2.7%(57/2095例)。
病因
LFS是由TP53基因的种系突变引起的。在LFS家族中发现了涉及基因编码区的广泛TP53种系突变,但20-40%的LFS患者和大多数Li-Fraumeni样综合征家族可能缺乏可检测的突变。TP53突变与经典LFS表型之间缺乏100%的一致性,可以用几种方式来解释,包括翻译后改变、完全缺失、修饰基因的影响以及影响特定种系改变产生的表型的其他基因的改变。突变可能发生在特定的热点密码子,这些密码子要么干扰DNA结合,要么破坏结合表面的结构,从而干扰其调节靶基因转录的能力。错义突变导致密码子改变,对新变异的功能解释提出了挑战。进一步的突变可能发生在DNA结合结构域之外,包括重排和缺失。未来使用新的测序技术(如下一代测序)的研究可能能够发现TP53以及LFS和Li-Fraumeni样综合征中其他基因的更多突变。
发病机制
TP53是最显著的肿瘤抑制因子之一,其激活会导致保护性细胞过程,包括细胞周期停滞、凋亡和衰老,以防止转基因细胞的繁殖,但最近在小鼠模型中的发现挑战了这些细胞反应的重要性。在正常情况下,p53蛋白由于其主要负调控因子MDM2介导的快速转换而保持在低水平。最近的证据表明,TP53功能与代谢调节和氧化还原平衡有关,以维持细胞内稳态。来自LFS患者的细胞表现出基因组不稳定性、端粒功能障碍和自发永生化。
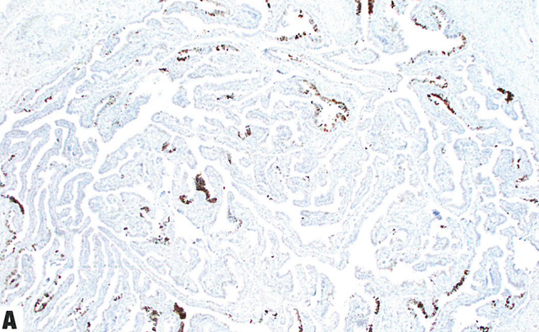

图16.02 Li-Fraaumei综合征输卵管中p53签名(译注:特征性病变)。A LFS患者输卵管横截面,低倍。存在许多p53染色灶,符合局灶性杂合性缺失。丰富的p53签名可能表明输卵管黏膜对促进DNA损伤的易感性。然而,真正的恶性肿瘤需要额外体细胞突变,这在输卵管罕见。B 高倍。
简表16.02应进行致病性种系TP53变异检测的癌症患者a

a应在开始治疗前进行致病性TP53变异检测,以尽可能避免变异携带者接受放射治疗和遗传毒性化疗,并优先考虑手术治疗。
大体检查
无临床相关性
组织病理学
妇科肿瘤在LFS中罕见;它们最常累及卵巢,其次是子宫体、子宫颈和阴道。在子宫内膜浆液性癌和输卵管癌中发现LFS已有报道,但第二次基因打击似乎对肿瘤的发展至关重要。据报道有一例并发高钙血症型卵巢小细胞癌和宫颈多形性脂肪肉瘤。
细胞学
无临床相关性
诊断分子病理学
最近更新了TP53种系检测候选人的选择指南(见简表16.02)。
诊断标准
必要标准:TP53致病性种系突变;适当的家族史。
分期
根据受影响的器官部位分期。
预后和预测
与临床无关。
05. Peutz-Jeghers综合征
定义
Peutz-Jegers综合征(PJS)是一种常染色体显性遗传性息肉和癌症易感性综合征,其特征是黏膜皮肤黑色素沉着和胃肠道息肉病,与STK11突变相关。
MIM编号
175200 Peutz-Jeghers综合征;PJS
ICD-11编码
LD2D.0 Peutz-Jeghers综合征
相关命名
无
亚型
无
部位
宫颈和卵巢、胃肠道、乳腺、皮肤和肺。
临床特征
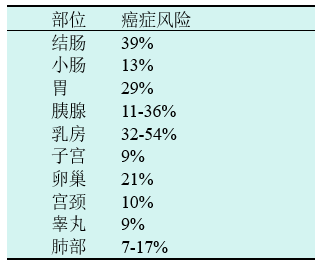
PJS与一系列恶性肿瘤的中高风险相关,70岁时患任何癌症的总风险为81%(见表16.01)。女性生殖道肿瘤包括宫颈胃型黏液腺癌和形状小管性索肿瘤(SCTAT),以及不太常见的卵巢Sertoli细胞肿瘤。其他肠外肿瘤包括乳腺癌和胰腺癌,以及睾丸Sertoli细胞瘤。PJS胃型黏液腺癌患者比非综合征患者年轻(平均年龄:33岁)。SCTAT发生在10-30岁。
出现的症状包括腹痛、肠出血、贫血和肠套叠,通常在生命的十几岁发病。如果存在特征性的黏膜皮肤色素沉着,可以诊断出家族性病例中的无症状患者,但特征性的黑斑息肉是主要的临床标志。宫颈肿瘤伴有异常阴道出血和水样分泌物。卵巢肿瘤可能是偶然发现,也可能出现与盆腔肿块相关的体征和症状。
流行病学
PJS的流行率为每5万-20万名新生儿中有1例。宫颈胃型黏液腺癌的累积风险为10%,卵巢肿瘤为21%。PJS与10%的宫颈胃型黏液腺癌和36%的SCTAT有关。
病因
90%以上的病例与肿瘤抑制基因STK11(染色体19p13.3)的遗传性种系突变有关。大多数种系缺陷是点突变和小的基因内缺失,但也有人描述了一个或多个外显子的较大缺失。
发病机制
PJS患者胃肠道癌症的直接前驱病变尚不清楚。Peutz-Jegers息肉可能是癌前状态的现象,而不是必然的恶性前驱病变。没有关于乳腺或女性生殖器肿瘤发病机制的数据。
大体检查
宫颈肿瘤通常是硬结、桶形,集中在转化区。SCTAT通常不明显,尽管它们可能形成双侧可见的黄色结节,而Sertoli细胞肿瘤通常形成具有黄色切面的实性肿块。
组织病理学
宫颈胃型黏液腺癌可发生从高分化(微偏腺癌)到明显恶性的肿瘤范围。也可发生小叶性子宫颈管腺体增生及其非典型形式,被认为是胃型黏液腺癌的前驱病变。子宫内膜、输卵管、卵巢、腹膜、膀胱和肠道可能出现罕见的同步化生和肿瘤性黏液病变。与非综合征性肿瘤相比,综合征患者的SCTAT通常是双侧和多灶性,并且通常伴有微钙化。Sertoli细胞肿瘤可能是嗜酸性或富含脂质。
另请参阅子宫颈腺癌(HPV非依赖性胃型)(原书第374页)和环形小管性索肿瘤(原书第111页)的组织病理学。
表16.01 65-70岁年龄特殊解剖部位的PJS癌症风险
细胞学
无临床相关性
诊断分子病理学
无临床相关性
诊断标准
必要标准:符合PJS的临床诊断标准。
分期
分期与其他宫颈和卵巢肿瘤相同
预后和预测
胃型黏液腺癌与侵袭性行为和不良预后有关。相比之下,SCTAT预后良好。Sertoli细胞肿瘤可能很少是恶性。肿瘤监测指南建议每年进行宫颈细胞学检查和经阴道超声检查。
06. 共济失调毛细血管扩张症
定义
共济失调毛细血管扩张症(AT)是一种常染色体隐性综合征,其特征是进行性小脑共济失调、动眼神经失用症、舞蹈手足徐动症、鼻窦感染、眼皮肤毛细血管扩张症、不同程度的免疫缺陷、不育、恶性肿瘤的高风险以及对电离辐射的敏感性,这些都是由ATM基因的种系突变引起的。
MIM编号
208900 共济失调毛细血管扩张症;AT
ICD-11编码
4A01.31除T细胞或B细胞联合免疫缺陷外的DNA修复缺陷——共济失调毛细血管扩张症
相关命名
可接受:免疫缺陷伴共济失调毛细血管扩张;Louis Bar综合征;小脑-眼皮肤毛细血管扩张症
亚型
经典型共济失调毛细血管扩张症;轻型共济失调毛细血管扩张症
部位
卵巢是唯一有肿瘤的妇科部位。卵巢、输卵管和子宫的缺失/萎缩已有描述。
临床特征
腹部肿块/疼痛是卵巢肿瘤的常见表现。AT患者AFP通常升高。
流行病学
AT的患病率估计为每4万-10万活产1例。在文献报道的病例中,卵巢肿瘤患者的年龄在10至17岁之间。
病因
AT由编码ATM蛋白的ATM基因突变引起。
发病机制
ATM蛋白协调细胞信号通路,以应对DNA双链断裂和几种形式的应激。ATM蛋白的缺失会影响基因组的不稳定性或DNA损伤反应,从而导致肿瘤的发生。
大体检查
肿瘤呈实性,大小范围为0.6-17cm。
组织病理学
大多数卵巢肿瘤是无性细胞瘤,罕见性腺母细胞瘤和卵黄囊瘤。
细胞学
无临床相关性
诊断分子病理学
鉴定ATM基因中的致病突变的有诊断价值。
诊断标准
根据临床特征和实验室特异性异常的组合怀疑AT。确认性测试结果包括ATM基因突变的鉴定。
分期
分期与附件/腹膜肿瘤相同
预后和预测
AT患者的预后较差,平均预期寿命为25年。没有明确的迹象表明妇科恶性肿瘤会影响生存。
07. Carney综合征
定义
Carney综合征(CNC)是一种多发性肿瘤综合征,其特征是皮肤和黏膜的色素性病变、心脏和皮肤的黏液瘤以及多种内分泌和非内分泌肿瘤。
MIM编号
160980卡尼综合征,1型;CNC 1
ICD-11编码
无
相关命名
无
亚型
无
部位
生殖器雀斑是最常见的妇科表现。卵巢病变、黏液样子宫平滑肌瘤、宫颈非典型间叶性肿瘤、外阴蓝痣和外阴黏液瘤已有报道。
临床特征
生殖器雀斑、外阴黏液瘤、卵泡囊肿、囊性畸胎瘤和浆液性囊腺瘤通常无症状。皮肤和黏膜雀斑/病变很小。文献报道的症状和体征是可变的,取决于病变。可能遇到伴有黏液样改变的平滑肌瘤。已经制定了完整的诊断标准。
流行病学
CNC罕见,患病率未知。其妇科表现通常在年轻时发现。
病因
CNC通常以常染色体显性方式遗传,但也可能从头发生。大多数病例是由于PRKAR1A基因(位于染色体17q)的种系突变引起的。
发病机制
PRKAR1A缺陷促进cAMP反应组织中细胞增殖和肿瘤形成。
大体检查
大体表现无特异性。
组织病理学
所有文献报道的病变均显示符合其组织类型的组织学特征。
细胞学
无临床相关性
诊断分子病理学
鉴定PRKAR1A基因的致病性种系突变有助于确认诊断,但20-30%的病例中可能不存在这种突变。
诊断标准
必要标准:两个主要标准,或一个主要标准加一个补充标准
分期
无临床相关性
预后和预测
与CNC相关的大多数妇科病变都是良性的。
08. DICER1综合征
定义
DICER1综合征是一种常染色体显性遗传疾病,其特征是多种罕见肿瘤的发生,包括胸膜肺母细胞瘤、甲状腺癌症、儿童囊性肾瘤、宫颈胚胎性横纹肌肉瘤和卵巢Sertoli-Leydig细胞瘤。
MIM编号
606241 DICER 1,核糖核酸酶Ⅲ;DICER1
ICD-11编码
无
表16.02与种系DICER1致病性变异相关的关键临床表型
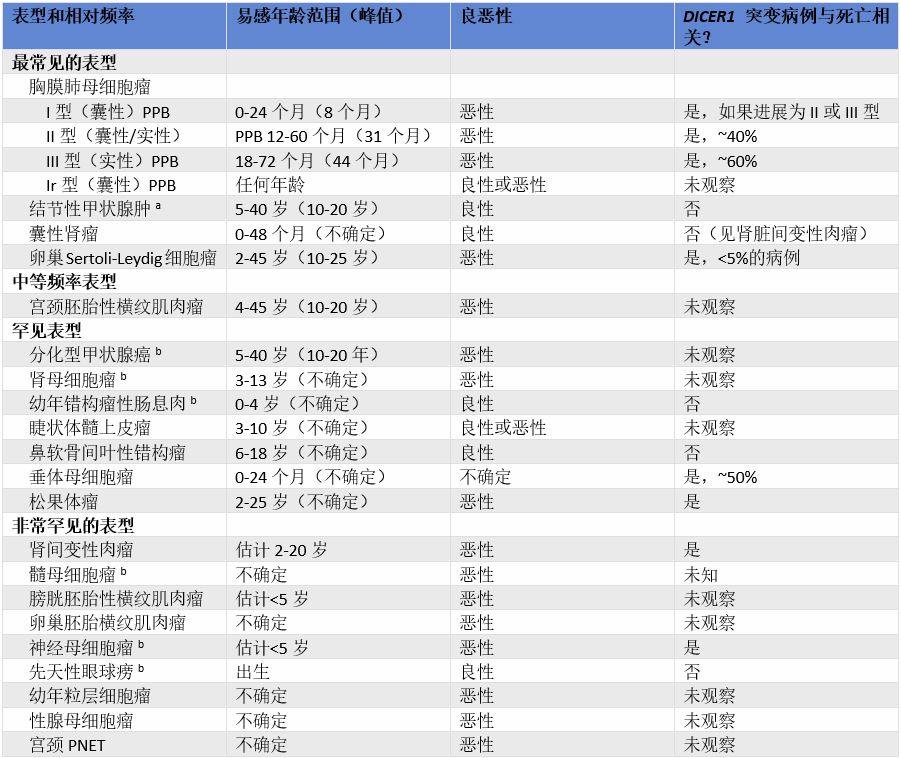
a 18岁之前发生的结节性甲状腺肿可能需要进行DICER1检测,即使是在患者或其家人没有其他综合征特征的情况下发生。
b在没有其他个人或家族史提示DICER1综合征的情况下,这些疾病可能与DICER1突变没有足够的相关性,因此不需要进行检测。
相关命名
可接受:Dcier
亚型
无
部位
不适用
临床特征
主要累及儿童和年轻人。大约5%的携带者在10岁前首次出现肿瘤(女性:4%;男性:7%)。50岁时肿瘤的平均发病率为19%,女性的风险更高(女性:27%;男性:10%)。妇科肿瘤在老年患者中占主导地位。表16.02列出了与种系DICER1致病性变异相关的关键临床表型。
流行病学
发病率未知。
病因
DICER1综合征是由DICER1中的遗传性致病突变引起的,这些突变也可能是从头发生的或导致体细胞嵌合。
发病机制
DICER1是一种RNase III内切核糖核酸酶,对于RNA干扰途径中的微小RNA加工至关重要。DICER1功能的改变破坏了发夹形前体微小RNA的加工,导致3p微小RNA过量和5p微小RNA缺乏,进而导致多个癌症基因网络的异常转录后调节。体细胞突变发生在非上皮性卵巢肿瘤中,尤其是Sertoli-Leydig细胞肿瘤。
大体检查
大体表现无特异性。
组织病理学
DICER1种系突变患者的Sertoli-Leydig细胞肿瘤通常为中至低分化。难以分类或混合性性索-间质肿瘤可能是DICER1综合征的一个线索。其他罕见的肿瘤包括性腺母细胞瘤和宫颈胚胎性横纹肌肉瘤。这些肿瘤在组织学上与其非综合征的对应肿瘤没有区别。
细胞学
无临床相关性
诊断分子病理学
必需证实DICER1的致病性突变。
诊断标准
关键:DICER1的种系突变。
分期
分期与相应部位的其他肿瘤相同。
预后和预测
无临床相关性
09. 卵巢发育不全
定义
卵巢发育不全包括先天性性性发育障碍,患性腺母细胞瘤和其他生殖细胞肿瘤的风险增加。
MIM编号
136435 促卵泡激素受体;FSHR
300697 HECT、UBA和WWE结构域包含蛋白1;HUWE1
480000 性别决定区Y;SRY
ICD-11编码
LD2A性发育畸形疾病
相关命名
可接受:性发育障碍;完全(纯)性腺发育不全;部分(混合)性腺发育不全;Turner综合征;Swyer综合征
亚型
46,XY完全性腺发育不全(Swyer综合征);46,XX完全(纯)性腺发育不全;45,X完全性腺发育不全(Turner综合征及其变异);部分性腺发育不全
部位
卵巢窝
临床特征
患有完全性腺发育不全(CGD)的个体通常表现为原发性闭经和缺乏继发性性征,而患有部分性腺发育不全(PGD)的个体在出生时通常表现为生殖器不明确。生殖器不明确的程度范围很广,从一个极端的阴蒂肥大的几乎女性表型到另一个极端的孤立性尿道下裂的几乎男性表型。有性腺母细胞瘤和生殖细胞瘤的可能性。
流行病学
流行病学尚不清楚。
病因
在46,XX CGD中,已经描述了FSHR(2p21-p16)的失活突变。在46,XY CGD(Swyer综合征)中,SRY的突变和缺失占病例的10-20%,许多与性别决定有关的其他基因也发生了改变,包括SOX9、WT1、DHH、GATA4、NR5A1、NROB1(DAX1)、DMRT1、CBX2、ATRX、MAP3K1和FGF9。45,X CGD是由X染色体的部分或完全缺失引起的。性腺发育不全在分子水平上的病因和发病机制在很大程度上仍然未知。
发病机制
推测性腺母细胞瘤候选基因DDX3Y和TSPY1存在于Y染色体短臂和长臂的近端。DDX3Y阳性和TSPY1阳性的性腺发育不全具有性腺母细胞瘤和生殖细胞瘤的最高患病风险。
大体检查
在CGD中,两个卵巢窝中都有未发育或不可见的性腺组织。在PGD中,一侧有正常发育的睾丸,覆盖着白膜,另一侧有未发育或发育异常的性腺组织。在这种综合征中发生的肿瘤显示出与非综合征对应肿瘤相似的大体变化。
组织病理学
CGD患者的双侧条纹性腺几乎完全由卵巢型间质组成,很少含有性索样结构。在PGD中,正常发育的睾丸组织一侧有发育良好的生精小管,另一侧有条纹性腺;条纹性腺具有多种组织学特征,包括由原始生殖细胞和性索样细胞(或仅由间质细胞组成)或卵巢型间质中仅由少数生殖细胞组成的小梁或条索状结构。在这种综合征中发生的肿瘤与非综合征对应肿瘤的组织学特征相同。
细胞学
无临床相关性
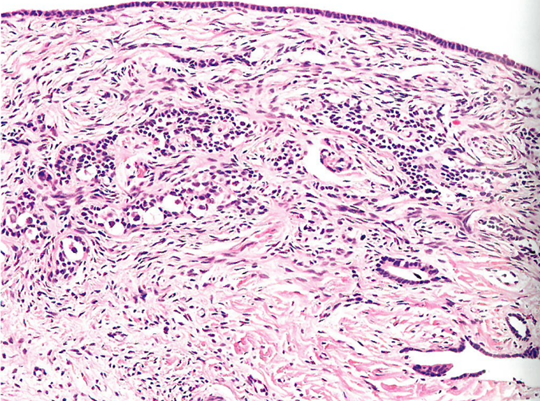
图16.03性腺发育不全。小梁或索状结构,仅由性索状细胞组成,或由原始生殖细胞和性索样细胞紧密混合而成,就像卵巢型间质中性腺母细胞瘤的特征。
诊断分子病理学
无临床相关性
分期
卵巢发育不全根据肿瘤分期。
诊断标准
由卵巢型间质组成的原始组织,没有任何发育良好的卵泡结构或原始的性索样结构,是性腺发育异常的诊断线索。
预后和预测
无临床相关性
10. Von Hippel Lindau综合征
定义
Von Hippel-Lindau综合征(VHL)是一种遗传性常染色体显性疾病,影响多个器官系统,由VHL基因的种系突变引起。
MIM编号
193300 Von Hippel-Lindau综合征;VHLS
ICD-11编码
无
相关命名
无
亚型
无
部位
VHL患者发生的肿瘤包括中枢神经系统和视网膜的血管母细胞瘤、内耳内淋巴囊肿瘤、肾细胞癌、胰腺浆液性囊腺瘤和神经内分泌肿瘤(NET)、嗜铬细胞瘤和副神经节瘤,以及生殖道乳头状囊腺瘤。
临床特征
发病年龄最常见的是18-30岁(平均26岁),范围5-65岁。女性和男性同样受累。临床症状取决于肿瘤的位置和大小。中枢神经系统的血管母细胞瘤引起头痛、呕吐、感觉或运动障碍以及共济失调;视网膜血管母细胞瘤可能导致视力丧失。嗜铬细胞瘤可能无症状,也可能引起与儿茶酚胺过量相关的症状,包括头痛、恐慌症、多汗和血压升高。内耳内淋巴囊肿瘤可能导致耳鸣、眩晕或听力丧失。阔韧带乳头状囊腺瘤通常无症状。诊断通常基于实验室和放射学结果。家族史对于揭示疾病的遗传性质很重要。
流行病学
美国的估计患病率为每3万-5万名新生儿中有1例。
病因
VHL是由位于染色体3p25.3上的VHL肿瘤抑制基因的种系突变引起的。
发病机制
异常或缺失的VHL蛋白导致HIF(一种负责细胞氧调节的蛋白质)以及多种下游生长因子的失抑制性上调,随后导致囊肿和血管瘤性肿瘤的形成。
大体检查
大体表现无特异性。
组织病理学
肿瘤可以是良性(血管母细胞瘤、嗜铬细胞瘤、内淋巴囊肿瘤)或恶性(肾细胞癌)。囊肿也很常见,发生在肾脏、胰腺和生殖道。生殖道可能发生乳头状囊腺瘤,在附睾中比在阔韧带或输卵管系膜中更常见(见乳头状囊腺瘤,原书第240页)。双侧发生者有致病特征性。
细胞学
无临床相关性
诊断分子病理学
鉴定种系VHL突变,对于确诊或确认临床疑似病例是必要的。
诊断标准
必要标准:乳头状囊腺瘤在VHL双侧性位置之外非常罕见,本质上是致病特征;早期肿瘤和囊肿;通过种系突变分析确认诊断。
见简表16.03。
分期
恶性肿瘤根据特定部位的TNM系统进行分期。
预后和预测
预后与各种疾病及其特定部位的并发症有关。
简表16.03 Von Hippel-Lindau综合征的诊断标准

11. 遗传性平滑肌瘤病和肾细胞癌
定义
遗传性平滑肌瘤病和肾细胞癌(HLRCC)是一种常染色体显性肿瘤易感性综合征,伴有是发性皮肤和子宫平滑肌瘤以及肾细胞癌(RCC),最常见的是2型乳头状RCC,与种系FH(富马酸酶)基因突变有关。
MIM编号
150800遗传性平滑肌瘤病与肾细胞癌症;HLRCC
ICD-11编码
无
相关命名
不推荐:遗传性多发性皮肤平滑肌瘤;多发性皮肤和子宫平滑肌瘤;Reed综合征
亚型
无
部位
皮肤、子宫和肾脏(见表16.03)。
临床特征
肿瘤通常发病较早(见表16.03)。
流行病学
HLRCC罕见,患病率不确定;迄今为止,已有300个家庭的文献报道,未经选择的子宫平滑肌瘤女性中有0.24%受到影响。
病因
HLRCC是由富马酸水合酶基因(FH;染色体1q42.3-q43)的常染色体显性遗传种系突变引起的。已知有80多种不同的FH致病性变异。没有基因型-表型相关性,但有高的外显率。子宫平滑肌瘤中富马酸水合酶缺乏症也可能是由于FH基因的零星遗传改变引起的,与HLRCC无关。
发病机制
三羧酸循环酶富马酸水合酶将富马酸转化为L-苹果酸。富马酸水合酶活性降低导致富马酸积累,由于HIFα的稳定导致肿瘤发生。
大体检查
见表16.03
组织病理学
子宫平滑肌瘤表现为鹿角型血管、腺泡状水肿、散在的奇异核、呈链状排列的卵圆形核、嗜酸性胞质包含体和明显嗜酸性核仁伴核周空晕(见表16.03)。
表16.03遗传性平滑肌瘤病和肾细胞癌(HLRCC)相关肿瘤的临床和病理表现
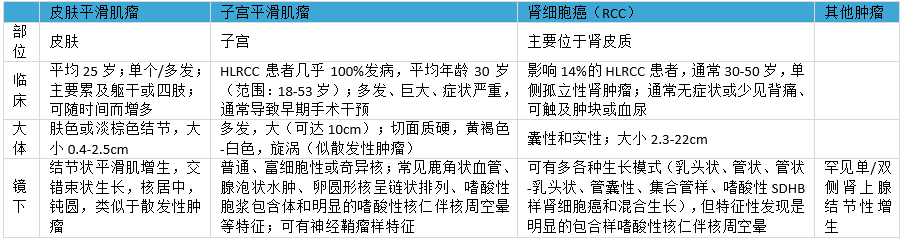
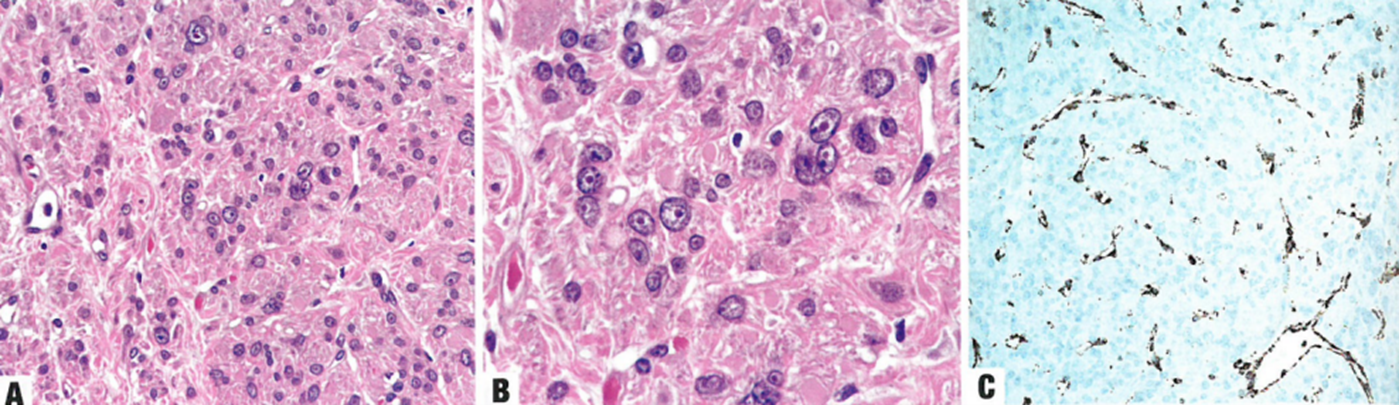
图16.04平滑肌瘤。A,B HLRCC患者的子宫平滑肌瘤。可见明显的嗜酸性核仁。C FH缺乏性平滑肌瘤。免疫组化,平滑肌细胞呈FH阴性。注意血管作为阳性内对照(DAB染色)。
免疫组化
这些肿瘤通常显示富马酸水合酶(FH)的免疫染色丧失,但有些病例可能由于FH错义突变而保留表达。2SC免疫染色阳性可能对FH缺乏症更敏感,但目前尚未广泛使用。
细胞学
无临床相关性
诊断分子病理学
鉴定FH种系突变或缺失,对于确诊是必要的。
诊断标准
如果符合简表16.04中的标准,则可以怀疑或确认HLRCC。
分期
RCC应根据国际癌症控制联盟(UICC)TNM分类进行分期。
预后和预测
这种综合征引起的RCC具有侵袭性。尽管平滑肌肿瘤可能表现出非典型细胞学特征,但很少有关于生物学恶性行为的报道。
简表16.04 疑似或确诊的遗传性平滑肌瘤病和肾细胞癌(HLRCC)诊断标准

12. 女性生殖道的其他遗传性肿瘤综合征
本节描述一组较罕见的遗传性肿瘤综合征,它们可能与妇科(主要是卵巢)肿瘤风险增加有关。
MIM编号
611731 APC基因;APC
601593 BRCA1相关环结构域1;BARD1
605882 BRCA1相互作用蛋白1;BRIP1
610355 BRCA2的伙伴和定位者;PALB2
601309 Patched1;PTCH1
602774 RAD51并行C;RAD51C
602954 RAD51并行D;RAD51D
607035 SUFU刺猬信号传导的负调节因子;SUFU
603254 SWI/SNF相关、基质相关、肌动蛋白依赖的染色质调节因子,亚家族A,成员4;SMARCA4
605284 TSC1基因;TSC1
613254 结节性硬化2型;TSC2
同源重组修复途径基因
在卵巢癌同源重组修复中最常显示种系致病性变异的基因是BRCA1和BRCA2。另外五个基因(BARD1、BRIP1、PALB2、RAD51C和RAD51D)也会增加卵巢高级别浆液性癌的风险。在0.5-1.5%的卵巢癌中检测到这些基因的种系致病性变异。与该基因家族中的致病性变异相关的高级别浆液性癌的生命周期风险尚不清楚,但PALB2的风险可能约为5%,BRIP1、RAD51C和RAD51D的风险约为10%。值得注意的是,乳腺癌风险是相反的,PALB2风险最高。与BARD1致病性变异相关的风险尚不清楚。
APC
APC中的种系致病性变异是家族性腺瘤性息肉病的病因,已在微囊性卵巢肿瘤中发现(见微囊性间质瘤,原书第97页)。然而,大多数微囊性卵巢肿瘤在CTNNB1(编码β-catenin)中获得了体细胞突变,家族性腺瘤性息肉病中很少报道微囊性卵巢肿瘤。
PTCH1/SUFU
卵巢纤维瘤(见原书第217页输卵管浆液性腺纤维瘤和乳头状瘤)可发生在PTCH1或SUFU致病性变异的女性,这两种变异都与痣性基底细胞癌综合征(Gorlin综合征)有关。
SMARCA4/SMARCB1
染色质重塑蛋白SMARCA4是SWI/SNF复合物的一部分,在高钙血症型卵巢小细胞癌中发生突变(见原书第149页,高钙血症型卵巢小细胞癌),高达43%的病例显示出种系突变。SMARCA2免疫组化在疑难病例可能有用。
结节性硬化
结节性硬化症患者中,据报道,罕见的血管周上皮样细胞瘤(PEComa)和淋巴结肌瘤发生在子宫内。
责任编辑:华夏病理 本站欢迎原创文章投稿,来稿一经采用稿酬从优,投稿邮箱tougao@ipathology.com.cn
相关阅读
 数据加载中
数据加载中
我要评论

热点导读
-

淋巴瘤诊断中CD30检测那些事(五)
强子 华夏病理2022-06-02 -

【以例学病】肺结节状淋巴组织增生
华夏病理 华夏病理2022-05-31 -

这不是演习-一例穿刺活检的艰难诊断路
强子 华夏病理2022-05-26 -

黏液性血性胸水一例技术处理及诊断经验分享
华夏病理 华夏病理2022-05-25 -

中老年女性,怎么突发喘气困难?低度恶性纤维/肌纤维母细胞性肉瘤一例
华夏病理 华夏病理2022-05-07







共0条评论