[导读] 编译整理:强子
细胞核表达STAT6和/或CK的肿瘤
孤立性纤维性肿瘤
孤立性纤维性肿瘤是以NAB2::STAT6融合为特征的成纤维细胞肿瘤,其发病部位较为广泛,在头颈部肿瘤占比5-27%不等,常见累及鼻腔和眼眶。
组织学上,孤立性纤维性肿瘤的特征是形态均一的胖梭形细胞,呈无序排列(即patternless),背景为程度不等的胶原至黏液样表现,伴分支的扩张血管。细胞也会存在某些变异,如脂肪样分化(脂肪形成型孤立性纤维性肿瘤)、上皮样细胞、透明细胞、多核巨细胞。罕见情况下,孤立性纤维性肿瘤还可出现间变性转化/去分化,形态学上出现显著恶性多形性形态、并伴大量核分裂及显著会阿斯。已知该肿瘤可异源性分化为其他间质成分(如横纹肌肉瘤样、骨肉瘤样)、上皮成分(如神经内分泌表现、鳞状),但极为少见。
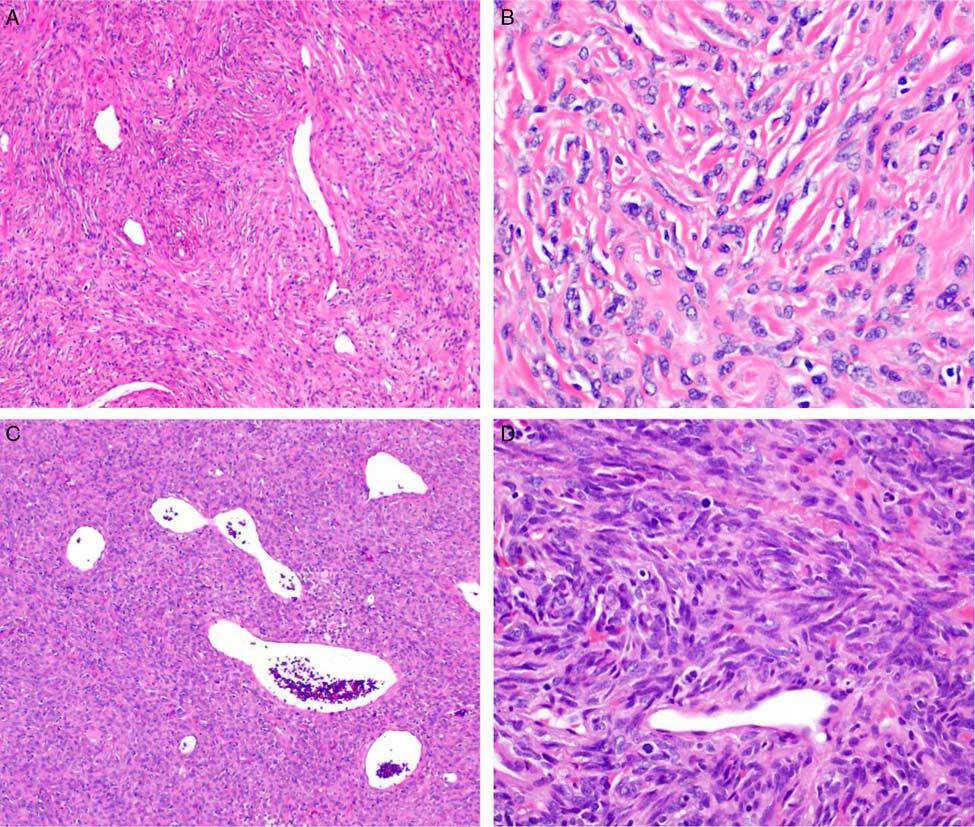 图3. (A)典型孤立性纤维性肿瘤,细胞密度低至中等,间质致密胶原化,伴“鹿角状”血管;(B)高倍镜下,瘤细胞为形态温和的卵圆形至纺锤形,混杂有胶原性间质,细胞分界不清,细胞核卵圆形至成角表现,染色质分布均匀。(C、D)富于细胞的孤立性纤维性肿瘤,细胞丰富,伴特征性的鹿角状血管;高倍镜下细胞呈致密、无序排列,细胞形态与经典型孤立性纤维性肿瘤的细胞并无区别。
图3. (A)典型孤立性纤维性肿瘤,细胞密度低至中等,间质致密胶原化,伴“鹿角状”血管;(B)高倍镜下,瘤细胞为形态温和的卵圆形至纺锤形,混杂有胶原性间质,细胞分界不清,细胞核卵圆形至成角表现,染色质分布均匀。(C、D)富于细胞的孤立性纤维性肿瘤,细胞丰富,伴特征性的鹿角状血管;高倍镜下细胞呈致密、无序排列,细胞形态与经典型孤立性纤维性肿瘤的细胞并无区别。
免疫组化方面,孤立性纤维性肿瘤弥漫、强阳性细胞核表达STAT6,该标记的敏感性近100%,特异性大于95%;90-95%的病例表达CD34。脑膜及头颈部也有CD34阴性孤立性纤维性肿瘤的报道。部分肿瘤可局灶表达S100、细胞核表达β-catenin、CK(AE1/AE3)、EMA。
目前对于孤立性纤维性肿瘤的诊断,推荐用STAT6免疫组化;但间变性/去分化区域可能会有STAT6及CD34的表达缺失。如果免疫组化STAT6阳性,则无需证实NAB2::STAT6融合即可做出孤立性纤维性肿瘤的诊断。由于该融合中涉及NAB2和STAT6的不同外显子而会产生多种类型的融合,因此其分子诊断更为复杂,需要可以检出包括内含子融合在内的20多种融合类型的多重检测。因此,对于证实孤立性纤维性肿瘤的诊断来说,免疫组化STAT6要比常规分子检测更为敏感。
尽管STAT在孤立性纤维性肿瘤的诊断中很有帮助,但有两个陷阱需要注意。约18-20%的去分化脂肪肉瘤及部分GLI1扩增的间叶性肿瘤也可表达STAT6,这是由于位于12号染色体q13.3-q15处的STAT6与MDM2、CDK4、和/或GLI1共扩增所致。需要注意的是,去分化脂肪肉瘤和GLI1扩增的间叶性肿瘤中,STAT6的表达见于细胞核和细胞质,而孤立性纤维性肿瘤中STAT6的表达局限于细胞核。此外,去分化脂肪肉瘤和GLI1扩增的间叶性肿瘤都表达MDM2和CDK4,而孤立性纤维性肿瘤不表达这些标记。GLI1改变的间叶性肿瘤特点为卵圆形至上皮样细胞呈巢状及片状,有纤细的毛细血管分隔,这与孤立性纤维性肿瘤中的扩张血管也是不同的。最后,去分化脂肪肉瘤在鼻腔鼻窦属于极为罕见病种,而GLI1改变的肿瘤也还未见发生于该部位的报道,因此这一免疫组化陷阱主要体现在其他解剖部位。
最近在头颈部报道了四例伴NAB2::STAT6重排、形态学有独特表现的肿瘤。其中两例发生于鼻腔,且有类似于畸胎癌肉瘤的双相型表现,即有数量不等的上皮成分和间质成分,前者如神经上皮、鳞状上皮、伴黏液的腺上皮,后者如横纹肌母细胞成分。免疫组化表现与其组织学分化相对应。此外,STAT6在梭形细胞区域细胞核阳性,而在上皮区域和神经上皮巢中均为阴性。这两例肿瘤都还有CCND1、CTNNB1、BRCA2基因的突变以及其他突变,这些一般都不见于孤立性纤维性肿瘤。另外两例发生于口腔及咽旁,形态学仅为均一的上皮样细胞,免疫组化表达STAT6、S100、AE1/AE3、p63、p40、desmin。尽管这些特征存在GLI1改变肿瘤的可呢个,但FISH检测GLI1改变为阴性。作者提出,还不清楚这组肿瘤是碰撞瘤、还是去分化的孤立性纤维性肿瘤、或者是与孤立性纤维性肿瘤在分子特征方面有重叠的新型病种。
滑膜肉瘤
关于滑膜肉瘤的临床及组织学特征,此处不再赘述。多年以来,滑膜肉瘤诊断中的免疫组化仅限于CK、BCL2、CD99的表达。对于滑膜肉瘤诊断具有较好敏感性和特异性的第一个指标是TLE1,这在基因表达谱研究中也得到了证实。如很多其他标记物一样,随着应用的增加,TLE1的表达已可见于多种肉瘤和癌。就梭形细胞肿瘤来说,TLE1的表达常见于血管瘤样纤维组织细胞瘤、BCOR改变的肉瘤、鼻腔鼻窦球周皮细胞瘤,罕见情况下可见于恶性外周神经鞘瘤、孤立性纤维性肿瘤。因此,鼻腔鼻窦梭形细胞肿瘤的诊断中,不要因此而误判。
据报道,针对滑膜肉瘤特征性SS18::SSX融合位点的抗体在诊断中的敏感性高达87-95%,特异性近100%;针对SSX中C末端的抗体检测则敏感性大于90%、特异性为93-96%,罕见的假阴性出现在未分化多形性肉瘤、平滑肌肉瘤、黏液纤维肉瘤等梭形细胞肉瘤中。有限的病例研究中,恶性外周神经鞘瘤、孤立性纤维性肿瘤、鼻腔鼻窦球周皮细胞瘤中均为阴性。因此,这两项标记是SS18::SSX基因融合所致滑膜肉瘤所特有,似乎是所有解剖部位滑膜肉瘤诊断的可靠替代性标记,可用于取代分子或细胞遗传学检测。伴特殊融合的罕见滑膜肉瘤也有描述,这类针对经典融合的抗体可能无法识别。
伴EWSR1/FUS::POU2AF3(COLCA2)融合的肉瘤
最近在多个解剖部位报道了一组伴EWSR1/FUS::POU2AF3(此前称为COLCA2)融合的肉瘤,好发于头颈部、尤其鼻腔鼻窦处。大部分病例发生于年轻至中年人,并无性别差异。该组肿瘤形态学为双相型,即梭形至星型细胞、围绕着肥胖上皮样细胞和圆形细胞形成的结节及细胞巢。
有作者在其8个病例中注意到有两种组织学表现:一组是低级别、轻度非典型的梭形细胞,另一组是细胞核深染、圆形至梭形的高级别细胞。此外,也有异源性分化,具体体现在个别病例出现上皮(产黏液的腺体、神经内分泌)、横纹肌母细胞、骨肉瘤样区域等。该报道中发现其免疫组化表达多种多样,程度不等的表达CK、EMA、神经内分泌标记、S100。
由于这类病例形态学为双相型,且免疫组化表达上皮标记,因此常与滑膜肉瘤混淆。所以实际工作中需要加做滑膜肉瘤特异性抗体(如SS18-SSX或针对SSX中C末端的抗体),或进行分子检测。此外,不管该组肿瘤的形态学表现如何,伴EWSR1/FUS::POU2AF3融合的肉瘤都是侵袭性行为,会有复发及转移。
——未完待续——
往期回顾
从免疫组化的角度解读鼻腔鼻窦处梭形细胞肿瘤(一)














共0条评论