第13章 下生殖道间叶性肿瘤
下生殖道间叶性肿瘤WHO分类表5ed
1、脂肪细胞肿瘤
8850/0 脂肪瘤NOS
8881/0 脂肪母细胞瘤样肿瘤
8850/3 脂肪肉瘤NOS
8850/1 非典型脂肪瘤
8852/3 粘液样脂肪肉瘤
8851/3 脂肪肉瘤,高分化,NOS
8858/3 去分化脂肪肉瘤
8854/3 多形性脂肪肉瘤
2、纤维母细胞肿瘤和肌纤维细胞肿瘤
手手术后梭形细胞结节
纤维上皮间质息肉
8810/0 纤维瘤NOS
8825/0 肌纤维母细胞瘤
9160/0 富细胞性血管纤维瘤
8826/0 血管肌纤维母细胞瘤
8815/1 孤立性纤维瘤NOS
8815/3 孤立性纤维瘤,恶性
8832/1 隆突性皮肤纤维肉瘤NOS
8833/1 色素性隆突性皮肤纤维肉瘤
8832/3 隆突性皮肤纤维肉瘤,纤维肉瘤性
NTRK重排梭形细胞肿瘤(新增)
3、血管肿瘤
9140/3 卡波西肉瘤
9120/3 血管肉瘤
4、平滑肌肿瘤
8890/0 平滑肌瘤NOS
8891/0 上皮样平滑肌瘤
8896/0 粘液样平滑肌瘤
8890/3 平滑肌肉瘤NOS
8891/3 上皮样平滑肌肉瘤
8896/3 粘液样平滑肌肉瘤
5、横纹肌肿瘤
8905/0 生殖器横纹肌瘤
8900/3 横纹肌肉瘤NOS
8910/3 胚胎性横纹肌肉瘤
8920/3 肺泡横纹肌肉瘤
8901/3 多形性横纹肌肉瘤
6、周围神经鞘瘤
9540/0 神经纤维瘤NOS
9560/0 神经鞘瘤
9580/0 颗粒细胞瘤NOS
9580/3 颗粒细胞瘤,恶性
7、分化不确定的肿瘤
8841/0 浅表血管粘液瘤
8841/0 侵袭性血管粘液瘤
8804/3 上皮样肉瘤
经典型上皮样肉瘤
近端或大细胞上皮样肉瘤
9581/3 肺泡状软组织肉瘤
8、未分化小圆细胞肉瘤
9364/3 尤因肉瘤
————
形态学代码来自《国际肿瘤疾病分类》,第三版,第二版(ICD-0-3.2)。生物学行为代码/0用于良性肿瘤;/1用于非特指、交界性或不确定行为;/2用于原位癌和III级上皮内肿瘤;/3用于恶性肿瘤的原发部位;/6用于恶性肿瘤的转移部位。癌症登记处通常不使用行为代码/6。
新分类来自第4版WHO分类的修订,考虑到我们对这些病变的理解发生了变化
*IARC WHO ICD-O委员会在2020年6月的会议上批准了标有星号的代码。
下生殖道间叶性肿瘤:简介
本章关于间叶性瘤的重点是女性生殖器官,特别是下生殖道最常见的疾病实体,但几乎任何软组织肿瘤都可能在任何部位出现,至少极少数情况下确实如此。某些间叶性肿瘤几乎总是局限于一个部位,因此放在这些部位的章节中(见第1章卵巢肿瘤、第6章子宫体肿瘤和第8章子宫颈肿瘤)。血管周上皮样细胞肿瘤(PEComa)和炎性肌纤维母细胞肿瘤在子宫外罕见,因此放在第6章。
发病率
软组织肉瘤的发病率相当稳定,为每百万人每年30-50例。良性软组织肿瘤的总体发病率至少高出100倍。每个良性间叶性实体的发病率范围从常见(如脂肪瘤)到罕见(如梭形细胞血管瘤)。肉瘤是原发性女性生殖器官肿瘤的较少见亚组,其发病率远远低于癌和良性间叶性肿瘤。
女性最常见的良性肿瘤是平滑肌瘤,可以发生在整个女性生殖道(FGT,包括外阴和阴道),最常见于子宫。无论手术指征如何,近80%的子宫切除术标本检出了子宫平滑肌瘤,可以证明这一点。平滑肌瘤在整个女性生殖器官中普遍存在,而其他几种软组织肿瘤仅仅或主要发生在远端FGT,如血管肌纤维母细胞瘤和富细胞性血管纤维瘤,因此认为它们具有相对的部位特异性。还可以看到皮肤和软组织的其他间叶性瘤类型,本书讨论了最常见和/或最具特征的肿瘤类型。软组织和骨肿瘤WHO分类涵盖了本书软组织肿瘤的全部范围。
病因和发病机制
大多数软组织肿瘤是自然发生的,其发病机制尚不清楚,但在某些情况下可以明确病因。与软组织肿瘤相关的病毒包括EBV(与免疫抑制患者某些平滑肌肿瘤有关)和HHV8(与卡波济氏肉瘤有关)。血管肉瘤可能涉及长期存在的淋巴水肿,肉瘤也可能出现在先前接受放射治疗的区域(如外阴)。远端FGT中的软组织肿瘤(良性和恶性)也可能与遗传综合征有关,如DICER1综合征(宫颈胚胎性横纹肌肉瘤)、Li-Fraumeni综合征(胚胎性横纹肉瘤)、神经纤维瘤病1型(神经纤维瘤)和Cowden综合征(脂肪瘤和血管瘤)。这些综合征在软组织肿瘤WHO分类中进有更详细的讨论。
大多数肉瘤的细胞起源仍然未知,前驱病变和原位病变尚未识别。
仍不确定某些放射后非典型血管病变是否代表皮肤血管肉瘤的前驱病变(或风险因素)。体细胞遗传因素,如重现性染色体易位,驱动了一些肉瘤的发病机制,但这些体细胞遗传因素如何致病,驱动什么细胞致瘤,在很大程度上仍然未知。
临床特征
良性和恶性软组织肿瘤通常表现为无痛肿块,其生长速度各不相同。在远端FGT,特别是在外阴,大多数良性软组织肿瘤在临床上通常被当成更常见的良性前庭大腺囊肿,直到切除后才认识到病变是实性肿瘤。一些病变具有息肉样特征,分为良性(纤维上皮间质息肉、浅表血管粘液瘤)和恶性(胚胎性横纹肌肉瘤)两类。
组织病理学
恶性软组织肿瘤可能表现出核多形性、核分裂象活性和坏死,但核异型性的意义应结合肿瘤类型的进行评估。如,在富细胞性血管纤维瘤中,可以看到核异型性,并且确实会影响生物学行为;在其他实体中,如孤立性纤维瘤,核多形性、核分裂象活性升高和坏死可能与侵袭行为有关。一般来说,形态学评估是区分远端FGT大多数相对部位特异性肿瘤的关键,因为它们的免疫组化表达谱呈现明显的重叠,并有一些罕见的例外情形。如,RB1缺失可见于富细胞性血管纤维瘤、梭形细胞脂肪瘤和乳腺型肌纤维母细胞瘤。
遗传学
良性软组织肿瘤具有简单的遗传特性,具有二倍体核型或单一特征性染色体重排。一种中间属性的肿瘤,深部血管粘液瘤,具有局部复发的倾向,但不转移,其特征是涉及染色体区域12q13-q15的核型畸变。在恶性肿瘤中,存在两种遗传类型:与重现性突变或易位相关的简单核型肉瘤(如肺泡状软组织肉瘤)和具有许多染色体畸变但通常缺乏重现性突变(除外TP53、RB1和ATRX等基因中的功能丧失突变)的复杂核型肉瘤(如平滑肌肉瘤),具体取决于肿瘤类型。
诊断程序
需要获取的信息包括对肿瘤大小和深度的临床评估、影像学检查(CT、MRI或超声)以及活检。影像学检查可用于评估原发性肿瘤的范围,确定其与相邻解剖结构的关系,并识别转移。如,影像学研究可用于评估局部侵袭性肿瘤的范围,如深部血管粘液瘤。
肿瘤行为
软组织和骨肿瘤WHO对分类认可四种肿瘤行为类别:良性、中间(局部侵袭性)、中间(罕见转移)和恶性。良性肿瘤,如血管肌纤维母细胞瘤、富细胞性血管纤维瘤和浅表血管粘液瘤,通常通过局部切除治愈,很少局部复发(任何复发都是非破坏性)。中间肿瘤可以是局部侵袭性(如硬纤维瘤病和深部血管粘液瘤,局部浸润周围组织),也可以是罕见转移(肿瘤转移风险非常低,<2%,但有明确的转移风险;如炎症性肌纤维母细胞瘤)。恶性肿瘤,如平滑肌肉瘤,可以局部复发和转移
分级
分级是根据组织学参数试图预测临床行为,但只能用于未经治疗的原发性肿瘤的材料。它不适用于所有肉瘤;如,血管肉瘤、透明细胞肉瘤和上皮样肉瘤总是认为高级别的。最广泛使用的软组织肉瘤分级系统是由法国癌症控制中心(FNCLCC)研发的三级系统。它结合肿瘤分化、核分裂象活性和坏死,将肿瘤分为低、中或高级别。然而,这种分级系统并不常用于妇科肉瘤。目前正在研发更广泛适用的分子方法。
分期
美国癌症联合委员会(AJCC)和国际癌症控制联盟(UICC)TNM分期系统被广泛使用。肉瘤分期包括组织学分级和受累部位,以及组织学类型、肿瘤大小、淋巴结受累程度和是否存在远处转移。还考虑了纳入年龄和性别等非解剖学参数的替代分期和风险评估方法。
预后和预测因素
完全切除是预防局部复发的最重要因素,这与浸润性边界(深部血管黏液瘤)或不规则边界(浅部血管黏液癌)的肿瘤尤其相关。一些肉瘤(特别是上皮样肉瘤)持续复发,通常伴有晚期转移。通常与更大转移风险相关的因素是肿瘤体积更大和级别更高。
1、脂肪细胞肿瘤
01. 脂肪瘤
定义
脂肪瘤是成熟脂肪细胞形成的良性肿瘤。
ICD-O编码
8850/0 脂肪瘤NOS
ICD-11编码
2E80.0&XH1PL8脂肪瘤&脂肪瘤NOS
相关命名
可接受:普通型或经典型脂肪瘤
亚型
无
部位
脂肪瘤最常见于外阴,但也可能发生在任何部位。
临床特征
脂肪瘤表现为浅表、孤立、柔软、可移动且无痛的肿块。
流行病学
脂肪瘤发生在育龄妇女和儿童。
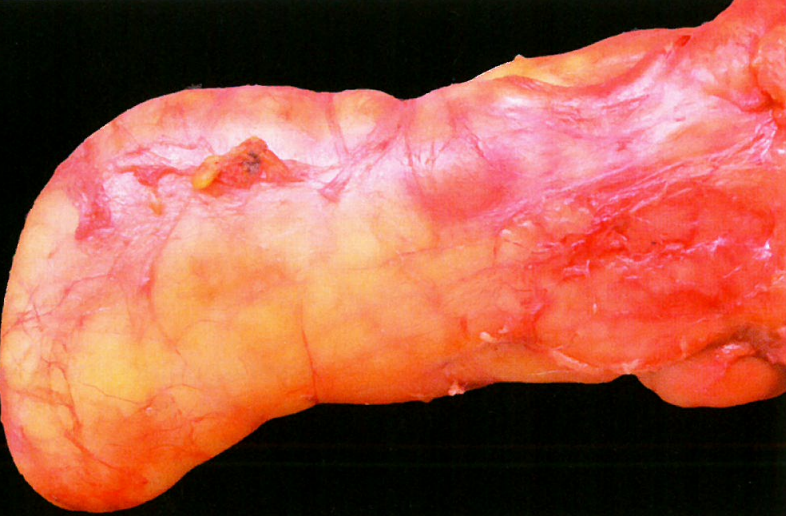
图13.01脂肪瘤。大体检查,特征性表现为分叶状黄色肿块,伴有薄的纤维包膜。
病因
未知
发病机制
大多数常规脂肪瘤存在异常核型。最常见的改变涉及12q13-q15,导致HMGA2与多种基因伴侣融合。其他报道的染色体异常包括6p和13q重排。
大体检查
脂肪瘤呈分叶状,边界清晰,有时有薄的纤维包膜。切面呈均匀的黄色,薄纤维间隔将肿瘤分为小叶,可出现局灶性出血。据报道,肿瘤的最大大小超过15cm。
组织病理学
肿瘤由相对均匀的成熟脂肪细胞组成,这些细胞排列成片状和/或被薄层纤维分隔成小叶。脂肪细胞和纤维间质细胞缺乏细胞学异型性;脂肪母细胞不存在。退行性变化,包括粘液样间质变化和脂肪坏死,可能发生,特别是较大的肿瘤。
细胞学
无临床相关性
诊断分子病理学
较大的肿瘤,缺乏MDM2扩增可能有助于排除非典型脂肪瘤。
诊断标准
必要标准:位置表浅;大小均匀的成熟脂肪细胞;纤维间隔中缺乏非典型间质细胞。
理想标准:大肿瘤(>10cm),免疫组化不表达MDM2或CDK4,或原位杂交MDM2不扩增。
分期
无临床相关性
预后和预测
脂肪瘤是良性肿瘤。
02. 外阴的脂肪母细胞瘤样肿瘤
定义
外阴的脂肪母细胞瘤样肿瘤是一种脂肪细胞肿瘤,与脂肪母细胞瘤、粘液样脂肪肉瘤和梭形细胞脂肪瘤共有某些组织形态学特征。
ICD-O编码
8881/0脂肪母细胞瘤样肿瘤
ICD-11编码
2E80.1脂肪母细胞瘤
相关命名
无
亚型
无
部位
外阴
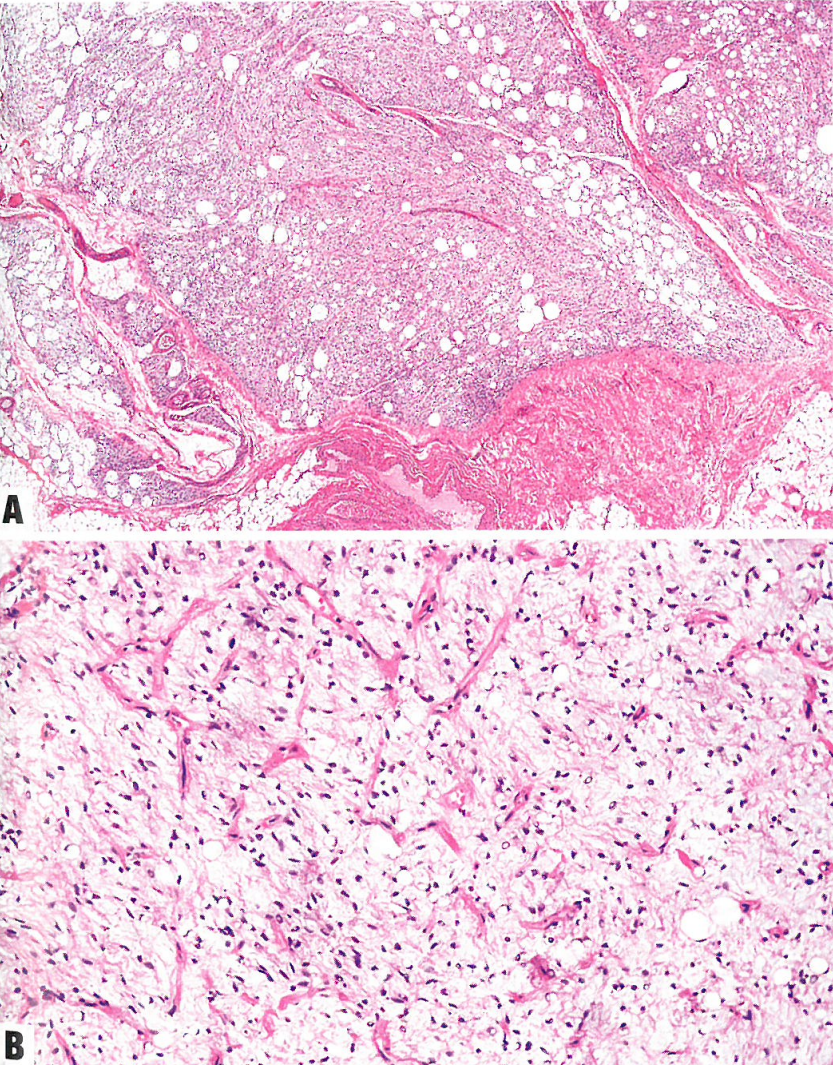 图13.02外阴的脂肪母细胞瘤样肿瘤。A由薄厚不一的纤维间隔和不同程度的粘液样间质勾勒出分叶状结构。B明显的薄壁分支血管。
图13.02外阴的脂肪母细胞瘤样肿瘤。A由薄厚不一的纤维间隔和不同程度的粘液样间质勾勒出分叶状结构。B明显的薄壁分支血管。
临床特征
外阴脂肪母细胞瘤样肿瘤是增大的、有时疼痛的肿块。
流行病学
外阴的脂肪母细胞瘤样肿瘤通常发生在育龄妇女。
病因
未知
发病机制
未知
大体检查
外阴的脂肪母细胞瘤样肿瘤最常见表现为单侧、大体粘液样或胶状、边界清晰、分叶状外阴肿块。
组织病理学
这些肿瘤的特征是分叶状生长,由大小不一的纤维间隔勾勒出分叶状结构,由成熟脂肪细胞、单空泡和双空泡脂肪母细胞以及细胞学温和的梭形细胞组成。梭形细胞的核两端变圆或变细,伴丰富的纤丝状胞质。有不同程度地明显的粘液样间质,并有薄壁血管并经常分支,类似于粘液样脂肪肉瘤和脂肪母细胞瘤中的血管。间质胶原可以表现为纤细的纤维或粗大的斑块。核分裂象不活跃,没有坏死。
 图13.03外阴的脂肪母细胞瘤样肿瘤。不同比例的成熟脂肪细胞、形态温和的脂肪母细胞和具有短粗核的梭形细胞。
图13.03外阴的脂肪母细胞瘤样肿瘤。不同比例的成熟脂肪细胞、形态温和的脂肪母细胞和具有短粗核的梭形细胞。
绝大多数肿瘤缺乏PLAG1和HMGA2,RB1核表达完全缺失或呈弱表达与阴性互相镶嵌的模式。在少数病例的研究中,它们呈S100阴性,MDM2和CDK4阴性(或罕见局部阳性)。梭形细胞可能呈CD34阳性。
细胞学
无临床相关性
诊断分子病理学
FISH未发现DDIT3和PLAG1重排(分别),可以区分粘液样脂肪肉瘤和脂肪母细胞瘤。FISH亦未发现RB1区域的获得或缺失,染色体微阵列的基因组拷贝数分析发现大多数肿瘤都有正常的二倍体特征,这表明外阴的脂肪母细胞瘤样肿瘤可能与梭形细胞脂肪瘤无关。
诊断标准
必要标准:分叶状生长,有不同大小的纤维间隔,成熟脂肪细胞、单/双空泡脂肪母细胞和形态温和的梭形细胞的混合;不同程度的粘液样间质和薄壁分支血管
理想标准:FISH没有DDIT3或PLAG1重排或RB1区域增益或损失;PLAG1和HMGA2表达缺失
分期
无临床相关性
预后和预测
肿瘤可能很少复发,这与切除边缘受累有关。尚未有转移的报道。
03. 脂肪肉瘤
定义
脂肪肉瘤是一种恶性脂肪细胞肿瘤,具有局部侵袭行为和远处转移的潜能。
ICD-O编码
8850/3脂肪肉瘤NOS
8850/1非典型脂肪瘤
8852/3粘液样脂肪肉瘤
8851/3脂肪肉瘤,高分化,NOS
8858/3去分化脂肪肉瘤
8854/3多形性脂肪肉瘤
ICD-11编码
2B59.Z脂肪肉瘤,非特指原发部位
相关命名
“非典型脂肪瘤(atypical lipomatous tumour,ALT)”这个术语用于肢体和其他容易手术切除的部位。“高分化的脂肪肉瘤(WDLPS)”保留用于后腹膜等部位,这些部位难以完全切除,局部复发和去分化的风险都升高。
亚型
无
部位
外阴,阴道
临床特征
下生殖道脂肪肉瘤罕见。ALT和粘液样脂肪肉瘤是该部位较频繁的文献报道类型,而去分化脂肪肉瘤和多形性脂肪肉瘤极少见。
流行病学
ALT患者诊断时年龄40-60岁。粘液样脂肪肉瘤患者较年轻,年龄范围为10-40岁。
病因
参考《软组织和骨肿瘤WHO分类》。
发病机制
参考《软组织和骨肿瘤WHO分类》。
大体检查
ALT/WDLPS由分叶状脂肪组织组成,切面黄色至褐色,可能含有肉眼可见的纤维组织。去分化区域呈红-褐-灰色,质硬或肉样。粘液样脂肪肉瘤边界清晰,多结节状,切面呈胶样,褐-白-灰色。粘液样脂肪肉瘤中的圆形细胞区域呈实性或肉样。多形性脂肪肉瘤具有不同的大体特征,从轮廓清晰到浸润性不等,切面呈黄褐色,伴或不伴坏死。
组织病理学
脂肪肉瘤组包括ALT/WDLPS、去分化脂肪肉瘤、粘液样脂肪肉瘤和多形性脂肪肉瘤。
ALT含有相对高分化的脂肪细胞,成片分布和形成小叶,细胞大小和形状各不相同,至少局灶性核增大、核深染。纤维间隔将脂肪细胞分开并形成小叶,纤维间隔含有散在的、增大的、深染的间质细胞。单空泡或多空泡脂肪母细胞可能存在,但不是诊断所必需的。在去分化脂肪肉瘤中,去分化区域通常由更高级别的肉瘤组成,可以呈现各种同源和异源的形态表现(细胞丰富、多形性、粘液样,等)。
粘液样脂肪肉瘤具有分叶状或多结节状,由非脂源性低级别梭形细胞、不同数量的单泡/多泡脂肪母细胞、大量的粘液样间质和明显的分支薄壁血管混合组成。肿瘤小叶/结节的周围往往细胞量增多。相比之下,圆细胞/高级别粘液样脂肪肉瘤的定义是≥5%的肿瘤体积包含明显的细胞丰富区域,伴更高的细胞学异型性和更多的核分裂象活性。
多形性脂肪肉瘤是一种形态学异源性高级别肉瘤,以大而深染的多空泡脂肪母细胞的形态显示脂肪分化。去分化脂肪肉瘤含有同源脂肪母细胞分化(存在传统型ALT成分),这与多形性脂肪肉瘤不同。
细胞学
无临床相关性
诊断分子病理学
ALT/WDLPS和去分化脂肪肉瘤与MDM2和(通常)CDK4的扩增有关。大多数(>90%)粘液样脂肪肉瘤携带重现性t(12;22)(q13;p11),产生FUS-DIT3基因融合;其余肿瘤携带重现性t(12;22)(q13;q12),产生EWSR1-DDIT3基因融合。多形性脂肪肉瘤具有非重现性复杂核型异常和频繁的TP53突变。
诊断标准
必要标准:ALT/WDLPS:成熟的非典型脂肪细胞和增厚的纤维间隔(其中的细胞含有非典型核)——脂肪母细胞可有可无;
去分化脂肪肉瘤:非脂细胞性肉瘤,其级别高于共存的ALT/WDLPS;
粘液样脂肪肉瘤:非脂源性梭形细胞、脂肪母细胞、粘液样间质和薄壁分支血管的混合;
多形性脂肪肉瘤:高级别肉瘤含有多空泡的增大的脂肪母细胞,排除其他更常见的肿瘤,如癌肉瘤。
理想标准:ALT/WDLPS和去分化脂肪肉瘤:MDM2扩增;粘液样脂肪肉瘤:DDIT3重排。
分期
该实体使用国际癌症控制联盟(UICC)TNM分期系统。
预后和预测
大多数下生殖道脂肪肉瘤很少发生局部和远处复发。圆细胞/高级别粘液样脂肪肉瘤含有≥5%的圆细胞或细胞丰富区域,患者的预后通常不利。
2、纤维母细胞肿瘤和肌纤维细胞肿瘤
01. 手术后梭形细胞结节
定义
手术后梭形细胞结节是一种良性、可能非肿瘤性的梭形细胞增殖,可能被误认为肉瘤。
ICD-O编码
无
ICD-11编码
无
相关命名
不推荐:术后假性肉瘤;炎性假瘤
亚型
无
部位
在女性生殖道中,阴道、外阴、宫颈和子宫内膜都报道过手术后梭形细胞结节。
临床特征
手术后梭形细胞结节通常在术后几周内在先前手术的部位形成。
流行病学
这些病变发生于广泛的年龄范围,但通常发生在育龄妇女。
病因未知
发病机制
手术后梭形细胞结节可能是反应性增生。
大体检查
手术后梭形细胞结节是界限模糊的结节,通常<3cm。
组织病理学
病变由松散的交叉束状的梭形细胞组成,胞浆嗜酸性至双嗜性,位于不同程度水肿间质中。常见纤细的血管网。此外,慢性炎症细胞通常出现在病变内及其周围,可能延伸到周围组织。如果病变伴有浅表溃疡,则可见急性炎症。核分裂象可能很多。梭形细胞表达vimentin,desmin和SMA可能阳性。重要的是,要排除炎性肌纤维母细胞肿瘤和纤维瘤病。
细胞学
无临床相关性
诊断分子病理学
无临床相关性
诊断标准
必要标准:事先进行过手术;梭形细胞呈松散的交叉束状排列;慢性炎性浸润。
分期
无临床相关性
预后和预测
手术后梭形细胞结节是良性病变。
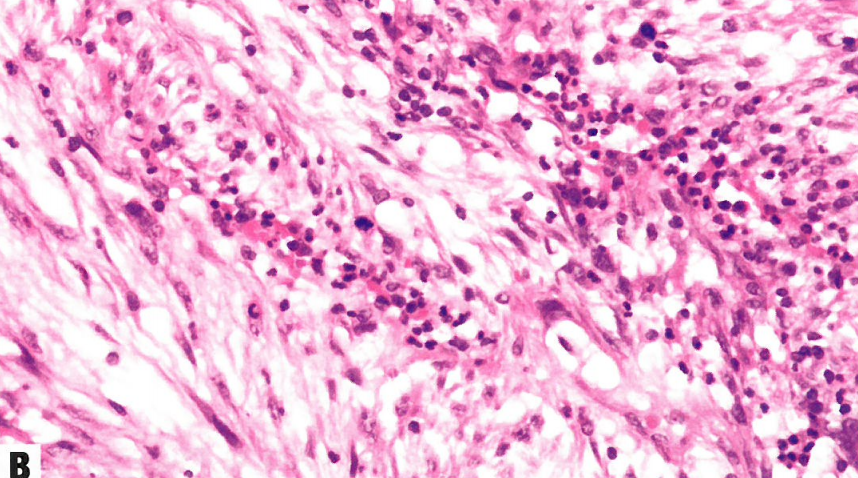
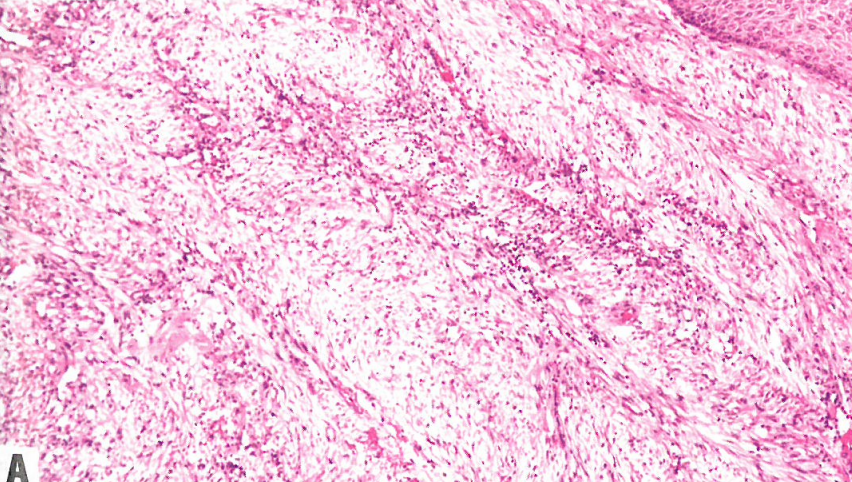 图13.04手术后梭形细胞结节。A外阴鳞状上皮下方存在相对富细胞性梭形细胞增殖。背景为水肿、纤细血管和炎性浸润。B 肿瘤细胞呈梭形,胞质丰富、淡染,核细长,染色质呈空泡状(部分有核仁)。有核分裂象活性。
图13.04手术后梭形细胞结节。A外阴鳞状上皮下方存在相对富细胞性梭形细胞增殖。背景为水肿、纤细血管和炎性浸润。B 肿瘤细胞呈梭形,胞质丰富、淡染,核细长,染色质呈空泡状(部分有核仁)。有核分裂象活性。
02. 纤维上皮间质息肉
定义
纤维上皮间质息肉是女性下生殖道的良性息肉样间叶性肿瘤。
ICD-O编码
无
ICD-11编码
无
相关命名
不推荐:纤维上皮性息肉;富细胞性假肉瘤性纤维上皮性间质息肉;葡萄状假肉瘤;中胚层间质息肉
亚型
无
部位
纤维上皮间质息肉最常见于阴道,也可见于外阴或(很少)宫颈。
临床特征
纤维上皮间质息肉通常是偶然发现。症状可能包括出血、阴道排液或不适。病例通常表现为孤立性病变;然而,妊娠期间可能出现多发性息肉
流行病学
纤维上皮间质息肉经常发生在妊娠期间,但也可能发生在接受激素替代治疗的绝经后妇女,或很少发生在婴儿。
病因
未知
发病机制
一般认为,纤维上皮间质息肉起源于女性下生殖道对激素有反应的上皮下方的间质细胞。
大体检查
纤维上皮间质息肉通常小于5cm,最大者可达18.5cm。外观变化较大,从无蒂到有蒂再到绒毛状,从柔软到橡胶状和灰红色。
组织病理学
纤维上皮间质息肉含有三种成分:纤维血管轴心、有蒂或息肉样增生的间质和被覆鳞状上皮。最典型的特征是存在星状和多核间质细胞,它们倾向于聚集在间质-上皮交界处和纤维血管轴心的血管周围。可能呈现显著丰富的间质细胞、核多形性、核分裂象活性增加>5个/mm2(相当于直径为0.5mm、面积为0.2mm2视野>10个/10HPF),以及非典型核分裂象(间质细胞的假肉瘤改变)。被覆鳞状上皮可能增生。免疫组化,间质细胞恒定表达desmin、ER和PR,有时表达SMA。罕见myogenin阳性。
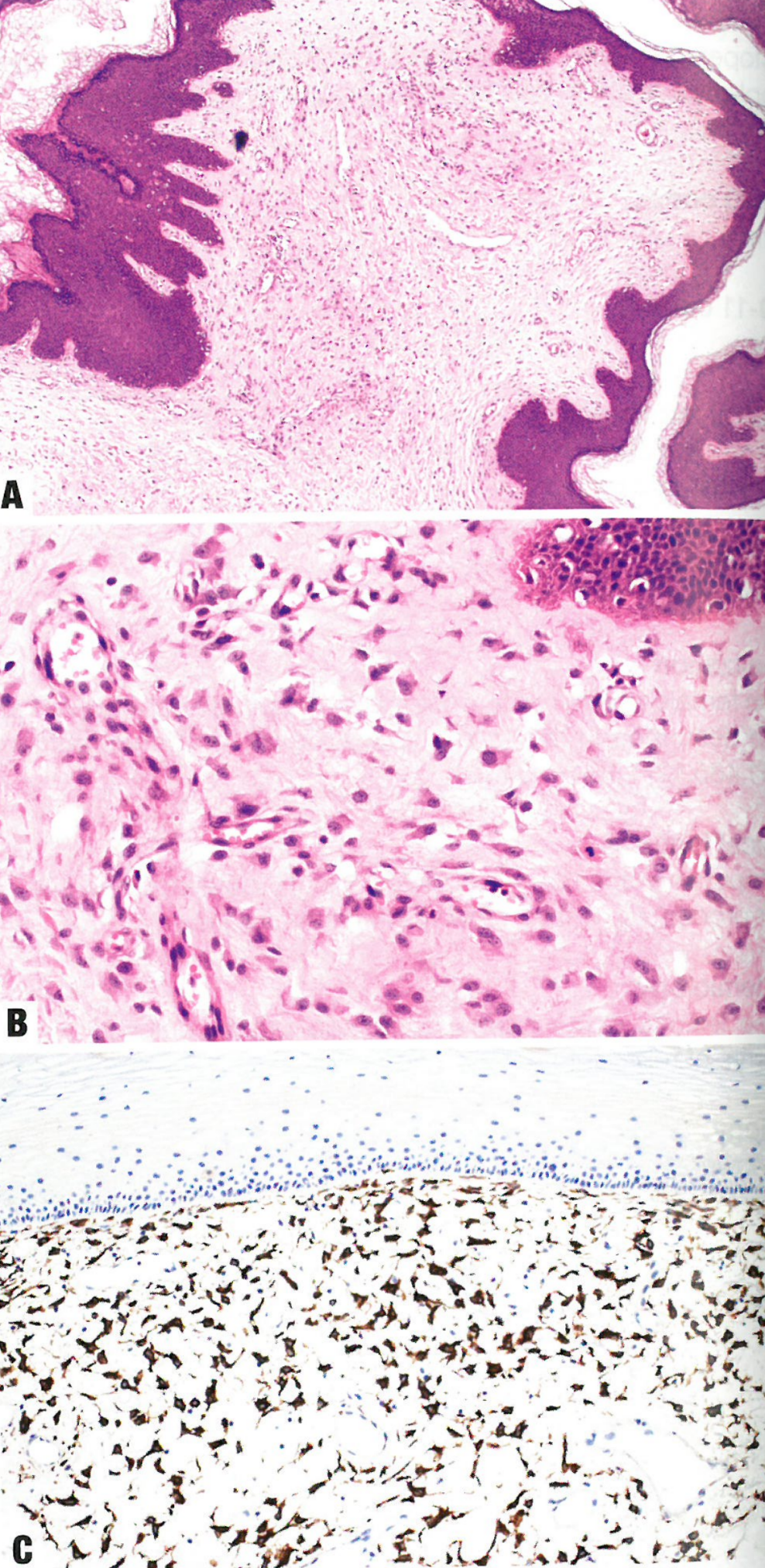 图13.05纤维上皮间质息肉。A 纤维上皮间质息肉是息肉样病变,具有不同程度的富细胞性间质、纤维血管轴心和被覆鳞状上皮。B间质细胞密度和核分裂象活性增加。C间质细胞呈desmin阳性。
图13.05纤维上皮间质息肉。A 纤维上皮间质息肉是息肉样病变,具有不同程度的富细胞性间质、纤维血管轴心和被覆鳞状上皮。B间质细胞密度和核分裂象活性增加。C间质细胞呈desmin阳性。
细胞学
无临床相关性
诊断分子病理学
无临床相关性
诊断标准
必要标准:息肉,具有可变的富细胞性间质、纤维血管轴心和被覆鳞状上皮;星形和多核间质细胞,通常位于间质-上皮交界处和血管周围。
分期
无临床相关性
预后和预测
病变是良性的,但可能局部复发,特别是如果切除不彻底或有持续的激素刺激。完全局部切除是首选的治疗方法。
03. 青春期前纤维瘤
定义
青春期前纤维瘤是一种良性间叶性肿瘤,可能是纤维母细胞分化,表现为外阴区梭形细胞呈边缘不清的浸润性增殖。大多数患者为青春期前女孩。
ICD-O编码
8810/0纤维瘤NOS
ICD-11编码
EE6Y&XH8E66皮肤和软组织的其他特指性纤维瘤性疾病&纤维瘤NOS
相关命名
不建议:儿童不对称性阴唇增大
亚型
无
部位
青春期前纤维瘤发生在外阴区域,表现为粘膜下或皮下病变。大阴唇是最常见的部位。
临床特征
外阴的青春期前纤维瘤表现为青春期前女孩外阴区域单侧无痛性肿块、肿胀或增大,表现为一侧阴唇不对称增大。病变生长缓慢,通常在几个月到三年内的时间段内增大。
流行病学
外阴的青春期前纤维瘤罕见,文献中可能包括儿童不对称性大阴唇增大和青春期前单侧大阴唇纤维增生的病例。大多数患者的年龄介于3-13岁之间。偶尔,成年患者(包括绝经后)可能出现与青春期前纤维瘤相同的病变。
病因
未知
发病机制
目前还没有已知的易感遗传或环境风险因素。据报道,6例接受细胞遗传学分析的病例核型正常。一些作者认为,病变是青春期前和青春期早期激素变化引起的不对称生理性增大。 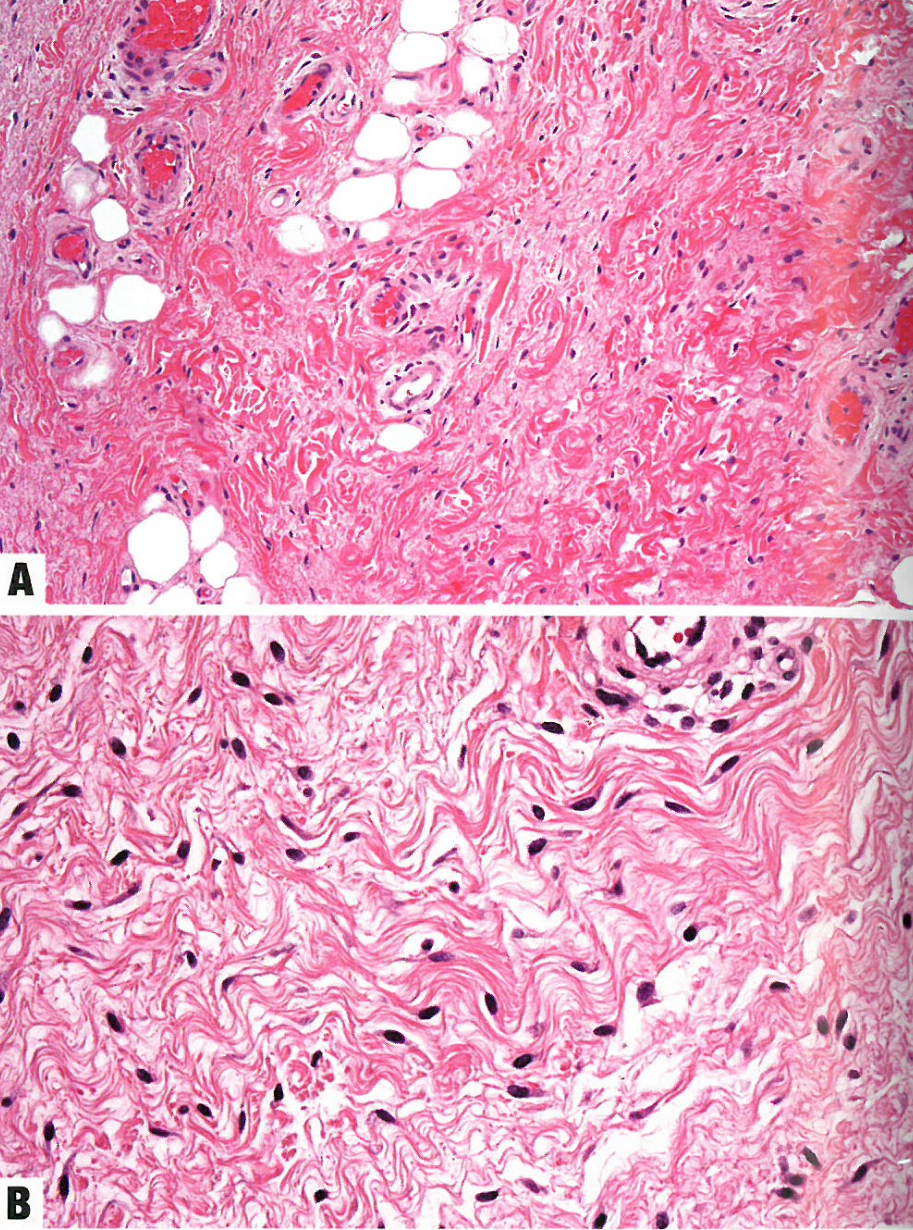 图13.06外阴的青春期前纤维瘤。A肿瘤呈少细胞和无结构模式,沿着先前存在的脂肪组织和血管呈浸润性生长。B形态温和的梭形细胞位于纤维间质内,有丰富的间质胶原纤维。
图13.06外阴的青春期前纤维瘤。A肿瘤呈少细胞和无结构模式,沿着先前存在的脂肪组织和血管呈浸润性生长。B形态温和的梭形细胞位于纤维间质内,有丰富的间质胶原纤维。
大体检查
肿瘤的大小范围为2.0至8.0cm,切面呈灰红色至褐色,质地柔软或橡胶状。间质可能粘液样。未见坏死和出血。
组织病理学
外阴的青春期前纤维瘤边缘不清,沿着先前存在的外阴结缔组织呈弥漫浸润性生长。病变主要累及粘膜下层和真皮,可能累及皮肤附属器。肿瘤表现为少细胞、无结构模式,含有形态温和的梭形细胞,位于多少不等的胶原、水肿或偶尔粘液样间质中。常见胶原纤维,从粗到细不等。形态一致的肿瘤细胞主要呈梭形,偶尔呈星状,核呈卵圆形,染色质细胞,核仁不明显。胞质界限不清,通常呈淡染的双染性。不存在核异型性、多形性和坏死。核分裂象活性低。免疫组化,CD34染色通常为多灶性到弥漫强阳性。S100、SMA和desmin均为阴性。ER和PR不同地报道为阴性、局灶性或阳性;都不是有用的诊断标记物。
细胞学
无临床相关性
诊断分子病理学
无临床相关性
诊断标准
必要标准:形态温和的梭形细胞,呈少细胞、无结节模式、弥漫浸润性生长;胶原、水肿或偶尔粘液样间质。
理想标准:CD34阳性。
分期
无临床相关性
预后和预测
外阴的青春期前纤维瘤在临床上是良性的,尽管至少30%的患者可能出现局部复发,特别是在不完全切除后。
未完待续......




















共0条评论