[导读] 作者:游乐园
1、病例资料
患者女性,66岁。患者1年半前于体检时行超声检查发现肝右叶低回声结节,大小约2.2x1.8cm,未予重视。2个月前再次体检时行超声检查发现肝占位增大至2.8x2.8cm,遂住院。患者自患病以来无肝区疼痛,无肝大或腹部肿块,无乏力、消瘦、食欲减退、黄疸、腹胀等全身症状。上腹部CT:肝表面光滑,各叶比例未见明显失调。平扫肝右叶前段可见结节样低密度灶,直径约26mm,增强动脉期明显均匀强化,延迟期呈等至稍低密度,余肝内见多发散在类圆形低密度无强化灶,肝内外门脉显影良好。行手术切除部分肝组织送检,显微镜下见大量巢团状、实性片状的上皮样细胞,胞浆淡染或嗜酸性,厚壁血管多见,局部见成熟脂肪细胞。免疫组化:HMB45、Melan-A、Vimentin、SMA阳性,Ki67(约5%+)。病理诊断:(部分切除肝)上皮样血管平滑肌脂肪瘤(AML)。
2、讨论
血管周上皮样细胞肿瘤(PEComa)是一组组织学及免疫组化均有特性的血管周上皮样细胞肿瘤家族,其中包括肾与肾外血管平滑肌脂肪瘤(AML)、淋巴管平滑肌瘤、肺及肺外透明细胞糖瘤、透明细胞肌黑色素细胞性肿瘤。AML是PEComa家族中最常见的类型之一,常累及肾脏,其次是肝脏,亦可见于其他部位,如心脏、纵隔、肺、小肠、四肢、上颚、阴道等。
组织起源:Ishak于1976年首次报道发生于肝脏的血管平滑肌脂肪瘤(HAML)。 HAML由血管、平滑肌细胞和成熟的脂肪组织按不同比例组成,该肿瘤的组织来源及发生机制至今仍存在争议,过去认为其是一种良性的间叶性错构瘤,近年来研究发现其为一种真性肿瘤。目前主要有以下几种观点:(1)来自于血管周上皮样细胞:血管周上皮样细胞是一种可向血管平滑肌细胞和血管内皮细胞分化的原始间叶细胞,但至今尚未发现对应的正常细胞或胚胎成分。曾有人描述此类肿瘤的主体细胞是一种围绕血管分布的类似上皮的细胞,包括血管平滑肌细胞和周细胞。周细胞具有多向分化潜能,能够转变成脂肪细胞、骨母细胞、吞噬细胞和平滑肌细胞。由于周细胞与血管平滑肌细胞具有显著的相似性,所以有学者认为周细胞是平滑肌细胞的特异性前体,是一种可向血管平滑肌和血管内皮细胞分化的原始间叶细胞。分子生物学研究显示其呈克隆性增生,血管、平滑肌成分为单克隆性,提示为肿瘤性生长,而脂肪成分为多克隆性,提示为化生性成分,提示该肿瘤细胞可能是一种具有多向分化潜能、可向血管平滑肌和脂肪细胞分化的原始间叶细胞。(2)来源于星形细胞:研究人员对人HAML、原始的鼠肝星形细胞和鼠星形细胞系进行基因表达分析,发现HAML和激活的星形细胞基因表达谱相同,提示HAML可向星形细胞分化。(3)与基因变异有关:有资料显示,约30%-40%的肾AML伴有结节性硬化病(TSC),HAML亦有5%-10%伴有TSC,在HAML的病例中检测出TSC1、TSC2和TSC3号染色体短臂杂合性缺失。恶性HAML可检测到P53基因5-9外显子发生突变。研究发现29例PEComa全部表达TFE3,其中4例出现基因重排,1例发生肺转移的子宫PEComa,出现TFE3基因扩增。因此,对于TFE3在PEComa中的作用值得进一步研究。
临床表现:HAML常发生于中青年女性,临床表现一般无特殊症状和体征,大多数为体检时发现肝占位,或偶然发现肿块,少数可有上腹部隐痛不适,个别病例瘤体积逐渐增大疑为恶性肿瘤。
影像学检查:通常情况下,由于HAML富含脂肪组织,在超声上主要表现为高回声结节或混合回声结节,边界清楚。超声造影时表现出一定特征性,即动脉期呈高增强,门脉期及延迟期呈现等或轻度高增强。CT平扫呈不均匀低密度灶,内见斑点状或片状更低密度区,边界清楚。增强扫描显示为动脉期明显强化,门脉期或延迟期呈中度或轻度强化。CT检查可见低密度占位,增强CT检查可见动脉期不均匀强化,门静脉期及延迟期呈低密度。MRI检查中多表现为T1W1低信号,T2W2高信号,T2W1脂肪抑制呈低信号或高低混杂信号。
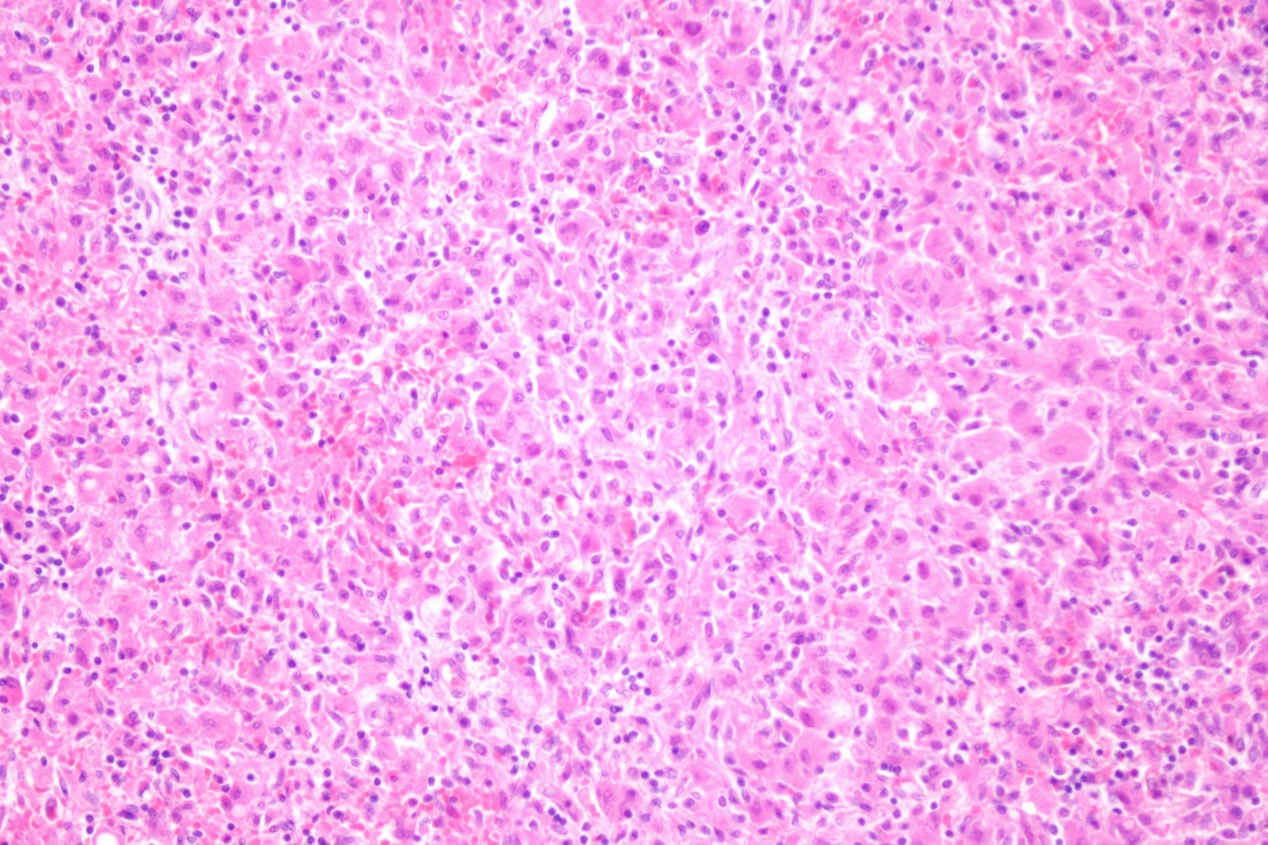
组织病理学:HAML肿瘤形态上由血管(通常为厚壁动脉、静脉血管或小血管样腔隙)、平滑肌细胞和成熟的脂肪组织等3种成分按不同比例组成,常见髓外造血。平滑肌细胞形态变异最大,是诊断的难点。平滑肌细胞按形态特点可分为上皮样、梭形及中间型。上皮样平滑肌细胞可表现为多种形态:(1)蜘蛛细胞型:胞质内可见大量空泡,有放射状细丝与细胞核黏附,形成所谓“蜘蛛细胞”,具有诊断意义。(2)透明细胞型:胞质透亮,核居中或偏位,需要与透明细胞癌鉴别。(3)嗜酸细胞型:胞质丰富、嗜酸性、颗粒状、无明显空泡。(4)多形细胞型:细胞核具有轻至中度异型,可见双核和多核,可见大的畸形核细胞散在,但无核分裂像。梭形细胞型瘤细胞的胞质及核沟成梭形,与一般平滑肌细胞相似。中间型平滑肌细胞形态则介于上皮样和梭形平滑肌细胞之间。
根据瘤组织成分的不同,HAML可分为:(1)经典型:血管、平滑肌、脂肪3种成分比例大致相等。(2)肌细胞为主型:有时细胞呈嗜酸性,并可形成小梁状结构。(3)脂肪细胞为主型:成熟的脂肪细胞占75%以上,偶见脂肪母细胞。(4)血管为主型:以小血管成分为主,血窦高度扩张,甚至有血湖形成,瘤组织往往含有铁血黄素沉着。免疫组化染色显示黑色素细胞和平滑肌细胞双向分化。不同程度表达黑色素细胞标记物HMB45、MelanA、PNL2、MiTF、MART-1及tyrosinase,其中HMB45阳性强度最高,MelanA及MART-1较弱且 局限,上皮样细胞较梭形细胞更易表达黑色素细胞标记物。表达平滑肌细胞标记物SMA及calponin,其中SMA表达最好,但多呈局灶性,瘤细胞越呈梭形及靠近血管,表达越强。约10%的PEComa呈TFE3核阳性。上皮样肿瘤细胞不表达上皮标记物、S-100和SOXll、CD31或CD34、HepPar-1和ARG-l。Ki-67增殖指数一般较低(<1%-15%),恶性EAML的Ki-67高表达。
良恶性鉴别:2005年Folpe等通过研究发生于软组织及女性生殖系统的PEComa病例,将PEComa分为良性、不确定恶性潜能和恶性3个等级。良性标准:肿瘤大小<5cm、非浸润性生长、无高级别核、细胞密度低、核分裂象≤1/50HPF、无坏死及血管侵犯。恶性潜能未定标准:仅有核多形性/瘤巨细胞,或仅肿瘤>5cm。恶性标准:出现2条或更多令人担忧的特点(>5cm,浸润性生长,高核级、细胞密度大,核分裂象>1个/50HPF,出现坏死及血管侵犯)。2009年Faraji等认为显著的细胞异型性和大片肿瘤性坏死与肿瘤进展相关。2010年Brimo等总结了肾上皮样血管平滑肌脂肪瘤进展的组织学因素:(1)肿瘤≥70%的上皮样细胞出现细胞异型性,(2)核分裂象>2个/10HPF,(3)非典型核分裂象,(4)坏死。2011年Nese等通过研究41例肾上皮样血管平滑肌脂肪瘤,提出影响疾病进展(复发、转移或直接致死)的5条形态学不良因素,分别为:(1)与结节硬化综合征有关或同时伴有血管平滑肌脂肪瘤,(2)坏死,(3)肿瘤大小>7cm,(4)肾外扩展和(或)肾静脉累及,(5)癌样生长模式。建立了以下恶性危险分层标准:当肿瘤存在<2条不良因素时被认为是低风险,15%的病例可能会疾病进展;当肿瘤存在2-3条不良因素时,被认为是中等风险,64%的病例会出现疾病的进展;当肿瘤存在4条或以上的不良因素,都会出现疾病进展。对于较大体积的肿瘤,强调应充分取材,以排除可能的危险指征。利用以上标准评定的3类肿瘤在追踪研究中证实了与其临床生物学有高度的吻合性。然而,对于经典型的AML,肿瘤可以在体内生长至巨大体积(>15cm),而临床生物学行为仍为良性。
鉴别诊断:(1)透明细胞型肝细胞癌:肿瘤细胞胞质呈透明,但细胞异型性较大,细胞排列呈梁索状或弥漫团片状,免疫组化表达上皮标记物及肝细胞标记物ARG-1、HepPar-1等,不表达黑色素标记物及平滑肌标记物有助于鉴别。(2)肝细胞腺瘤:细胞分化较好,无明显核分裂像,无正常肝小叶结构,瘤组织内门管区和胆管缺如,常见散在分布、管腔扩张的薄壁小静脉或小动脉分支。免疫组化无特殊的诊断标志物,免疫组化HMB45阴性可辅助诊断。(3)脂肪性肿瘤:HAML的脂肪成分比例变化很大(10%-90%),因而需与肝脂肪瘤或高分化脂肪肉瘤鉴别。HAML瘤组织多由分化成熟的脂肪细胞组成,细胞大小较一致,核无异型,通常可以找到上皮样平滑肌细胞。(4)原发或继发性上皮样胃肠道间质瘤:肿瘤细胞表达CDl17、DOG-1和CD34,不表达黑色素标记物,支持胃肠道间质瘤。(5)原发或继发性恶性黑色素细胞瘤:核分裂象多见,表达S100,不表达平滑肌标记物有助于鉴别。(6)肝上皮样血管肉瘤:表达血管内皮标记物CD31、CD34、FLI-1及ERG,不表达黑色素标记物,支持上皮样血管肉瘤。(7)平滑肌肿瘤:当HAML上皮样平滑肌细胞丰富时,需要与平滑肌瘤和高分化平滑肌肉瘤鉴别,肿瘤细胞表达平滑肌标记物,不表达黑色素标记物。
处理原则:如果影像学明确是HAML时,行一年一次或两年一次的随访。当出现症状或侵袭性/浸润性生长时行手术治疗。影像学诊断不明确时行活检,当病理诊断明确且没有非典型的上皮样细胞或高增殖活性,行一年一次或两年一次的随诊,当出现症状或侵袭性/浸润性生长时行手术治疗。如果活检诊断不明确,或者出现不典型上皮样细胞或高增殖活性时,行手术切除。
病例图片:
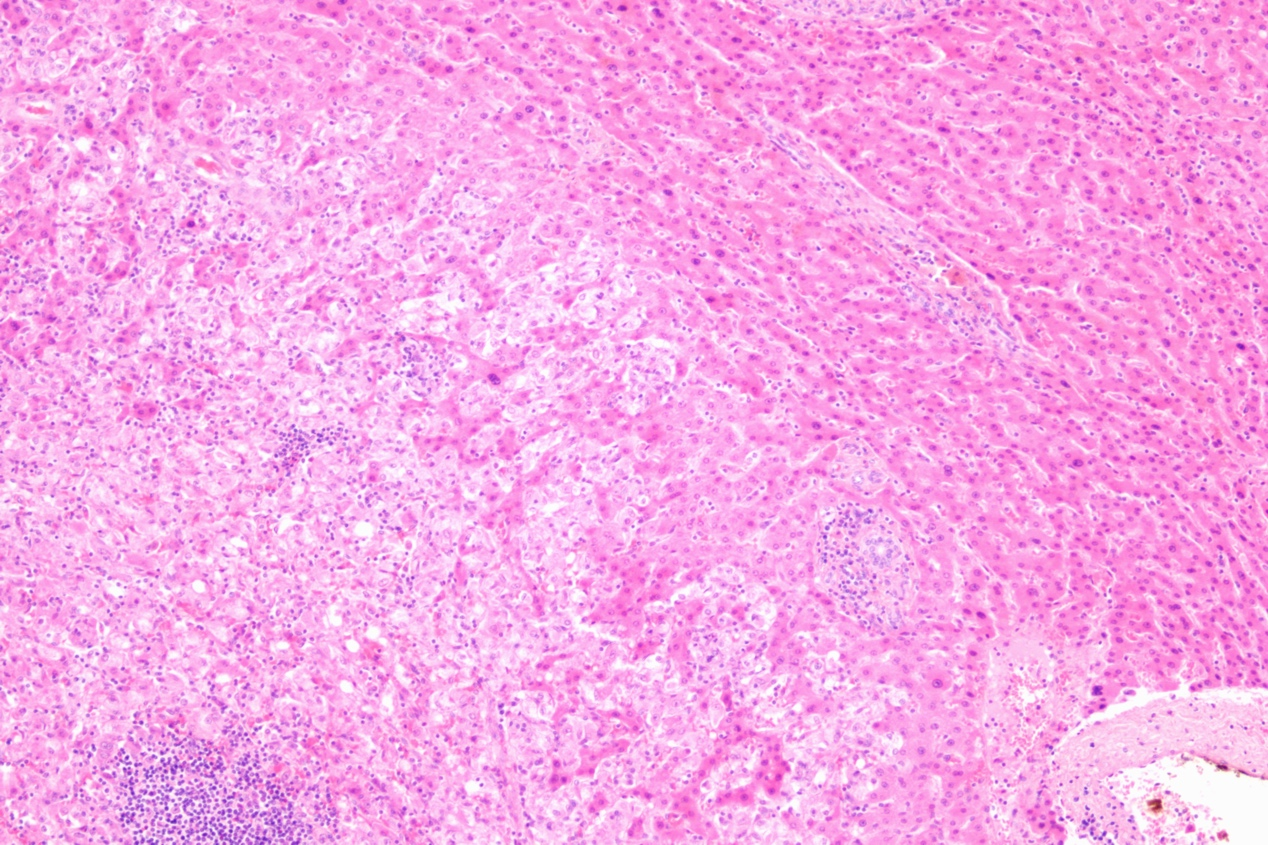
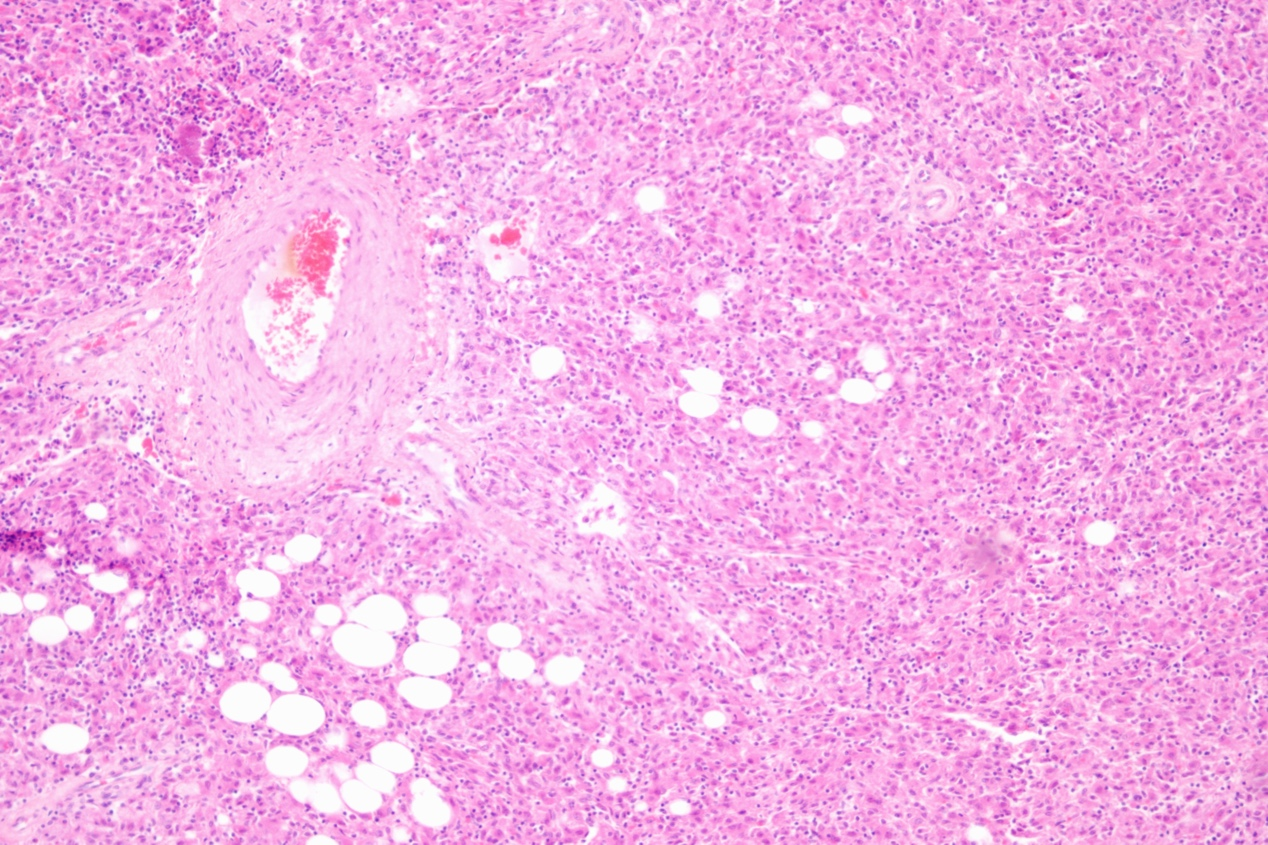
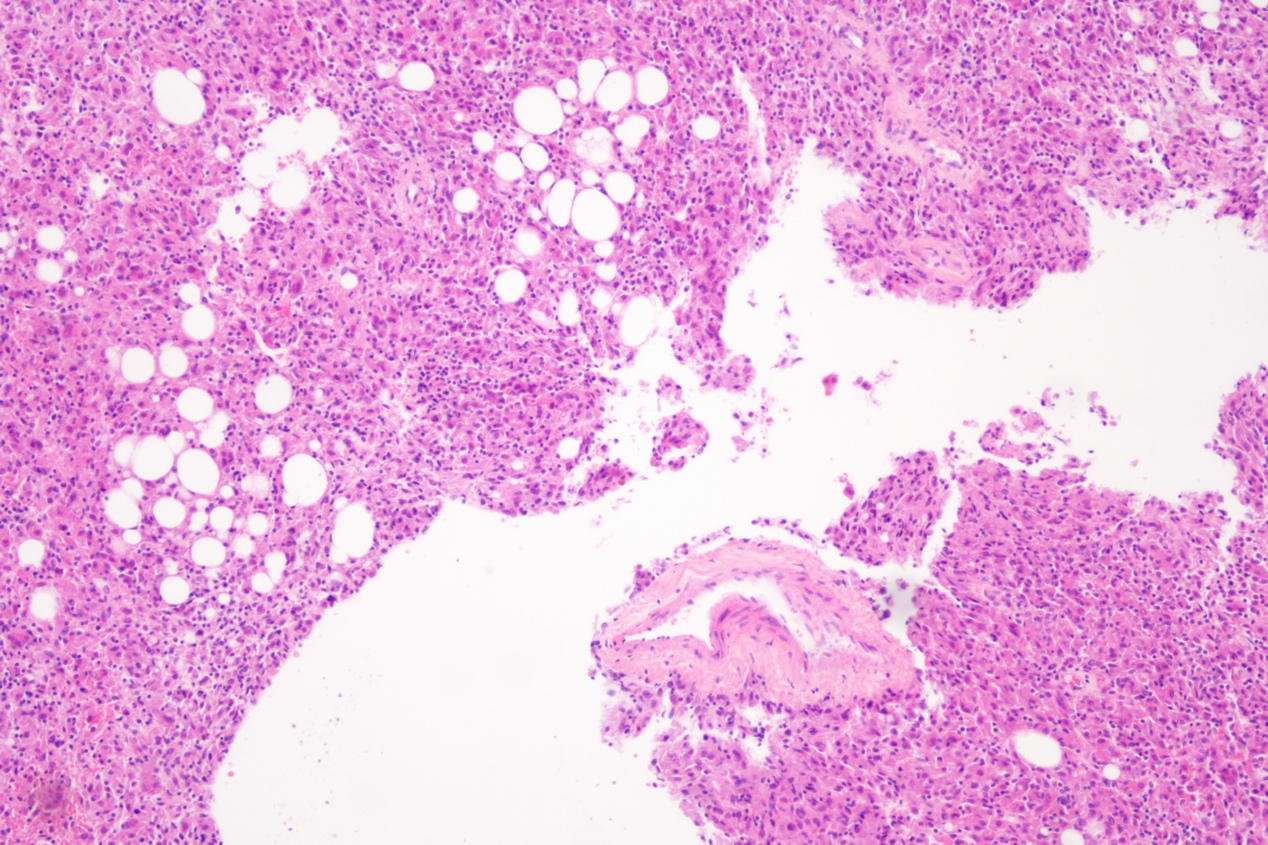

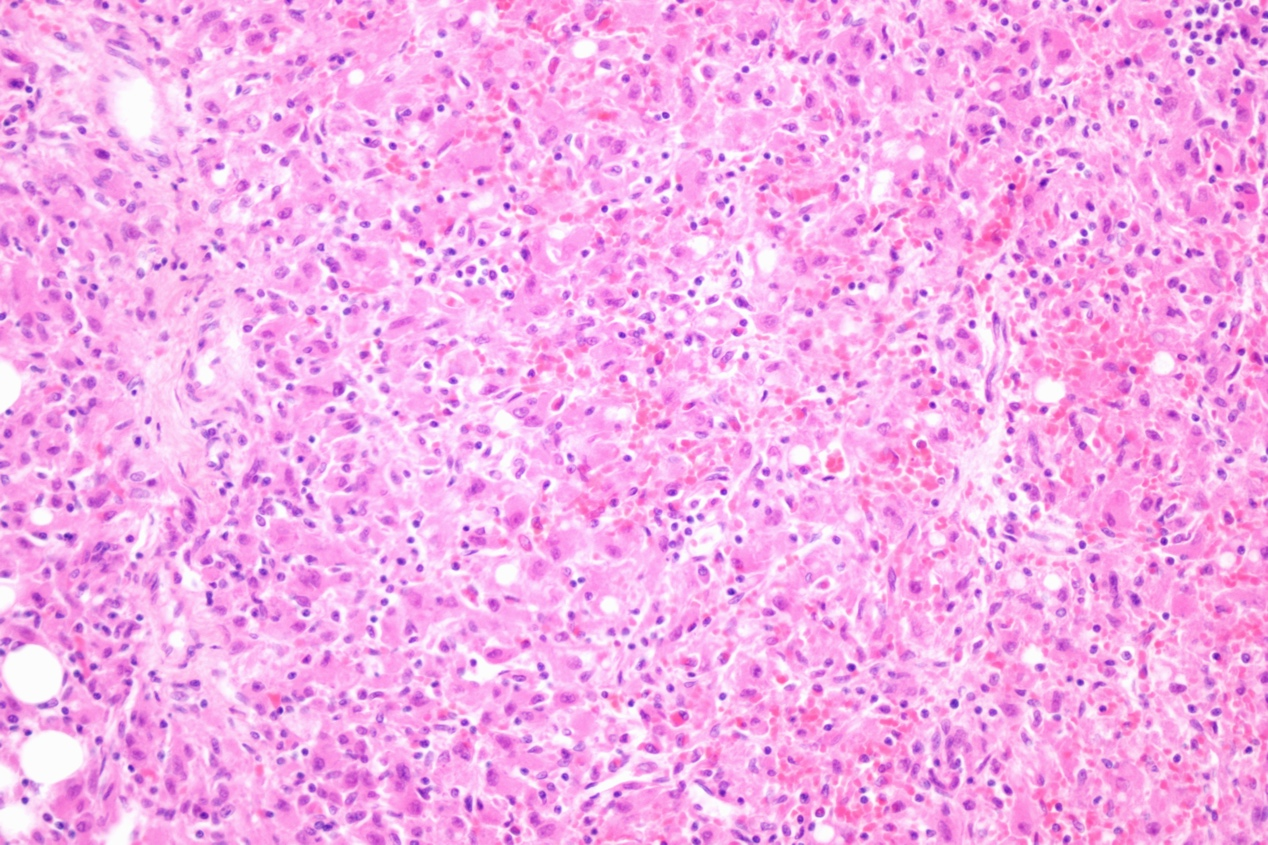
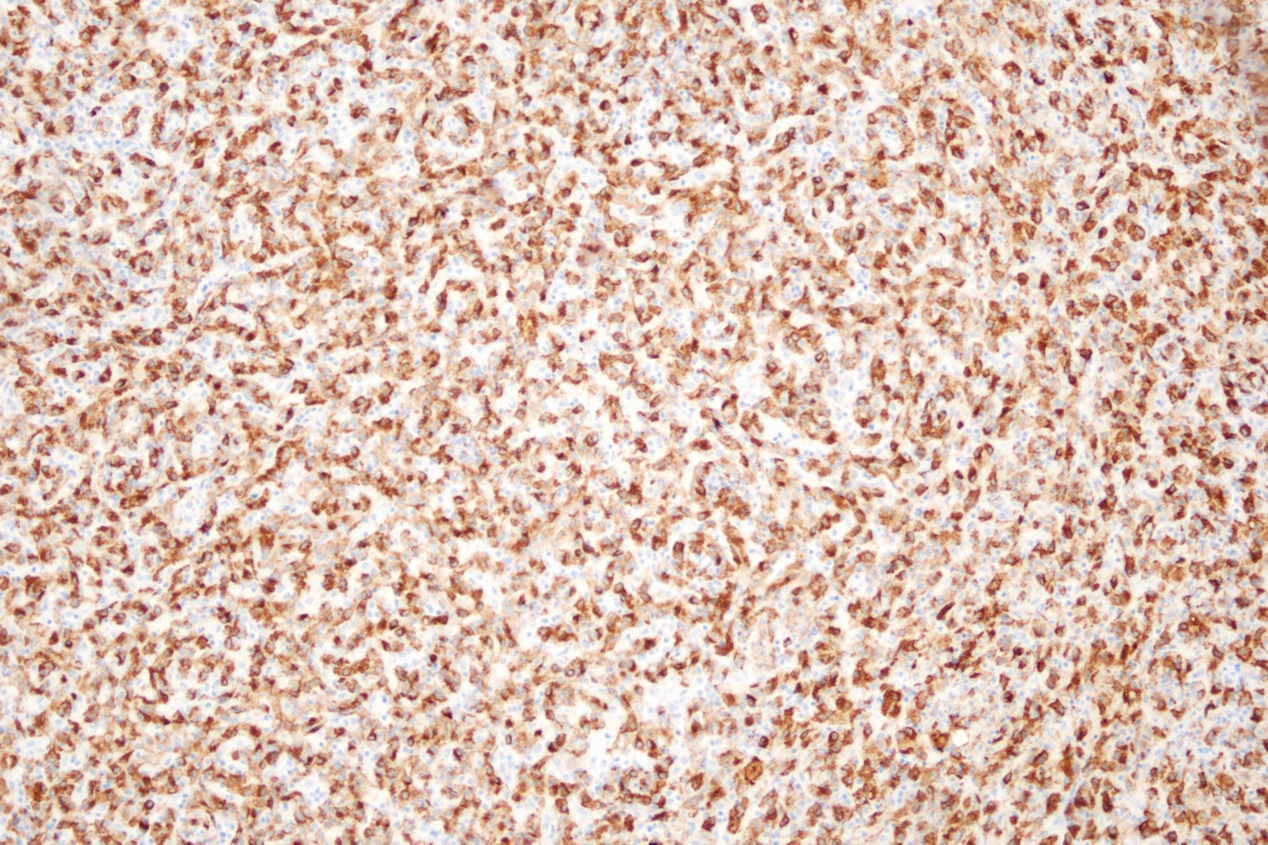 免疫组化:HMB45(+)
免疫组化:HMB45(+)
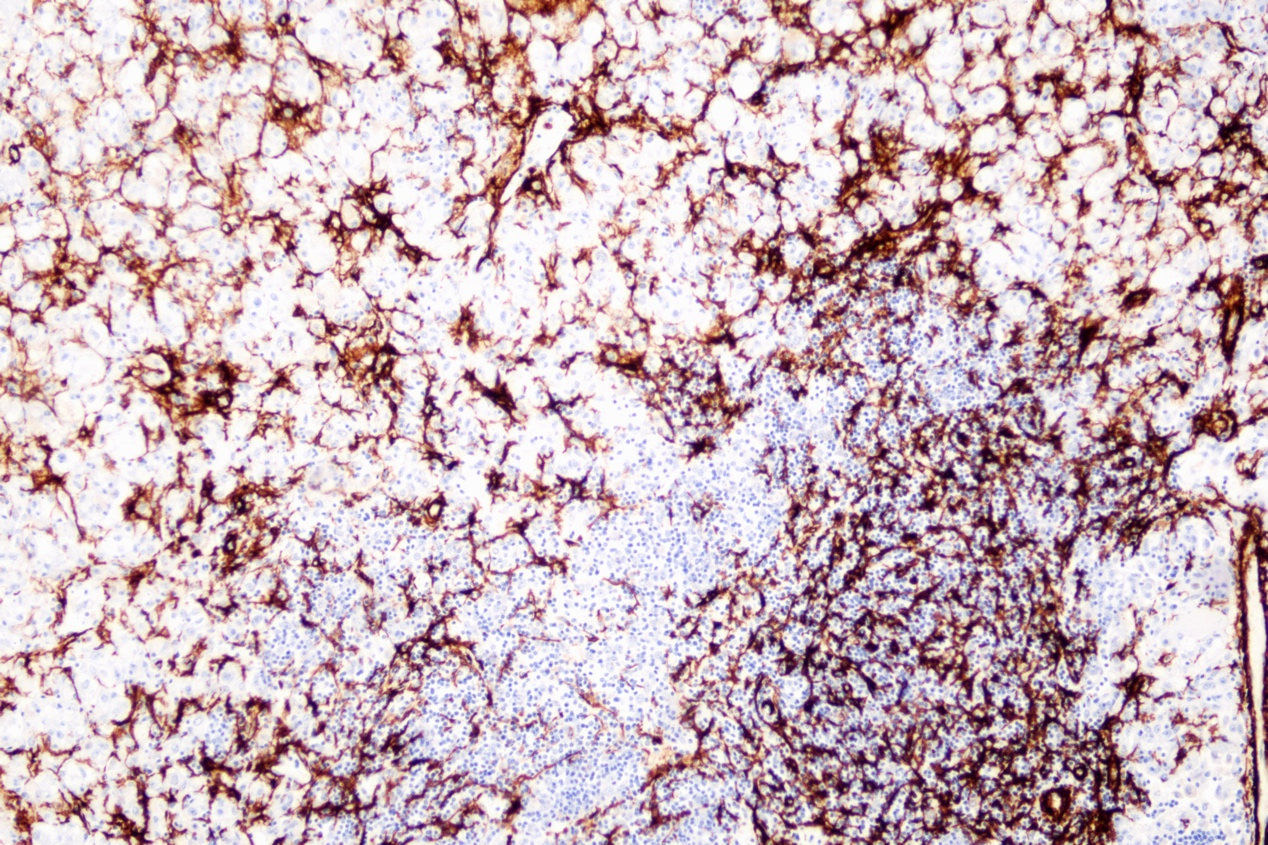 免疫组化:SMA(+)
免疫组化:SMA(+)
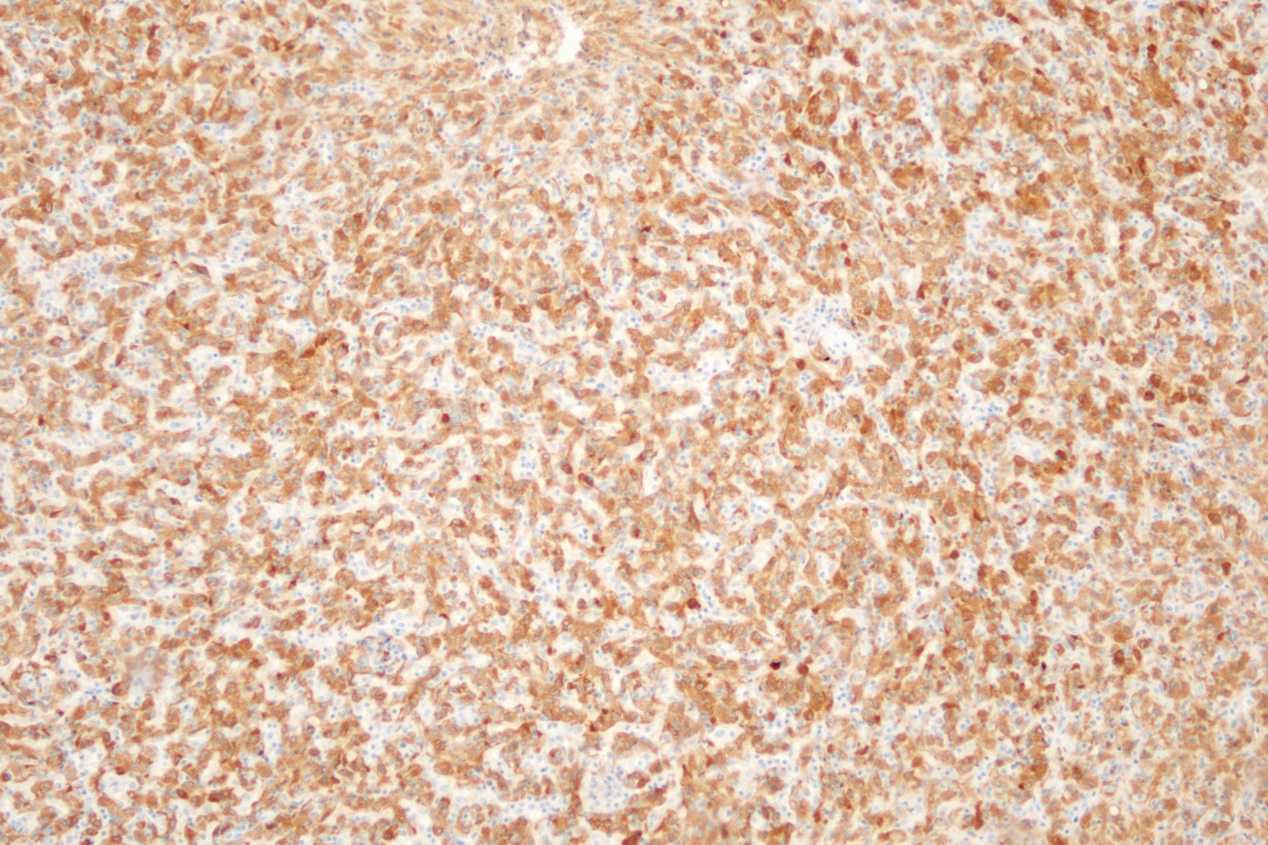 免疫组化:MelanA(+)
免疫组化:MelanA(+)
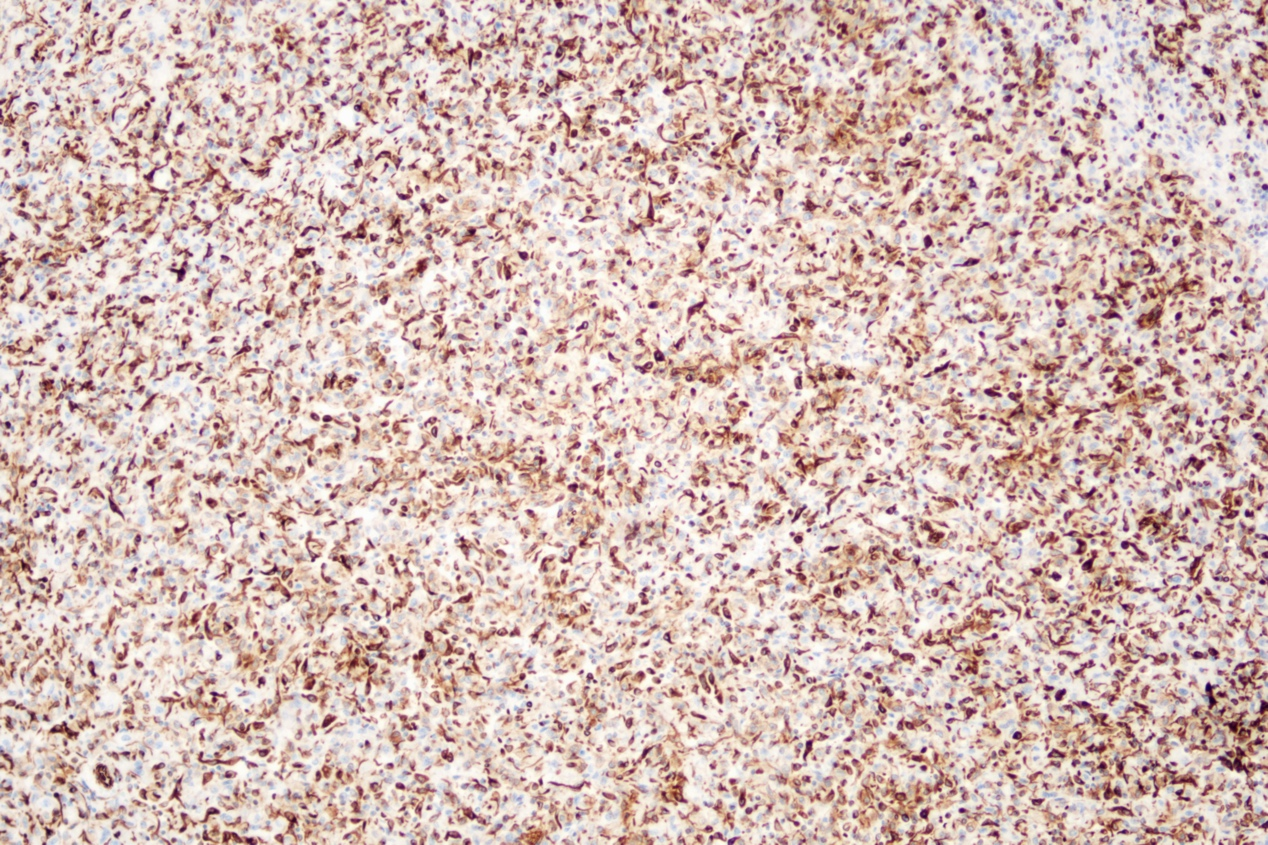 免疫组化:Vimentin(+)
免疫组化:Vimentin(+)
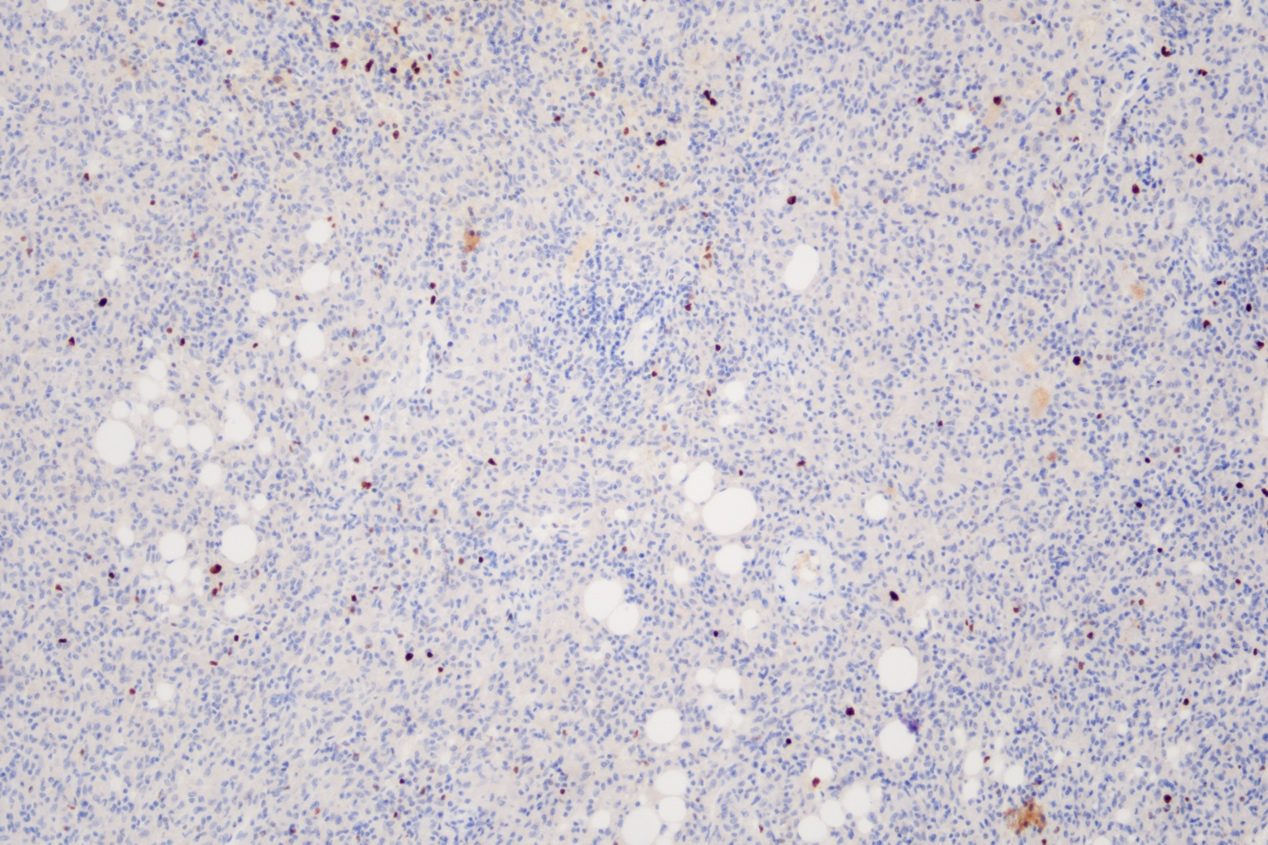 免疫组化:Ki-67(约5%+)
免疫组化:Ki-67(约5%+)
























共0条评论