[导读] 编译整理:强子
EWSR1::WT1融合病种简述
最初有文献报道了一组具有特殊表现的促纤维增生性小圆细胞肿瘤:该组肿瘤发生于青少年和年轻成人男性腹腔内,具有被视为相对特异的基因重排(即EWSR1与WT1基因重排)。该组肿瘤形态学方面,表现为大小不一的浸润性细胞巢,瘤细胞主要为形态均一的圆形细胞,伴丰富的致密促纤维增生性间质。免疫组化方面,该肿瘤一般有CK、EMA、desmin、神经内分泌标记(如NSE)的共表达。促纤维增生性小圆细胞肿瘤的生存一般较差,且化疗效果一般较差,大部分患者会死于该肿瘤。
已有报道称EWSR1::WT1融合可见于形态学和免疫组化表现特殊的肿瘤中,有时可能生存预后更好。比如文献中已有伴EWSR1::WT1融合、形态学及免疫组化不符合促纤维增生性小圆细胞肿瘤的病例预后相对好的报道。这些肿瘤形态学均主要为梭形,并无促纤维增生性间质,免疫组化弥漫阳性表达desmin,CK表达不一或局限,阴性指标有h-caldesmon、S100、ERG、myogenin、S100。还有研究报道了3例伴EWSR1::WT1融合但并无促纤维增生性小圆细胞肿瘤典型形态的病例。其中2例发生于盆腹腔,1例发生于腋窝软组织。这三例都没有促纤维增生性间质,且为实性及囊性结构,伴纤维间隔。免疫组化方面,该组肿瘤表达SMA、desmin,程度不等的表达AE1/AE3,EMA罕见阳性。2例做了C末端WT1免疫组化检测,结果为阳性。尽管有人质疑这些少见肿瘤到底是不是促纤维增生性小圆细胞肿瘤谱系的一部分,但本文原作者认为它们并不是促纤维增生性小圆细胞肿瘤。
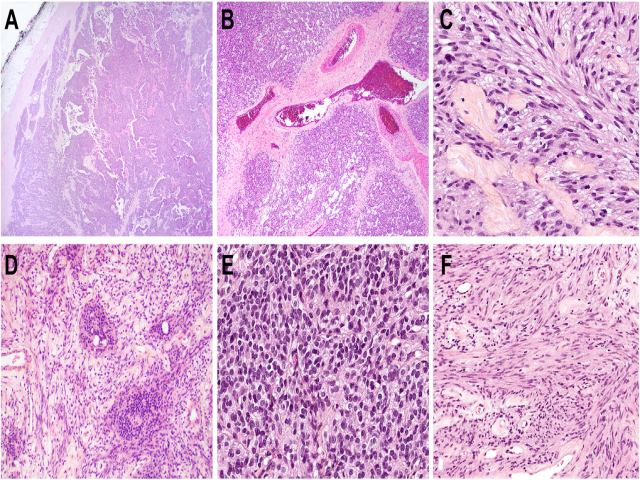
图16.EWSR1::WT1融合病种实例。(A)该肿瘤境界相对清楚,伴纤维性假包膜,呈巢状至弥漫性生长;(B、C)有些病例的肿瘤内有纤维性间隔,有时伴扩张的血管;还有些病例呈双相型表现(D),即上皮样细胞形成的富于细胞区(E)、和梭形细胞形成的细胞稀疏区(F)混杂。所有病例的级别都要低于经典型促纤维增生性小圆细胞肿瘤。
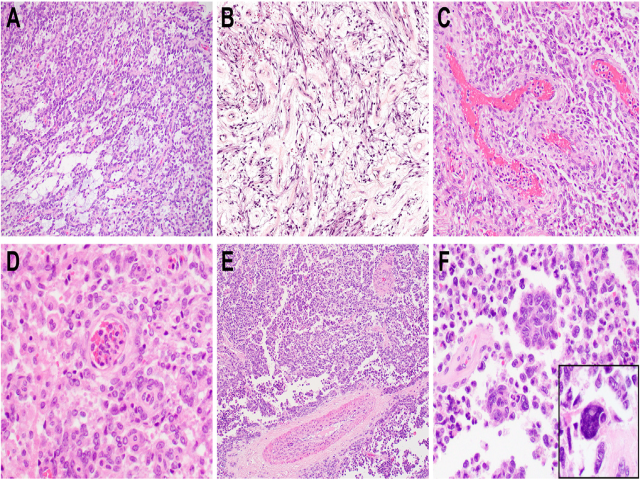
图17.EWSR1::WT1融合病种其他形态学特征。每个病例都会有不同的形态学变化,比如局灶黏液样变(A)、间质水肿改变(B),且黏液样变有时会导致假腺管状结构。所有病例都有血管显著区域(C),且瘤细胞常呈血管周围丰富、伴肾小球样或黏液样表现(D)。细胞失黏附会导致形成不规则腔隙(E、F),部分病例伴有散在的巨细胞(F)。
ETV6::NTRK3融合病种简述
1998年,有人在一例先天性(或婴儿型)纤维肉瘤中首次报道了t(12;15)易位及ETV6::NTRK3基因融合。同年又发现先天性中胚叶肾瘤具有相同的基因融合,这说明该肿瘤与婴儿型纤维肉瘤间存在分子相关性。此外,也有具有这一典型融合的炎性肌纤维母细胞肿瘤、胃肠道间质瘤、梭形细胞肿瘤的罕见病例报道。不过,目前发现这一分子事件似乎并不局限于间质性肿瘤,比如最近发现急性髓系白血病、乳腺分泌性癌、甲状腺癌、神经胶质瘤、涎腺分泌性癌中这一融合可能也是其分子驱动事件。
YAP1::MAML2融合病种简述
以往曾被称为Dabska瘤的乳头状淋巴管内血管内皮瘤可能属于网状血管内皮瘤谱系,且这两种病变的特征都是存在“靴钉样”内皮细胞。网状血管内皮瘤谱系中的病变有些会具有YAP1::MAML2基因重排。
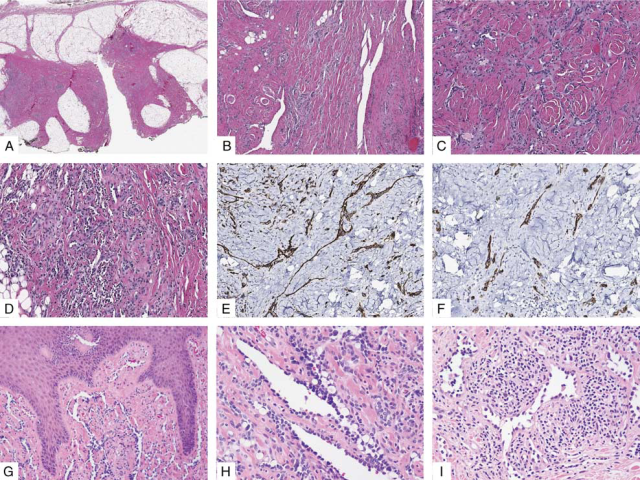
图18.YAP1::MAML2基因重排的网状血管内皮瘤形态特征。(A-F)本例发生于10岁男孩膝部的表浅软组织。(A)低倍镜下,肿瘤呈模糊的结节状,且呈浸润性生长,位于皮下,伴显著纤维化;中倍镜下,背景间质致密硬化,伴拉长、鹿角状血管(B)或较短的网状血管结构(C),衬覆胞质稀少、体积小的内皮细胞;(D)伴显著淋巴细胞浸润,甚至可能会掩盖血管的增生。免疫组化方面,瘤细胞一般共表达CD31(E)和D2-40(F)。(G-H)本例为发生于皮肤的病例,结构为拉长的血管腔,在真皮表浅处浸润,衬覆靴钉状内皮细胞。(I)另一例成人(50岁女性,膝部)皮肤的病例,形态学为成角的扩张管腔,且有凸起的内皮细胞,部分脱落且类似微乳头结构;间质伴大量淋巴细胞浸润。
此外,本文原作者及其他作者还曾在所谓坏死亚型的黏液炎性成纤维肉瘤中见过相同的基因融合。文献中报道过具有YAP1::MAML2融合的其他间叶性及非间叶性肿瘤还有:梭形细胞型横纹肌肉瘤,胸腺瘤,汗孔瘤,室管膜瘤。
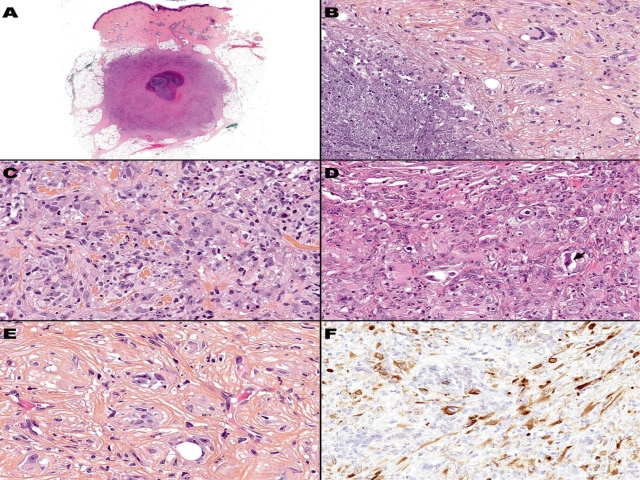
图19.坏死亚型的黏液炎性成纤维肉瘤形态学及免疫组化特征。(A)本例低倍镜下境界邢队清楚,为真皮内的细胞稀疏结节,伴中央坏死;(B)本例坏死区域高倍镜,瘤细胞上皮样,局灶伴血管壁破坏(leukocytoclasia,图中左侧),且伴Langerhans型多核巨细胞(图中右侧);(C、D)上述两例相对应的高倍,上皮样细胞呈片状分布,胞质丰富、嗜酸性,细胞核空泡状、怪异表现,可见大核仁;同时有大量中性粒细胞及干尸样瘤细胞(箭头所示);(E)粗大胶原束形成的硬化区域,围绕在肿瘤细胞巢周边;存在极为局灶的间质黏液样变(细胞周围的蓝染基质),这一表现极为罕见。(F)免疫组化广谱CK(AE1/AE3)阳性。
MDM2扩增病种简述
MDM2扩增曾被视为脂肪源性肿瘤的标志性特点,具体如非典型脂肪瘤样肿瘤/高分化脂肪肉瘤、去分化脂肪肉瘤;但现在已明确MDM2扩增不仅局限于脂肪肉瘤。就骨原发肿瘤来说,低级别的骨肉瘤、尤其骨旁骨肉瘤和低级别中央型骨肉瘤的特征也是MDM2扩增。与非典型脂肪瘤样肿瘤/高分化脂肪肉瘤相似,这两种骨肉瘤也可能貌似温和表现,在标本有限的活检组织、和/或无影像学信息的情况下,可能诊断难度较大。此外,这两种骨肉瘤的预后都较好,且化疗仅用于伴去分化的情况下,因此准确诊断出来还是有重要意义的。
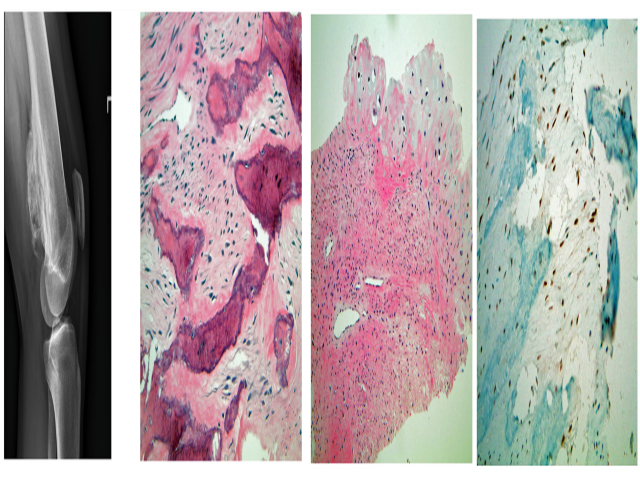
图20.骨旁骨肉瘤。X线平片中,表现为程度不等的硬化,本例位于股骨远端后方的表面,是该肿瘤的典型好发部位;典型形态学为位于致密纤维母细胞性间质内的编织骨骨小梁,一般仅有轻度非典型;被覆于肿瘤上方的软骨帽,有时会很明显,这也是一个有助于诊断的线索。免疫组化MDM2,肿瘤细胞的细胞核阳性表达。
心脏或躯体/肺部血管来源的动脉内膜(或内膜样)肉瘤也存在MDM2的扩增,但形态学为低分化高级别肉瘤,常无明显分化谱系表现,预后差。文献中还报道过很多其他肉瘤可呢个会有MDM2扩增、或MDM2癌蛋白过表达,具体如:黏液纤维肉瘤、横纹肌肉瘤、滤泡树突细胞肉瘤、子宫内膜间质肉瘤、平滑肌肉瘤、恶性外周神经鞘瘤等。上述病种有些是伴MDM2扩增的已知类型肉瘤、还是去分化的脂肪肉瘤,这一点还不清楚。关键是要明白,与MDM2扩增为前述类型脂肪肉瘤、低级别骨肉瘤、动脉内膜肉瘤遗传学驱动事件不同,MDM2扩增在其他肉瘤和癌中可能仅仅是个过客型事件(passenger event)。
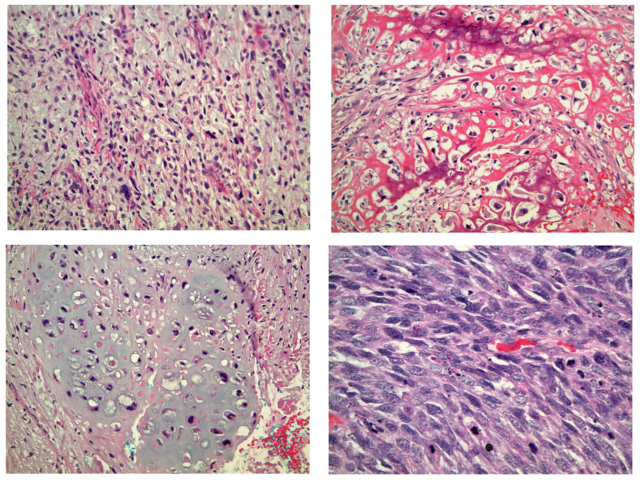
图21.动脉内膜肉瘤伴异源性分化,具体包括(左上)类似黏液纤维肉瘤的黏液样区域、(右上)骨肉瘤区域;(左下)软骨肉瘤区域;(右下)高级别梭形细胞区域。
——全文完——
往期回顾:
遗传学特征相同但形态学和免疫组化不同的某些骨和软组织肿瘤(一)
遗传学特征相同但形态学和免疫组化不同的某些骨和软组织肿瘤(二)



















共0条评论