[导读] 编译整理:强子
骨和软组织肿瘤具有高度异质性,病理诊断中主要是根据其分化谱系进行分类。不过,由于某些病种相对罕见、且组织形态学特征或临床表现方面存在重叠,因此有时候诊断较为困难。毫无疑问,分子病理的进展对该组肿瘤的诊断帮助极大,甚至有了针对某些遗传学改变的免疫组化替代性标记。
不过,随诊临床应用经验的增加,目前发现同一基因融合可能会出现于不止一种的不同表型和生物学行为瘤种中,甚至有时候临床行为完全不同的肿瘤却有相同的遗传学改变。有鉴于此,美国病理专家Dashti等人在《Hum Pathol》杂志发表文章,介绍了具有相同遗传学特征、但形态学和免疫组化有所不同的某些骨和软组织肿瘤。为帮助大家更好的了解相关知识点并应用于临床实践,我们将该文要点编译介绍如下。
概述
Ewing肉瘤是第一个完全阐明具有基因易位的肉瘤,是1983年通过核型分析发现的。不过,虽然经典的核型分析可以识别易位、缺失及扩增,但也存在某些缺陷,比如需要短期的细胞培养及中期细胞收集。此外,核型分析无法证实很多骨和软组织肿瘤中的分子驱动事件。
其实,查见特异性的肿瘤基因扩增、肿瘤抑制基因缺失、以及最重要的相关易位所致的基因融合,会加强我们对相关肿瘤的了解,并有望找出更具靶向性且更加容易的治疗检测方案,具体方法比如荧光原位杂交。测序基础上的检测方案以及聚类甲基化图谱分析(clustering methylation profiling analysis)则可以对基因改变更为复杂、肿瘤突变负荷大的肿瘤进行检测。
总之,相关技术有助于确定某些尚未完全明确的新型病种。从实际工作的角度来说,免疫组化替代性标记也已经可以检出某些特异性分子改变,如SSX、STAT6等。这些都促进了我们对具有特殊分子改变的骨和软组织肿瘤的进一步认识。
不过,随着分子检测的应用及进展,目前我们越来越认识到很多看似特异性的遗传学事件一旦被视为特征性表现,似乎就并不那么特异了。实际也已有诸多实例表明相同的基因融合可能是某些完全为良性或低级别病种的致癌驱动,这样的肿瘤可能术后无需进一步治疗;同时相同的基因融合也是某些明确为高级别恶性肿瘤的致癌驱动,这样的肿瘤则转移风险较高,术后还需放疗或化疗。具有特殊分子事件的某些骨和软组织肿瘤具体列举如下:
EWSR1::CREB(ATF1、CREB1)融合:透明细胞肉瘤,胃肠道恶性神经外胚层肿瘤,血管瘤样纤维组织细胞瘤,黏液样间充质颅内肿瘤/肉瘤,肺原发黏液性肿瘤;还可见于:玻璃样变透明细胞癌,恶性间皮瘤,炎性及巢状睾丸性索肿瘤。
EWSR1/FUS::NFATC1/2融合:未分化圆细胞/梭形细胞肉瘤,单纯性骨囊肿,血管肿瘤。
EWSR1::WT1融合:促纤维组织增生性小圆细胞肉瘤,伴相同融合、但形态学不同的一组女性生殖道及非生殖道肿瘤。
ETV6::NTRK3融合:婴儿型纤维肉瘤,先天性中胚叶肾瘤,急性髓系白血病,乳腺分泌性癌,涎腺分泌性癌,神经胶质瘤。
YAP1::MAML2融合:网状血管内皮瘤,复合性(composite)血管内皮瘤,黏液炎性成纤维细胞肉瘤的坏死性亚型,梭形细胞型横纹肌肉瘤;还可见于:胸腺瘤,汗孔瘤,室管膜瘤。
EWSR1/FUS::CREB3L1/CREB3L2融合:低级别纤维黏液肉瘤,硬化性上皮样纤维肉瘤。
MDM2扩增:非典型脂肪瘤样肿瘤/高分化脂肪肉瘤,去分化脂肪肉瘤,骨旁骨肉瘤,低级别中央型(髓内)骨肉瘤,动脉内膜肉瘤。
总之,虽然分子检测是间叶性肿瘤诊断中的重要组成部分,但不结合临床及形态学特征而仅从分子检测结果来做出判断,可能会存在诸多风险。
EWSR1/FUS::NFATC1/2融合病种简述
圆细胞/梭形细胞肉瘤
伴EWSR1/FUS::非ETS融合的圆细胞/梭形细胞肉瘤是最近才得以认识的骨和软组织未分化肉瘤。2009年的最初报道中,是将其视为Ewing肉瘤亚型的,目前已明确这类肉瘤是单独的类型,且DNA甲基化谱系研究也支持这一观点。
与Ewing肉瘤相似,NFATC2融合的肉瘤主要发生于骨,具有破坏性及渗透性。其形态学特征为单一表现的圆形/梭形原始细胞,细胞形态具有非典型,排列呈条索状、小巢状、梁状,常伴黏液样或玻璃样变的黏液样间质。个别情况下,会有实性皮状生长;罕见情况下会有显著的细胞核非典型。免疫组化方面,约50%的病例弥漫表达CD99,有时会表达NKX2.2和PAX7。分子层面上,EWSR1::NFATC2融合肉瘤会有融合产物的扩增,而FUS::NFATC2融合肉瘤则没有证实扩增。转录分析表明EWSR1::NFATC2融合肉瘤和FUS::NFATC2融合肉瘤是不同的病种。有趣的是,按照本文原作者所述,文献中还没有NFATC1重排肉瘤的报道。
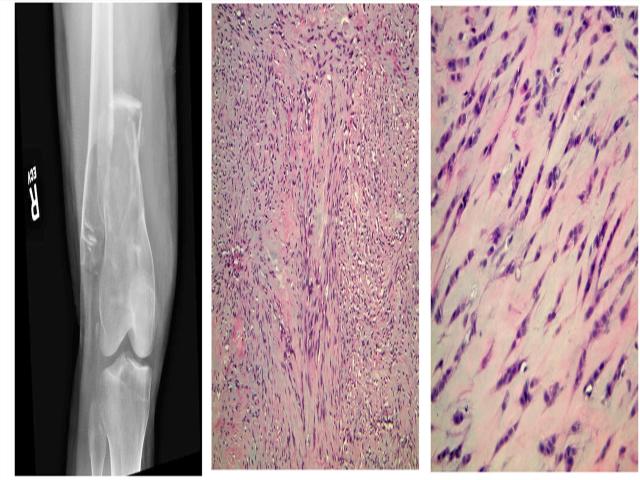
图1.FUS::NFATC2融合肉瘤。(A)X线评判表现为股骨远端程度不一的溶骨性及浸润性病变,伴骨折;(B)形态学为梭形细胞呈相互交织的束状,背景为黏液样间质;(C)高倍镜下,瘤细胞呈条索状表现。
该组肿瘤预后不一,但对新辅助化疗有效,不过和经典型Ewing肉瘤相似,预后一般较差。
单纯性(单房或孤立性)骨囊肿
与NFATC2重排的原始肉瘤形态形成鲜明对比,很大一部分单纯性骨囊肿也具有类似的遗传学融合。单纯性骨囊肿一般发生于骨不成熟患者,年龄多小于10岁,在长骨形成影像学上透光、非膨胀性囊性病变。由于病变为囊性、且内有液体,因此活检所得标本可能很少,且可能因此而导致诊断困难。
形态学方面,单房囊腔内并无真正上皮被覆,具体为薄层纤维性至纤维骨性组织,且有特征性的无定型牙骨质样至纤维素样物质。细胞更为丰富的区域可能会类似动脉瘤样骨囊肿,这种情况在病变中总是只占少数。
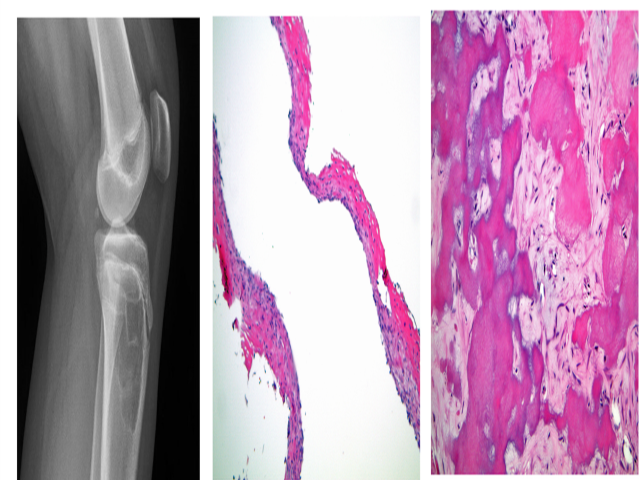
图2.单纯性骨囊肿。(左)X线平片中,表现为胫骨上段的界清、溶骨性病变,周边伴一圈硬化;且有典型的骨片陷落征(fallen fragment sign);(中)组织学上,单房囊壁厚薄不一,常为薄层的形态温和的纤维母细胞性梭形细胞,伴纤维素及类骨质;(右)其他较厚区域一般为典型的纤维素性-骨样组织形成的“牙骨质样”区域。
单纯性骨囊肿的治疗方面,包括刮除、减压、类固醇激素注射,但局部复发率15-20%,且似乎与治疗无关。需要注意的是,颌骨骨囊肿中尚未见NFATC2融合的报道。
血管肿瘤
具有EWSR1/FUS::NFATC1/2融合的血管肿瘤似乎有两种类型:一种是无任何细胞学异型性,符合良性血管病变,也就是血管瘤和血管畸形的情况;另一种是伴上皮样特征、形态表现不一、有细胞学非典型的情况。
有文献报道了14例伴NFATC1/2重排的血管性肿瘤,其中包括独特配体FABP4的情况。该组肿瘤患者男女性别比相近,病变部位主要发生于骨,个别位于软组织。尽管影像学上有侵袭性表现,但临床行为惰性。形态学方面,具体表现不一,为衬覆靴钉状内皮细胞的完好管腔、纤维性及出血性间质的混杂,实性区有较为显著的非典型表现。该组肿瘤表现独特,并不符合目前血管肿瘤分类中的任何类型。
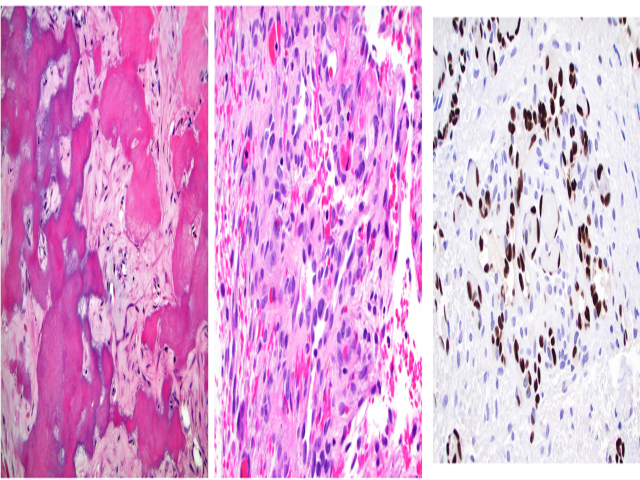
图3.伴FUS::NFATC2重排的上皮样血管性肿瘤。(左、中)上皮样内皮细胞,伴轻度非典型,背景为出血性及纤维性间质;(右)免疫组化ERG,内皮细胞的细胞核阳性着色。
——未完待续——
点此下载原文献
参考文献
[1]Dashti NK, Schukow CP, Kilpatrick SE. Back to the future! Selected bone and soft tissue neoplasms with shared genetic alterations but differing morphological and immunohistochemical phenotypes. Hum Pathol. 2024;147:129-138.
doi:10.1016/j.humpath.2024.03.005
















共0条评论