[导读] 作者:游乐园
1、临床资料
患者女性,70岁。患者6个月前无意间发现右颈部一鹌鹑蛋大小包块,无局部皮肤红肿、破溃、疼痛不适,无发热、寒战、咳嗽咳痰、心悸胸闷。3个月前,患者感夜间间断潮热、盗汗不适,包块未见增大,于医院就诊,颈部彩超检查提示:双侧颈部多发肿大淋巴结,结核可能,肿瘤性病变待排。行PPD试验:+++,局部水泡,诊断结核。遂予以HEZRft方案抗结核治疗3个月,包块未见缩小,患者自觉治疗效果不佳,遂再次就诊。专科检查:右侧颈部颌下可见大小约2.5x2cm的包块,质硬,边界不清,活动度差,轻度压痛,无波动感,局部皮肤无红肿、破溃。临床医师初步考虑颈部淋巴结结核,因恶性淋巴瘤往往生长迅速,与该患者临床表现不相符,可能性小,故排除。考虑到患者抗结核治疗效果较差,手术意愿强烈,故择期行颈部淋巴结结核病灶清除术。术中见多枚肿大淋巴结,伴明显脓液及坏死组织,病灶与颌下腺等周围组织黏连严重,分离困难。巨检:灰黄色碎组织一堆,总体积约4x2.5x2cm。显微镜下见异型淋巴样细胞部分呈结节性生长,部分弥漫性生长。免疫组化:Bcl-2、Bcl-6、CD10、CD20、PAX-5、CD21阳性,CD3、CyclinD1、C-myc、CD5、CD30、MUM-1、CK、ALK、CD15,Ki67(约80%+)。原位杂交:EBER阴性。分子检测:TB-DNA(+)。病理诊断:(右颈部淋巴结)滤泡性淋巴瘤(3A级),滤泡性和弥漫性混合性生长,局部向弥漫大B细胞淋巴瘤转变,合并结核。确诊后患者继续抗结核治疗,拒绝淋巴瘤化疗。
2、讨论
滤泡性淋巴瘤(follicular lymphoma,FL) 是一类起源于滤泡中心B细胞的非霍奇金淋巴瘤(NHL),临床呈高度异质性,以无症状的肿大淋巴结、骨髓受侵、脾大为特征,结外器官受累较少见,80%以上的病例存在t(14,18) (q32; q21)。我国FL的发病率占B细胞NHL的8%-23%,低于欧美地区,滤泡性淋巴瘤诊断时中位年龄约53岁,女性发病率略高于男性,滤泡性淋巴瘤患者病程长,基本上不能治愈,病程呈复发/缓解交替,5年的无进展生存(PFS)率及总生存(OS)率分别为61%和89%,但是30%-50%的患者可转化为高侵袭性的淋巴瘤亚型,其中以弥漫大B细胞淋巴瘤(DLBCL)较为多见,从而影响预后。
滤泡性淋巴瘤的组织学特征是淋巴组织正常结构被破坏,代之以紧密排列、大小和形状相对单一的肿瘤性滤泡,常累及整个淋巴结并浸润至被膜外,伴或不伴局部弥漫性生长。肿瘤细胞由中心细胞和中心母细胞混合组成,小和中等大小细胞核不规则,有裂沟,胞质少而淡染,大细胞核可呈泡状。根据滤泡和弥漫成分所占比例不同可以将滤泡性淋巴瘤分为:(1)滤泡为主型(滤泡比例>75%),(2)滤泡-弥漫型(滤泡比例25%-75%),(3)局灶滤泡型(滤泡比例
滤泡性淋巴瘤特殊亚型:(1)原位滤泡B细胞肿瘤(ISFN):通常淋巴结或淋巴组织结构形态无明显异常,但滤泡生发中心内部分B细胞发生 (t14;18)(q32;q21)易位,导致BCL2过表达。ISFN需与FL累及部分淋巴结鉴别。少数ISFN有进展为普通FL或其他类型淋巴瘤的风险,需要随访。(2)儿童型FL(PTFL):多见于儿童、青少年。多表现为头颈区、偶为腹股沟区等部位孤立性淋巴结肿大,形态学多表现为高级别FL,但遗传学特征与cFL不同,多无BCL2、BCL6和IRF4重排。局部治疗(如手术切除)即可治愈,预后良好。(3)十二指肠型FL(DTFL):以侵犯肠道为特征,多局限于小肠,尤多见于十二指肠降部,其形态、免疫表型与低级别FL一致,也有BCL2重排,但遗传特征和cFL不尽相同。通常仅累及黏膜层,少有肠外淋巴结受累。临床表现为惰性,预后较好。
免疫表型及分子特点:滤泡性淋巴瘤典型的免疫表型为:CD20+、CD10+、BCL6+、BCL2+、CD23-/+、CD3-、CD5-、cyclin D1-,CD21、CD23等染色能显示滤泡树突细胞网络的存在;此外,还需注意Ki-67或 MYC升高的预后相关性。部分病例(特别是3B级)可以出现CD10-或BCL2-。滤泡性淋巴瘤的分子遗传学检测主要是BCL2重排,细胞遗传学或荧光原位杂交(FISH)检测BCL2基因相关断裂或融合、1p36及IRF4重排可以协助诊断和鉴别诊断。
鉴别诊断:(1)反应性滤泡增生:滤泡大小不一,中心细胞和中心母细胞极性分布,富含星空细胞,套区完整且不对称。不表达BCL2,无t(14;18)(q32;q21)。极少数滤泡性淋巴瘤和有的亚型不表达BCL2,也无BCL2基因易位,需要结合形态和其他免疫组化及分子生物学特征加以鉴别。(2)B小淋巴细胞淋巴瘤:弥漫生长伴散在增殖中心形成假性滤泡,但细胞构成不同,无套区,缺乏滤泡网状组织(CD21阴性),不表达CD10和BCL6。(3)淋巴结边缘区淋巴瘤:呈弥漫性、边缘区或滤泡间生长,细胞大小不等或单核样形态,可发生滤泡植入性浸润,如同时伴有滤泡增生,则很难与滤泡性淋巴瘤鉴别。但以滤泡间浸润为主、细胞多形性伴浆细胞分化及残存的明显反应性滤泡有助于边缘区淋巴瘤的诊断。(4)其他:结节性淋巴细胞为主型霍奇金淋巴瘤、套细胞淋巴瘤、大B细胞淋巴瘤伴MUM1/IRF4基因重组等。
转化型淋巴瘤是指低度恶性的惰性淋巴瘤转化为其他高侵袭性的淋巴瘤亚型,可发生于滤泡性淋巴瘤、边缘区淋巴瘤、小淋巴细胞淋巴瘤、套细胞淋巴瘤以及结节性淋巴细胞为主型霍奇金淋巴瘤。转化型淋巴瘤发病率低,疾病发展的过程具有时间依赖性,10年发生率约为30%。转化型淋巴瘤的恶性程度高,缓解后易复发,更容易出现多重耐药,大大降低了患者的生存期。滤泡性淋巴瘤是常见的惰性B细胞淋巴瘤,总生存期大于10年,一般认为1-2级滤泡性淋巴瘤呈惰性表现,3级滤泡性淋巴瘤为侵袭性病程。在转化的过程中,滤泡性淋巴瘤向侵袭性较高的弥漫大B细胞淋巴瘤转化较为常见。有研究表明,发生转化的滤泡性淋巴瘤与普通惰性滤泡性淋巴瘤的区别在于肿瘤微环境中突变、缺失、嵌插、重排的核苷酸的数目以及肿瘤基因的激活和抑癌基因的失活,且滤泡性淋巴瘤和弥漫大B细胞淋巴瘤均起源于B细胞,有共同来源的祖细胞,且正常生发中心的B细胞中可出现体细胞类型转换等机制,导致生发中心B细胞来源肿瘤(如滤泡性淋巴瘤)的发生,并可能进一步向弥漫大B细胞淋巴瘤转化,转化被认为是滤泡性淋巴瘤病程中的固有生物学事件。
滤泡性淋巴瘤的某些不良预后因素与其转化的危险因素是相同的:患者的体力状态突然下降、高LDH、分期晚、贫血、诊断时高IPI评分、新的结外侵犯(如肝脏、骨骼、中枢)、β2-MG升高、高钙血症、出现新的B症状、淋巴结突然增大这些危险因素易驱动转化型淋巴瘤的发生。
随着病程的延长,滤泡性淋巴瘤发生转化的几率增加,PET-CT检查可以为明确滤泡性淋巴瘤发生转化提供帮助。文献报道,SUV>10有80%的可能性发生DLBCL转化,SUV>13发生转化可能性为90%,SUV>17为100%发生了转化。病理活检是诊断的金标准,可取SUV值高的组织进行病理活检。滤泡性淋巴瘤是由滤泡内或滤泡外的类似正常的生发中心B细胞组成,其肿瘤组织中正常组织学结构部分或全部破坏,FDC网密集增多,显微镜下可见大小不一、边界不清、疏密不等、形状不规则的结节结构。而侵袭性弥漫大B细胞淋巴瘤则是由破坏滤泡结构的弥漫性增殖的大细胞组成,镜下细胞形态较单一,细胞核大,表现为圆形或者不规则形,可见大片坏死。CD21是滤泡树突状细胞的主要标记物,存在于淋巴结或结外的淋巴组织内,表达于淋巴滤泡的树突细胞,也分布于B淋巴细胞的胞膜上,正常情况下CD21显示完整的球形滤泡网,且在活化的B淋巴细胞中逐渐减少。Ki-67是早期判断肿瘤癌细胞分化程度、临床治疗效果以及预后的重要参数,与细胞增殖活跃程度有关,Ki-67越高,提示肿瘤负荷越大,疾病进展越快,生存期越短,预后越差。1-2级滤泡性淋巴瘤的Ki-67增殖指数一般
滤泡性淋巴瘤发生转化后常选用弥漫大B细胞淋巴瘤的一线方案化疗。滤泡性淋巴瘤转化的弥漫大B细胞淋巴瘤患者的近期疗效有差于原发弥漫大B细胞淋巴瘤患者的趋势,而远期预后则明显较差。有学者认为滤泡性淋巴瘤患者发生转化的时机可能影响其疗效及预后。这可能是由于以下原因所致:相比于复发转化的滤泡性淋巴瘤,确诊时即发生转化的淋巴瘤组织中尚存在有惰性淋巴瘤成分,肿瘤细胞分裂增殖缓慢,侵袭性较低,对治疗的反应性较好。而复发转化的淋巴瘤患者经多次治疗后,肿瘤细胞易产生多药耐药基因,对化疗的敏感性下降,患者机体自身耐受力减弱,难以承受肿瘤细胞对机体的消耗,导致患者的治疗效果差,生存期缩短。
病例图片:
一、HE
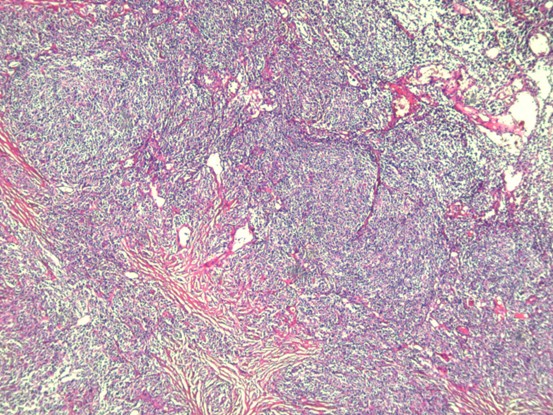
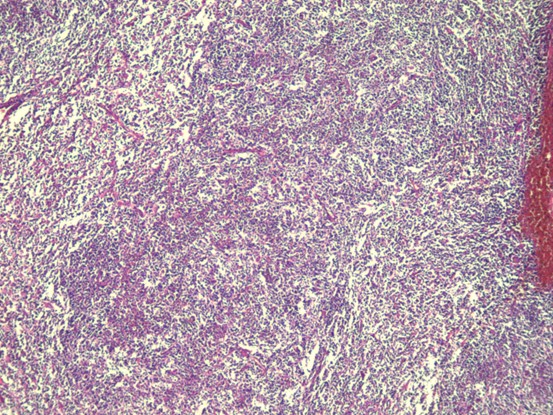
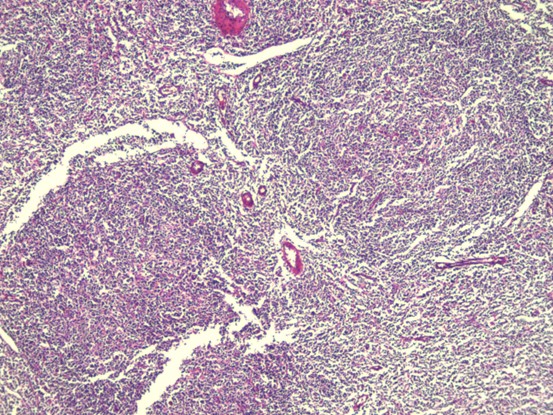
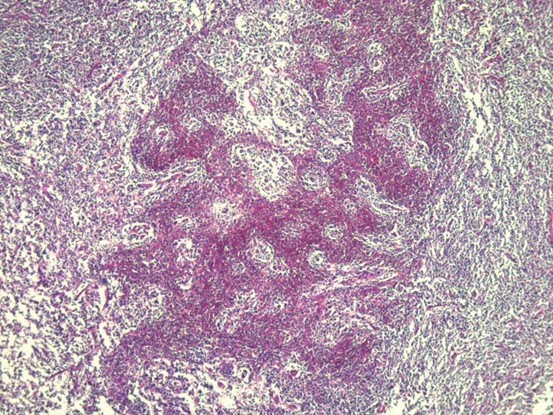
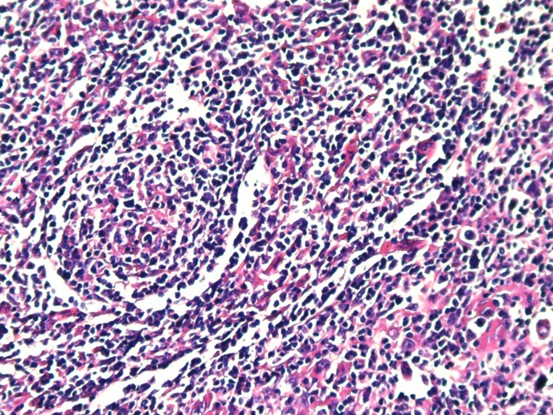
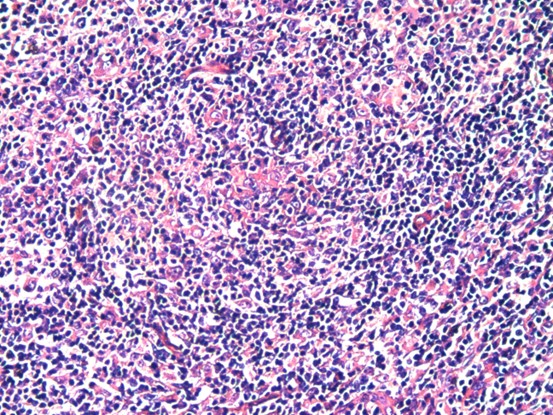
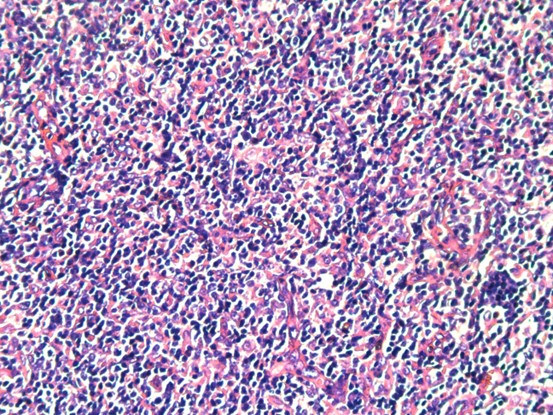
二、免疫组化
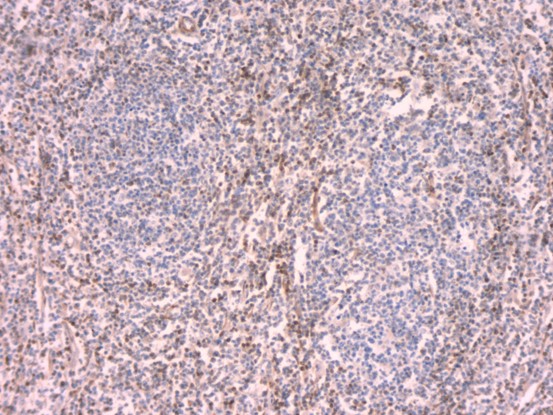
BCL2
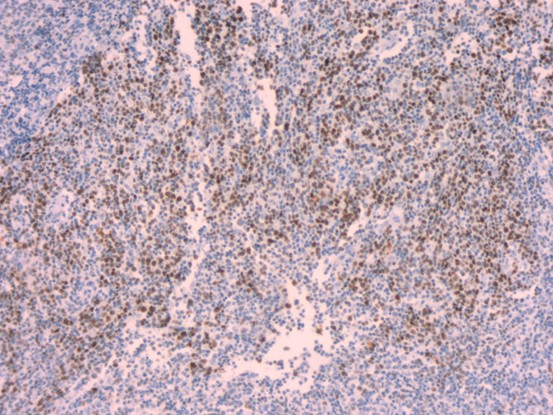
BCL6
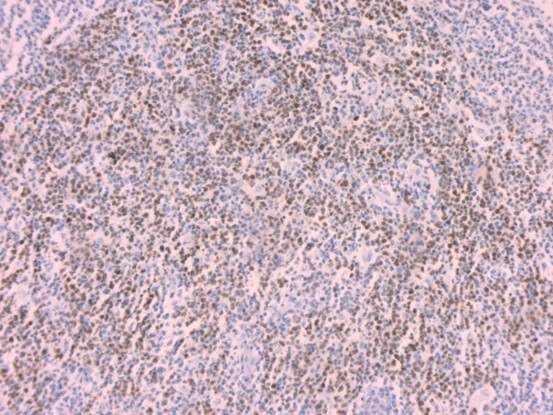
BCL6
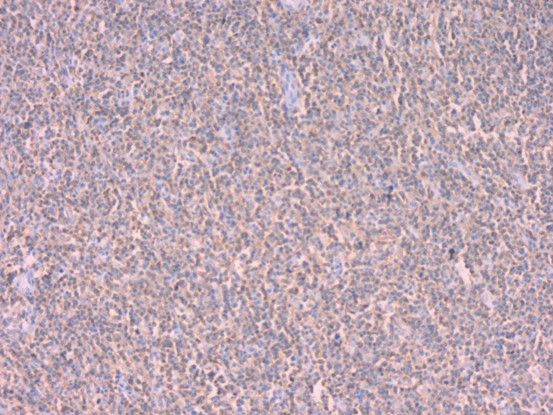
CD20

CD21
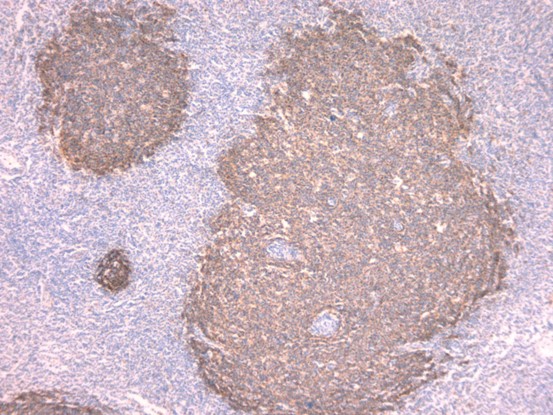
CD21
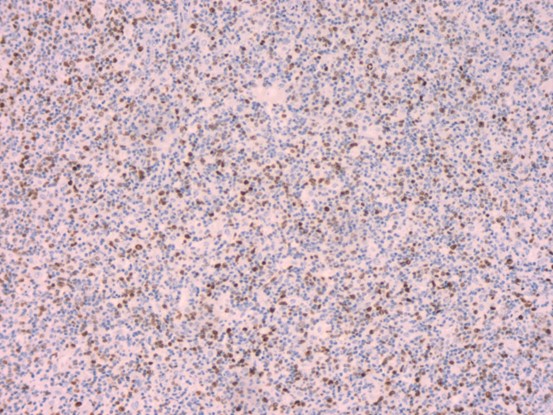
Ki67



























共0条评论