[导读] 编译整理:强子
大体特征
大体上,CIC重排肉瘤为灰白色、质软或鱼肉状表现。一般周边呈分叶状生长,中央伴显著坏死及出血。
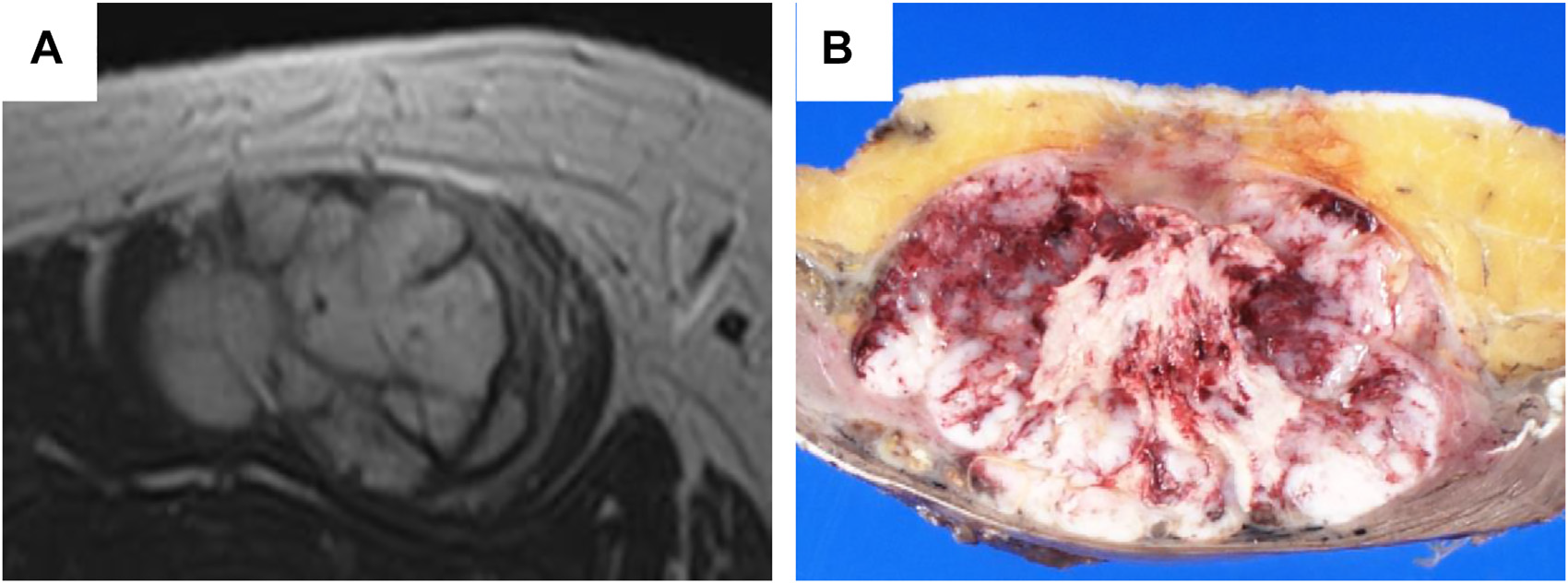 图1.CIC重排肉瘤的影像学及大体特征。(A)MRI的T2加权相中,CIC重排肉瘤表现为一个较大的分叶状肿物,伴异质性信号;(B)大体上,CIC重排肉瘤为灰白色、肉质样表现,呈分叶状生长,伴广泛坏死及出血。
图1.CIC重排肉瘤的影像学及大体特征。(A)MRI的T2加权相中,CIC重排肉瘤表现为一个较大的分叶状肿物,伴异质性信号;(B)大体上,CIC重排肉瘤为灰白色、肉质样表现,呈分叶状生长,伴广泛坏死及出血。
镜下特征
低倍镜下,肿瘤周边一般呈分叶状,背景呈纤维性。常见地图样坏死及出血。肿瘤一般呈弥漫片状。常见局灶黏液样改变剂网状或裂隙样结构,且这些特征有助于诊断。局灶可为梭形细胞的束状增生。
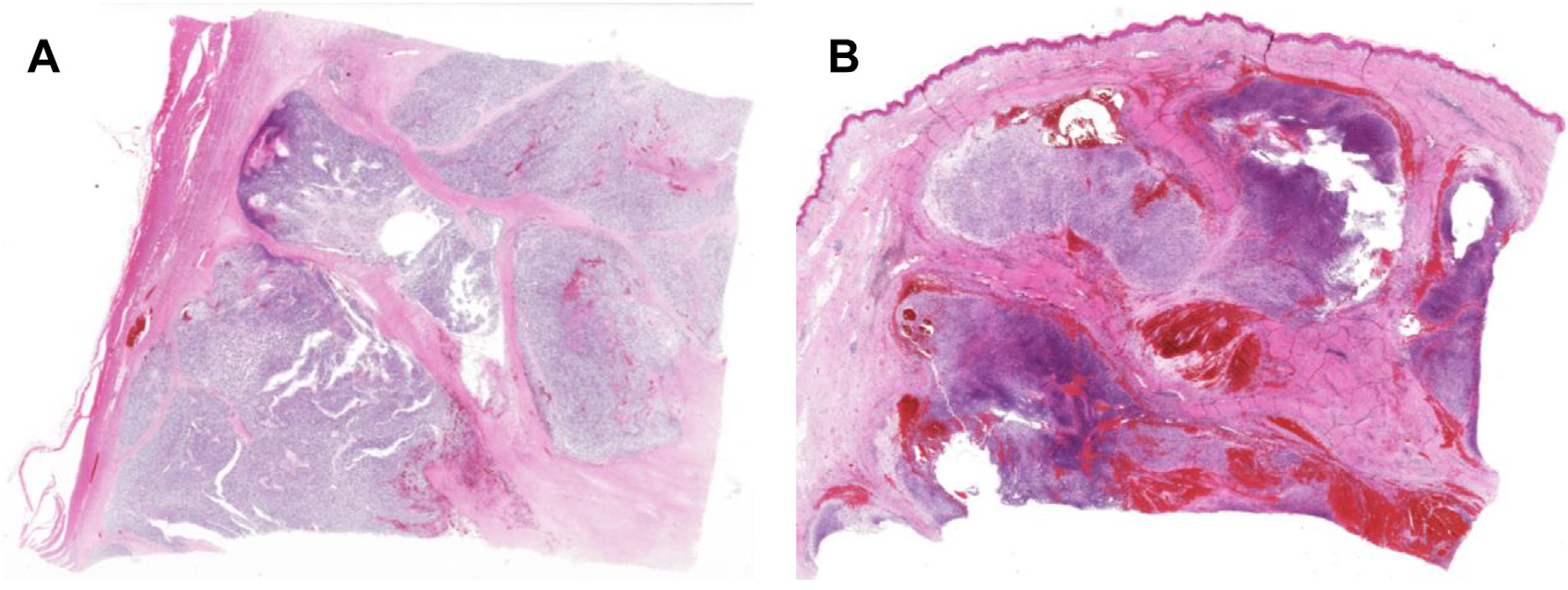 图2.CIC重排肉瘤的组织学特征:低倍镜下,呈纤维间隔分隔的分叶状生长。
图2.CIC重排肉瘤的组织学特征:低倍镜下,呈纤维间隔分隔的分叶状生长。
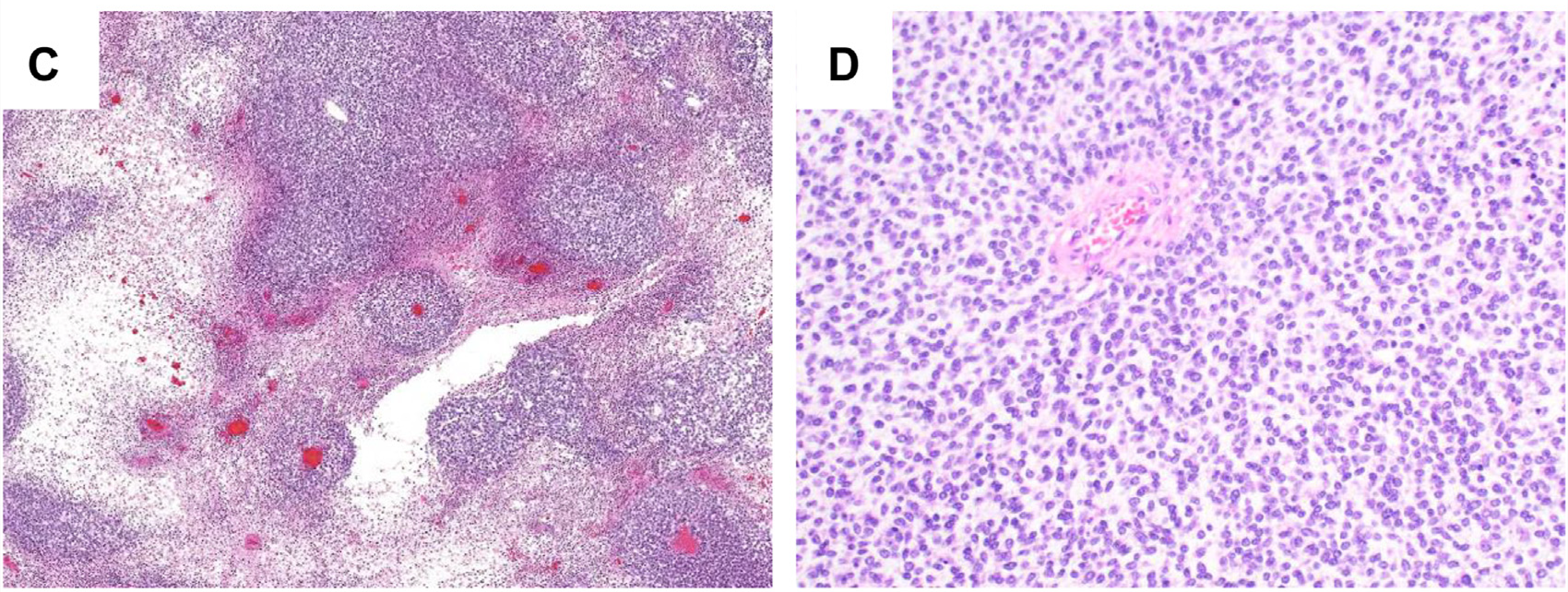 图3.CIC重排肉瘤的组织学特征:(左)常见地图样坏死及出血;(右)圆形肿瘤细胞,呈弥漫片状生长。
图3.CIC重排肉瘤的组织学特征:(左)常见地图样坏死及出血;(右)圆形肿瘤细胞,呈弥漫片状生长。
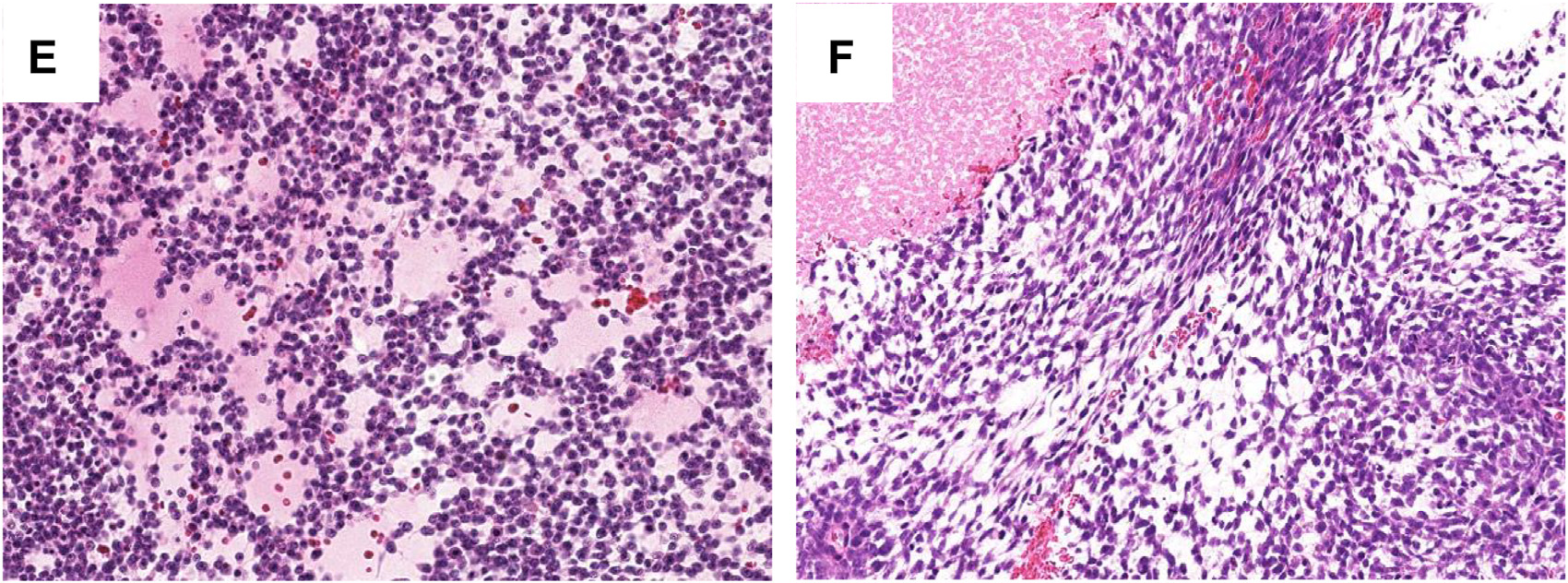 图4.CIC重排肉瘤的组织学特征:(左)局灶黏液样改变、伴网状生长,是该肿瘤的特征,且有助于诊断;(右)局灶可能会有梭形瘤细胞的束状增生。
图4.CIC重排肉瘤的组织学特征:(左)局灶黏液样改变、伴网状生长,是该肿瘤的特征,且有助于诊断;(右)局灶可能会有梭形瘤细胞的束状增生。
高倍镜下,瘤细胞为相对均一的小圆形。不过,仔细观察,几乎都能发现细胞核大小及形状存在轻度的变化,如细胞核轻度多形性。染色质空泡状,一般容易查见核仁。可能会局灶查见上皮样及横纹肌样细胞形态。胞质轻度嗜酸性,偶见透明表现。很少会看到完全为形态均一小圆细胞形态 、与Ewing肉瘤无法区分的情况。核分裂活跃。罕见形态亚型还有:主要呈黏液网状生长,显著上皮样形态。胞质内嗜酸性小球及软骨分化的情况极为罕见。新辅助化疗后,瘤细胞可能会有显著多形性。
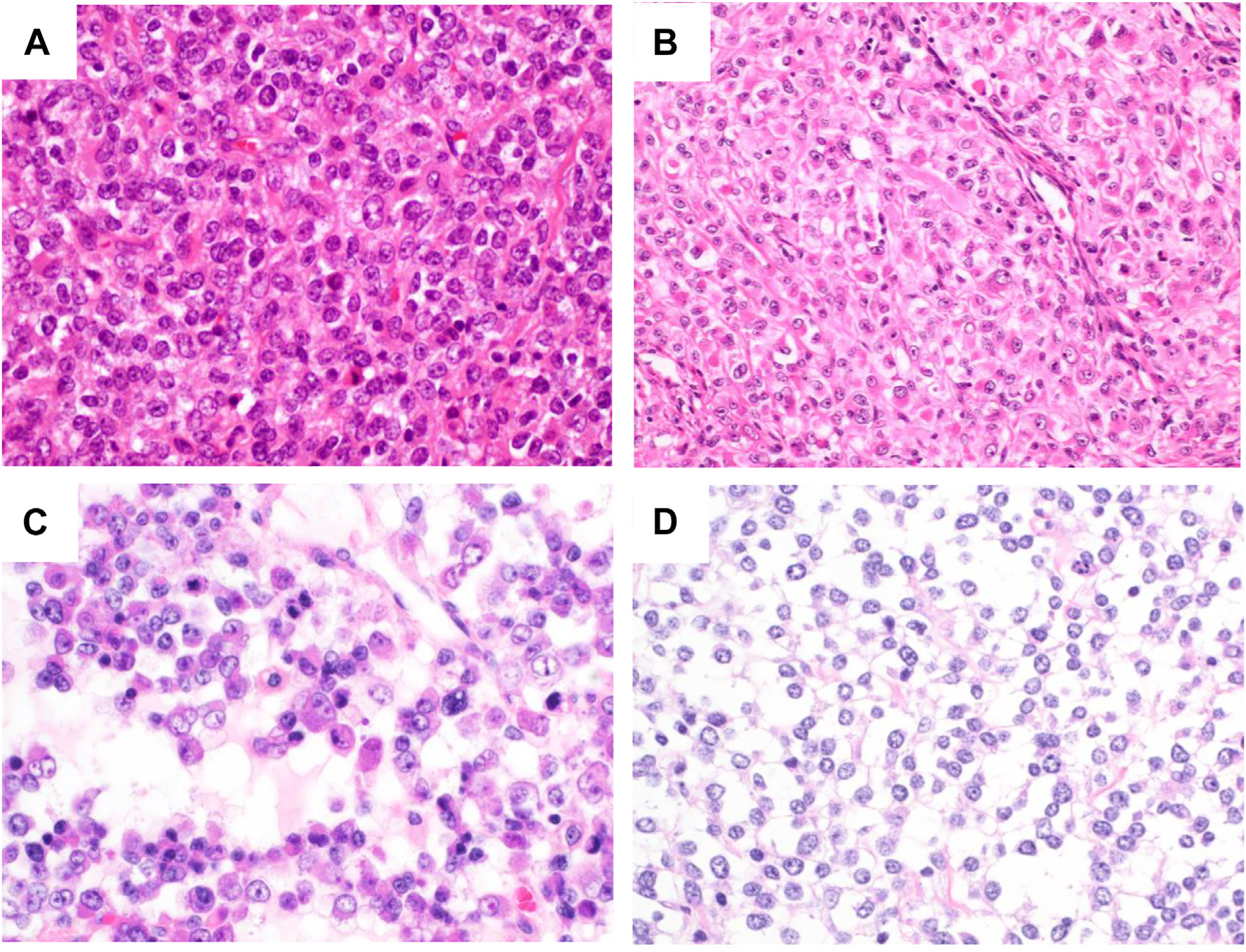 图5.CIC重排肉瘤的组织学特征:高倍镜下,圆形瘤细胞形态相对均一,但有轻度多形性,细胞核空泡状,右显著核仁,胞质嗜酸性至嗜双色性。瘤细胞可呈圆形、上皮样、和/或横纹肌样形态,偶见胞质透明改变。
图5.CIC重排肉瘤的组织学特征:高倍镜下,圆形瘤细胞形态相对均一,但有轻度多形性,细胞核空泡状,右显著核仁,胞质嗜酸性至嗜双色性。瘤细胞可呈圆形、上皮样、和/或横纹肌样形态,偶见胞质透明改变。
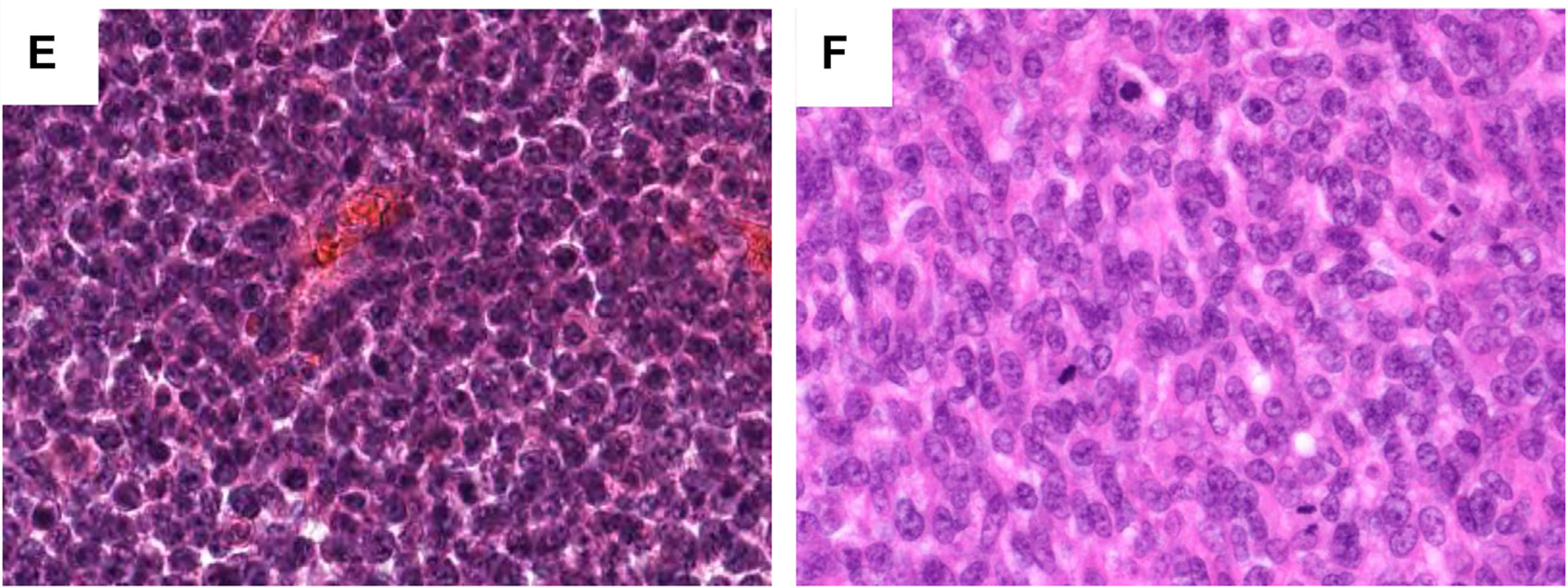 图6.CIC重排肉瘤的组织学特征:该肿瘤罕见情况下可呈均一的小圆形细胞形态,与Ewing肉瘤无法区分;核分裂活跃。
图6.CIC重排肉瘤的组织学特征:该肿瘤罕见情况下可呈均一的小圆形细胞形态,与Ewing肉瘤无法区分;核分裂活跃。
免疫组化特征
大部分CIC重排肉瘤都阳性表达CD99。不过,这一标记的着色常为异质性,与Ewing肉瘤中典型的细胞膜弥漫强阳性不同。ETV4是单项来说最有帮助的诊断标记物,其在小圆细胞肉瘤中诊断CIC重排肉瘤的敏感性和特异性均为90-95%。用WT-1的N末端抗体进行检测,70-95%的病例可见细胞核阳性,一般会伴有胞质着色。DUX4(C末端抗体)也为阳性;CIC::NUTM1融合肉瘤还会有NUT蛋白的细胞核弥漫阳性,但此时的着色模式并不是BRD4/3::NUTM1融合癌中的核旁点状阳性。
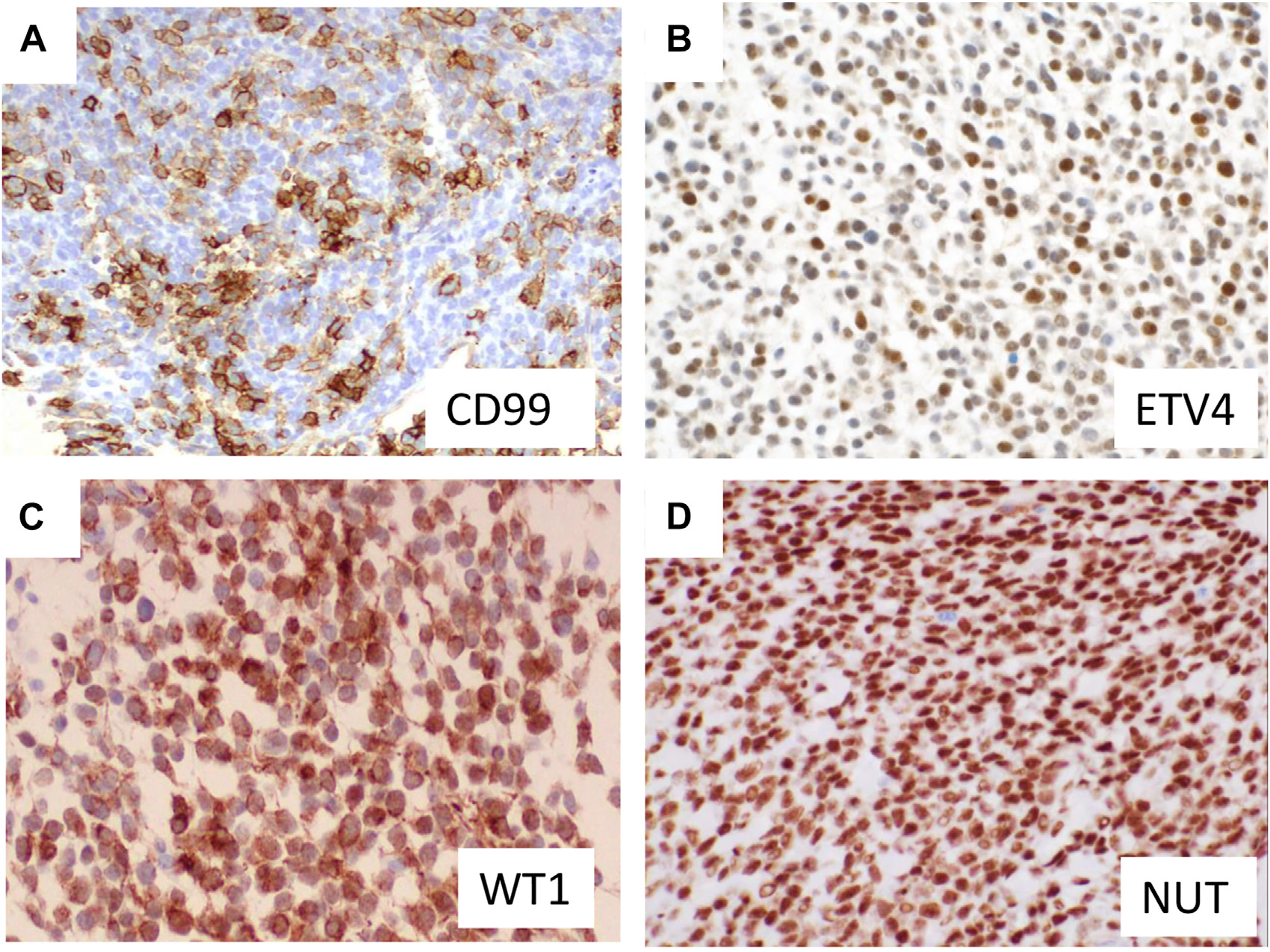
图7.CIC重排肉瘤免疫组化:(A)尽管大部分CIC重排肉瘤都是CD99阳性,但其着色一般为局灶、异质性;(B)ETV4为高度敏感且特异性的标记;(C)WT1细胞核阳性、常伴胞质着色,是CIC重排肉瘤中相对敏感及特异的标记;(D)CIC::NUTM1重排阳性的病例会有NUT的细胞核弥漫着色。
与其他融合驱动的肉瘤相似,CIC重排的肉瘤会表现出一些模棱两可的免疫表型而可能导致诊断困难。CK和MUC4可局灶阳性,TLE1和calretinin也常有表达。S100、desmin、Syn罕见阳性。CIC重排肉瘤常见表达ERG,少数病例中还会有CD31的共表达,一般为异质性着色。NKX2.2、PAX7、BCOR、SOX10、myogenin、CD45一般为阴性。
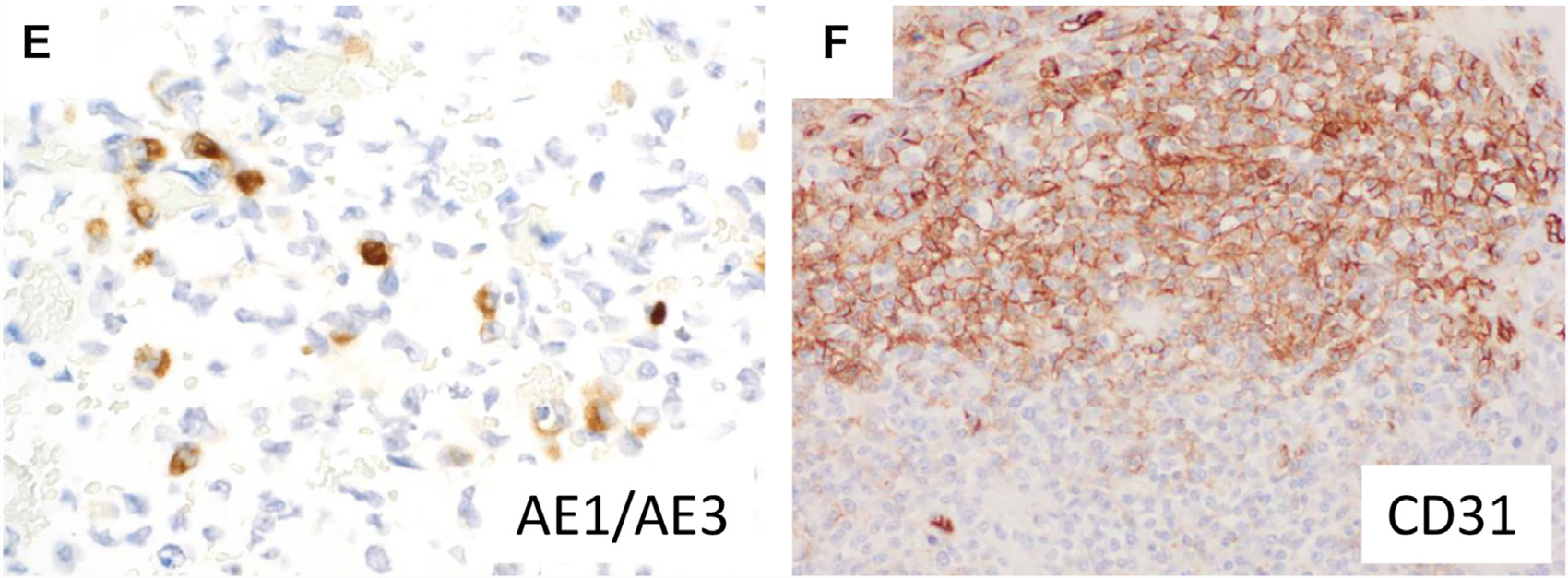 图8.CIC重排肉瘤免疫组化:CK可局灶阳性(左);CD31(右)和ERG也可异质性的共表达。
图8.CIC重排肉瘤免疫组化:CK可局灶阳性(左);CD31(右)和ERG也可异质性的共表达。
用于诊断的分子检测
FISH
CIC断裂探针FISH检测已有广泛应用,因为这一检测仅需一张未染色的切片、无需了解配体基因。阳性断裂模式一般有断裂的5’信号和3’信号、有一个正常的5’/3’融合信号。约10%的病例中可仅见5’端信号,此时不要误判为阴性。与其他FISH检测一样,需要有定量评估,应该有一个客观的重排阳性细胞比值的阈值,如20%。不过,CIC断裂探针FISH检测并非高度敏感的方法:14-25%的病例会存在CIC融合、但FISH信号为阴性。这样的假阴性FISH结果大部分是CIC::DUX4融合。CIC::LEUTX融合也可能会难以检测。
RT-PCR
RT-PCR也是广泛应用的方法之一。不过,由于存在多个外显子内的断裂点、以及非DUX融合配体的存在,因此RT-PCR的敏感性可能很有限。此外,福尔马林固定、石蜡包埋组织中抽提的RNA呈碎片状,也会影响融合转录的检测可靠性。
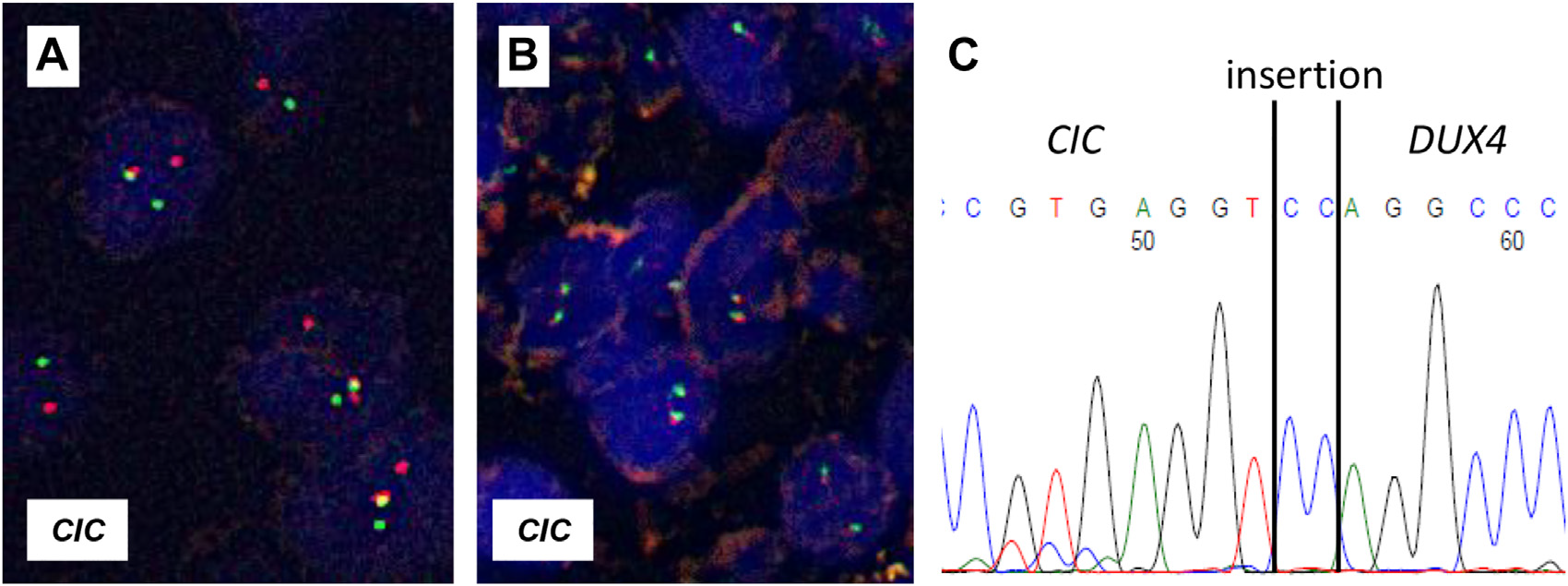 图9.CIC重排肉瘤的分子检测。(A)CIC::DUX4融合肉瘤中,CIC断裂探针FISH检测一般呈阳性;(B)但约15%的CIC::DUX4融合肉瘤呈阴性结果。如图B这种情况,RT-PCR可以成功的检测出CIC::DUX4融合转录本(C)。
图9.CIC重排肉瘤的分子检测。(A)CIC::DUX4融合肉瘤中,CIC断裂探针FISH检测一般呈阳性;(B)但约15%的CIC::DUX4融合肉瘤呈阴性结果。如图B这种情况,RT-PCR可以成功的检测出CIC::DUX4融合转录本(C)。
二代测序
靶向RNA测序及全转录组测序是新兴的诊断工具。重要的是,采用融合检查方案时,尽管嵌合阅读框(chimeric reads)定位在CIC基因中,但CIC::DUX4融合常被遗漏。这种情况下,二代测序报告中并无CIC::DUX4融合,但结合特征性的肿瘤表型、会促使我们对相关基因检测结果中的CIC阅读框进行仔细检查,会发现有CIC::DUX4的重排。这类假阴性结果的原因,可能是因为DUX4序列的特殊性而导致嵌合阅读框被判为了干扰。相反,CIC::LEUTX、CIC::FOXO4、CIC::NUTM1常通过融合检查方案而检出。
鉴别诊断
相比Ewing肉瘤来说,分叶状、局灶黏液样改变、局灶梭形细胞改变、显著核仁,都明显更常见于CIC重排肉瘤。相比Ewing肉瘤来说,CIC重排肉瘤的细胞核更为多形性、胞质更为丰富、黏附性更好。Ewing肉瘤的CD99一般为弥漫、强阳性的细胞膜着色,而CIC重排肉瘤中一般为异质性着色。Ewing肉瘤中更加特异性的标记NKX2.2和PAX7在CIC重排肉瘤中一般为阴性;相反,Ewing肉瘤并不表达WT1和ETV4。Ewing肉瘤的遗传学标记是EWSR1/FUS和ETS家族基因(如FLI1和ERG)的融合。
伴BCOR遗传学改变的肉瘤一般表现为均一的卵圆形字梭形细胞增生,背景为程度不等的黏液样或血管性间质;该肿瘤一般阳性表达BCOR和STAB2,但不表达ETV4和WT1。
促纤维组织增生性小圆细胞肿瘤为促纤维组织增生性间质内的圆形细胞巢,且可能会类似CIC重排的肉瘤。该肿瘤的特点是表达CK和desmin;WT1的C末端抗体为细胞核阳性,而N末端抗体则并不表达。该肿瘤的分子特点是EWSR1::WT1融合。
CIC重排肉瘤中如黏液样改变显著、且伴网状生长,很可能会误判为细胞性骨外黏液样软骨肉瘤:后者一般见于中年至年龄较大患者,儿童及年轻人诊断该肿瘤则值得警惕,尤其肿瘤具有侵袭性时。该肿瘤不表达ETV4和WT1,但程度不等的表达S100和神经内分泌标记,其分子特征是NR4A3融合。
CIC重排肉瘤主要为上皮样形态的时候,可能会误判为癌或间皮瘤,尤其是体腔活检标本中。CIC重排肉瘤可阳性表达CK,且一般表达WT1和calretinin,有时表达D2-40;因此圆细胞恶性肿瘤诊断中,这类“间皮瘤免疫组化”标记的解读要慎重。BAP1表达缺失、HEG1阳性是间皮瘤诊断的有用标记,癌则为claudin-4阳性。
如前所述,少数CIC重排肉瘤中会有ERG和CD31的共表达,此时可能会误判为上皮样血管肉瘤,加之CIC重排肉瘤中偶尔会有出血裂隙样腔隙及胞质内空泡,使得这一问题进一步复杂化。CIC重排肉瘤并无真正的血管结构。该肿瘤中的ERG和CD31表达为异质性,常为局灶、弱阳性,而不是血管肉瘤中所见的均一、弥漫、强阳性。
其他需要考虑鉴别的病种还有横纹肌肉瘤、SWI/SNF缺陷型肿瘤,也包括上皮样肉瘤。CIC重排肉瘤并无myogenin和myoD1表达,且总是有SMARCB1/INI1和SMARCA4/BRG1的表达。
——全文完——
往期回顾:
系列文献学习-软组织病理新病种-CIC重排肉瘤(一)






















共0条评论