[导读] 作者:游乐园
巨细胞病毒(cytomegalovirus,CMV)属疱疹病毒科β属双链DNA病毒,一旦感染可终生潜伏,在机体免疫力下降时再活化而致病。令人惊讶的是,CMV感染无明显季节性且非常普遍,血清阳性率为40%-100%。通过密切接触、体液传播等方式首次感染后长期携带,通常是亚临床的,在出现免疫功能低下或免疫抑制、器官移植和造血干细胞移植等情况时再活化而引起临床症状,致CMV病。但也有报道CMV感染亦可发生在没有明显基础疾病免疫功能正常的成人身上,但此类患者既往多有一过性免疫功能下降的病史。由于CMV具有广泛嗜细胞和组织特性,故CMV感染可累及消化道、肝、神经系统、肺、眼、心血管等多个系统,但多好发于消化系统中的食管、胃和结肠。消化系统CMV感染的临床表现一般是缺失的且不明显,但当机体免疫功能下降时临床表现就出来了,包括:发热、乏力、不适、淋巴结肿大、呕吐、腹胀腹痛腹泻、出血、肠炎、肠狭窄、肠梗阻、肠穿孔等症状。CMV引起的胃肠道受累在内镜检查无特异性,黏膜溃疡最常见。CMV相关胃肠疾病的发病机制是黏膜下血管炎,血栓形成,局部缺血导致溃疡,肠壁增厚和偶然的坏疽或穿孔。CMV感染是溃疡性结肠炎(UC)最易合并的机会感染之一,可导致患者病情加重、治疗应答欠佳,甚至增加手术及死亡风险,且与病情严重程度相关。UC所致肠黏膜屏障破坏和肠道菌群失调是促进肠道CMV激活的重要原因,UC患者肠道炎症和免疫异常,产生多种炎症因子,如TNF-α、白细胞介素(IL)-6和IL-23等。其中TNF-α可募集含有潜伏CMV病毒的单核细胞至肠道,使其分化为巨噬细胞后产生CMV病毒颗粒。此外,TNF-α与相应受体结合激活蛋白激酶C和核因子κB(NF-κB)通路,刺激极早期基因转录,导致CMV病毒复制,CMV激活促进结肠黏膜炎症引起UC复发,加重黏膜破坏,缩短临床缓解时间。患者感染CMV缺乏特异性临床表现,可表现为系统性症状,如发热、颈部淋巴结肿大和脾肿大,在肠道可导致病情加重,病变范围进展,常累及全结肠或右半结肠,导致黏膜溃疡、出血,增加穿孔风险。
CMV感染呈现原发、潜伏及再活化的不同情况,原发感染后可长期无临床症状,呈潜伏状态,通常血浆检测可阳性,但在HIV抗体阳性患者及某些免疫功能低下的患儿中,潜在的免疫缺陷使机体未能产生足够IgM亦未能检测其抗体,所以,在临床中最初的血清学检测是阴性的,并不排除CMV感染。因此,对于这类CD4水平较低的患者,应该同时进行PCR检测,有研究表明CMV激活时pp65抗原在6-24小时内表达于外周淋巴细胞、单核细胞、多型核白细胞和血管内皮细胞,其与患者尿中PCR拷贝呈正相关性,pp65检测目前被认为是诊断活动性CMV感染的“金标准”之一 。
CMV病用于再活化有临床症状和器官受累的情况,其中消化道疾病可累及消化道全程,比较常见,并且较为容易获得活检标本,组织学诊断占有重要的地位。在“CMV 胃肠疾病”的情况下,定义包括来自上下胃肠道的临床症状,内镜检查的宏观黏膜病变的发现,以及胃肠道组织活检中CMV感染的证据。CMV感染的金标准是组织学检查发现含有大细胞的炎症和肉芽组织(图1-3),其中细胞核显示典型的CMV包涵体或免疫组织化学染色发现CMV阳性(图4-5)。免疫组织化学染色能凸显CMV感染细胞,避免HE观察的假阴性,而且被认为是活动性感染伴高CMV复制的标志,在感染早期,呈细胞核染色,在感染晚期,呈弥散式核染色和胞质染色。
一般来说CMV感染首选更昔洛韦,其为首个批准应用的抗CMV药物,诱导期间5mg/kg每12小时1次,持续2周,维持阶段5mg/kg每天1次,持续2-8周。用药期间注意监测肝功能以及中性粒细胞,必要时可用集落刺激因子提高白细胞,同时行药物浓度测定,血药达到40-60μg/ml,治疗效果较好,伐更昔洛韦以及磷甲酸,可作为更昔洛韦替代品,合并胃肠道穿孔或肠狭窄肠黏连的患者一般需要手术治疗,但术后患者生活质量总体不好。
综上所述,消化系统CMV感染临床表现多种多样且无特异性,有的甚至是很隐匿,其对器官造成严重损害,故早诊断早治疗是该病预后的关键。

图1.食管活检-巨细胞病毒感染细胞,细胞明显增大,均匀深染
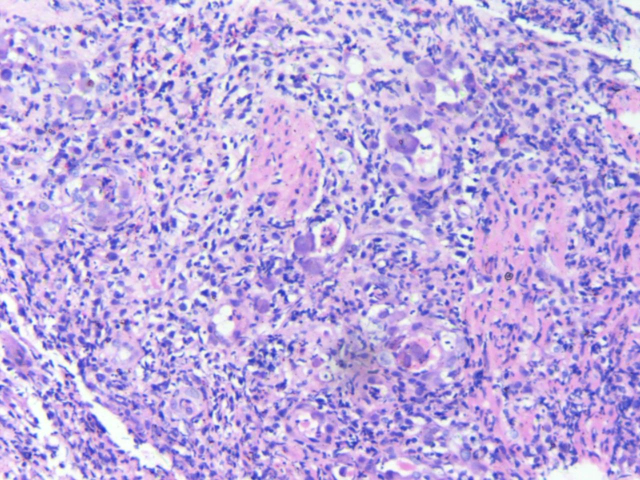
图2.炎性背景下大量巨细胞病毒感染细胞
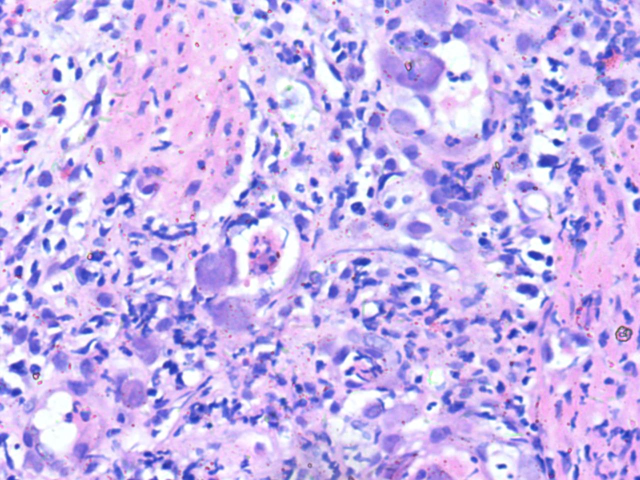
图3.巨细胞病毒感染细胞的胞核嗜碱性,呈“猫头鹰眼样”
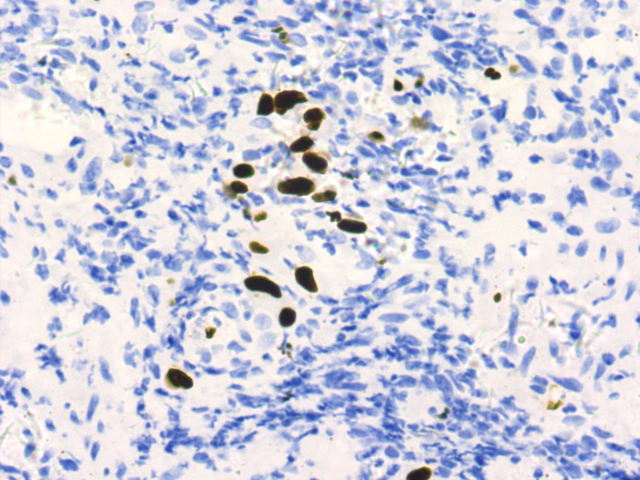
图4.食管活检不同区域-免疫组化CMV(+)

图5.食管活检不同区域-免疫组化CMV(+)


















共0条评论