[导读] 编译整理:强子
免疫组化p53在多癌种中的应用
1.胃肠道病理:
Barrett食管中的异型增生:低级别中≥80%、高级别中几乎全部可见突变型着色;
非异型增生的Barrett食管风险分层:2-5%存在突变型着色;
无蒂锯齿状病变中细胞学异型性的诊断:25-33%可见突变型着色;MLH1缺陷型病变中比例更高;
胰胆管肿瘤的诊断(尤其小活检标本中):约50%为突变型着色,其他生物学标记可能作为补充;
可能可以用于胃炎和特发性炎症性肠病中异型增生的诊断:尚不完全清楚。
2.泌尿道病理:
区分尿路上皮原位癌和反应性尿路上皮:p53联合CK20和CD44a一起检测;
3.妇科病理:
区分高级别浆液性癌(突变型着色)和低级别浆液性癌(野生型着色);
区分高级别浆液性癌(突变型着色)和3级的子宫内膜样腺癌(一般为野生型):在卵巢,则p53联合WT-1一起检测;子宫内膜中突变型着色的情况下,也需联合一组指标;
区分外阴分化型上皮内肿瘤(突变型着色,有时候为基底层过表达的着色)和反应性鳞状黏膜(野生型表达)、高危型HPV相关病变(基底层不着色);
区分平滑肌肉瘤、子宫未分化肉瘤(一般为突变型着色)与遗传学定义的子宫间质性肿瘤(几乎均为野生型着色)。
4.神经内分泌病理
区分低分化神经内分泌癌(一般为突变型着色)和高分化神经内分泌瘤3级(几乎总是野生型):p53联合Rb、Ki-67、SSTR2及其他标记物一起检测;
5.血液病理:
支持套细胞淋巴瘤中母细胞亚型和多形性亚型的识别,并有独立的预后不良意义;
支持低级别B细胞淋巴瘤高级别转化的识别;
检出TP53突变的骨髓增生异常综合症和急性髓系白血病:有预后意义和治疗意义;
在大B细胞淋巴瘤中有预后不良意义:尚不完全清楚。
6.神经病理:
区分弥漫性星形细胞瘤(突变型着色)和反应性胶质增生、少突胶质细胞瘤(后二者均为野生型着色):p53常和IDH1 R132H、ATRX、Ki-67一起联合应用;
区分TP53突变型和TP53野生型的sonic hedgehog活化型髓母细胞瘤:TP53突变型者预后极差,且与Li-Fraumeni综合征有关;sonic hedgehog活化型髓母细胞瘤的识别是根据GAB1强阳性着色而得出;GAB1和YAP1、β-catenin联合免疫组化检测,可用于分子分型的替代性标记。
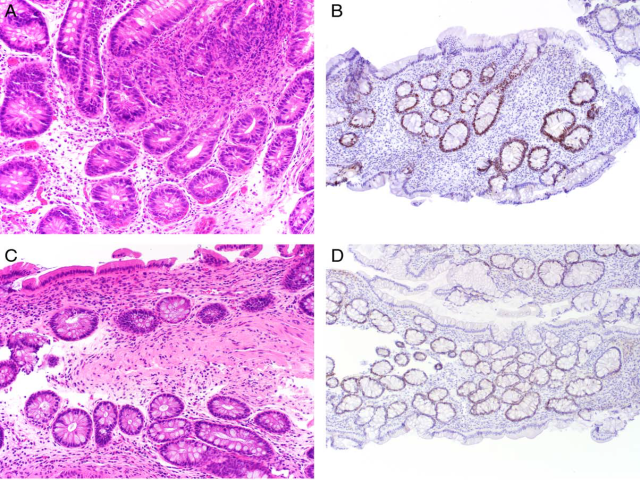
图7.炎症性肠病相关异型增生评估中,免疫组化p53和SATB2联合检测。本例患者有广泛溃疡性结肠炎病史8年。(A)隐窝细胞有非典型,本文原作者诊断为“异型增生不确定,倾向于低级别异型增生”;本例加做p53免疫组化后,结果解读为不确定(B)。(C)相同患者的来一次活检,本文原作者解读为未见异型性,加做免疫组化,结果解读为野生型着色(D)。比较图(A)和图(C)中的细胞核大小、染色质表现,二者相似;两次免疫组化p53结果因为终末分化表现。
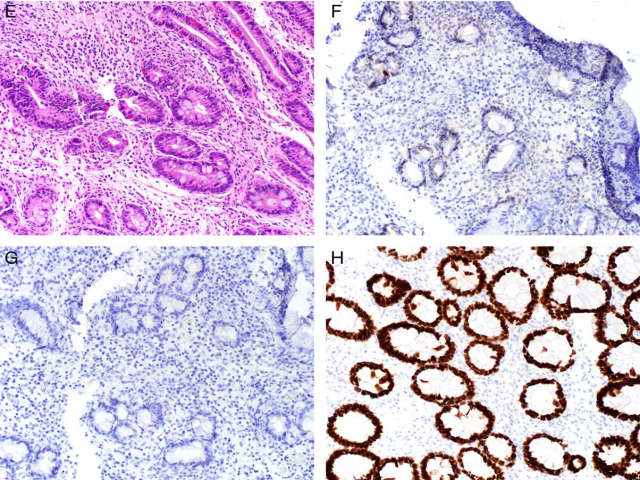
图8. 图7后续随访活检,(左上)形态学解读为平坦型低级别异型增生,当然至少部分是根据SATB2免疫组化中的完全不着色而做出的(左下);(右上)免疫组化p53也是野生型着色。(右下)另一处区域SATB2免疫组化呈完整的(正常)着色。SATB2是一项可用于支持形态学考虑炎症性肠病相关异型增生的新型免疫组化标记;这种情况下加做免疫组化p53可提供分子信息。

图9.无蒂锯齿状病变,伴异型增生。本文原作者表示,常遇到这类病变,一般异型增生主要位于隐窝基底。考虑有异型增生可能的情况下,作者以前是进行MLH1免疫组化检测,但现在开始应用p53等指标。(A)低倍镜下,为多个碎片状的锯齿状息肉;(B)一处碎片的高倍镜,图中右侧有细胞核增大、假复层、黏液缺失等表现;(C)免疫组化MLH1,整个病灶中均为完整着色;但免疫组化p53在非典型区域为错义突变的着色模式(D)。
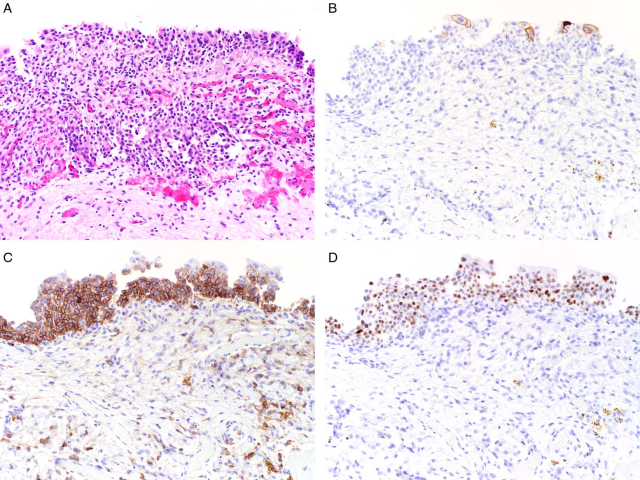
图10.尿路上皮原位癌和反应性非典型鉴别中的免疫组化。(A)一例复发性尿路上皮原位癌患者、BCG灌注治疗并腔内应用吉西他滨/多西他赛后活检所见;(B)免疫组化CK20,散在伞细胞阳性,这是正常结果;(C)免疫组化CD44a,可见广泛/全层的细胞膜着色,这一般是反应性非典型的特点;(D)免疫组化p53,阳性信号增强,可能可以解读为野生型,也可能可以解读为不确定。结合其他免疫组化指标的结果,本例支持反应性非典型,因此p53的免疫组化结果还是解读为了野生型。本文原作者表示,他们还遇到过放射性膀胱炎、免疫组化p53表现为强阳性而倾向于错义突变的情况。对于所有器官系统来说,都存在放疗和化疗所致细胞毒性损伤导致的野生型信号增强。
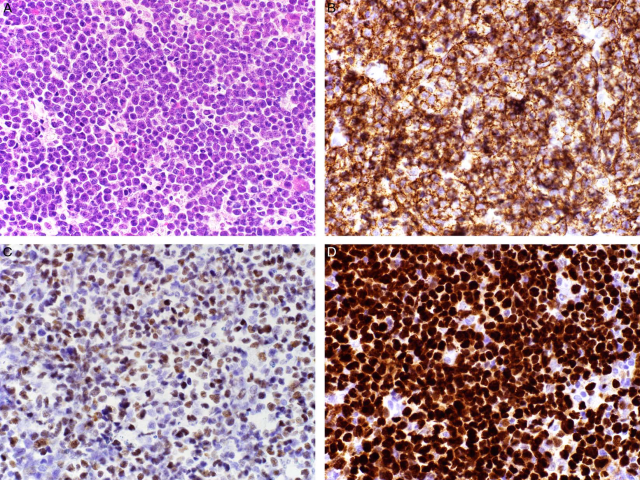
图11.低级别B细胞淋巴瘤高级别转化中的免疫组化p53。(A)本例患者有脾脏边缘带淋巴瘤病史,目前表现为肝脏多发肿物;(B)免疫组化CD20,支持该肿瘤为B细胞谱系,且可体现出肿瘤细胞的体积较大;(C)免疫组化c-Myc,为过表达,这对应FISH检测中MYC为异常结果;(D)免疫组化p53证实为错义突变着色模式。免疫组化p53染色异常、和/或c-Myc免疫组化异常,常见于低级别B细胞淋巴瘤的高级别转化。
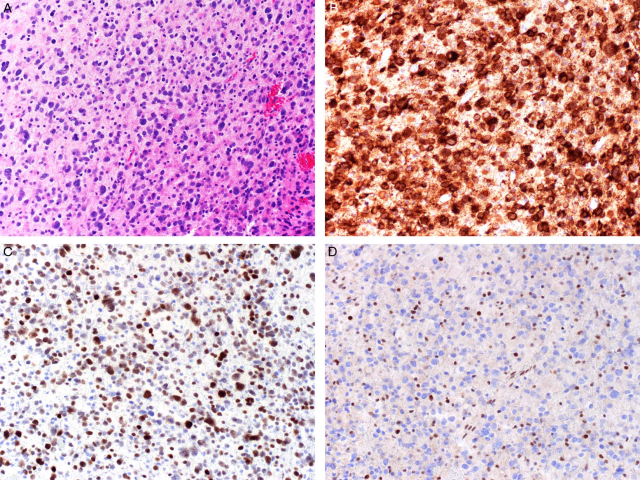
图12.免疫组化区分弥漫性星形细胞瘤和反应性胶质增生、少突胶质细胞瘤。(A)胶质肿瘤的特点是细胞密度增多,且有显著非典型;(B)免疫组化IDH1 R132H突变特异性抗体检测为阳性;(C)p53表达增强,ATRX表达缺失,但内对照为完好着色(D)。ATRX缺失的胶质瘤为星形细胞谱系;就IDH突变型胶质瘤来说,TP53突变常见于弥漫性星形细胞瘤,而不见于少突胶质细胞瘤。这些免疫组化标记的结果都不见于反应性胶质增生。
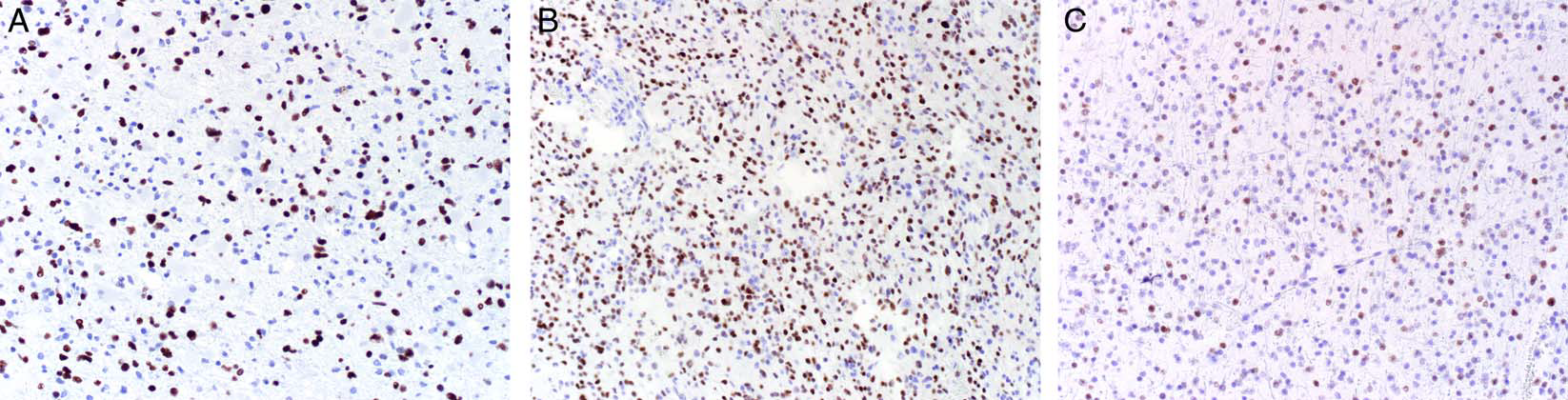
图13.TP53突变型弥漫性星形细胞瘤中的免疫组化结果。神经病理医师采用“>10%的病灶细胞核强阳性着色”这一标准来作为TP53突变的替代,不过大部分肿瘤都会是更为广泛的着色。该组肿瘤均有TP53突变,且图C中有两个不同的突变。TP53突变型弥漫性星形细胞瘤免疫组化p53判断阈值的降低,部分是因为免疫组化玻片中难以鉴别单个细胞核到底是肿瘤性、还是反应性。
——全文完——
往期回顾:
病理检测指标p53大揭秘(一)
病理检测指标p53大揭秘(二)




















共0条评论