[导读] 编译整理:魏建国,王强
自20世纪90年代早期在Ewing肉瘤中发现EWSR1::FLI1融合以来,间质肿瘤中已报道了数以百计的基因融合,且仍在持续发现中。这些融合事件的相关特征,导致软组织病理诊断策略出现了改变,提高了分类的准确性,且很多已常规应用于临床病理诊断。此外,相关基因融合的确定除了对肿瘤发生机制有了新认识,还因此而出现了某些新的治疗方案。
上述问题在皮肤和皮下间质性肿瘤也有所体现。对于皮肤和皮下间质性肿瘤来说,不同瘤种间的形态学有显著重叠,且有时取材有限,更是增加了诊断难度。哈佛大学附属布列根和妇女医院著名软组织病理专家Fischer等在《Semin Diagn Pathol》杂志发表综述,对具有基因融合的某些表浅肿瘤新进展进行了相关介绍,具体涉及其诊断与治疗方案、比分子检测要便捷和廉价的相关免疫组化替代性标记等,同时介绍了分子检测用于相关诊断时的一些注意事项。为帮助大家更好的了解和掌握相关新知识,我们将该文要点编译介绍如下。
纤维母细胞性/肌纤维母细胞性肿瘤
隆突性皮肤纤维肉瘤
隆突性皮肤纤维肉瘤(dermatofibrosarcoma protuberans,DFSP)是一种具有纤维母细胞分化的局部侵袭性肿瘤。患者年龄分布宽泛,多为青年至中年,最常见于躯干处。DFSP局部复发几率高达50%;经典型DFSP不会转移,但级别较高的纤维肉瘤亚型约有10-15%的几率出现远处转移。组织学上,DFSP为细胞非常丰富的浸润性、增生表现,细胞形态均一,为温和的梭形,排列呈席纹状;免疫组化检测,95%的病例为CD34阳性。
DFSP一般为t(17;22)(q22;q13),这与超数环状染色体r(17;22)有关,且导致COL1A1::PDGFB融合转录。大部分DFSP根据形态学即可做出诊断,但部分病例需进行分子检测,尤其某些难以识别的形态学亚型或者标本有限的活检情况下,前者如黏液样DFSP。FISH检测既敏感、又直接,可在96%的病例中检出相应融合,包括所有形态学亚型。以细胞数量增多、束状生长、生物学行为更具侵袭性为特征的纤维肉瘤样转化病例中,伴有融合基因拷贝数量的增多。占比4%的FISH检测PDGFB重排阴性病例中,约半数为COL1A1::PDGFB重排,最近发现其余病例大部分为COL6A3::PDGFD、EMILIN2::PDGFD融合。
具有PDGFD融合的肿瘤形态学上与PDGFB融合者相似,但前者似乎更多见于乳腺。PDGFB融合者,RNA原位杂交有望取代FISH和二代测序,因为前者更快、且费用更低。研究发现,RNA原位杂交对于经典型DFSP的敏感性为92%,对于纤维肉瘤型DFSP的敏感性为100%,但并不是100%的特异。
DFSP因为有PDGFB信号通路的激活,因此瘤细胞对于受体酪氨酸激酶抑制剂伊马替尼敏感。这一治疗一般会有部分缓解、诱导病变稳定、导致肿瘤缩小以利于手术切除,尤其肿瘤位于某些特殊解剖部位者。
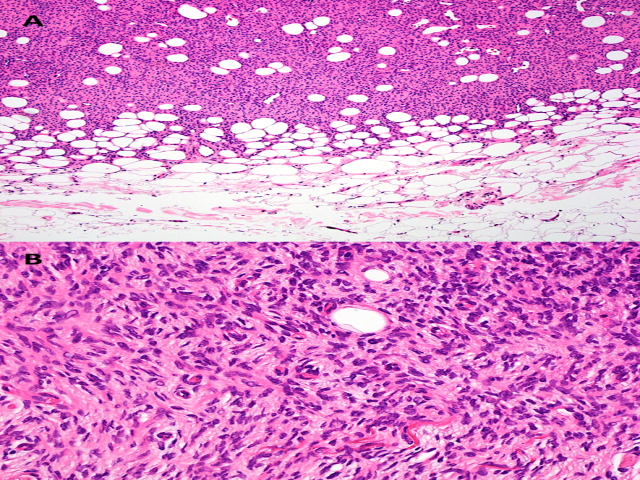
图1.具有PDGFD重排的DFSP一例。(A)瘤细胞形态单一、梭形表现,周围有所谓“蜂窝状”的陷入脂肪组织;(B)形态单一的瘤细胞呈席纹状生长。本例经RNA测序证实有PDGFD的重排。
良性纤维组织细胞瘤
良性纤维组织细胞瘤也称为真皮纤维瘤,是一种发病年龄宽泛、涉及部位较广的真皮常见肿瘤。组织学上,其特点为梭形细胞排列呈短束状及轮辐状,周围有陷入的真皮胶原。病变内的生长方式要比DFSP变化更多,但多为更加均一的席纹状。个别病例可有细胞数量的增加(即细胞型纤维组织细胞瘤)、细胞核非典型显著增加(非典型纤维组织细胞瘤)、显著含铁血黄素沉积(含铁血黄素沉积型纤维组织细胞瘤)、动脉瘤样改变(动脉瘤样纤维组织细胞瘤)。
与隆突性皮肤纤维肉瘤不同,纤维组织细胞瘤一般表达SMA;5%的病例表达CD34,这可能是一个诊断陷阱。最近发现,良性纤维组织细胞瘤具有PRKC-B及PRKC-D的融合,融合配体有PDPN、CD63、LAMTOR1。还有一例报道为PRKC-A的融合。总体而言,上述基因改变见于多种情况的良性纤维组织细胞瘤,包括深部和表浅的病例、以及不同形态学的病例(如细胞型、动脉瘤样亚型),这也说明这些亚型属于同一家族。
——未完待续——
点此下载原文献
参考文献
[1]Fischer GM, Papke DJ Jr. Gene fusions in superficial mesenchymal neoplasms: Emerging entities and useful diagnostic adjuncts. Semin Diagn Pathol. 2023;S0740-2570(23)00046-1.
doi:10.1053/j.semdp.2023.04.014














共0条评论