[导读] 译者:陈旭
导读
乳腺组织的外科病理活检,在日常病理工作中较为常见。在这其中,有许多疾病需要鉴别,诊断的陷阱较多。2022年12月10日,爱尔兰圣文森特大学附属医院的Cecily Quinn教授,在病理学知名期刊《Histopathology》(IF值为7.504分),发表题为“Pitfalls in breast pathology”综述性文章,详尽总结了乳腺病理诊断常见的诊断陷阱。下面笔者将综述全文编译如下,供相关医师参考。
摘要
准确的病理诊断,是乳腺疾病患者临床治疗的基石。由于非手术诊断,逐渐成为病理诊断标准,病理医师每天都需要在有限的乳房核心针吸活检(CNB)材料上,做出明确诊断,这一过程具有挑战性。使用H&E 染色,以及免疫组织化学(IHC),对CNB样本进行仔细评估,提供必要的信息,以告知临床医师下一步的治疗措施。一些病变在小组织样本上可能难以区分,如果不确定,应建议进行诊断性切除活检。这篇综述讨论了(1)类似于恶性肿瘤的良性乳腺病变,(2)容易误诊为良性疾病的恶性疾病,(3)可能被错误诊断为原发性乳腺癌的恶性病变,以及(4)一些IHC陷阱。这篇综述的目的,是提高对乳腺病变诊断中潜在缺陷的认识,这些缺陷可能导致诊断不足、过度诊断或恶性肿瘤的错误分类,从而对患者治疗产生潜在的不良后果。
简介
“过度诊断比诊断不足更常见,特别是对于经验不足10年的病理医师”和“切勿使用没有低倍物镜的显微镜”,John Azzopardi于1979年,在他的教科书《乳腺病理学问题》中写道。40多年后,在个性化治疗、分子病理学和多基因检测、数字显微镜和人工智能的时代,进行正确诊断的重要性,从未如此重要。非手术诊断,目前已逐渐成为诊断标准,病理医师可以根据小组织样本,做出诊断。仔细评估H&E染色的切片,结合模式识别和分析思维,辅之以适当使用免疫组织化学(IHC)和其他测试,仍然是组织学诊断的支柱。这篇综述旨在强调解释乳腺病变的诊断陷阱,这些陷阱可能会以不同的方式,导致漏诊、过度诊断或恶性肿瘤分类不正确,对患者治疗有潜在的不良后果。该综述侧重于HE和IHC在乳腺病理学中的作用,旨在补充有关该主题的现有文献。在这篇综述中,不讨论单个实体的分子病理学特征。同样,与非手术诊断程序、次优放射学-病理学相关性,以及大体检查取样质量相关的陷阱的讨论,超出了本文的范围。
易误诊为恶性肿瘤的良性疾病
一些良性乳腺病变,具有模仿恶性病变的“浸润性”外观,可能被误诊为浸润性癌(IC)。这些疾病包括乳头腺瘤、乳头良性汗管瘤性肿瘤、放射状疤痕/复杂硬化性病变、硬化性腺病和微腺腺病。良性导管内乳头状瘤,可能表现出丰富的普通导管增生(UDH)、反应性上皮变化或硬化,这些可能被误认为是恶性肿瘤。
乳腺病理学中,存在过度诊断恶性肿瘤风险的其他病变,特别是空芯针活检 (CNB)标本,包括那些缺乏典型的上皮-肌上皮腺体双层的病变,例如,多形性腺瘤和硬化性腺肌上皮瘤(MBC),可能被误诊为化生性乳腺癌;肌纤维母细胞瘤的上皮样变体,由黏性异常的雌激素受体(ER)阳性上皮样细胞组成,类似于浸润性小叶癌(ILC),常见脂肪坏死伴有明显的组织细胞反应,可能被误认为大汗腺ILC;乳头Toker细胞增生,易误诊为乳头佩吉特病。在这里,作者描述了一些根据组织学发现,可能会误诊为恶性肿瘤的良性疾病。
腺体、硬化和乳头状病变
乳头腺瘤
乳头腺瘤,也称为乳头糜烂性乳头状瘤病,发生在乳头浅表,可能表现为乳头糜烂或溃疡,临床上类似于佩吉特病。它可能见于男性,最常见于50岁的女性。临床检查通常显示真皮结节,超声可以显示肿块,但通常是非特异性的。
组织学上,由于腺体增生的不规则轮廓,乳头腺瘤可能被误认为是IC,通常受累病灶,具有坏死灶的丰富UDH,类似于原位导管癌(DCIS)(图 1)。乳头腺瘤引起的恶性肿瘤,目前已有报道,但并不常见。了解病情和典型的临床表现,通常可以做出正确的诊断。在可疑情况下,肌上皮细胞(MEC)IHC ,可用于鉴别腺体的良性性质,并明确伴随的上皮细胞增殖的性质。在某些病变中,MEC层可能会减弱或出现局灶性缺失,建议在疑难病例中,至少使用两种MEC标记物(参见肌上皮细胞免疫组织化学部分)。
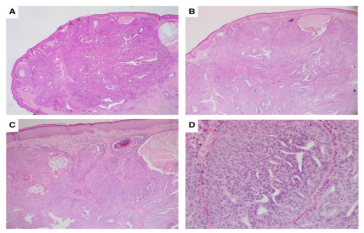
图1.乳头腺瘤伴有丰富的UDH(H&E)。
乳头汗管瘤
乳头汗管瘤与乳头腺瘤发生在同一位置,被认为是一种惰性、局部浸润性病变,通常体积较小,有可能局部复发,但不会转移。它显示出与低级别腺鳞癌的一些形态学重叠。这些病变在CNB上,可能难以区分,了解精确的解剖位置,可能会对鉴别有所帮助。汗管瘤性肿瘤通常位置浅表,可浸润乳晕的平滑肌,但很少延伸至真皮。肿瘤由小巢和索组成,有数量不等的鳞状上皮样细胞,位于中央,可形成充满角蛋白的小囊肿。单个细胞形态温和,罕见核分裂。相反,低级别腺鳞癌发生在乳腺间质组织的更深处,具有较大体积,很少浸润乳头,并且还可能具有瘤性梭形细胞成分。在免疫表型上,汗管瘤性肿瘤的主要细胞类型是肌上皮细胞,表达p63、高分子量(HMW)细胞角蛋白(CK),以及其他MEC标志物。
放射状瘢痕/复杂硬化性病变
放射状瘢痕/复合硬化性病变,很少有症状,最常在筛查性乳房X光检查时检测到。由于其星状结构,这些病变在影像学上,可能类似于IC,但据报道,射线可透中心的存在,强烈支持放射状疤痕。使用乳腺影像报告和数据系统(BIRADS)评估时,大多数病变被归类为4级(疑似恶性肿瘤)。
大体观察,这些病变可能产生针状外观,类似于IC。在显微镜下,管状/腺体结构的增生,具有典型的放射状排列,可能会产生浸润性管状癌的假象,特别是在低倍或CNB上。仔细辨认中央纤维弹性组织巢、小管未延伸至外周脂肪、无细胞学异型以及两种细胞类型的存在,可以做出正确诊断。由于小管的塌陷,可能难以识别外围MEC层。IHC通常对于鉴别诊断有帮助(图 2),但由于细胞衰减,MEC也可能难以观察,尤其是在p63核染色(参见肌上皮细胞免疫组织化学部分)。
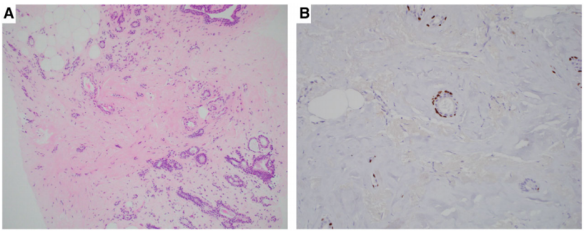
图2.(A)径向疤痕,其中可见截留和塌陷的小管,被MEC的衰减层(H&E)覆盖。(B)即使在IHC(p63染色)上,MEC 也可能难以识别。
伴随良性变化,常见的为上皮增生、囊肿形成、乳头状瘤病和硬化性腺病。多达三分之一的病例,会出现更严重的病变,例如扁平上皮异型、非典型导管增生、DCIS或浸润性乳腺癌(IBC)。CNB诊断的放射状瘢痕/复杂硬化性病变,应按照相关标准进行评估。
放射状疤痕/复杂硬化性病变的增殖期,可能显示腺鳞状细胞增生,当呈红色时,可能会引起诊断医师对低级别腺鳞癌的怀疑。在这种情况下,建议手术切除,以检查周围的乳腺组织,在低级别腺鳞癌中,浸润性腺鳞状细胞巢通常会累及周围乳腺组织。
硬化性腺病
硬化性腺病,是一种以小叶为中心的良性病变,经常在乳房活检,以及其他乳房疾病切除术中偶然发现的,也是放射状疤痕/复杂硬化病变的一个组成部分。硬化性腺病累及的多个小叶,可能合并形成肿块,有时称为“结节性腺病”。
受影响的小叶通常会增大,腺体结构的数量会增加,这些腺体结构,会因间质胶原蛋白的积累,而被压缩、拉长和扭曲。单个腺体由上皮细胞和MEC包裹,后者经常增生。早期病变往往是细胞性的,并可能产生梭形细胞外观,钙化很常见。
明显的腺体变形,可能会导致轮廓不规则,以及索状生长模式,并延伸到脂肪中。这种外观可能,会被误认为是ILC病灶,特别是当标本中也含有ILC时,可能导致高估疾病范围和错误评估边缘状态(图 3A )。
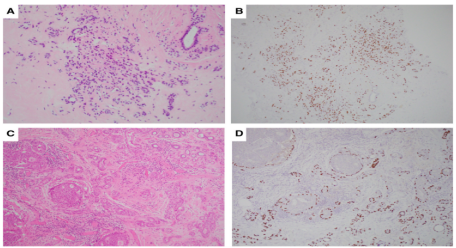
图3.(A)硬化性腺病可以模仿ILC。(B)p63染色突出显示与硬化性腺病相关的MEC。(C)涉及硬化性腺病的 DCIS,与淋巴细胞相关,类似于IC。(D)p63染色突出显示MEC并有助于解释为涉及硬化性腺病的DCIS。
大汗腺改变引起的硬化性腺病和原位癌,可能与IC相似。花状小叶原位癌(LCIS)在硬化性腺病上的定植,可能会导致受影响的小叶融合,从而掩盖周围的肌上皮细胞、间质和腺泡结构,导致IC样外观。DCIS对硬化性腺病的参与,也可能被误解为IC。这在广泛的DCIS病例中,尤其成问题,伴有硬化小叶和伴随的腺周淋巴细胞定植,可以模仿高级IC的形态(图 3C,D)。在硬化性腺病中,也可能观察到神经周围浸润,如果病理医师没有意识到这一缺陷,可能会导致误诊。
硬化性腺病,是最常被误诊为恶性的乳腺良性病变。对正确诊断最有帮助的线索,是在低倍H&E上观察到受影响的小叶,以小叶为中心的排列,并且尽管腺体可以延伸到脂肪中,但它们不会破坏它。(图3A、B )。外周MEC层的IHC染色非常有用,特别是在原位癌涉及的硬化性腺病病例中,用于排除IC。
微腺腺病
微腺腺病是一种罕见的浸润性乳腺病变,形态可能类似于乳腺管状癌。微腺腺病的小管通常是圆形的,被基底膜包围,内衬单层上皮细胞,S100阳性(图 4),ER、PR和HER2呈现阴性。该病没有外周MEC 层,小管游离在基质和脂肪中,没有伴随的基质反应。最初这种疾病,被认为是一种完全良性的病变。然而目前,微腺腺病是三阴性乳腺癌(TNBC)的可能前驱病变。与管状癌的区别,对于确保适当的治疗很重要。微腺腺病通常通过手术切除,而无需辅助治疗。微腺腺病,包括非典型形式,与乳腺腺泡细胞癌具有共同的形态和分子特征。这两种疾病都缺乏外周MEC,在腺泡细胞癌的背景下,类似于非典型微腺腺病的非典型实体簇,应被视为腺泡细胞癌谱的一部分。
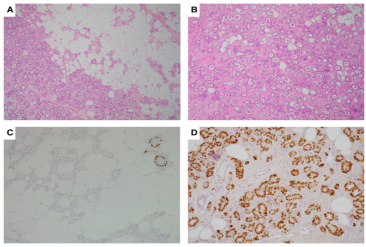
图4. 微腺腺病。(A)微腺腺病具有浸润性外观,脂肪中可见小管。(B)小管含有嗜酸性分泌物。(C)小管缺乏外周MEC层,与混合的正常腺体乳腺组织(p63染色)形成对比。(D)微腺腺病S100阳性。
导管内乳头状瘤
不伴有UDH的良性导管内乳头状瘤,很少与有包膜或实性乳头状癌混淆,这是因为其保留的结构、发育良好的纤维血管结缔组织核,被上皮和MEC覆盖,以及可见清晰的外周MEC层。导管内乳头状瘤内的UDH 很常见,但通常是局灶性的,伴有大汗腺化生,很少造成诊断困难。然而在一些病例中,导管内乳头状瘤伴有大量UDH,并可见有丝分裂,类似于DCIS的实体外观(图5 )。鉴别两种疾病,需要IHC的支持。
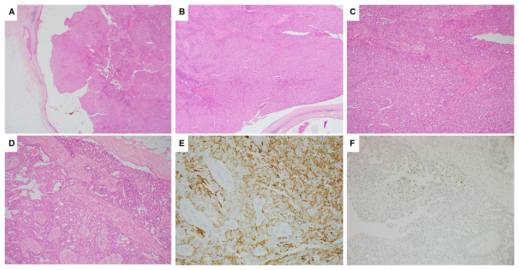
图5.(A–D)伴有旺盛UDH的导管内乳头状瘤,可能与形态上与实性乳头状癌相似。(E,F)CK5/6和ER的特征性镶嵌染色模式,证明了上皮增殖的多克隆性质,支持伴有丰富UDH的导管内乳头状瘤的诊断。
CNB后导管内乳头状瘤,可能发生梗死,并发展为鳞状化生,类似于化生癌或粘液表皮样癌的表现,这种情况很少见。病变周围纤维化引起的残余活导管上皮的扭曲,也可能与IC相似。病变的低倍外观、不存在恶性肿瘤的细胞学特征,以及外周MEC的存在,是排除IC诊断的有用标准。上皮细胞沿针道移位,可能发生在CNB之后,不应被误认为是癌。
具有粘液样基质的良性乳腺病变
纤维腺瘤是CNB常见且通常直接的诊断。在极少数情况下,具有突出的粘液样间质和稀疏腺体成分的纤维腺瘤可能会产生基质产生癌的印象。意识到这种潜在的陷阱和放射学-病理学的相关性应该可以避免误诊。
多形性腺瘤在乳腺中很少见,由于突出的粘液样间质含有轻度非典型上皮细胞,可能表达基底型CK且激素受体阴性,因此在CNB上可能会出现混淆的外观。
梭形细胞/间充质病变
乳腺良性梭形细胞病变(SCL)包括多种情况,其中一些病变在组织学上表现出类似恶性肿瘤的形态学特点,尤其是CNB。对于所有乳腺病变,除了评估H&E和IHC结果外,还应调查临床病史,包括症状持续时间、放射学发现和病变的精确解剖位置,这可能有助于避免误诊。一些专家建议,将SCL分为“温和表现”和“恶性表现”,这样分类,鼓励进行广泛的鉴别诊断,并在出现恶性表现病变时,考虑良性诊断,反之亦然,如下所述(恶性情况可能被解释为良性)。
可能被误诊为恶性的良性乳腺SCL,包括瘢痕、纤维瘤病、结节性筋膜炎、肌纤维母细胞瘤和细胞假性血管瘤样间质增生。罕见的良性乳腺SCL,包括炎性肌纤维母细胞瘤、孤立性纤维瘤、梭形细胞脂肪瘤、良性平滑肌和神经肿瘤、腺肌上皮瘤的梭形细胞变体、细胞硬化性腺病和肌样错构瘤。
瘢痕
疤痕组织在CNB上很常见,通常用于评估钙化或肿块病变,一些患者有同侧乳房手术史或乳房外伤史,因此,在分析乳房SCL时,应要与疤痕鉴别。最近的疤痕,可能表现为具有非常活跃的成纤维细胞的增殖,在其最旺盛的阶段,可以形成术后梭形细胞结节。了解任何相关的临床病史,并寻找伴随的变化,例如含铁血黄素沉积、泡沫状巨噬细胞、脂肪坏死和异物巨细胞,有助于诊断(图6 )。瘢痕组织可能表达SMA,CK、p63、CD34和β-catenin均为阴性。
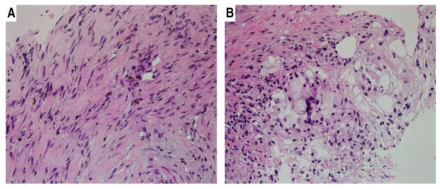
图6.(A)含铁血黄素沉积(H&E)的梭形细胞增殖。(B)相关脂肪坏死(H&E)。这些特征支持疤痕的诊断。
纤维瘤病
纤维瘤病是一种罕见的乳腺病变,其形态与纤维瘤样MBC(下文讨论),有明显的相似性。两种病变都倾向于具有浸润性轮廓外观,并伴有外周脂肪和淋巴细胞炎症。纤维瘤细胞缺乏细胞学异型性,有丝分裂难以识别(图7A),这种病变可能会在局部复发。
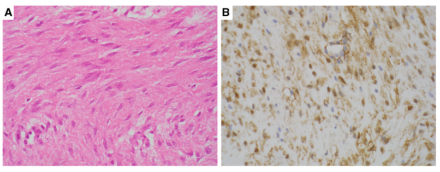
图7.纤维瘤病。(A)H&E染色显示细胞学上温和的梭形细胞增殖;(B)纤维瘤病的核β-catenin。
β-catenin核染色(图7B)和SMA细胞质染色,是IHC的特征性表现。CK、p63和CD34通常为阴性。
结节性筋膜炎
结节性筋膜炎,也是一种罕见的良性乳腺SCL,可能有快速生长史,通常是自限性的。成纤维细胞通常具有星状结构,具有相对温和的外观和羽毛状生长模式。基质可以是粘液样或胶原质,并含有渗出的红细胞(图 8)。一些病变是高度细胞化的,伴有频繁的核分裂,可能导致误诊为恶性肿瘤。对该疾病的认识、对临床病史的了解,以及对不存在异常核分裂的认识,将有助于避免这种诊断陷阱。结节性筋膜炎的细胞,SMA是阳性。CK和p63为阴性。
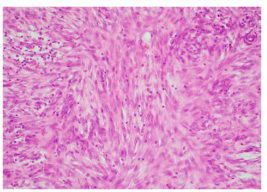
图8.结节性筋膜炎。H&E染色显示,成纤维细胞组成的梭形细胞增生,外观相对温和,并伴有一些外渗的红细胞。
细胞假性血管瘤性间质增生(PASH)
由于假血管通道的相互连接,细胞假性血管瘤性间质增生(PASH),可能被误认为是血管肉瘤。在这些通道中,排列着相对温和的纺锤形肌成纤维细胞,并且不含红细胞(图9),这会提醒病理医师做出正确的诊断。内衬细胞为CD34和PR阳性,可表达actin和desmin。其他血管标志物均为阴性。
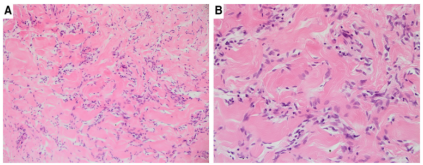
图9.(A,B)假性血管瘤性间质增生(PASH)。
肌纤维母细胞瘤
乳腺肌纤维母细胞瘤,可能类似于梭形细胞MBC。放射学上通常界限清楚的病变性质,以及H&E上的蛛形纲纤维和介入脂肪细胞的识别,可能有助于病理医师做出正确的诊断。除ER外,肌纤维母细胞瘤细胞通常呈CD34、SMA和desmin阳性。CK和p63是阴性的。
如前所述,肌纤维母细胞瘤的上皮样变体,可能类似于ILC,由于ER阳性,而进一步可能出现假阳性诊断(图10)。
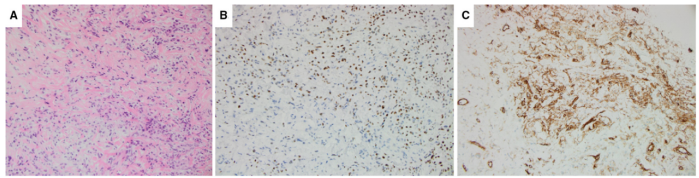
图10.(A)上皮样肌纤维母细胞瘤可能类似于ILC(H&E)。(B)肌纤维母细胞瘤细胞表达ER。(C)CD34染色肌纤维母细胞瘤。
嗜酸性粒状病变
组织细胞炎症和颗粒细胞瘤等乳腺嗜酸细胞性病变的鉴别诊断,包括嗜酸细胞癌和大汗腺癌。
组织细胞炎症
大量组织细胞性炎症,可能由导管或囊肿破裂引起,或继发于先前的乳房手术。在组织学上,可能类似于大汗腺癌形态学表现,特别是在CNB上(图11 )。组织细胞为CD68阳性和CK阴性。
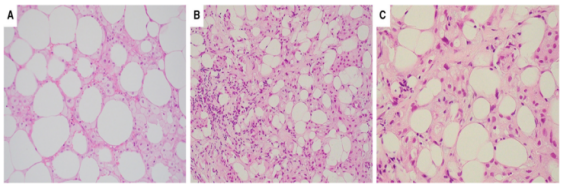
图11.(A)组织细胞炎症(H&E),可能类似于B和C中显示的组织细胞样癌(H&E) 。
颗粒细胞瘤
颗粒细胞瘤是一种罕见的、良性的乳腺肿瘤,通常发生在女性身上。它具有浸润性生长模式,可能在临床和组织学上,都与IC相似。由于溶酶体的积累,肿瘤由圆形或多边形细胞组成,具有丰富的嗜酸性粒状细胞质,可能与大汗腺癌相似。可以看到神经周围和血管周围的受累,并且位于真皮的病变,可能与覆盖的假性上皮瘤样增生有关,存在误诊的可能性。正确诊断的线索,包括确定小的、位于中心的、深染的细胞核、稀少的核分裂,以及模糊的细胞边界。病变细胞呈S100强阳性,同时呈CD68和NSE阳性。CK、melan-A和HMB45均为阴性,可将此肿瘤与癌和黑色素瘤区分开来(图 12)。
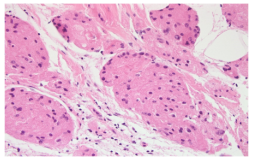
图12.颗粒细胞瘤(H&E)。
其他
针刺操作后上皮细胞移位
乳腺组织中的上皮细胞移位,可能发生在诊断性针刺操作之后,并导致进行后续切除的标本判读困难。如上所述,这种现象最常见于乳头状病变, 也可见于男性乳房发育抽脂术后、桡骨瘢痕活检、DCIS和IC穿刺活检后。
虽然移位的上皮细胞,被认为在生物学上无关紧要 ,但它们在上皮基质界面或血管通道内,没有MEC 层的乳腺组织中的存在,可能会误诊为IC。恶性肿瘤中上皮移位的存在,可能会影响肿瘤/病变大小和边缘状态的评估,并导致淋巴血管浸润(图13)和IC的过度诊断,特别是在DCIS 中,具有潜在的临床诊断意义。IHC不协助区分移位的上皮细胞与IC病灶,因为它们通常没有MEC层。通过了解先前的针刺程序,以及伴随的组织学变化,包括出血、肉芽组织、急性和慢性炎症,以及脂肪坏死和空泡化和富含含铁血黄素的巨噬细胞的积累,有助于正确判断移位的上皮细胞。
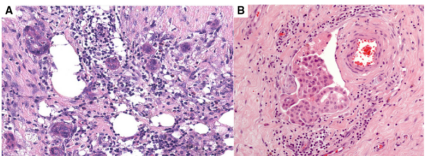
图13.(A)上皮移位可能模仿IC(H&E);(B)良性导管内乳头状瘤患者淋巴管腔内的上皮移位,类似于淋巴血管浸润。
相反,有包膜的乳头状癌的早期浸润性病灶,可能伴有退行性间质变化,造成上皮移位的假像。区别特征包括早期侵袭的多灶性与反应性间质变化。后者是由于囊性乳头状结构的反复破裂形成,而不是继发于诊断性针刺操作。
DCIS的人为移位(“牙膏效应”)
与针刺操作无关的DCIS人工移位(ADDCIS),可能继发于乳房标本的机械压迫,可能误诊为IC。研究者 Shabihkhani报道了16例与针道变化无关的ADDCIS病例,大多数发生在乳房肿瘤切除标本中;病灶的大小范围为1到5毫米,并且涉及非小叶分布的乳腺间质。所有测量>4mm的病灶,都显示出线性位移模式,这是一个有用的诊断标准。污迹斑斑的染色质,以及没有基质反应,也是有用的诊断线索。类似于针刺操作后移位的上皮,MECIHC为阴性。可获得随访的患者均未发生转移,表明ADDCIS不属于IC 。
胶原小球症
胶原性小球病,是一种相对罕见的良性病变,其特征是无细胞、嗜酸性或嗜碱性基质沉积物,被基底膜、肌上皮细胞和导管上皮细胞包围。这通常是偶然发现的。LCIS可能涉及胶原小球体,产生具有筛状外观的“碰撞”病变,可能被误认为是低级别筛状DCIS。
两种病变的特征,都是小细胞与均匀细胞核和圆形、穿孔空间的结合。识别间隙内的嗜酸性基底膜,或嗜碱性粘液样物质,观察筛状间隙周围无极化上皮细胞,并注意到增殖由具有胞浆内空泡的粘附性异常的上皮细胞组成,可能会促使病理医师考虑这一诊断。
意识到这一疾病可能会促使病理医师使用IHC,进一步考虑活检结果,并避免误诊低级别DCIS。LCIS 细胞通常为E-cadherin阴性,而DCIS细胞为E-cadherin阳性。MECIHC将在胶原球体空间周围展示MEC,而 DCIS的筛状空间,没有MEC排列(图14)。
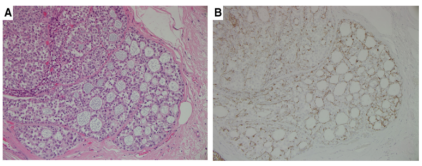
图14.(A)由LCIS(H&E)定植的胶原小球。(B)E-cadherin在LCIS中呈阴性。
由于基底膜样物质的存在,胶原小球体也可能类似于腺样囊性癌。与腺样囊性癌相反,胶原性小球体很少形成肿块病变,通常为c-kit(CD117)阴性。
泌乳变化
哺乳期变化可伴有显着的细胞核变化,包括核肥大、多形性和鞋钉样外观,这可能会误诊为扁平型或分泌过多型DCIS的诊断(图15 )。DCIS的诊断,仅限于结构异型性的病例,包括筛状、实性或微乳头状生长模式,以及明确的中央(粉刺型)坏死或HER2IHC阳性(IHC评分3+)。p53的表达、高Ki67评分也有利于DCIS的诊断。
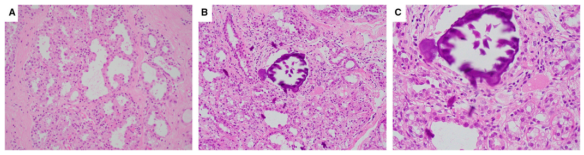
图15.泌乳变化。(A)泌乳变化(H&E)。(B, C)泌乳变化与磷酸钙沉积。
甲状腺样腺病
分泌过多的甲状腺样腺病,是最近描述的一种罕见疾病,由多个大小不等的扩张腺体组成,具有保留的小叶结构,并含有致密的嗜酸性淀粉酶PAS阳性胶体样分泌物。腺体由ER阴性上皮细胞排列,并被致密的基底膜包围,外围MEC不存在。上皮细胞不显示细胞学异型或有丝分裂活性,如果存在,则应怀疑IC。
淋巴结中的异位乳腺组织
腋窝淋巴结中异位乳腺组织的存在,可能被误解为淋巴结转移,尤其是当乳腺组织出现增生性改变时。
可能被误诊为良性的恶性疾病
一些恶性乳腺病变可能看似平淡无奇,常误诊为良性、增生性或局部浸润性。一些侵袭性肿瘤,由于其惰性生物学行为,也更适合归类为原位病变。
——未完待续——
点此下载原文献




























共0条评论