[导读] 本文作者:薛德彬
往期回顾:
乳腺浸润性癌病理模板
CAP模板
一、乳腺浸润性癌切除标本(注释)
2022年6月 v4.7.0.0
注释
A.手术方式
乳腺标本类型和手术方式的以下类型,可写入病例摘要中:
乳腺切除术标本:手术切除乳腺组织,而不是试图切除整个乳房。常不包括乳头。切除术标本包括“部分乳腺切除术”、“肿块切除术”和“象限切除术”标本。
全乳腺切除术:切除全部乳腺组织,一般包括乳头和乳晕。
· 单纯乳腺切除术:该术式切除全部乳腺组织但不切除腋窝淋巴结。
· 保留皮肤的全乳腺切除术:切除全部乳腺组织和乳头,仅切除周围狭窄的一圈皮肤。
· 保留乳头的全乳腺切除术:切除全部乳腺组织,保留皮肤或乳头。检查乳晕下组织,如果有癌累及,再切除乳头。
· 改良乳腺根治术:该术式是全部乳腺组织切除和腋窝淋巴结清扫。在病例摘要中分开记录乳腺和淋巴结标本状况。有时会切除少部分胸肌。
· 乳腺癌根治术:该术式切除全部乳腺组织、胸大肌、胸小肌以及腋窝淋巴结。这种标本类型和手术方式可以写入病例摘要的“其他”项中。
病例摘要旨在报告有最大浸润性癌灶的患者标本。如果同一手术中,进行了额外的切缘切除,其结果写入“切缘”评估项中。如果在切除的主要切缘或边缘切缘中另有较小的浸润性癌灶,癌灶的特征(即大小、组织学类型和组织学级别)应记录在“其他发现”项中。如果较小浸润性癌灶表现为不同的组织学类型或组织学级别,推荐进行辅助检查。如果是事后行切缘切除(如另外一天),标本中无更大的浸润性癌灶,不必写入病例摘要中。
如果患者一次手术过程中分两次切除同侧两个浸润性癌灶,应将较大的浸润性癌写入病例摘要中。较小浸润性癌的报告可以不使用病例摘要。如果患者于不同日期分别切除同侧两个浸润性癌,较大浸润性癌应记录于病例摘要,参照美国癌症联合委员会(AJCC)分期系统的T分类来报告该癌。如果患者有两侧乳腺癌,应在两个病例摘要中分开报告。
如果将其他标本的信息写入病例摘要(如,之前粗针活检的激素受体结果或之前淋巴结活检的转移情况),应在“备注”项清楚注明,并记录其他标本的病理号。
以下类型的标本不应使用该模板:
· 很小的切开活检标本(包括粗针活检标本)
· 活检部位大部分癌灶切除后的二次切除标本
浸润性癌标本取材有以下目的1-5:
· 因临床或影像学发现病变而手术,必须镜下检查这些病变。如果是影像学发现的病变而临床未触及,有必要对标本行钼靶和/或其他影像学检查,以识别病变。如果可行,应将全部病变或有影像学异常的整个区域按顺序取材,提交病理检查。
· 如果标本以DCIS为主伴微浸润,推荐完整提交全部标本,或至少全部提交肉眼有癌累及的整个区域,以确定其他区域有无癌浸润和/或淋巴管-血管侵犯。
· 所有的其他大体可见的病变都必须取材。
· 必须评估每个指定的切缘有无浸润性癌和DCIS累及。如果标本已被切开或切碎,应注明,因为会影响评估切缘状况。
只能在不影响评估浸润性癌、淋巴结等预后因素及切缘状况的情况下,可以用组织学检查剩余的组织做研究分析(如RT-PCR)。
最好是单次手术完整地切除整个癌灶。如果标本已被切开或切碎,则可能无法准确地评估切缘。如果超过1块碎片组织中有浸润性癌,则很难或不可能判断浸润性癌灶的病理大小或出现浸润性癌灶的数量。对方对这些病例结合乳腺影像学检查,并可用于确定pT。当标本破碎,影响评估肿瘤大小和/或切缘时,应将该信息写入“其他发现”项中。
大体描述应记录所有标本的三维大小。最终诊断里也可以报告标本大小。切除组织的体积有助于估计癌的范围,并确定可能需要切除多大组织才能获得阴性切缘。
如果是单独切除并送检的有定向的切缘,其最终切缘状况可写入病例摘要的“切缘”项里。如果未定向,可记录在“其他发现”项中。
B.肿瘤部位
由外科医生、乳腺影像学资料或以前病理报告提供的浸润性癌部位,有助于资料整合,将患者之前的检查(如,粗针活检)或后来的活检或癌症事件结合分析。肿瘤部位可以用象限和/或钟面位置表示。
乳腺切除术标本可确定肿瘤大概部位。然而,因切下的标本摆放位置与其原来在胸壁位置存在差异(即,表面椭圆形的皮肤可以是水平位的或朝向腋窝),肿瘤部位有时候很难与活体确定的位置准确对应。如果可能,参考临床或影像学肿瘤部位有助于定位癌灶。
如果患者术前(新辅助)治疗过,手术标本中没有残留的浸润性癌,其肿瘤部位参考之前的浸润性癌灶(即,瘤床)。
References
1. Association of Directors of Anatomic and Surgical Pathology. Immediate management of mammographically detected breast lesions. Hum Pathol. 1993;24:689-690.
2. Connolly JL, Schnitt SJ. Evaluation of breast biopsy specimens in patients considered for treatment by conservative surgery and radiation therapy for early breast cancer. Pathol Annu. 1988;23(pt 1):1-23.
3. Schnitt SJ, Wang HH. Histologic sampling of grossly benign breast biopsies: how much is enough? Am J Surg Pathol. 1989;13:505-512.
4. Schnitt SJ, Connolly JL. Processing and evaluation of breast excision specimens: a clinically oriented approach. Am J Clin Pathol. 1992;98:125-137.
5. Lester SC. Manual of Surgical Pathology. 3rd ed. New York, NY: Elsevier; 2010.
C.组织学类型
本模板适用于乳腺的所有浸润性。推荐WHO乳腺癌分类,但本模板不排斥使用其他的组织学分类系统。可以根据HE染色而不需要免疫组化检测进行乳腺癌分类。
根据最常见的浸润性癌类型和广泛使用的术语,在病例总结中提供修改的列表。修改是为了涵盖大多数肿瘤,减少将肿瘤报告为“其他”。对于具有混合特征的肿瘤,和具有部分而不是全部特定组织学类型特征的肿瘤,增加了选择。
WHO 浸润性乳腺癌分类1
□无残留的浸润性癌
□非特殊型浸润性癌(浸润性导管癌,非特指)
□微浸润性癌
□浸润性小叶癌
□浸润性癌伴混合性导管和小叶特征
□浸润性癌伴混合性特征(注明)
□小管癌
□浸润性筛状癌
□黏液癌
□浸润性微乳头状癌
□大汗腺腺癌
□包裹性乳头状癌伴浸润
□实性乳头状癌伴浸润
□导管内乳头状腺癌伴浸润
□腺性囊性癌
化生性癌
□化生性癌NOS
□低级别腺鳞癌
□纤维瘤病样化生性癌
□梭形细胞癌
□化生性癌伴间叶性分化
神经内分泌肿瘤
□神经内分泌肿瘤NOS
□神经内分泌肿瘤,1级
□神经内分泌肿瘤,2级
神经内分泌癌
□神经内分泌癌NOS
□神经内分泌癌,小细胞
□神经内分泌癌,大细胞
□浸润性癌,类型无法确定(说明原因):
□其他组织学类型
□浸润性乳头状癌
□嗜酸细胞癌
□富于脂质的癌
□富于糖原的癌
□皮脂腺癌
□粘液性囊腺癌NOS
□腺泡细胞癌
□典型腺样囊性癌
□实性-基底样腺样囊性癌
□腺样囊性癌伴高级别转化
□分泌性癌
□黏液表皮样癌
□高细胞癌伴极性翻转
□腺肌上皮瘤伴癌
□上皮-肌上皮癌
□以上未列出的其他组织学类型(注明):
References
1. WHO Classification of Tumours Editorial Board. Breast tumours. Lyon (France): International Agency for Research on Cancer; 2019. (WHO classification of tumours series, 5th ed.; vol. 2).
D.组织学分级
所有的浸润性乳腺癌应有分级1。报告应使用Nottingham组织学分级(Scarff-Bloom-Richardson分级系统Elston-Ellis 修改版)。每一临床分期组中,组织学分级与预后相对应。
Nottingham组织学分级评估腺管状结构形成的数量、核多形性程度和核分裂象数目(或核分裂率)。每项变量记为1、2或3分,三项相加产生组织学级别。核分裂象评分通过计数肿瘤核分裂最活跃区连续10个高倍镜(HPF)确定。只计数可以清楚辨认的核分裂,不包括核深染、核碎裂和核凋亡。因视野大小不同,须根据每个显微镜HPF大小,相应地确定合适的评分值。推荐用毫米测量视野大小。当然,HPF直径也可以通过下列方法计算。
用标尺测量HPF大小
用清晰的标尺测量一个低倍视野的直径。用这一数值通过下列公式计算一个常数:
目镜放大倍数×物镜放大倍数×镜下视野直径=一个常数
当常数值已知,用下列公式可以计算其他倍数物镜一个高倍视野的直径:
未知视野直径=常数/(目镜放大倍数×物镜放大倍数)
视野直径的一半是视野半径(r),可用于计算HPF面积:
3.1415×r2=镜下视野面积
如果镜下视野直径或视野面积已知,可以用表1确定不同评分值相对应的核分裂数。
表 1 视野直径和核分裂计数对应的分值
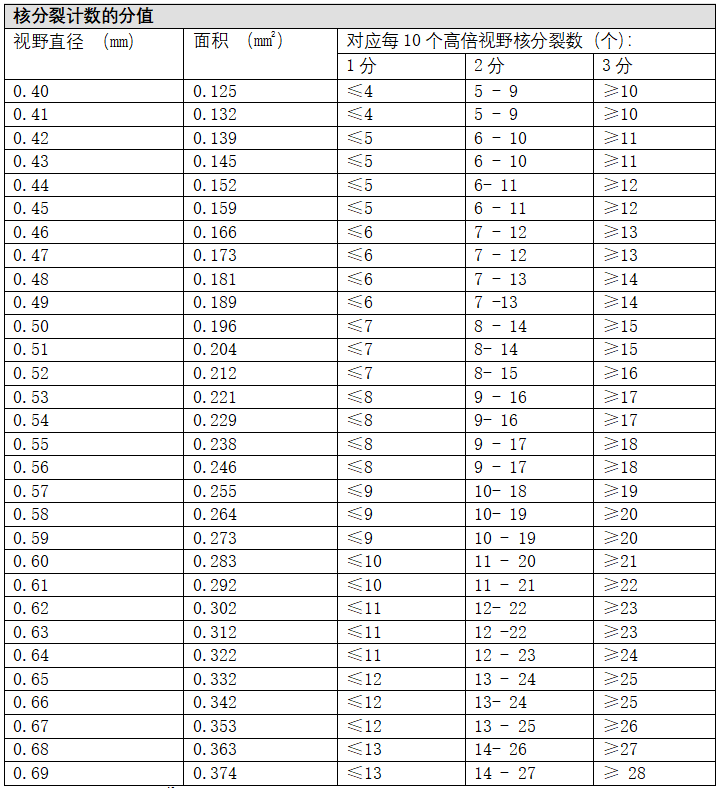
摘自乳腺疾病病理报告2。2005年版国家卫生服务癌症筛查方案和英国皇家病理学院。经许可改编。
References
1. Ellis IO, Elston CW. Histologic grade. In: O’Malley FP, Pinder SE, eds. Breast Pathology. Philadelphia, PA: Elsevier; 2006:225-233.
2. Royal College of Pathologists. Pathology reporting of breast disease in surgical excision specimens incorporating the dataset for histological reporting of breast cancer. June 2016.
https://www.rcpath.org/profession/publications/cancer-datasets.html. Accessed September 18, 2018.














共0条评论