[导读] 编译整理:强子
口腔上皮异型增生的细胞学特征
外科病理医师一般都很熟悉细胞学方面的非典型特征,其实不同的器官系统中这些特征都是相同的。口腔上皮异型增生的细胞学特征有:细胞和细胞核具有多形性,细胞的大小和形状不一,细胞核大小和形状不一;细胞核增大且有多个核仁;有核分裂并有非典型核分裂;黏膜表浅部分可见核分裂及凋亡。
口腔上皮异型增生的分级
口腔上皮异型增生不同病例间的结构非典型和细胞学非典型差别颇大,表明各自出现恶性转化的风险不同。并非所有的病例都进展为口腔鳞状细胞癌,但一般结构和细胞学非典型程度越重、出现恶性转化的风险越高。根据这一概念,也就有了提示口腔上皮异型增生恶性转化风险的分级方案。1969年提出了第一个分级方案,鉴于观察者自身及观察者间重复性方面的问题,后续又提出了多项分级方案。
目前最广为接受的分级方案是根据出现细胞学非典型和结构非典型的黏膜所累及范围来确定分级的三级方案:局限于黏膜下三分之一者归为低级别,累及下三分之二者归为中级别,累及全层者归为高级别或重度异型增生。该方案中,重度异型增生视为原位癌的同义词。
评估分级时,需要注意非典型的背景及整个组织的背景。比如,局限于基底带的显著增大、多形、深染细胞核,无任何炎症背景,可能提示重度异型增生;如背景伴有显著炎症细胞浸润,则细胞非典型的分级可能需“下调”。
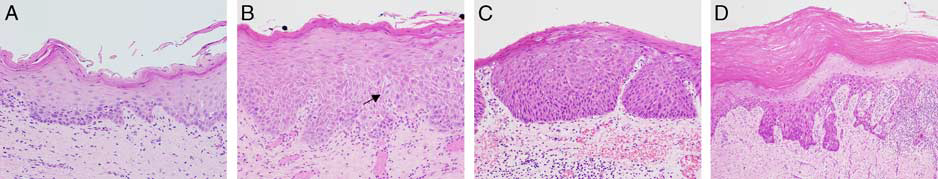
图1. 根据细胞学及结构非典型累及黏膜的范围而做的口腔上皮异型增生三级分级方案。(A)表层有角化不全,基底层细胞核增大、深染且大小不一,有轻度的细胞黏附性缺失表现,这些特征可解读为低级别异型增生;(B)非典型累及下三分之二,解读为中级别异型增生;病变中可见表层角化不全、表皮突呈水滴状拉长,黏膜下层可见细胞角化表现,而表浅部分可见核分裂(黑色箭头所示);(C)高级别异型增生累及的黏膜范围超过了三分之二或累及全层,可见角化不全、层次显著异常、细胞核极向缺失、成熟现象缺失、表层出现细胞核增大。(D)基底层黏膜出现显著细胞学非典型表现时,可能分级需上调至重度或高级别异型增生。
口腔上皮异型增生的分级其实代表的是病变的谱系性,但分级方案高度主观,且是对病变过程的人为评估。尽管存在这样的问题,但HE切片中对口腔上皮异型增生的分级还是可以用于恶性转化的风险评估,并对患者的后续处理起到关键作用。有报道称,15年时间内出现恶性转化的几率在低级别异型增生约为6%,中级别异型增生为18%,高级别异型增生为39%。大部分单位对于低级别异型增生采取保守治疗方案,控制危险因素并持续随访,出现临床可疑改变时(如病变的颜色和质地不均、黏膜糜烂加重、显著溃疡)再次活检。中级别及高级别异型增生患者则可能需切除病变。不过,相关决策取决于多个因素,如要结合年龄、性别、相关危险因素、病变部位、病变大小、持续时间、近期的临床改变(如溃疡加重)等。
口腔上皮异型增生诊断中的分子方法
尽管分子病理已有显著进展,但口腔上皮异型增生的诊断仍主要依赖于组织病理学评估并结合临床。口腔上皮异型增生的分子表现是一个逐渐进展为鳞状细胞癌的相关分子改变的多步骤过程,具体包括杂合性缺失、拷贝数改变、体细胞性突变、超甲基化等。
相关分子改变中最为显著的,是3p和9p的杂合性缺失;癌前病变中检出的其他分子改变还有EGFR表达增加、cyclin D1扩增、Rb缺失、p53的突变型表达。已有研究尝试用相关分子改变的免疫组化替代指标来对口腔上皮异型增生进行诊断和分级,尤其是p53和Ki-67,但尚未完全证实其在临床实践中的意义。
未完待续
往期回顾:
当口腔上皮遇到异型增生(一)
当口腔上皮遇到异型增生(二)














共0条评论