[导读] 译者:慧海拾穗
【摘要】
背景:巨大的先天性黑素细胞痣(GCMN)发生于约0.1%的活产儿中。大约6%的病例可能会发展为恶性黑色素瘤。儿童和成人的恶性黑色素瘤都可能源于巨大的先天性痣。高达95%的GCMN携带NRAS突变,也可存在BRAF、MC1R、TP53和GNAQ基因突变。个体化治疗是必要的,但诊断和预后标准仍然存在争议。
病例报告:例1是出生一个月患儿出现巨大先天性痣的黑色素瘤并发神经皮肤黑素病(neurocutaneous melanosis);例2是患儿出生后6个月内出现巨大先天性痣的黑色素瘤。对肿瘤组织进行病理、免疫组织化学和遗传分析。病例1只显示TP53基因的非致病性P72R多态性。病例2检测到NRAS基因Q61K突变。
结论:恶性黑色素瘤与GCMN伴发是罕见的,因此知之甚少。预后与诊断分期有关,但未发现其他病理预后因素。在GCMN中最常见的遗传事件是NRAS突变。为积累改善疾病预后和预后的证据,先天性黑素细胞痣患儿应从出生开始就应纳入系统性随访研究。
【前言】
恶性黑色素瘤是儿童期一种罕见的肿瘤,占儿童恶性肿瘤的0.9%。先天性黑素细胞痣(congenital melanocytic nevus,CMN)是临床上定义的一种黑素细胞病变,存在于出生或在婴儿期由先前存在的黑素细胞发育而来。CMN通常累及躯干、四肢、头皮和颈部皮肤,但也可能累及任何其他皮肤表面。先天性黑素细胞痣通常根据大小来分类。CMN发生黑色素瘤的风险被认为与痣的大小成正比,小痣和中痣的风险在2.6~4.9%之间,大痣的风险在6~20%之间。黑素瘤的发病率和CMN的临床治疗一直存在争议,部分原因是组织学诊断的困难,部分原因是对恶性病例的报道偏多。
巨大先天性黑素细胞痣(Giant congenital melanocytic nevus,GCMN)通常被定义为一种黑素细胞病变,在出生时就存在,成年时将达到直径≥20厘米。它的发病率估计为小于1/2万新生儿,其中约6%在痣的部位发生黑色素瘤。GCMN是儿童期发生黑色素瘤的主要危险因素。目前,关GCMN应如何治疗存在巨大的不确定性。标准方法主要基于两个考虑:(1)获得可接受的美容效果,以减少患者的心理社会不适;(2)最大限度地减少恶性肿瘤的风险。然而,有临床病例描述,在摘除巨大痣后和和老年人巨大痣发生黑色素瘤。
GCMN通常是偶发的,但也有罕见的家族性病例报道。一篇单卵双胞胎GCMN不一致的报告提示可能与后合子事件(postzygotic event)有关。GCMN的病因和发病机制尚不完全清楚。目前已经提出了多种机制,如神经嵴发育缺陷、激活突变导致不受控制的黑色素细胞增殖、皮肤镶嵌现象和显性遗传。黑色素母细胞起源于神经嵴细胞,它们的增殖、迁移和分化受到复杂的相互作用的基因网络的调控。该网络的突变,如MITF和KIT基因的突变,可能还有肝细胞生长因子/c-Met信号通路的突变,可能会在胚胎发生过程中破坏色素沉着系统,导致各种先天性疾病。
另一个控制黑素细胞增殖的基因网络是RAS/RAF/MAPK信号通路。在该通路中发现了多种激活突变,涉及基因NRAS、BRAF和GNAQ。在80%的病例中,NRAS基因的后合子突变被认为是CMN形成的原因,因为在同一个人的不同皮肤病变以及受影响的神经和恶性组织中发现了相同的突变。NRAS突变通常导致61号密码子的氨基酸替换。BRAF V600E突变也可在同一患者的不止一处病变中发现,因此不能确定为因果。此外,在CMN中发现了MC1R和TP53突变,可能参与了CMN的形成。BRAF或NRAS突变的存在并不增加恶性转化的风险,进一步的突变需要CMN中黑色素瘤的形成。
儿童和成人都可能因GCMN而发生恶性黑色素瘤,这是一种双峰分布,约70%的病例发生在儿童时期。应进行鉴别诊断,以区分恶性和良性增生,这些增生可能类似于恶性黑色素瘤,但通常缺乏渐进性生长或溃疡。CMN内的良性增生是常见的,主要发生于大的或多发痣,但也不是唯一的。了解它们的特征有助于监测恶性肿瘤。除了增生性结节外,GCMN常伴有“卫星痣”,这是出生时或数月或数年后出现的较小的CMN。
只有几家大医院描述的结果与诊断时的阶段和存在严重并发症有关,如中枢神经系统的神经皮肤黑素病或黑色素瘤。神经皮肤黑素病是一种罕见的综合征,以中枢神经系统内良性或恶性增生的黑素细胞结节为特征,并与先天性黑素细胞病变相关。
迄今为止(2019年),尚未建立治疗GCMN的绝对指南,因此,这一课题仍然是皮肤外科和皮肤肿瘤学中最具争议的问题之一。我们描述了两个罕见的CMN病例:一例在出生的第一个月发生GCMN的黑色素瘤并发NCM,另一个病例在出生后6个月内发生GCMN。本文描述了这些患者的临床、病理和遗传特征,为这种罕见疾病提供了证据,并产生了建立个人诊断和预后标准所需的数据。
【病例介绍】
病例1:男,出生后22天入院,根据菲茨帕特里克分级,该患者为皮肤II型。怀孕第37周出生。怀孕期间没有并发症,也没有黑色素瘤或其他类型癌症的家族史。出生时在背部和臀部的皮肤上发现了一颗巨大的色素痣,一直延伸到耻骨和阴囊的一部分。在色素痣内,父母还注意到腰骶部有一个异常形成的中心,表面潮湿出血(图1)。临床检查发现身体背侧见一颗巨大色素痣(大于20厘米),部分为毛发覆盖,色素沉着不规则。颜色从粉红色到深棕色或黑色不等。在腰骶部发现一个快速生长的不规则黑色结节(3.5×3.7 cm),呈溃疡状(图1b)。在头发覆盖的头部、身体和四肢上有单个卫星灶。进行了皮肤镜检查。基于回顾,临床研究和皮肤镜检查,我们诊断巨大先天性痣伴卫星灶,并有先天性恶性黑色素瘤导致的腰骶部溃疡。完成淋巴结、腹部、腹膜后部分和骨盆的超声检查,以及胸部X片。2015年7月在麻醉下行局部组织整形切除活检。组织病理学显示结节状上皮样和含痣样色素的黑色素瘤(图2a),发生于先天性痣,核分裂象1个/ mm2,出现溃疡(图2b),垂直生长期,Clark侵犯3级,Breslow厚度1.5mm。没有血管侵犯。免疫组化检测黑素细胞标记物(Melan A, HMB45)阳性表达,肿瘤细胞Ki67增殖指数为20~30%(图3)。使用诊断生物芯片(EIMB RAS,俄罗斯)对肿瘤组织进行遗传分析,以检测BRAF、NRAS、KIT、GNAQ、GNA11、MAP2K1和MAP2K2基因中最常见的体细胞突变。上述基因均未检测到突变。此外,下一代测序用于NRAS、PDGFRA、KIT、RASA1、RAC1、MET、BRAF、PTEN、AKT1、MAP2K1、MAP2K2、TP53和TERT基因的外显子分析。通过Sanger测序分析CDKN2A基因的外显子,确定生发突变。结果仅发现TP53基因72密码子Arg/Arg多态性,不具有致病性。全身磁共振成像(MRI)显示大脑结构中存在黑色素。黑色素中心的MRI未显示黑色素瘤转移,为典型的NCM(图4)。这一发现说明了对巨大先天性痣患儿进行MRI检查的重要性。患者无癫痫等局灶性神经系统症状,无颅内压升高的体征和症状。根据患者病理资料及全面检查,诊断为黑色素瘤T2bN0M0期IIA + NCM,建议动态观察。目前(2018年6月)患儿正在观察中,无疾病进展症状。局灶软脑膜沉积物是稳定的。
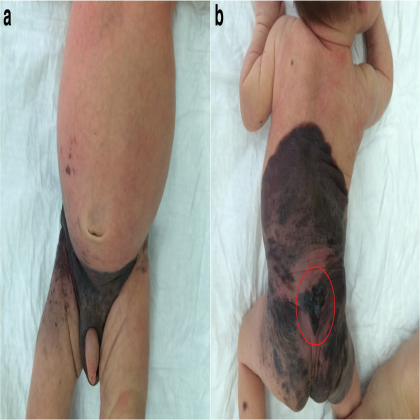
图1 患者,22天。背部和臀部的皮肤上发现了一颗巨大的色素痣,一直延伸到耻骨和阴囊的一部分。腰骶部诊断为结节(用红色圆圈标记)。
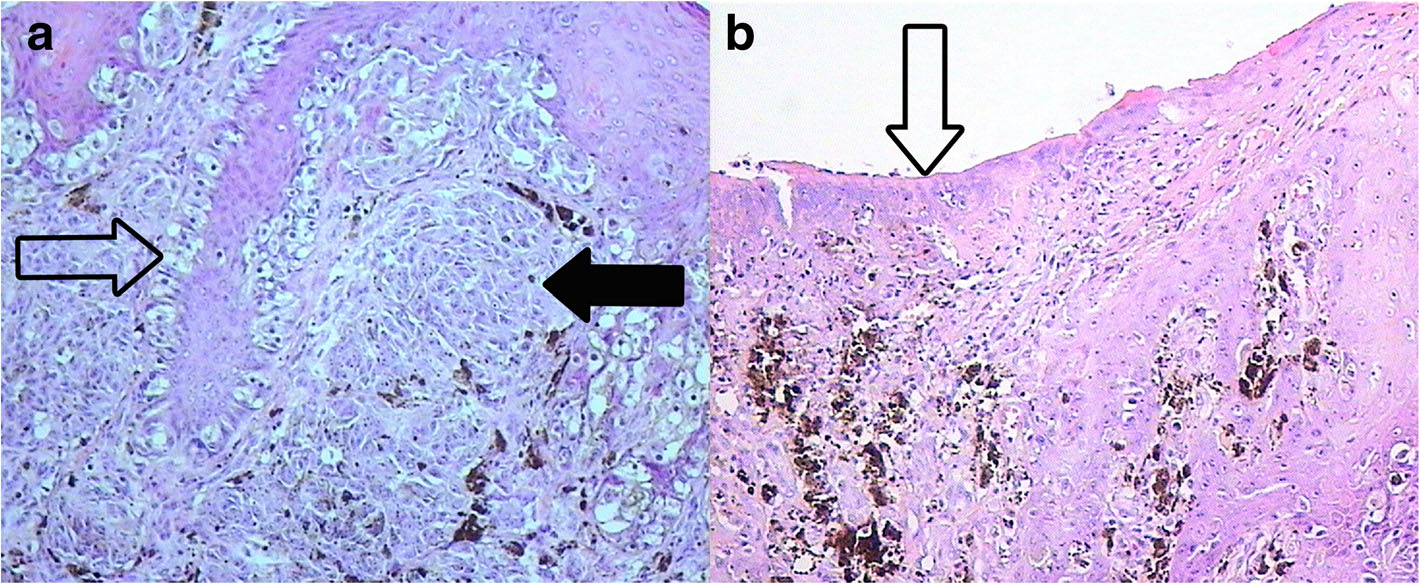
图2 皮肤黑色素瘤:(a)结节性黑素瘤的真皮表皮基底层多形黑素细胞(透明箭头),巢状(黑色箭头)分布;(b)肿瘤表面可见溃疡(箭头)。
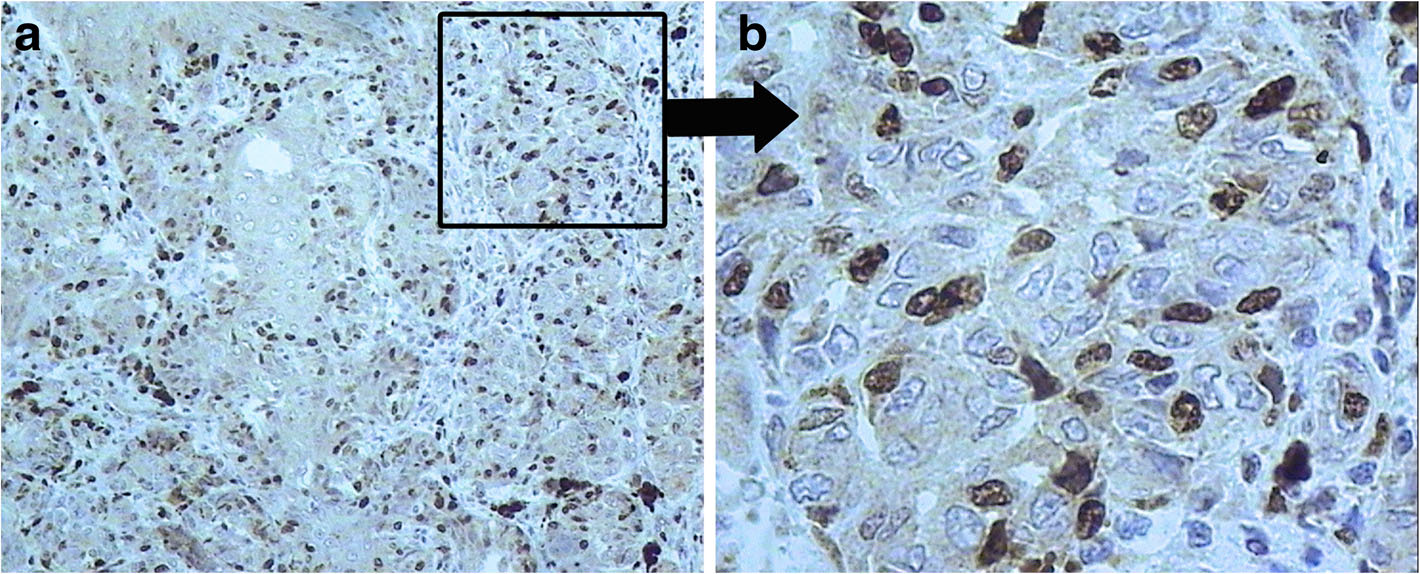
图3 皮肤黑色素瘤:Ki-67免疫组化染色。(a)×10,(b)×40
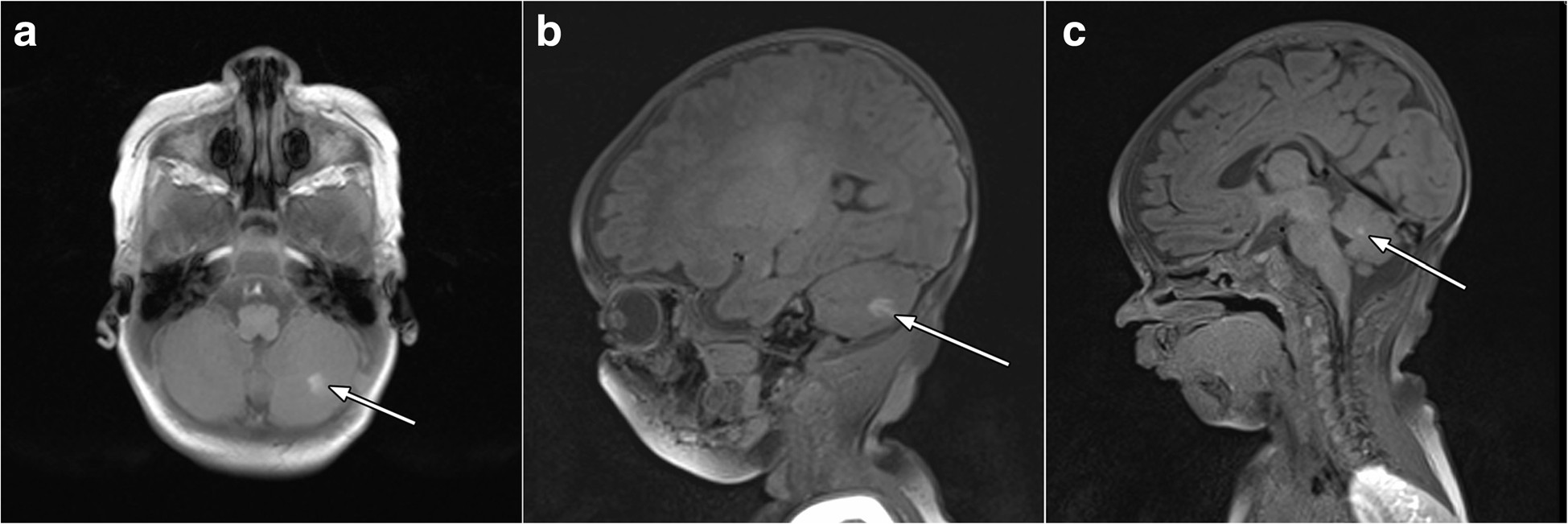
图4 磁共振成像显示大脑结构中存在黑色素:MRI轴位增强T1W和(b)矢状位增强T1W图像,聚焦于小脑左半球的MR信号改变。(c)矢状位T1W,聚焦小脑软脑膜异常MR信号。所描述的影像表现为神经皮肤黑变病的诊断。
病例2:男,在转诊时5个月大。患者为菲茨帕特里克皮肤II型。怀孕第39周出生。患者出生时就长了一颗巨大的色素痣(大于20厘米),部分被毛发覆盖,其特征是不规则的色素沉着,颜色从粉红色、浅棕色到灰黑色。主要位于患儿头枕部,并延伸至颈后部、肩上部、背部和胸部。在躯干和四肢也有大量散在色素团块(图5)。在颈后部新出现一个大的着色的肿瘤。皮肤镜检查图没有提供任何信息。根据回顾及临床检查,我们诊断为先天性巨型痣伴卫星及先天性颈部后皮肤黑素瘤。2014年10月给予麻醉,行诊断性切除活检。超声检查周围淋巴结,腹部,腹膜后和盆腔器官。还进行了胸部CT扫描和颈部MRI检查。超声检查和颈部MRI静脉造影发现了转移卫星。组织病理学显示上皮样细胞黑色素瘤,有2个核分裂象/mm2和卫星,没有溃疡或血管侵犯。没有卫星的 Breslow厚度为2mm。在皮下组织中检测到形状清晰的肿瘤结节(图6中箭头所示),并确定为黑色素瘤卫星(图6)。采用诊断生物芯片对肿瘤进行遗传分析,检测BRAF、NRAS、KIT、GNAQ、GNA11、MAP2K1和一个MAP2K2基因的体细胞突变,Sanger测序寻找CDKN2A基因的生发突变。最终,在NRAS基因中发现了Q61K突变。根据病理报告和全身检查,我们诊断为黑色素瘤T2aN2cM0期IIIB。由于患者的年龄,建议进行观察。该儿童目前(2018年7月)正在接受观察,没有出现疾病进展的症状。
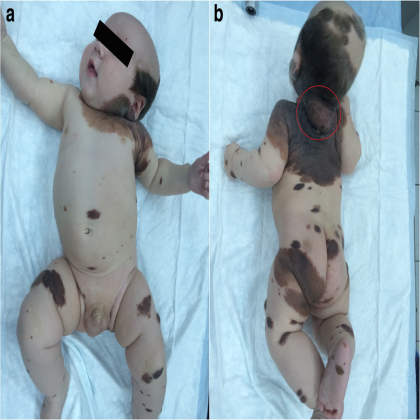
图5:病变位于患儿头枕部,并延伸至颈后部、肩上部、背部和胸部。在躯干和四肢也有大量散在色素团块。
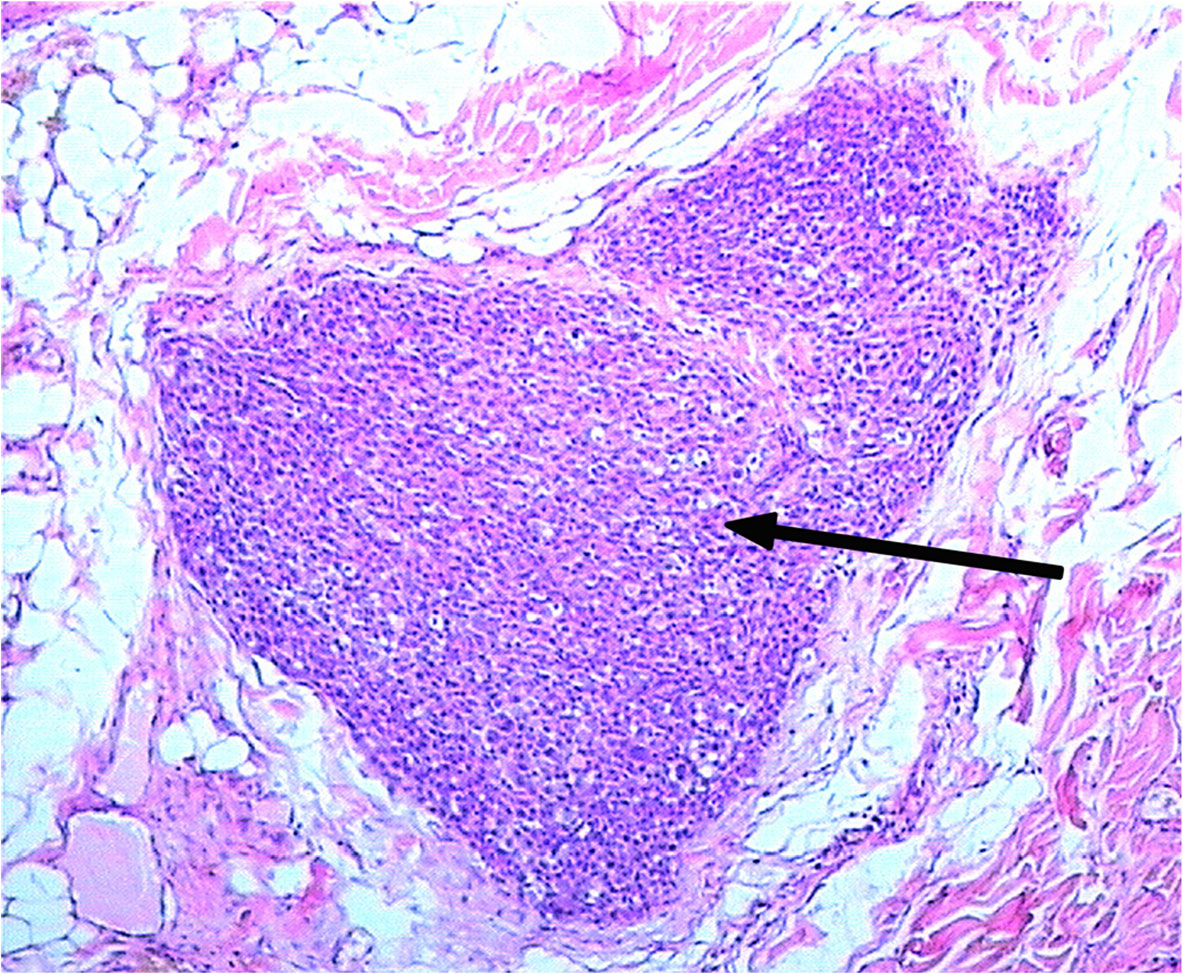
图6 皮下组织中的黑色素瘤卫星。
【讨论】
恶性黑色素瘤在儿童患者中是一种罕见的肿瘤,但CMN患儿患黑色素瘤的风险更大。CMN的大小和位置及其与多个卫星痣的关联似乎也影响恶性肿瘤和黑色素瘤的发展。CMN发生黑色素瘤的风险被认为与痣的大小成正比。根据文献报道,67%的病例显示原发黑色素瘤位于痣内,14%的病例显示原发部位不明的转移性黑色素瘤,8%的病例显示皮肤以外的黑色素瘤。CMN发生的皮肤黑色素瘤通常表现为一种新的结节或肿块,主要发生在真皮深层或皮下组织。大多数临床报告(高达90%)表明在躯干上有恶性黑色素瘤。本文仅对孤立的临床病例或小系列病例作了描述,证实了其发生的罕见性及积累资料和临床经验的必要性。
当CMN患者怀疑有皮肤黑色素瘤时,应进行活检(如果可能的话通过切除),并由至少两名专家进行详细的组织病理学检查。来自先天性巨大痣的黑素瘤主要是由真皮黑素细胞发育而来,而来自小和中等大小痣的黑素瘤则来自于表皮。
Clark报告说,在组织学水平上的诊断问题是由于在先天性黑素细胞病变中出现的一些结节性过度生长的复杂细胞组成。在出生或新生儿期CMN中观察到四种主要的组织学模式:(1)类似于浅表播散性黑色素瘤,大的上皮样黑色素细胞数量增加;(2)类似于结节性黑色素瘤,上皮样黑色素细胞形成黑色结节;(3)结节状增生性神经嵴错构瘤;(4)生物学行为恶性的黑色素瘤,最大特征是小的“母细胞样”多形性黑素细胞,核分裂率高。Clark认为真正具有转移潜能的黑色素瘤通常发生在新生儿期之后。我们的病例证实了Clark的发现,因为这两个孩子现在都在观察中,尽管处于黑色素瘤发展的早期阶段,并接受了后续的手术治疗,但没有疾病进展的迹象。
组织学检查是恶性黑色素瘤的诊断标准,在我们的两个病例中,第1例组织病理学显示结节型黑色素瘤(图2a),发生于先天性痣背景,核分裂象1个/mm2,有溃疡形成(图2b),垂直生长期,Clark侵犯3级,Breslow厚度1.5 mm,无任何血管侵犯症状。免疫组化分析显示,肿瘤细胞黑色素瘤特异性标志物MelanA和HMB45阳性。
Ki67常被用作细胞增殖的指标,Ki67在肿瘤细胞中的增殖指数为20~30%(图3)。根据文献,Ki67指数在黑素瘤负载的GCN患者中并不是判断预后或确定恶性的良好指标。黑色素瘤有时可能是GCMN中核分裂活跃的增生性结节。在黑素细胞病变中遇到这种特征是令人担忧的,但在没有其他恶性组织学标准的情况下,它本身不应该考虑黑素瘤的诊断。我们使用Ki67作为额外的标记。病例2的组织病理学显示上皮样细胞黑色素瘤,有2个核分裂象/mm2,有溃疡伴卫星结节,无血管侵犯。Breslow厚度为2mm。皮下组织可见肿瘤结节(黑素瘤卫星)(图6)。
对获得的活检标本进行分子分析,并对几个可能在GCMN的发展和恶性转化中发挥作用的基因进行了研究。对于病例1,我们评估了GNAQ和GNA11基因中BRAF、NRAS、KIT、GNAQ、GNA11、MAP2K1/2、PDGFRA、RASA1、RAC1、MET、PTEN、AKT1、TP53、tertgene和体细胞突变的存在情况。还对CDKN2A基因的种系突变进行了研究。仅检测到TP53密码子72的非致病性Arg/Arg多态性。对病例2进行BRAF、NRAS、KIT、GNAQ、GNA11、MAP2K1、MAP2K2基因的体细胞突变和CDKN2A基因的胚系突变分析。最终,在NRAS基因中只发现了Q61K突变。NRAS基因突变发生在80~95%的GCMN中,被认为是CMN形成的原因之一,尽管恶性转化还需要其他因素。在我们的两个病例中,都没有发现可以解释黑素瘤的特定突变。我们的同事之前发表了一个8岁女孩的临床病例,她的黑色素瘤发生在一个中等大小的先天性痣,伴有NRAS Q61K突变。Kinsler等人发表了他们在先天性黑素细胞痣黑色素瘤研究中心25年的研究结果,包括肿瘤的分子特征。在12例黑色素瘤患者中,6例为中枢神经系统黑色素瘤,3例为未知黑色素瘤部位,3例为皮肤黑色素瘤。有9名患者在生命的前5年患上黑色素瘤,7名患者发现NRAS基因Q61K突变。在1例3例皮肤黑色素瘤患者中,Q61K发现与病例2相同。当临床上怀疑CMN引起的皮肤黑色素瘤时,应立即进行活检,并至少由两名专家进行组织病理学检查。建议采用敏感方法进行NRAS和BRAF热点基因分型,以提高诊断准确性和指导治疗。
GCMN中的黑色素瘤通常发生在青春期前,即5岁以前,而小痣和中痣通常发生在青春期后。CMN的治疗是外科和皮肤肿瘤学中最复杂的领域之一,并且没有普遍接受的标准来治疗这种病变。目前还不清楚是否有必要去除CMN以降低黑素瘤的风险。在一些报道中,尽管几乎完全切除了GCMN,但手术未能阻止恶性黑色素瘤的发生,GCN手术切除的作用仍存在争议。虽然手术不能降低皮肤外黑色素瘤的风险,但去除黑色素细胞似乎可以降低痣内黑色素瘤的风险。GCMN治疗的一些手术选择包括连续切除、皮肤移植等。
神经皮肤黑素病是一种罕见的并发症,可恶化GCMN患者的预后。NCM是与CMN相关的神经黑素病,描述软脑膜和脑实质内黑素细胞增生(良性或恶性,结节状或弥漫性)。Kadonaga描述了NCM,并将其重新定义为存在大于20cm的CMN或多发性CMN(3个以上),并伴有脑膜黑素病或黑色素瘤。我们的第一个病例有NCM和恶性黑色素瘤,具有大于20厘米的GCMN。恶性黑色素瘤和NCM最常发生在CMN患者,直径> 40厘米,多发卫星痣,和躯干位置。几乎三分之一的NCM患者有大量的中型CMN。对于6个月以下有NCM风险的患者,推荐使用钆增强扫描MRI进行长期神经观察。神经黑素病患者可有症状或无症状。在我们的病例中,MRI显示在大脑结构中存在黑色素,这是在没有神经症状的情况下进行的。因此,应对新生儿GCMN(特别是多卫星痣)进行MRI评估。
CMN患者确诊为黑色素瘤的建议检查如下:(1)全血计数和乳酸脱氢酶水平;(2)中枢神经系统MRI加钆造影剂、全身PET-CT或CT检查;(3)组织标本进行组织病理学、NRAS和BRAF热点基因分型和拷贝数分析(CGH阵列或SNP阵列或FISH)。基因分型可能对治疗策略很重要,包括在NRAS突变的肿瘤中使用丝裂原活化蛋白激酶激酶(MEK)抑制剂。
【参考文献】
[1] Belysheva et al. Melanoma arising in a Giant congenital melanocytic nevus: two case reports[J].Diagnostic Pathology,2019.doi.org/10.1186/s13000-019-0797-1.



















共0条评论