1 概述
甲状腺样滤泡性肾细胞癌(thyroid-like follicular renal cell carcinoma,TLFRCC)又称肾脏甲状腺样滤泡癌(thyroid-like follicular carcinoma of the kidney)或甲状腺滤泡癌样肾肿瘤(thyroid follicular carcinomalike renal tumor),是近年来新认识的一种少见肾细胞癌亚型。1996年由Angell等首次报道,研究发现该肿瘤具有特征性甲状腺滤泡样结构,但不表达甲状腺相关免疫组化标记物,且临床检查未发现甲状腺相关病变。虽然该肿瘤具有独特的组织形态学、免疫表型及临床特征,但目前国内外范围内报道仍较少,不超过五十例。2012年国际泌尿病理协会(the In ternational Society of Urological Pathology ,ISUP)肾肿瘤共识会议中对其做了详细介绍,而WHO(2016)肾肿瘤分类中仅将其列为暂定的肾细胞癌亚型。本文对其临床特征,病理形态学特征及免疫表型,临床治疗及预后情况进行初步阐述,望能提高对该肿瘤的认识。
2 临床特征
TLFRCC病情进展缓慢,大部分患者无明显临床症状,于体检中偶然发现,部分患者可出现肉眼血尿、腰腹部疼痛等症状,少见症状有体重减少、高血压及尿路感染等。文献报道TLFRCC发病年龄分布较广泛,发病年龄为19-83岁,中位数为45岁,主要发生于中青年女性。文献报道所有病例均为单侧肾病变,62%发生于右肾,明显多于左肾;转移病例有肺、骨(包括颅骨、股骨、耻骨支等)、脑膜、肾门、腹膜后淋巴结转移等。
以往文献认为术前CT、MRI等影像学检查几乎不能将其与其他类型肾细胞癌区分开来。 新近发现TLFRCC在CT平扫上呈高密度影,而在增强扫描中多不强化或强化不明显,这与乏血供肾肿瘤的影像学表现很相似,不同于其他类型肾细胞癌在增强期的明显强化特征;同时在肿瘤周边可出现蛋壳样钙化影,而其他类型肾细胞癌的钙化一般出现于肿瘤中心;可能对术前考虑TLFRCC具有一定的提示价值,单纯从临床表现和影像学资料并不足以做出正确诊断,故确诊尚需进行病理学检查。
3 病理学特征
大体TLFRCC界限清楚,切面灰白或灰黄色,可有出血及囊性变,可见小灶性坏死,部分病例可侵犯肾盂或肾周脂肪,大多数肿瘤都有厚薄不一的纤维包膜。镜下肿瘤由大小不一的滤泡结构混合构成,滤泡腔内含嗜酸性粉染甲状腺胶质样物,肿瘤细胞呈单层扁平、柱状或立方,胞质中等量且嗜酸性或嗜双色,细胞核圆形或卵圆形,染色质细腻,部分可见小核仁,胞核异型性小,核分裂象罕见或无,WHO/ISUP核分级为2-3级。
部分病例中可出现乳头状或实性排列结构,个别病例甚至以乳头状结构为主要排列模式。虽然有的病例可有局灶乳头状结构,但肿瘤细胞核均无甲状腺乳头状癌的经典核改变(毛玻璃样核、核沟及核内假包涵体等),也无典型透明细胞癌及其他类型肾细胞癌的组织形态学特征。另外各病例还有其各自特点,伴局灶或地图状大片坏死;胶体样物中胆固醇晶体形成;间质玻璃样变;出现灶区乳头状生长;局部区淋巴细胞聚集,甚至形成生发中心;假肉瘤样生长方式;化生性骨形成等。
文献报道免疫组化标记特征不明确,但一致显示TTFl和TG阴性,而CD10、CAIX、CK7、CA9、CD117、vimentin、P504S、PAX8等可不同程度阳性,Ki-67增殖指数表达较低,提示该肿瘤的生物学行为比较惰性,但可发生淋巴结或远处转移。
4 分子遗传学
Jung等通过比较基因组杂交方法发现1例TLFRCC中存在染色体7q36,8q24,12,16,17p11-q11,17q24,19q,20q13,21q22.3与Xp的获得及染色体lp36,3与9q21-33的丢失,与已知类型肾细胞癌的细胞遗传学改变均明显不同,未见肾细胞癌中最常见的遗传学异常(染色体3p缺失)。Amin等同样应用比较基因组杂交技术对1例肿瘤进行检测,却未发现任何细胞遗传学改变。Sterlacci等用荧光原位杂交技术在TLFRCC中发现了染色体l,3,7,9p21,1 2,1 7及x的丢失,与嫌色细胞癌的细胞遗传学改变(染色体1,2,6,10,13,17,21及x丢失)类似。Amin等还采用微阵列技术对比研究肾透明细胞癌、嫌色细胞癌及TLFRCC的基因表达谱,与前两者相比TLFRCC中有135个基因过表达、46个基因低表达。有趣的是他们还发现MLL基因在TLFRCC中表达是肾透明细胞癌和嫌色细胞癌的2.5倍,基因异常在TLFRCC中的作用还需要大量的病例进一步研究证实。
5 鉴别诊断
TLFRCC镜下显示甲状腺滤泡样结构,与甲状腺滤泡癌组织学形态高度相似,因此需与以下疾病鉴别。
①甲状腺滤泡癌转移:少见,约半数为甲状腺滤泡癌,该肿瘤易发生血道转移,转移至肝、肺、骨、肾等部位,常由于转移灶出现首发症状就诊。多数患者有明显甲状腺原发病灶,超过90%病例具有肾或肾外脏器受累而引起的症状,且相当一部分比例的患者为肾双侧和(或)多灶受累。肿瘤细胞TTF-1、TG强阳性。而TLFRCC生长缓慢,多为体检发现,部分患者有血尿和腰痛等症状。肿瘤细胞TTF-1、TG为阴性。PAX8在肾源性和甲状腺源性肿瘤鉴别中无参考价值,诊断时需要同时结合临床病史及甲状腺相关检查综合判断。
②卵巢甲状腺肿:卵巢甲状腺肿是一种卵巢单胚层畸胎瘤,仅由甲状腺成分构成,约占卵巢肿瘤的2%,部分病例可恶性,其恶变率为5%-10%,约5%可以发生转移,主要转移至肝及腹膜。因此诊断时也需要参考临床病史、影像学检查及免疫组化标记物TTF-1及TG等综合评价除外。
③肾脏管状囊性细胞癌:大体上具有特征性多囊性或海绵状外观,囊腔大小形状相对较为一致,囊壁薄,镜下显示肿瘤由大小相对较为一致的管状或囊状结构组成,部分融合成较大囊腔,管腔衬覆单层立方、柱状、靴钉样细胞,胞核较大不规则(WHO/ISUP核分级多为3级),胞质粉染嗜酸,可见纤维化的间质,可含有差分化或肉瘤样区域。
④肾脏甲状腺化和肾脏甲状腺异位:良性非肿瘤性病变,前者是慢性肾盂肾炎或尿路梗阻或晚期肾病的继发性病变,是终末期肾病常见现象,特点是肾小管或集合管萎缩,管腔内充满胶样物质,镜下形态与甲状腺滤泡结构相似,常常广泛累及双侧肾,而TLFRCC是具有纤维包膜的单发性肿块,再者TLFRCC一般无其他肾脏疾病。肾脏甲状腺异位的病例报道罕见,异位组织表达TTF-1和TG等。
⑤肾神经内分泌癌:由于TLFRCC某些区域排列成筛状、梁索状和实体片状,并可见小灶性坏死,因此要注意与神经内分泌癌鉴别。但后者罕见滤泡样结构和腔内的红染胶体样物,肿瘤细胞异型性更明显,核分裂更多见。免疫组化染色肿瘤细胞显示NSE、CD56及CgA等神经内分泌标记物强阳性,则支持后者诊断。
⑥上皮型肾母细胞瘤:该肿瘤好发于儿童,成人罕见,多见未分化胚芽组织、上皮成分和间叶成分,单向分化的上皮型肾母细胞瘤罕见。其上皮常呈菊形团样结构,有时可见小管状和乳头状结构,有时可见黏液上皮和鳞状上皮,但未见呈滤泡样结构伴腔内红染胶体样物的报道。免疫组化染色肿瘤细胞核的WTl阳性支持该肿瘤的诊断。
⑦BHD综合征(BirtHogg-Dubé)伴发肾细胞癌:组织学类型多为嫌色性肾细胞癌或多种类型混合的肾细胞癌,多表现为多囊性或双侧肾脏多发肾癌,对高度怀疑BHD相关性肾癌患者应行FLCN基因检测。
⑧后肾腺瘤: 肿瘤细胞小而一致,呈胚胎样或腺泡状排列,50%可有乳头状结构,似不成熟的肾小球,可见瘢痕样间质或骨化;免疫组化CK、CD57和WT-1等阳性表达。形态学与TLFCK有相似性,但其他形态结构不一致及免疫组化有助于鉴别诊断。
⑨伴滤泡样结构的其他肾脏肿瘤:乳头状肾细胞癌、肾透明细胞癌、肾嗜酸性细胞腺瘤等有时可出现腔内含嗜酸性物质的滤泡样结构,但这种结构在这些肿瘤中相当少见,且通常为局灶性分布。
6 临床治疗与预后
献报道显示TLFRCC生物学行为相对比较惰性,无论是根治性肾切除、部分肾切除还是腹腔镜部分肾切除,手术切除肿块是主要的治疗方法。即使发生远处转移,行转移病灶切除即可。TLFRCC总体预后好,但也有发生转移的报道,TLFRCC具有一定的侵袭转移能力,这提示它可能不是一个低度恶性肿瘤,但需要长期大量病例随访进一步研究。
综上所述,TLFRCC是肾细胞癌的一个少见亚型,主要发生于中青年女性,具有独特的形态学及免疫组织化学特点,确诊有赖于病理学和免疫组织化学,外科切除是首选治疗方法。总体预后良好,但部分病例报道显示它具有一定的侵袭转移能力,彻底认识该肿瘤,掌握其生物学行为并为诊断和治疗提供有价值的信息依赖更深入的遗传学资料,更多病例的积累和更长时间的随访。
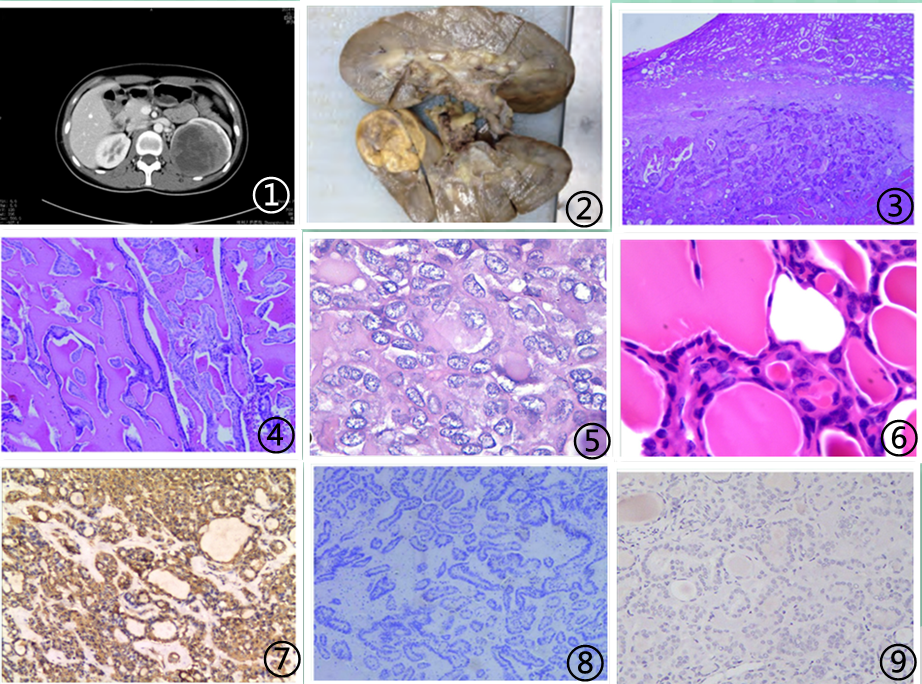
图1 CT示左肾上极类圆形肿物;图2 肿块位于肾上极,切面棕黄色,境界清,实性质稍韧,无明显坏死;图3 肿瘤细胞呈乳头状排列,乳头间可见大量嗜酸性甲状腺胶质样物;图4肿瘤性滤泡结构衬覆单层柱状上皮,胞核异型性明显,可见核沟;图5 肿瘤中见髓外造血灶形成;图6肿瘤细胞核圆形、卵圆形,核异型性小,染色质细腻,分布均匀,核仁不明显;图7肿瘤细胞CK7阳性,EnVision法,图8 肿瘤细胞TG阴性,EnVision法;图9 肿瘤细胞TTF1阴性,SP法;图片来自于参考文献5,6,7,8,如有侵权,请联系删除。
参考文献:
[1]连婧[1], 王丽霞[1], 马海霞[1],等. 甲状腺样滤泡性肾细胞癌4例临床病理分析[J]. 诊断病理学杂志, 2018.
[2]武翀, 陈路遥, 陈鑫,等. 甲状腺滤泡癌样肾细胞癌临床诊疗分析[J]. 微创泌尿外科杂志, 2016, 5(001):30-33.
[3] Angell S K , Pruthi R , Freiha F S . Primary thyroidlike carcinoma of the kidney[J]. Urology, 1996, 48(4):632-635.
[4] Amin M B , Gupta R , Ondrej H , et al. Primary thyroid-like follicular carcinoma of the kidney: report of 6 cases of a histologically distinctive adult renal epithelial neoplasm.[J]. American Journal of Surgical Pathology, 2009, 33(3):393-400.
[5]陈鑫, 窦富贤, 程学斌,等. 甲状腺样滤泡性肾细胞癌五例临床病理特征分析[J]. 中华病理学杂志, 2016, 45(010):687-691.
[6]刘泽平, 陶群星, 汤晓晖,等. 伴髓外造血的甲状腺滤泡样肾细胞癌一例[J]. 中华病理学杂志, 2017, 046(009):644-645.
[7]孙阳阳, 蔡雷铭, 程羽青,等. 甲状腺滤泡癌样肾细胞癌临床病理观察[J]. 诊断病理学杂志, 2017(3).
[8]杨迷玲, 徐宪伟, 杨金花. 甲状腺样滤泡性肾细胞癌的临床病理特点[J]. 临床与病理杂志, 2017, 037(009):1989-1995.
[9]崔勇, 郑滔, 徐浩,等. 甲状腺滤泡样癌肾转移1例报告并文献复习[J]. 现代泌尿生殖肿瘤杂志, 2017, 009(001):38-40,47.
[10]岳振营, 吴秀贞, 宋殿行,等. 甲状腺滤泡样肾细胞癌1例[J]. 诊断病理学杂志, 2017(4).
[11]汪红燕, 宋文静. 甲状腺滤泡样肾细胞癌一例报告[J]. 天津医药, 2018.














共0条评论