[导读] 译者:慧海拾穗
【定义】毛细胞型星形细胞瘤一种具有双相组织学特征的星形细胞瘤,由含Rosenthal纤维的致密双极细胞和疏松的含微囊及偶见颗粒小体的多极细胞组成。遗传学上,毛细胞型星形细胞瘤的特征是编码参与MAPK途径的蛋白质的基因存在突变。最常见的遗传学改变是涉及BRAF基因的染色体7q34串联重复,产生致癌的BRAF融合蛋白。毛细胞型星形细胞瘤是儿童和青少年中最常见的胶质瘤,男性比女性稍微更多见。毛细胞型星形细胞瘤好发于小脑和大脑中线结构(即视觉通路、下丘脑和脑干),但也可能出现在沿神经轴的任何地方。毛细胞型星形细胞瘤通常为局限性包块,生长缓慢,可能是囊性的。毛细胞型星形细胞瘤在组织学上很大程度属于WHO I级,患者可以通过手术切除治愈。然而,在某些部位,如视神经通路和下丘脑,完全切除可能做不到。特别是那些涉及视神经通路的毛细胞型星形细胞瘤是1型神经纤维瘤病(NF1)的标志。毛黏液样星形细胞瘤被认为是毛细胞型星形细胞瘤的一种亚型。
【ICD-0 编码】 9421/1
【分级】毛细胞型星形细胞瘤在组织学相当于WHO I级。
【流行病学】毛细胞型星形细胞瘤占所有胶质瘤的5.4%;是儿童最常见的胶质瘤,无明显性别差异;它占0~14岁年龄组所有胶质瘤的33.2%,占所有儿童原发性脑肿瘤的17.6%。同样,在一项对来自一家机构的1195例儿童肿瘤的研究中,毛细胞型星形细胞瘤是脑室内最常见的肿瘤(占总病例的18%)。在成人中,毛细胞型星形细胞瘤往往比WHO II级的弥漫性星形细胞瘤早出现约十年(患者平均年龄22岁),但在年龄>50岁的患者中出现的相对较少。
【部位】毛细胞星形细胞瘤发生于整个神经轴;然而,在儿童病例中,好发于幕下区域。好发部位包括视神经(视神经胶质瘤)、视交叉/下丘脑、丘脑和基底神经节、大脑半球、小脑(小脑星形细胞瘤)和脑干(背外侧脑干胶质瘤)。脊髓毛细胞星形细胞瘤不常见,但并不少见。大下丘脑、丘脑和脑干病变可能主要是脑室内的,其起源部位难以确定。
【临床特征】毛细胞星形细胞瘤产生局灶性神经功能缺损或非定位体征,如畸形巨头、头痛、内分泌病和由于肿块或脑室梗阻引起的颅内压升高。 癫痫发作并不常见,因为病变很少累及大脑皮层。由于毛细胞肿瘤的生长速度较慢,其临床表现通常进展缓慢。视神经通路的毛细胞星形细胞瘤通常会导致视力丧失。发生于眼眶者表现为眼球突出。早期影像学检测到的病变可能与视觉症状或眼科缺陷无关。下丘脑/垂体功能障碍,包括肥胖和尿崩症,通常在大的下丘脑肿瘤患者中很明显。发生幼儿的一些下丘脑/视交叉病变与软脑膜播散和不良预后有关;参见毛细胞星形细胞瘤的一种亚型---毛细胞黏液样星形细胞瘤。丘脑毛细胞星形细胞瘤通常表现为由于内部包膜压迫引起的脑脊液阻塞或神经功能缺损(如偏瘫)。小脑毛细胞星形细胞瘤通常发生于二十岁之前,表现为笨拙、头痛加重、恶心和呕吐。脑干的例子最常见的原因是脑积水或脑干功能障碍的迹象。与脑桥的弥漫性星形细胞瘤不同,脑桥的弥漫性星形细胞瘤产生对称的所谓脑桥肥大,脑干的毛细胞肿瘤通常是背侧的,向外生长到小脑桥脑角。脊髓的例子产生了肿块扩张的非特异性迹象。
【影像学】大多数小脑和大脑毛细胞星形细胞瘤界限清楚,呈圆形或椭圆形,边缘光滑。 偶尔出现钙化。典型的异质性是囊肿样区域与通常强烈增强的软组织成分混合的结果。与肿瘤的低生物活性一致,周围血管源性水肿(如果存在)的范围远小于更高级别的胶质肿瘤。约2/3的病例表现为囊肿样肿块,伴有增强的壁结节;另1/3呈现为具有中央非增强区的囊肿样肿块,或者呈现为具有最小或没有囊肿样部分的主要为实性的肿块。在囊肿样形态的患者中,囊肿壁可能增强,也可能不增强,囊肿壁增强可能表明也可能不表明肿瘤受累。这些肿瘤偶尔的非典型影像特征包括多个囊肿样肿块和出血。大多数视神经胶质瘤是毛细胞星形细胞瘤,其特征性表现为视神经扭结或弯曲增大。取决于患者是否患有NF1,该部位的肿瘤通常具有不同的影像学表现。NF1相关肿瘤更常见地影响视神经,很少延伸到视神经通路之外,并且通常不是囊肿样的,而那些与NF1无关的肿瘤通常涉及视交叉,延伸到眼睛外,并且通常是囊肿样的。
【播散】另外,典型的毛细胞星形细胞瘤偶尔会播散到神经轴,少数情况下发生于原发性肿瘤被检测到之前。这些病例增值指数不一,但通常较低。因此,不能预测毛细胞星形细胞瘤的这种非典型行为。下丘脑通常是主要部位。神经轴播散不一定表示将来会出现侵袭性生长;原发病灶和植入病灶都可能缓慢生长。植入病灶可能没有症状,即使没有辅助治疗,也有可能长期存活。毛细胞黏液样星形细胞瘤亚型(见毛细胞黏液样星形细胞瘤)通常发生于下丘脑区域,更常发生颅脊髓扩散。

图1 大多数毛细胞星形细胞瘤呈强而广泛的强化:左视神经(A)、下丘脑(B)、基底神经节(C)、顶盖(D)、小脑(E)、脊柱(F)。一些肿瘤是实性的(A、B、D),另一些是囊性的,伴有增强的壁结节(C、E、F)。
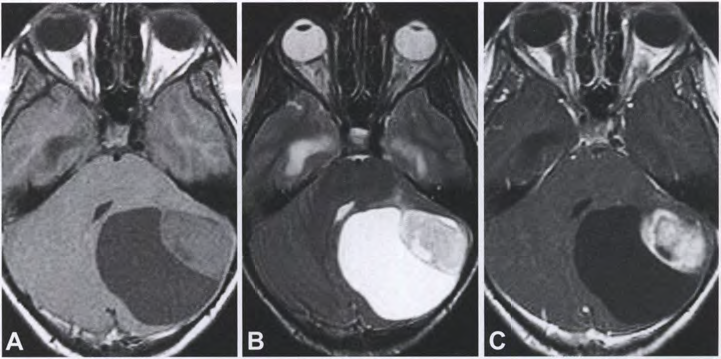
图2 小脑毛细胞星形细胞瘤:轴向T1加权磁共振成像显示左侧小脑囊肿样肿块,沿其侧缘有轻度高信号壁结节(A)。轴向T2加权磁共振成像显示肿块囊样部分高信号,壁结节低信号(B)。扫描后轴位T1加权磁共振成像显示壁结节不均匀强化(C)。
【肉眼所见】大多数毛细胞星形细胞瘤质软、灰白色。瘤内或瘤旁囊肿形成是常见的,包括附壁肿瘤结节。在脊髓病例中,脊髓空洞形成可以延伸到许多节段。慢性损伤者可见钙化和含铁血黄素沉积。视神经肿瘤通常沿周向累及蛛网膜下腔。

图3毛细胞型星形细胞瘤:海马和邻近结构的弥漫性浸润。注意局灶囊肿形成(A)。大的,部分囊性的小脑毛细胞星形细胞瘤,有典型的壁结节(B)。延伸至基底池的大的毛细胞型星形细胞瘤(C)。
【显微镜检查】这种低到中等细胞密度的星形细胞肿瘤通常具有双相模式,具有不同比例的Rosenthal纤维的致密双极细胞和微囊松散结构的多极细胞。双相模式在小脑肿瘤中最常见。然而,毛细胞星形细胞瘤可以表现出广泛的组织模式,有时在同一病变中有几种。当细长细胞不太紧密但被黏蛋白分开时,出现一种变型的紧密毛状结构。在这种情况下,可以看到单个的细胞突起,并且细胞形状不同,包括更加丰满和多形性的、不太明显的毛状细胞。当软脑膜受累引起韧带增生反应时,会出现一种独特的小叶模式。在这个部位,组织结构不同,但Rosenthal纤维通常较多。罕见的核分裂象、深染和多形性细胞核、肾小球样血管增生、梗死样坏死和软脑膜浸润与毛细胞型星形细胞瘤的诊断相符,不是恶性肿瘤的征象。由于组织学特征的异质性,毛细胞型星形细胞瘤的涂片显示出相当大的细胞学变异,并且基本的细胞学模式经常组合出现。肿瘤的致密部分产生双极毛状细胞;长的毛发状突起和Rosenthal纤维,通常遍布整个显微镜视野。细胞核通常是细长的,细胞温和。由于其高含量的折射性嗜酸性纤维,这些微囊区的细胞GFAP强阳性,这些细胞圆形至卵圆形、细胞核温和;小细胞体和相对较短的蛛网状突起含有少量纤维,GFAP染色弱阳性。这种生长模式可能与嗜酸性颗粒小体有关。与弥漫性星形细胞瘤无法区分的细胞可能会聚集在周围浸润性更强的区域。与少突胶质细胞非常相似的细胞通常不太常见,但在某些病例中,尤其是在小脑,可以比较明显看见。这些细胞强烈表达OLIG2,尽管其他组织模式也可能表达OLIG2。细胞呈片状排列或分散在薄壁组织中,整体外观可能类似少突胶质细胞瘤,特别是在小标本中。典型毛细胞星形细胞瘤病灶的发现通常能使这类病变得到正确分类。在一些毛细胞星形细胞瘤中,致密栅栏状(一种所谓的胶质母细胞瘤[spongioblastoma]模式)是一个显著的特征。虽然许多毛细胞星形细胞瘤是良性的,但有些表现出明显的核深染和多形性。核分裂象罕见,但核分裂活跃,特别是弥漫性核分裂活跃,是间变性改变的特征,具有预后意义。在少数(通常是小脑的)肿瘤中,弥漫生长模式掩盖了更典型的致密和微囊特征。在这些病例中,深染细胞核或核分裂像的存在会引起与高级别弥漫性星形细胞瘤的混淆。不太令人担忧的是明显的退化性非典型性,伴有多形性和核质假包涵体,常见于长期病变者。大细胞或巨细胞内的多个细胞核位于圆周上。透明血管和肾小球样血管是某些病例的显著特征。任何非栅栏状坏死通常是梗死样的。血管周围淋巴细胞也可能出现。由于毛细胞型星形细胞瘤在一定程度上超越正常组织,预先存在的神经元有时会被内陷,一些病变甚至表现出有限的细胞学非典型性。这种病变应与神经节细胞肿瘤相区别。毛细胞黏液样变异型的特征是黏液样背景下均匀的双极细胞和频繁的血管周围排列。有时这种模式与更传统的毛细胞区域或所谓的中间肿瘤有关。尽管儿童星形细胞瘤通常被分为毛细胞型或弥漫型,但事实上,仅根据组织学,许多病例并不明确属于这两种类型。越来越多的分子谱在这种区分中起着辅助作用。在某些病例中,小的活检标本导致分类困难,尤其是脑干或脊柱部位的病例。

图4 毛细胞型星形细胞瘤的典型组织学特征:术中细胞学涂片(A)和组织切片上(B)可见由双极细胞组成的密集纤维区,有长而细的突起,富含Rosenthal纤维。嗜酸性颗粒小体(嗜酸性颗粒小体在星形细胞突起内形成球状聚集物。它们在切片中呈明亮的嗜酸性,PAS染色阳性,对α-1-抗胰蛋白酶和α-1-抗胰蛋白酶有免疫反应。虽然嗜酸性颗粒小体可能存在于毛细胞型星形细胞瘤中,但它们在其他胶质或神经胶质肿瘤中更常见,尤其是神经节细胞肿瘤和多形性黄色瘤型星形细胞瘤)。肿瘤细胞核深染。出现了一个罕见的核分裂像(箭头)(C)。松散排列的微囊区(D)。毛细胞型星形细胞瘤是一种典型的富含血管的肿瘤,显示肾小球样血管(E)和厚壁透明血管(F)。血管变化与影像上经常出现的对比增强相关。

图2.06毛细胞型星形细胞瘤:典型的双相模式,具有交替的密集和松散结构模式(A)。假少突胶质细胞模式。有规则的圆形细胞,细胞核圆形,偶尔有微囊性变(B)。
【免疫表型】毛细胞型星形细胞瘤是星形细胞谱系中分化良好的胶质瘤,强表达GFAP、S100和OLIG2。突触素(Syn)可能表现出部分或弱阳性,这不应作为胶质神经元肿瘤的证据。Rosenthal纤维表达α-B-crystallin,GFAP染色仅限于其周边。与弥漫性星形细胞瘤不同,p53蛋白染色弱阳性或阴性,这与毛细胞型星形细胞瘤中TP53突变的罕见性一致。R132H-突变IDH1蛋白的免疫组织化学被认为有助于区分毛细胞型星形细胞瘤和弥漫性胶质瘤,因为几乎所有的毛细胞型星形细胞瘤都是阴性表达。然而,儿童弥漫性星形细胞肿瘤也可能缺乏IDH1或IDH2突变。此外,可靠的抗体目前仅可用于132位最常见的IDH1氨基酸取代,因此阴性结果不排除132位的其他取代或IDH2蛋白的突变。因为基本上所有毛细胞型星形细胞瘤在MAPK途径的组成部分都有激活性遗传改变,磷酸化MAPK免疫染色是一个一致的特征。用mTOR途径激活的免疫组织化学标记(如磷酸化S6)进行标记更具可变性。V600E-突变BRAF的免疫组织化学在缺乏KIAA1549-BRAF融合和其他MAPK途径改变的小部分中呈阳性。Ki-67增殖指数在大多数毛细胞型星形细胞瘤病例中较低,与低增殖率一致。在一些研究中,Ki-67增殖指数的增加与更具攻击性的行为有关,但在其他研究中则没有。
【遗传表达谱】毛细胞型星形细胞瘤中最常见的异常(>70%的病例)是大约2 Mb的7q34重复,包括BRAF基因。这是一个串联重复,导致了KIAA1549和BRAF之间基因融合。KIAA1549蛋白的N末端取代了BRAF的N末端调节区,保留了BRAF激酶结构域,因此不受控制并组成性激活MAPK途径。这种异常在所有解剖位置都有发现,但最常见于小脑肿瘤,在其他部位不太常见。基因融合涉及KIAA1549和BRAF外显子的九种不同组合,使得通过RT-PCR或免疫化学进行鉴定变得困难,导致许多中心接受7q34重复的证明(通常使用FISH探针)作为KIAA1549-BRAF融合的证据。在少数情况下,还确定了BRAF融合的另外8个伴侣基因(FAM131B、RNF130、CLCN6、MKRN1、GNA11、QKI、FXR1和MACF1),融合通过各种遗传重排(包括缺失和易位)发生,所有这些都导致BRAF蛋白的N端调节区丢失,激酶结构域保留。除了含有BRAF融合基因之外,基本上所有详细研究的毛细胞型星形细胞瘤都显示出影响MAPK通路某些成分的改变。这些改变包括有据可查的NF1突变、热点BRAF突变(通常被称为V600E突变)、KRAS突变、影响FGFR1和NTRK家族受体激酶基因的重现性异常,以及非常偶然的RAF1基因与SRGAP3的融合,其发生方式与BRAF融合相似:在3p25发生串联复制,融合蛋白缺乏RAF调节结构域,但保留激酶结构域,失去激酶控制。在NTRK基因改变的情况下,这些改变也是以基因融合的形式出现的,几个不同的5’伴侣含有一个二聚化结构域。据推测,这将导致NTRK融合蛋白的组成型二聚化和激酶的激活。FGFR1的变化更大。它们包括热点点突变(N546K和K656E)、与成人胶质母细胞瘤相似的FGFR1-TACC1融合、FGFR1激酶结构域的新内部复制和FGFR1的内部串联复制。据报道,青少年和成年人的肿瘤中存在染色体多体(尤其是第5、6、7、11和15号染色体)。各种MAPK通路改变的发生率在所有解剖位置并不一致。KIAA1549-BRAF融合在小脑极为常见(在~90%的病例中发现),但在幕上不常见(在~50%的病例中发现)。FGFR1的改变主要局限于中线结构,而BRAF V600E突变和NTRK家族融合在幕上肿瘤中更常见。毛细胞型星形细胞瘤的转录组和甲基化也存在变异,幕下和幕上肿瘤可根据其基因表达或DNA甲基化特征进行区分。起源位点/细胞与某些分子改变之间的这种关系的原因尚不清楚。与弥漫性星形细胞瘤不同,毛细胞型星形细胞瘤的平均突变率较低。TP53突变似乎在这些肿瘤的发展中不起作用。有间变性改变的毛细胞型星形细胞瘤尚待详细研究。然而,在最近对26例进展为高级别胶质瘤的病例进行的研究中,没有一例BRAF基因融合。KIAA1549-BRAF融合在合适的形态学背景下的存在以及其他发现支持毛细胞型星形细胞瘤的诊断。然而,缺乏这种融合并不能提供诊断信息,因为已经发现在毛细胞型星形细胞瘤中有许多其他方式激活MAPK途径。KIAA1549-BRAF融合也在几例成人胶质瘤中有报道,但在其他组织学中很少报道,除了罕见的弥漫性软脑膜胶质神经元肿瘤(以前称为播散性少突胶质样软脑膜肿瘤),其中融合经常与单独的1p缺失出现。不幸的是,许多MAPK-KIAA1549-BRAF改变在毛细胞型星形细胞瘤的鉴别诊断中最常见的肿瘤类型中也被发现有类似的异常。例如,BRAF V600E突变发生在一小部分毛细胞型星形细胞瘤中,但在神经节细胞瘤和多形性黄色瘤型星形细胞瘤中是常见的改变,在胚胎发育不良型神经上皮肿瘤中也有报道。现在可以使用特异性识别V600E突变BRAF蛋白的单克隆抗体来鉴定这种突变。
【预后和预测因素】毛细胞型星形细胞瘤是一种典型的生长缓慢的低度恶性肿瘤,预后良好。仅手术干预后,5年和10年的总生存率> 95%。WHO分级保持几十年不变。肿瘤甚至可能自发退化,尽管这种情况很少见。非常偶然的病例在一个可变的时间间隔后进展为更多的间变性特征,最常见的是在放疗或化疗后。很少有长期研究记录毛细胞型星形细胞瘤患者的最终结果。患者年龄和切除范围是关键的预后因素。根据肿瘤的位置和大小,毛细胞型星形细胞瘤可能不适合完全切除,并且可能复发或进展,最终导致死亡。然而,这通常是在具有多次复发的长期临床过程之后。NF1患者的视神经毛细胞星形细胞瘤似乎比其偶发性的对应肿瘤表现得更为惰性。毛细胞型星形细胞瘤组织学恶性肿瘤少见;在一项经典的毛细胞型星形细胞瘤研究中,自发发生的恶性肿瘤发生率为0.9%,放射后发生率为1.8%。毛细胞型星形细胞瘤间变性特征的描述主要来自孤立病例报告和小样本系列,其中恶性组织学特征与预后的相关性不如弥漫浸润型星形细胞瘤患者可靠。恶性转化经常被报道与先前的治疗有关。一项对34例具有自发性间变性组织学特征的毛细胞星形细胞瘤的回顾性研究发现,与典型的毛细胞型星形细胞瘤相比,这些肿瘤表现出广泛的形态学,表现出更具侵袭性的方式,存活率降低。然而,尽管间变的形态特征与弥漫性星形细胞肿瘤相似,但它们的行为并不具有攻击性。即使是具有间变性和坏死特征的所谓高级别毛细胞型星形细胞瘤的表现也不像胶质母细胞瘤。在各自的研究中,具有间变性特征如核分裂象计数增加(即> 4个核分裂象/10个高倍视野)和坏死的毛细胞星形细胞瘤表现得更类似于弥漫性低级别或间变性星形细胞瘤,而不是间变性星形细胞瘤或胶质母细胞瘤。毛细胞黏液样星形细胞瘤是一种公认的毛细胞型星形细胞瘤亚型,通常发生在幼儿,几乎只发生在下丘脑/第三脑室区域,据报道,其局部复发的频率较高,并可能发生脑脊液播散。
•••End•••


















共0条评论