1、概述
获得性囊性肾病(acquired cystic kidney disease,ACKD)在1977年由Dunnill等首次报道,定义为发生于肾衰竭终末期或透析患者一类肾脏慢性进行性多发囊肿性疾病。目前随着医疗技术不断进展,延长了终末期肾病患者生存期,致使ACKD患者不断增多,而ACKD癌变文献报道率因此亦有所升高,目前ACKD已被公认为一种癌前病变,从而受到了广泛重视。Lin等文献报道长期血透患者ACKD发生率约为40%-50%,获得性囊性肾病相关肾细胞癌(Acquired cystic disease-associated renal cell carcinoma,ACD-RCC)发病率较普通人群肾癌发病率高14-17倍,目前国内外ACD-RCC诊断和治疗文献报道却甚少。
1977年Dunnill等首次报道ACKD发病率在长期血透患者中为47%,Lin等认为长期血透患者中ACKD发生率为40-50%,ACKD发病率与血透时间呈明显相关性,血透时间1-3年患者发生率为10%-20%,3-5年者为40%-60%,5-10年者则高达90%以上。ACKD本身不影响血透患者寿命,但ACKD患者RCC发生率显著高于普通人群。Ishikawa报道维持性血透患者进展为RCC平均时间为8.8年,发生率更高达2.3%-3.7%。由于国内大样本长期血透患者ACD-RCC文献报道较少,随着我国经济发展、医疗技术水平提高和人民群众医疗健康意识不断增强,维持性血透患者数量增多及存活时间延长,ACD-RCC成为目前影响长期血透患者寿命的重要因素之一。目前公认针对ACKD其诊断务必具备以下3点:①长期血液透析终末期肾病;②单侧肾囊肿数目≥3个,且慢性肾病发病前未发现囊肿;③无遗传性囊性病家族史或其他遗传性囊性病证据。
2、发病机制
ACD-RCC发生机制尚不明确,可能与多种因素直接或间接作用有关。有文献研究认为与肾脏功能衰竭时,因有效肾单位锐减从而促使体内促肾生长因子代偿性增加,可促进肾系膜细胞及上皮细胞等代偿性增生肥大,间质纤维化从而形成囊肿;局部缺血及草酸盐堆积致肾小管栓塞和尿毒素代谢降低;也有人认为癌变本质为囊内液体通过酶解作用于上皮,从而最终导致恶变,关键在于原癌基因的激活。也有研究认为ACKD癌变机制可能与一些能够通过破坏DNA而抑制细胞复制的物质存在于ACDK囊液中,长期损伤DNA及DNA自身修复过程中发生错误修复,因而导致基因突变有关。囊肿上皮多表现为“增生-不典型增生-腺瘤-癌”发展过程,而肾小管上皮增生原因尚不明确,但与终末期肾脏分泌某种生长因子作用于尚存的肾细胞导致增生有关,与常染色体染色体疾病多囊肾类似,由内衬细胞增生,由一层变为多层,分泌囊液而形成。
3、临床症状
ACD-RCC患者早期常无症状,可因囊内出血或感染引起腰痛、血尿,但肾癌典型“三联征”少见,同散发性肾癌相比,血尿相对多见,镜下血尿、无痛性肉眼血尿均可见,但大多数患者起病隐匿,多是由体检或其他原因检查偶然发现。因此ACD-RCC诊断主要依靠定期体检及规范筛查,因此目前认为终末期肾病患者血液透析治疗超过3年,应定期行泌尿系超声检查,必要时应行肾脏多排CT平扫。ACKD由于肾实质呈多发囊肿,特别囊壁增厚、有明显分隔、钙化及软组织或血块密度影者,应高度怀疑肿瘤,应尽快行临床肿瘤TNM分期。ACD-RCC患者多为男性,双侧或多发比例较普通人群RCC发生率高。
4、病理学特征
ACD-RCC病理类型与上皮增生密切相关,普通人群RCC病理类型中透明细胞肾细胞癌为主,其次为乳头状肾细胞癌及嫌色细胞肾癌。但ACD-RCC病理类型有所不同,其大体形态多较局限,常为双侧性或多灶性病变,与周围肾有致密纤维包膜,边界清楚,周围可见多囊肾背景。组织学表现常见筛状、微囊状、实性片状、乳头状等结构;镜下肿瘤细胞胞浆呈嗜酸性,胞核分级高,WHO/ISUP核分级多为3级,可见明显核仁;肿瘤内见丰富嗜酸性草酸盐结晶,在偏光显微镜下呈多彩状。文献报道个别具有肉瘤样或横纹肌样分化者预后差,可发生转移。免疫组化标记物P504s、CD10、RCC、Vim等阳性表达,而CK7为阴性。
ACD-RCC主要鉴别诊断是透明细胞乳头状肾细胞癌(clear cell papillary renal cell carcinoma,CCPRCC),该肿瘤是一种新近被描述的肾脏低度恶性肾细胞癌类型。文献报道终末期肾病相关肾癌中ACD-RCC约占36%,CCPRCC则是第二常见,约占21%,而透明细胞肾细胞癌及乳头状肾细胞癌少见。CCPRCC多为单发,境界清楚,切面囊实性或实性,镜下具有囊性、小管/腺泡、乳头及巢状等典型生长方式;显著分支管状结构及突出于囊内的小乳头状结构是其特征性组织形,肿瘤细胞温和、胞质透明和胞核远离基底膜是其细胞学特征表现,肿瘤细胞呈立方形或柱状,胞核圆形或卵圆形,核仁不明显,细胞核分级低;肿瘤间质见平滑肌分化及“流产型”血管;免疫组化特征性表现CK7阳性和CD10阴性,CAIX多为弥漫性杯口状阳性。
5、临床治疗及预后
治疗方案应同散发性肾癌一致,根治性肾切除术是治疗ACD-RCC唯一有效方法,手术方式首选后腹腔镜下根治性肾切除术,考虑大部分患者处于尿毒症或肾移植状态,若进一步行放化疗治疗,应根据临床情况调整用药。鉴于此病发病隐匿,易伴发肾癌,威胁患者生命,因此对伴ACKD患者定期规范筛查极为重要。此外ACD-RCC恶性程度相对较低,行根治手术后5年生存率与普通肾癌无明显差异,因尿毒症患者多伴有心血管、糖尿病及高血压等基础疾病,可程度影响患者生存时间,因此基础疾病治疗亦应引起重视。
随着我国医疗水平提高,维持性血透患者增多及寿命延长,临床医师需树立ACD-RCC筛查观念和合理筛查机制,对长期维持性血透患者进行规范筛查,可及早发现并行后腹腔镜下根治性肾切除术,降低血透患者死亡率,与此同时重视术后随访复查,延长无瘤存活时间,进一步延长维持性血透患者寿命。
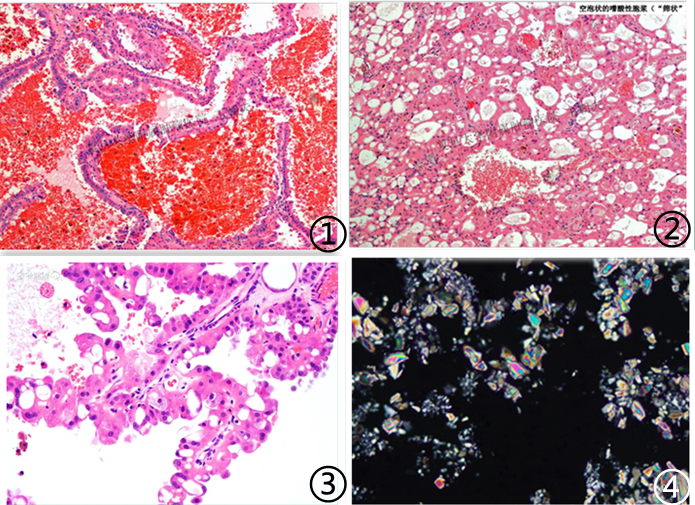
图1低倍镜下呈微囊状结构;图2低倍镜下表现为微囊状结构;图3高倍镜下肿瘤细胞胞浆嗜酸性,胞核分级高,见明显核仁;图4肿瘤内见丰富嗜酸性草酸盐结晶,偏光显微镜下呈多彩状;图片来自于参考文献课件5,6及网络,如有侵权,请联系删除。
参考文献:
[1]陈恕求, 陈明, 张晓文,等. 长期血透患者获得性囊性肾病合并肾癌8例报告并文献复习[J]. 临床泌尿外科杂志, 2012, 027(001):33-35.
[2]杨建勋, 付启忠, 董圣芳,等. 获得性肾囊性疾病合并肾癌11例临床分析[J]. 中华泌尿外科杂志, 2011.
[3]Eyzaguirre, Eduardo, Foshat, et al. Acquired Cystic Disease-Associated Renal Cell Carcinoma Review of Pathogenesis, Morphology, Ancillary Tests, and Clinical Features[J]. Archives of Pathology & Laboratory Medicine, 2017.
[4]Rivera M , Tickoo S K , Saqi A , et al. Cytologic findings of acquired cystic disease-associated renal cell carcinoma: a report of two cases.[J]. Diagnostic Cytopathology, 2010, 36(5).
[5]2016版WHO肾脏肿瘤新分类型解读,2016World Health Organization (WHO) Classifi- cation of Tumors of the Kidney: An Update。南京军区南京总医院,饶秋,周晓军
[6]肾脏肿瘤病理及新进展,复旦大学附属肿瘤医院,王朝夫
[7]朱冠辰, 宋剑楠, 连惠波,等. 长期血液透析的终末期肾病患者合并肾癌二例[J]. 江苏医药.














共0条评论