[导读] 作者:王学利
1 概论
管状囊状肾细胞癌(tubulocystic RCC, TCRCC)是近年来发现且逐渐被认识的一种罕见的肾脏肿瘤类型,至今全世界报道该肿瘤不足100例,国内亦仅有个案或小宗报道。曾在文献中被报道为“低级别集合管癌”或“集合管上皮瘤”,但现在认识到该肿瘤与集合管癌并无关联,因此在2012年ISUP肾肿瘤分类中,TCRCC被正式认定为肾细胞癌的一种独立的组织学亚型。2016版WHO肾脏肿瘤分类纳入了6种新的肾细胞癌亚型,TCRCC就是其中之一。为对该肿瘤有更深入的认识,笔者复习相关文献TCRCC的临床特征、病理组织形态学及免疫表型特点,临床治疗及预后情况,现报告如下。
MacLennan等在1997年首次描述13例具有管囊结构的肾细胞肿瘤,大体表现为实性、囊性或囊实性,肿块边界清楚,出血坏死少见,可见纤维包膜,肿瘤细胞核级别低,核分裂象罕见,认为是肾集合管癌的一类低度恶性亚型。 Osunkoya等人在2009年比较7例TCRCC与8例集合管癌的免疫组化特点,发现TCRCC不同于集合管癌。Amin等人于同年研究TCRCC的电镜特点,显示肿瘤细胞兼有近端小管和中间管的特点,细胞有大量具有刷状缘的微绒毛,胞浆内有大量线粒体,认为应将TCRCC视为一种独立类型低度恶性肾脏肿瘤。生物学行为上,大多数TCRCC表现为惰性的临床进程,少数病例可出现局部复发或远处转移。
2 临床特征
TCRCC患者均为成人,好发于男性,男女比在7∶1,发病年龄18-94岁(平均约54岁),占全部肾癌不足1%。临床表现不典型,多数为无意发现或体检时发现,也有尸检时发现的报道,少数患者有肾区疼痛,腹部包块和血尿的症状或体征。影像学检查常呈囊性肿物。肿瘤直径0.7-17cm,大体上表现为位于肾皮质的界限清楚的灰白色囊性肿块,常见包膜。切面几乎完全由薄壁的半透明囊肿组成,切面呈海绵状或蜂窝状。
3 病理诊断
组织学上,TCRCC由比例及大小不等的小管及囊肿构成,管壁衬覆单层上皮组织,上皮呈立方状、扁平或鞋钉样,部分病例可见肿瘤细胞呈分支乳头状增生突向囊腔,类似于乳头状肾细胞癌。肿瘤细胞胞质丰富,胞核大,可见明显核仁,(细胞核形态相当于WHO/ISUP 3级),囊性结构被不等量的纤维组织分隔,偶尔可见慢性炎细胞浸润。免疫表型显示肿瘤来源于近曲小管及远曲小管,TCRCC弥漫表达PAX8、CK19、CD10、AMACR以及vimentin,半数表达PAX2、CAIX,少数表达CK7和34βE12,肿瘤细胞增殖指数低。
荧光原位杂交(FISH)分析表明TCRCC存在第7号和第17号染色体的获得以及Y染色体的丢失,提示其与乳头状肾细胞癌存在密切的关系,两者具有相似的免疫表型和遗传学特征,这些证据均表明TCRCC有可能是乳头状肾细胞癌的一种多囊性变异型。Osunkoya等人报道在分子水平TCRCC和集合管癌完全不同,进一步分析证实其分子表达模式类似于乳头状肾细胞癌,通过比较基因组学分析,TCRCC显示17号染色体获得,而非7号染色体,然而大数乳头状肾细胞癌具有17号染色体和7号染色体的三聚体。因此基于其独特的病理形态学特点和分子学特征,TCRCC应被视为单独的肾细胞癌亚型。
3 鉴别诊断
①混合性上皮间质肿瘤(mixed epithelial and stromal tumor, MEST)/囊性肾瘤(cystic nephroma,CN)在2012年ISUP温哥华肾肿瘤分类中,MEST与CN被认为是同一病变的两种不同的组织学变异型。在于MEST与CN在临床表现、组织形态学特点、免疫表型和遗传学特征方面存在明显的相似性。常为偶然发现,较大的肿瘤可表现为腹痛、血尿以及季肋部肿块。绝大多数患者为女性或常有外源性女性激素使用史。大体上通常位于肾中央,肿瘤界限清楚,但无包膜,切面上CN几乎完全由薄壁囊肿构成,而MEST则为囊实性。组织学上,CN几乎均由大小不等的薄壁囊肿构成,缺乏实性成分,囊壁衬覆单层扁平/立方细胞或鞋钉样细胞,间质为少细胞的纤维性间质或致密的类似于卵巢皮质的短梭形间质。而MEST的上皮和间质则可表现出明显的组织学异质性,囊肿可呈腺管、小囊、微囊等。内衬上皮可为扁平或立方状细胞、鞋钉样细胞、柱状上皮或尿路上皮,偶尔可为透明细胞。MEST的间质可表现为少细胞的玻璃样间质、致密的卵巢样间质、平滑肌瘤样间质或非特异性的梭形细胞间质,罕见情况下可出现类似于卵巢的性索样间质、脂肪化生、黏液变性、钙化和骨化等。免疫表型特征,上皮细胞表达PAX8、PAX2以及CK7;间质细胞表达ER、PR和SMA。
②多房囊性肾细胞癌(multilocular cystic renal cell carcinoma, MCRCC)/低度恶性潜能的多房囊性肾细胞肿瘤(multilocular cystic renal cell neoplasm of low malignant potential)MCRCC是一种完全由囊肿和透明细胞构成的罕见类型的肾细胞肿瘤,临床上多数患者为偶然发现。影像学上常表现为复杂的囊性肿块伴局灶钙化。大体切面肿瘤界限清楚,几乎完全为囊性,囊肿直径大小不等互不交通,囊壁平滑,内容清亮或血性液体。囊壁间隔薄,无实性膨胀性结节。组织学上囊肿被覆单层透明或弱嗜酸性的上皮细胞,少数可为复层,偶尔可见上皮呈低乳头状增生突向囊腔,有些囊壁无上皮衬覆。上皮细胞核级别低,通常WHO/USUP为1级,偶尔可为2级。囊肿间隔为富于血管的纤维性间质,常见水肿及炎细胞浸润,偶见钙化或骨化。间隔内可见小簇状的肿瘤细胞灶,但不形成膨胀性的实性细胞巢。免疫表型特征,常表达PAX8、EMA、CAⅨ,大多数表达CK7,半数左右表达CD10和Vimentin。分子遗传学研究表明MCRCC存在VHL基因突变以及第3号染色体短臂的缺失,支持其为CCRCC的一种囊性组织学亚型。
③血管平滑肌腺瘤样肿瘤(renal angiomyoadenomatous tumor,RAT)RAT是由上皮性小管和成熟的血管平滑肌瘤样间质构成的一种具有独特组织形态学特征的肾脏肿瘤,好发于中老年男性,临床上肿瘤多为偶然发现,少数表现为腹痛或血尿,偶尔发生于终末期肾疾病。大体上直径较小,切面实性为主,可见不同程度的囊性变,常见厚的纤维性假包膜。RAT的镜下表现取决于上皮与间质的比例,肿瘤周边一般为厚的致密的平滑肌束,平滑肌细胞有明显的嗜酸性胞质,常见厚薄不等的血管性间质。肿瘤的中央为上皮成分,具有透明或弱嗜酸性胞质,排列成致密的腺泡/小管或大小不等的囊肿,包被于致密的血管平滑肌瘤样间质中,囊肿内可见突向囊腔的分支乳头状结构。上皮细胞的核级别低,一般胞核WHO/ISUP为1级或2级,偶尔可见细胞核远离小管的基底部朝向腔面分布,类似于分泌期子宫内膜的核下空泡。免疫表型特征,上皮细胞弥漫表达PAX8、CK7、CAIX、Vimentin及34βE12,局灶或弱表达CD10,不表达RCC和AMACR;血管平滑肌样间质弥漫表达SMA和Desmin,不表达HMB45、Melan A以及ER和PR。分子遗传学研究表明RAT无透明细胞肾细胞癌常见的第3号染色体短臂缺失和乳头状肾细胞癌常见的第7号和第17号染色体的三体性以及Y染色体的丢失。
④囊性部分退变的透明细胞肾细胞癌(cystic partially regressed clear cell RCC)透明细胞肾细胞癌常见出血、坏死以及囊性变,罕见的情况下广泛的出血坏死可导致肿瘤出现广泛的退变或囊性变。囊性部分退变的透明细胞肾细胞癌大体上表现为多房性囊肿,囊肿间隔的厚薄不均匀,较厚的区域仔细检查常可发现小灶的灰黄实性结节。组织学上,囊壁衬覆多数为低核级透明细胞,间隔内的肿瘤细胞呈小灶状至实性结节状分布,间质通常为厚的少细胞的玻璃样间质,偶尔可为富于细胞的肌纤维母细胞性间质,常见含铁血黄素沉积及营养不良性钙化,这些组织学特征均为透明细胞肾细胞癌退行性变的证据。
⑤获得性囊性肾病相关的肾细胞癌(acquired cystic disease–associated RCC,ACD–RCC)终末期肾病患者容易罹患,特别是在接受长期透析而伴有获得性囊性肾病。大多数为在透析随访过程中由影像学检查偶然发现,大体上常表现为起源于囊肿的实性结节或表现为囊肿附近的实性肿块,界限相对清楚,常见纤维性包膜;切面质地软,常见出血和坏死。组织学上显示多种结构和生长方式,可见腺泡、小管、微囊、巨囊、乳头状以及实性片状的组织构型。瘤细胞大多数具有丰富的嗜酸性胞质,偶尔可为透明胞质,核级别高,可见明显的核仁。免疫组化方面表达AMACR、CD10、RCC和Vimentin,大部分CK7阴性表达。分子遗传学方面存在第3号、7号、16号、17号和Y染色体的获得。
4 治疗及预后
TCRCC的大宗病例报道较少,因此未有合适的临床治疗方案可供参考。有文献报道采用舒尼替尼进行治疗的成功个案。术后发生骨和肝转移的报道中2例转移者均可见灶状透明细胞改变,其中1例转移灶呈温和的管状和巢状透明细胞两种结构。也有出现盆腔淋巴结转移的报道。有学者认为转移和复发是因为合并乳头状肾细胞癌的缘故,伴有低分化区域者增加TCRCC发生侵袭的几率。这些不良预后结果提示需慎重对待TCRCC的恶性程度评估。建议对TCRCC患者应长期密切随访,以获得更全面的患者临床预后资料。
综上所述,TCRCC有别于普通肾细胞癌,是具有形态特异性和临床病理特点的肾细胞癌亚型,大部分生长缓慢,预后良好,属于低度恶性潜能的肿瘤。目前,对TCRCC的生物学特性尚不清楚,需积累更多的临床资料总结其生物学特性。
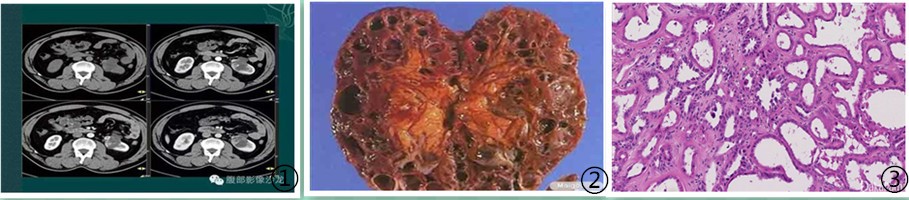 ①TCRCC影像学呈囊性;②TCRCC大体呈囊性,海绵状;③低倍镜下TCRCC由比例及大小不等的囊肿构成,管壁衬覆单层上皮组织,上皮呈立方状。
①TCRCC影像学呈囊性;②TCRCC大体呈囊性,海绵状;③低倍镜下TCRCC由比例及大小不等的囊肿构成,管壁衬覆单层上皮组织,上皮呈立方状。
参考文献略。 图片来源于网络。














共0条评论