[导读] 作者:青海涛;来源:南方医院消化科青海涛大夫 公众号
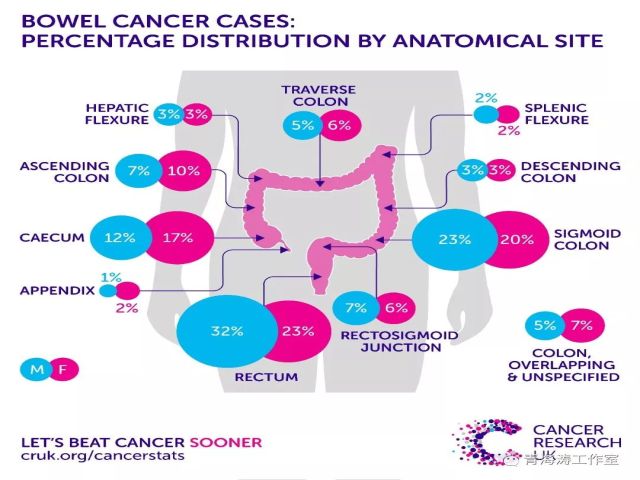
结直肠癌(CRC)是一个主要的健康问题,尤其是在西方国家。根据美国癌症协会的估计,CRC在美国的死亡人数约为50000人,在2016年确诊了近130000例新病例,为第三种最常见的癌症。因此,有效的鉴别结直肠癌及其癌前病变至关重要的。
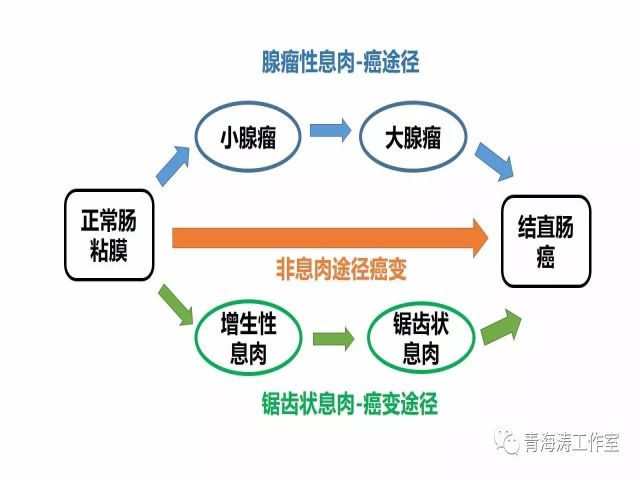
结直肠癌变的3种主要途径
散发性结直肠癌是最常见的肠癌(占比95%,其余为遗传性结直肠癌),其最常见的3种致癌模式如下:
1.小腺瘤→大腺瘤→癌的途径约占癌症的50%-70%;
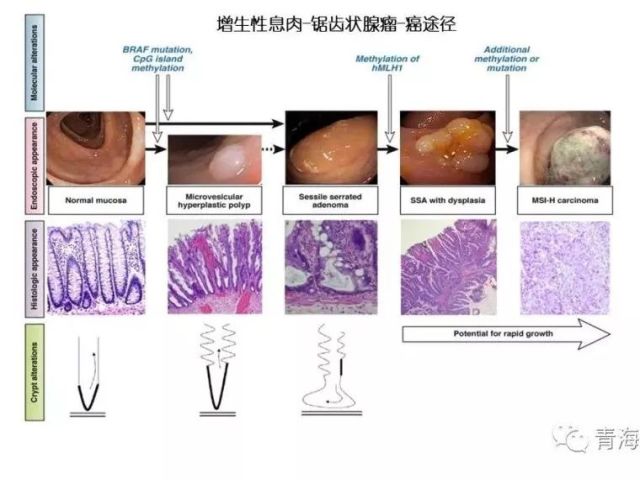
2.锯齿状病变至癌途径(30%-35%),基本过程为「增生性息肉→锯齿状腺瘤→腺癌」;
3.通过Lynch综合征途径致癌(3%-5%)。
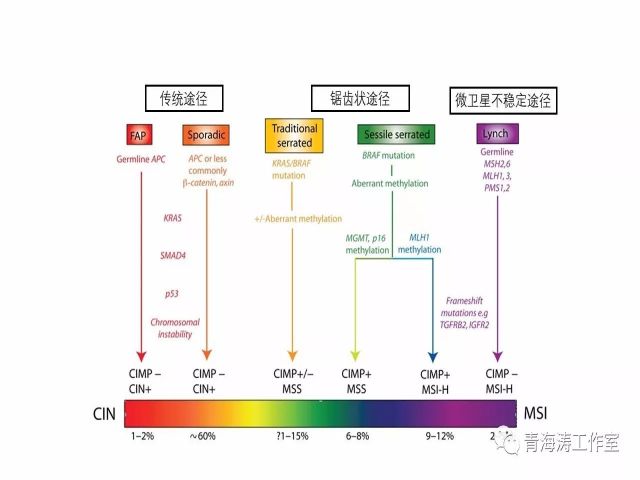
在过去的几十年中,腺瘤到腺癌的途径已经得到了很好的认识。有一段时间,它被认为是除了“林奇综合症”路线之外的导致CRC的唯一途径。在预防结直肠项目中,发现和根除腺瘤是主要的努力目标。Zauber等表明在息肉切除术后的前10年,结肠镜切除腺瘤性息肉导致CRC死亡率降低了53%。腺瘤息肉是传统上被认为是唯一的结肠直肠癌的癌前病变,锯齿状病变致癌途径是近年来认识肠癌演进模式的一个重要的里程碑。大约20-30%%的散发性结直肠癌通过这条通路发展,主要的癌前病变为无蒂的锯齿状腺瘤/息肉(SSA/P)。SSA/P具有恶变潜能, 且进展快, 与右半结肠癌的发生密切相关。其他癌变模式还有:炎症→癌途径和De novo途径(由正常粘膜不经过腺瘤途径而直接癌变)。
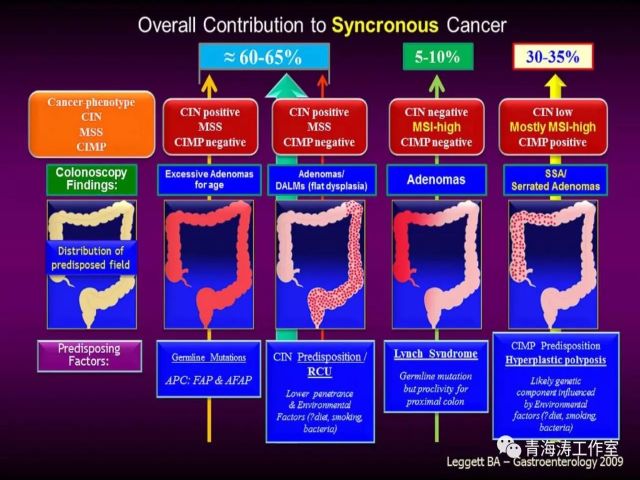
结肠息肉是结肠癌最常见的癌前病变,常因体检结肠镜检查或出现便血等其他症状而被发现。大多数情况下它们可以分为腺瘤(管状腺瘤超过80%,绒毛腺瘤5-15%,管状绒毛腺瘤5-15%)、锯齿状(无蒂或传统)腺瘤或非肿瘤(增生性和幼年性)。增生性息肉最常见,具有极低的恶性潜力,他们在远端结肠遇到更多。无蒂锯齿状腺瘤/息肉(SSA/Ps)占所有锯齿状息肉的20%,通常为无蒂或扁平病灶,多见于右结肠。息肉可以是凹陷、平坦、无蒂或有蒂。
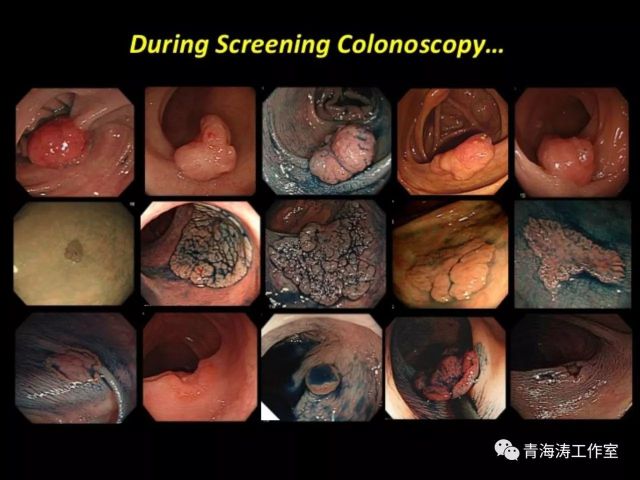
什么样的息肉需要内镜下切除?息肉的具体管理方法,主要参考日本胃肠病学会(JSGE)发布的大肠息肉的管理2014版。
>6毫米腺瘤建议切除,<5毫米的腺瘤一般建议随访
内镜切除应该用于>6毫米的病变(证据等级C)。然而扁平和凹陷的微小病变(<5毫米)也应该内镜切除(证据级别D)。
因为>6毫米的病灶癌变率高于5毫米,而且单靠结肠镜检查通常很难区分良性腺瘤和癌。根据英国的一项研究,如果<5毫米病灶的癌变相对风险被认为是1,而6毫米、10毫米、11-20毫米和>20毫米病灶癌变风险分别增加到7.2,12.7,和14.6倍,因此>6毫米应切除。然而,对于<5毫米的扁平或凹陷腺瘤,因为癌变率比隆起型腺瘤的高,也建议内镜下切除。
如何管理≤5毫米的小腺瘤?
一般建议随访(证据水平C)。然而,对于难以区分是否为腺瘤或癌(证据水平D)的小而平坦或凹陷性病变,应行内镜切除。
≤5毫米腺瘤样息肉,至少在原则上,在结肠镜检查中除外癌变后可以随访。在结肠镜检查中被怀疑为腺瘤或癌的扁平或凹陷性病变,最好由内镜切除治疗。
小腺瘤癌变的主要征象
(1)膨胀性的外观(类似粘膜下肿瘤);
(2)表面凹陷;
(3)外观粗糙(表面粗糙无光泽);
(4)V型腺管开口(表面结构不规则或消失)。
为了证实这些发现,建议对可疑病变使用染色内镜或放大结肠镜检查。一项关于微小结肠直肠病变的队列研究报告显示,在随访2-3年后,病变的大小或形状几乎没有变化。据报道,西方国家微小的结直肠病变癌变率从0.03-0.05%不等。根据一项大规模队列研究,息肉切除相关并发症的总发生率为0.7%,穿孔率为0.1%(每千次切除1例)。此外,为减少不必要的健康个体风险和降低费用成本,并不是所有的微小病变(≤5毫米)需要内镜下切除。
如何管理增生性息肉?
≤5毫米的直肠乙状结肠增生性息肉建议随访(证据级别D)。≥10毫米的右半结肠病变建议内镜切除,因为很难区分它们是否为无蒂锯齿状腺瘤/息肉(SSA/P),而这些病变的癌变率约9.4%(证据级别D)。
两项1800例关于肿瘤筛查的大型研究提示,首次结肠镜检查时发现有增生性息肉的患者再次检出增生性息肉的风险明显升高(OR 3.67;p<0.001)在。此外,首次检查时发现腺瘤息肉后腺瘤复发的风险也明显增高(OR 2.08;p <0.01)。
如何治疗锯齿状病变?
锯齿状病变指一组以上皮锯齿状结构为特征的病变。包括:
1.广基/无蒂的锯齿状腺瘤/息肉(SSA/P)
2.传统锯齿状腺瘤(TSA)
3.增生性息肉(HP)。
前两种病灶有可能发展为腺癌,因此建议治疗(证据级别D)。
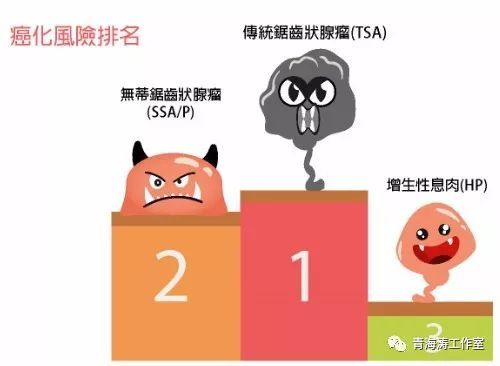
SSA/P与BRAF突变和CpG岛甲基化相关,被认为是结直肠癌的癌前病变。最近的研究报告SSA/P的癌变率从1.5到20%不等,因此对SSA/P应进行积极的切除。Pohl等人发现与常规腺瘤相比,锯齿状息肉的不完全切除率更高。不完整切除SSA/P可能是导致间期癌的主要原因,建议在术后3个月后进行肠镜检查。
TSA是一种罕见且特殊的锯齿状息肉,它占所有结肠息肉的1%,往往发生在远端结肠和直肠,通常有一个绒毛状外观,表面显著发红隆起。TSA通常会显示出异型增生,可能是锯齿状或肠型,或两者混合。近年来的研究表明TSA可能是侵袭性结肠直肠癌的癌前病变。在组织学上,TSA被认为有可能进展到癌,类似于SSA/P。因此对于对≥5毫米的TSA建议内镜下切除。至于SSA/P,大多数研究都建议切除≥10毫米的病灶。HP可能是SSA/P和TSA的前期病变,≤5毫米的HP不需要进行治疗。
侧向发育型肿瘤(LST)均建议内镜下切除
大肠侧向发育型肿瘤(Laterally spreading tumor,LST)的概念最早于1985年由日本学者工藤提出。是指起源于大肠粘膜的一类平坦隆起型病变,这类病变主要沿粘膜表面呈侧向浅表扩散,故称为侧向发育型肿瘤。实际是一种特殊类型的大肠腺瘤。它的定义包含三部分内容:
1.直径大于10 mm;
2.生长方式为侧向发展而非向深层垂直生长;
3.依据其表面形态可分为颗粒型(颗粒均一型和结节混合型)和非颗粒型(平坦隆起型和假凹陷型)。
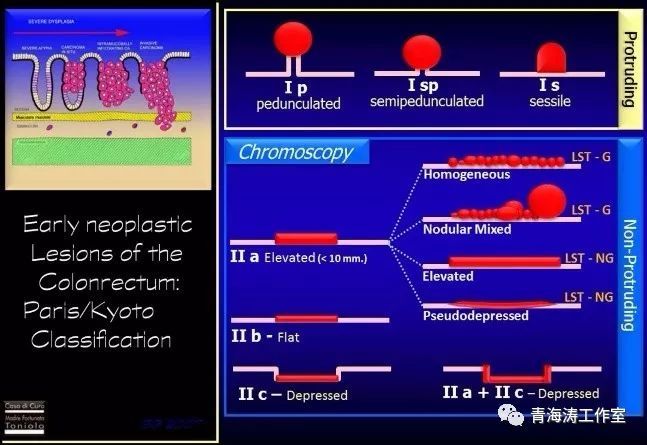
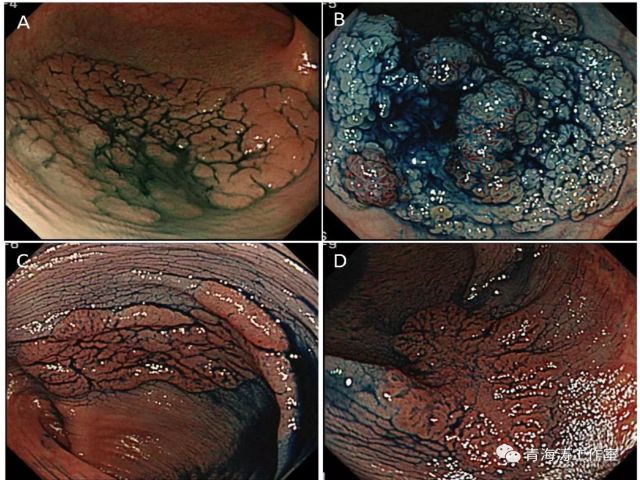
A:颗粒均一型;B:结节混合型;C平坦隆起型;D假凹陷型
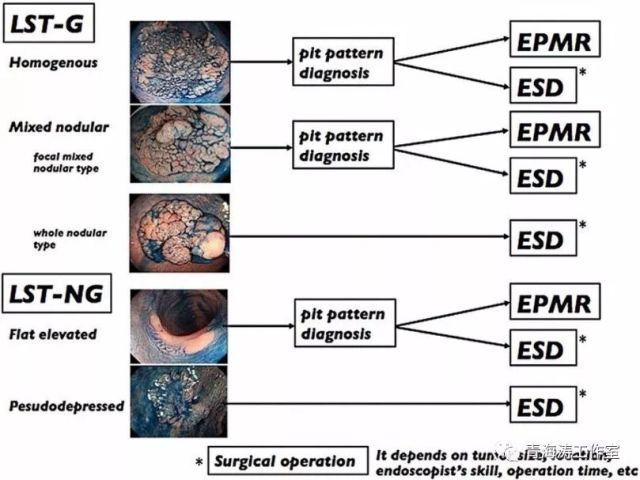
治疗应以LST亚型为基础来选择EMR与ESD,并酌情使用放大内镜和内镜超声检查(证据水平C)。
1.颗粒均一型(LST-G)中癌或粘膜下浸润的发生率极低,可以通过分片EMR或ESD切除(依据内镜专家技术水平而定)。
2.结节混合型的LST-G中的大结节容易出现黏膜下的浸润应进行ESD整块完整切除。
3.平坦隆起型LST-NG的治疗应根据腺管开口类来确定采用分片EMR或ESD切除。
4.假凹陷型LST-NG因存在多灶粘膜下浸润的可能性,不应拘泥于其大小或腺管开口类型,应进行ESD整块完整切除。
综上所述,应根据LST亚型来选择采用ESD或分片EMR治疗;同时需要放大内镜和超声内镜进行术前评估。
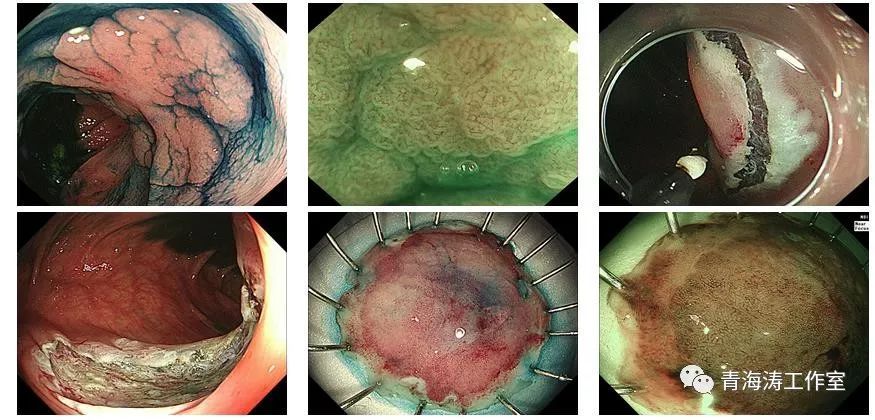
本人内镜下切除的肝区LST病例,大小约20*15mm,术后病理腺瘤性息肉,高级别上皮瘤变
什么是锯齿状病变?
锯齿状息肉是指在显微镜下有锯齿状或锯齿状的隐窝的病变,分三种类型,包括
1.具有结构异型性的无蒂锯齿状腺瘤/息肉(SSA/P)
2.具有腺瘤性细胞异型性的传统锯齿状腺瘤(TSA)
3.增生性息肉(HP)(无结构及细胞异型性)

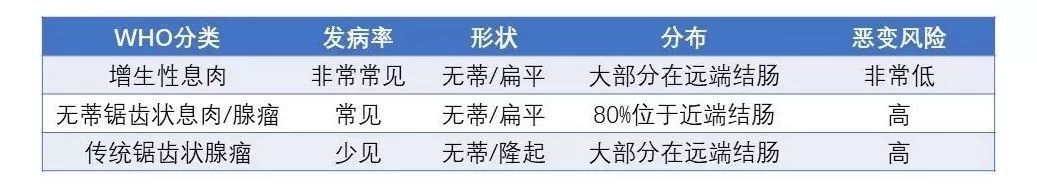
 增生性息肉是最常见的锯齿状息肉,占锯齿状息肉的80%,并无恶性潜能,多位于左半结肠,直径多<5 mm,形态学上表现为隐窝拉长并伴有隐窝表面程度不等的锯齿状结构。根据形态学分类,HP又可分为3型:
增生性息肉是最常见的锯齿状息肉,占锯齿状息肉的80%,并无恶性潜能,多位于左半结肠,直径多<5 mm,形态学上表现为隐窝拉长并伴有隐窝表面程度不等的锯齿状结构。根据形态学分类,HP又可分为3型:
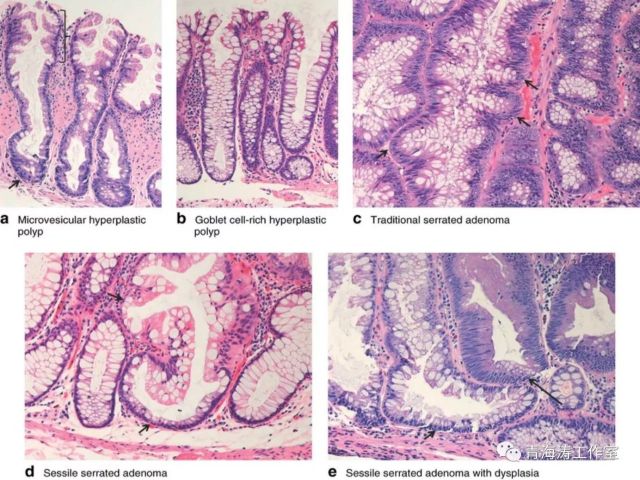
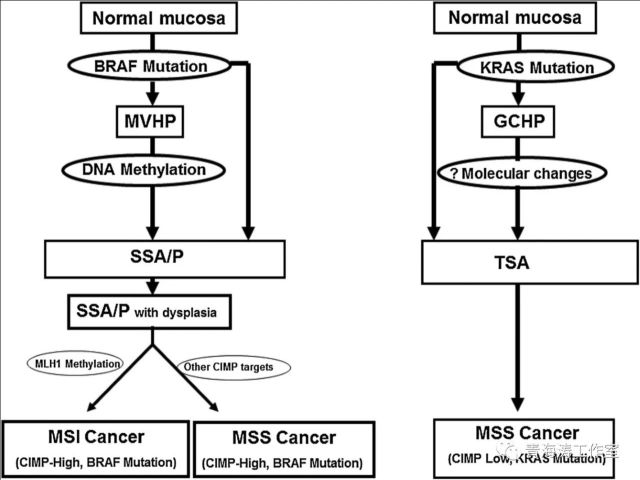
1.微泡型(MVHP)
2.杯状细胞丰富型(GCHP)
3.黏液缺乏型(MPHP)。
不同类型的HP可向SSA/P或TSA演进,研究表明,微泡型HP(MVHP)可能是SSA/P的前体;杯状细胞丰富型HP(GCHP)与TSA之间有关联。
TSA发病率很低,占全部息肉的1.0-1.6%,左半结肠多见,形态上以隆起型为主伴有部分平坦的双层隆起型病变,表面构造呈绒毯样或珊瑚状。确诊需要组织病理学。
SSA/Ps占锯齿状息肉的20%,通常为无蒂或扁平病灶,多见于右结肠,多大于5-10毫米。内镜下观察其表面呈云雾状,不规则,有黏液,边缘模糊。在内窥镜检查中,SSA/Ps扁平的形态导致很难被发现,经常有覆盖的黏液,这使得它们比传统的腺瘤更容易被忽视。而清洗粘液之后,则较难区分息肉和周围的正常黏膜,因此若遇到较差的肠道准备,很容易被遗漏。若想提高SSA/P的检出率,必须有高质量的肠道准备,仔细检查黏膜并反复冲洗、肠管的充分扩张以及缓慢的退镜。SSA/Ps的边界不清增加了不完全切除的风险。SSA/Ps被认为是与大肠间期癌密切相关,被认为是结直肠癌的癌前病变。
SSA/Ps的内镜诊断标准
Hazewinkle Y 等总结了SSA/Ps的内镜下特点,认为:边界不清、云雾样表面、NBI 下隐窝内黑点、形状不规则、pit pattern II-O 型腺管开口及正常血管密度为 SSA/Ps 内镜下特点。
1. SSA/Ps白光内镜及 NBI窄带光内镜显示息肉边界不清,颜色与周围粘膜相似
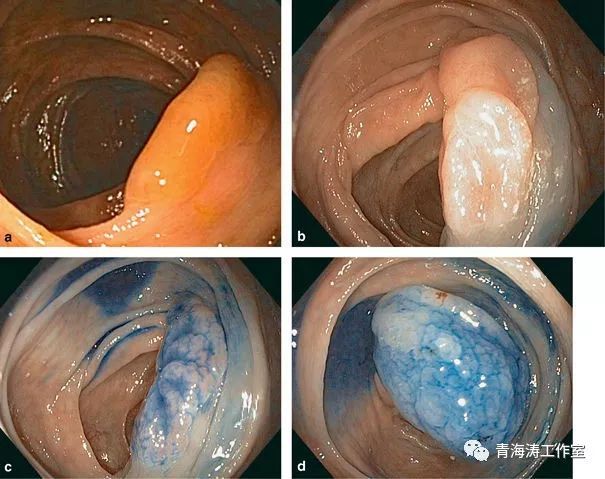
2. SSA/Ps平坦,积云样表面,NBI窄带光下呈红帽症,WLE 下可见隐窝内红点,NBI 下见隐窝内黑点
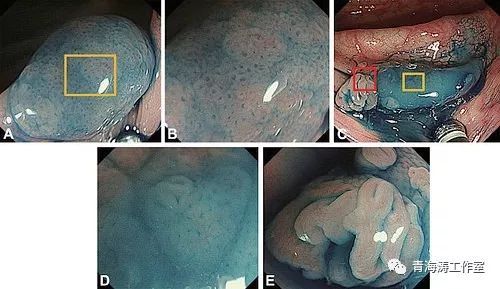
3. SSA/Ps Pit pattern II-O(open)示意图,腺管开放,呈星状延长
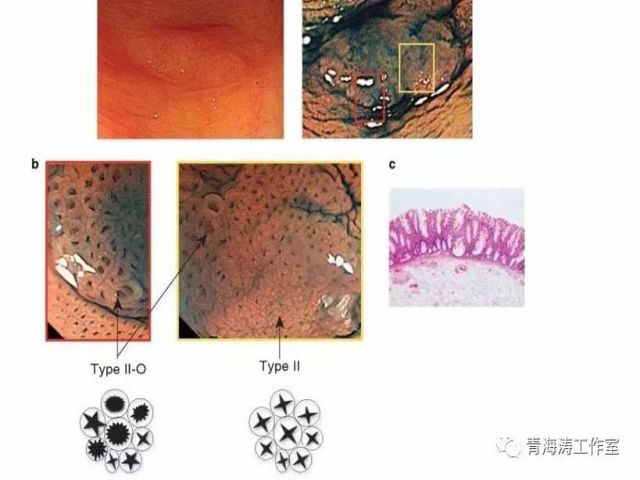
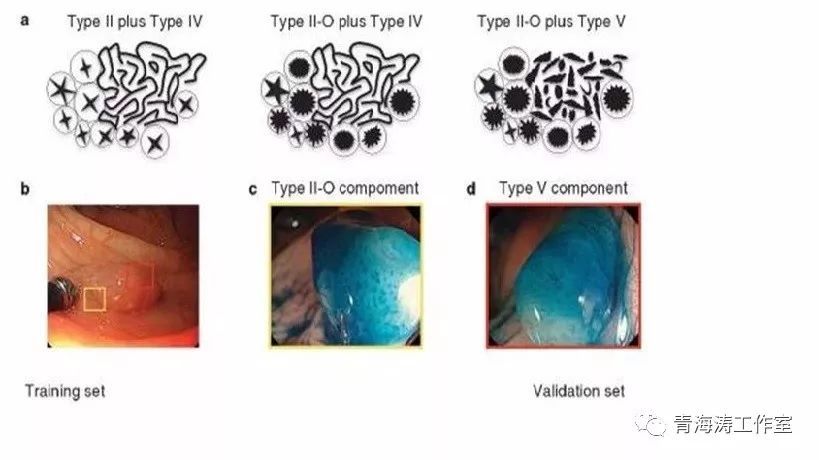
WASP 分类诊断SSA/P
当前的内镜下息肉分类法是建立在窄带成像技术(NBI)的基础上的,没有把无蒂锯齿状息肉包含在内。为此,来自荷兰的 IJspeert 教授等多位专家成立了 WASP 工作组,提出了一项新的分类方法,发表于近期的 Gut 杂志。专家们将现有的 NICE 分类方法和 Hazewinkel 等人提出的关于无蒂锯齿状息肉的诊断原则整合起来,设计出了内镜下诊断小/微腺瘤、增生性息肉和无蒂锯齿状息肉/腺瘤的新分类方法——WASP 分类
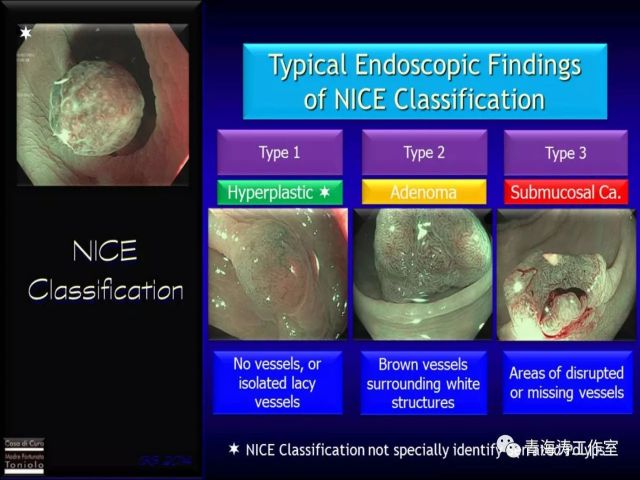
NICE 分类诊断增生性息肉、腺瘤、癌
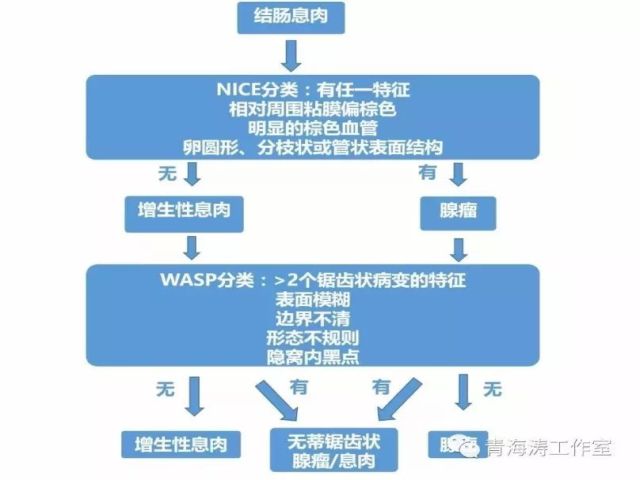
WASP 分类诊断增生性息肉、SSA/P、腺瘤
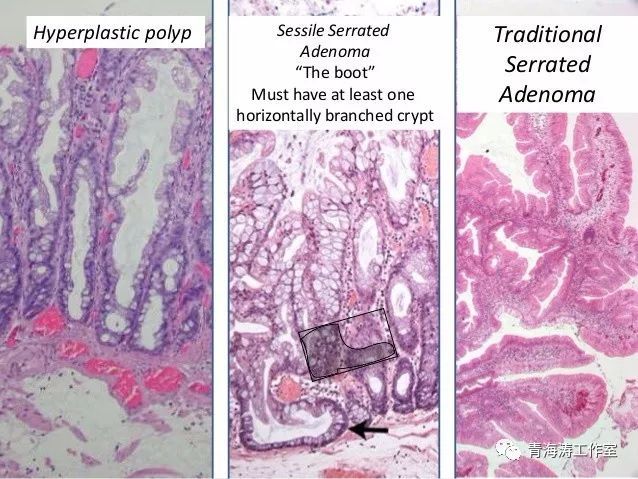
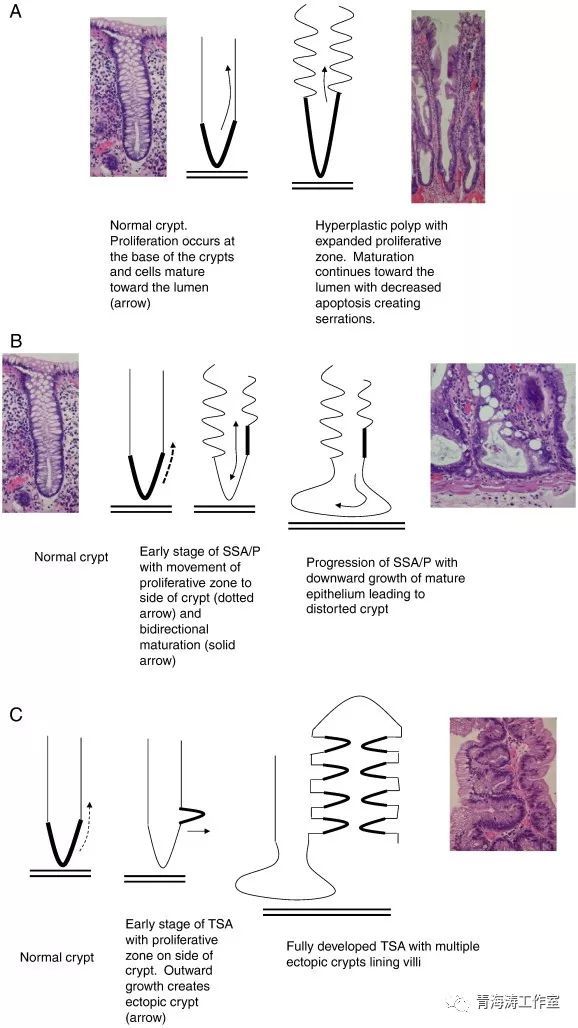
锯齿状病变各亚型病理诊断要点----主要依据是否存在结构或细胞异型性分类
HP镜下隐窝结构完整,中上部可见锯齿样结构,基底部较窄、无扩张,无细胞异型性,细胞核位于细胞中下部;
SSA镜下隐窝结构扭曲,可见弥漫的锯齿样结构,隐窝基底部常扩张膨大形成L型或倒T型,底部可见杯状细胞营养不良是其特征性改变,细胞核上升至细胞的中上1/3处;
TSA镜下可见隐窝呈复杂锯齿状结构,胞浆嗜酸,缺少粘液颗粒,杆状核,核异型性明显,假复层现象多见。
部分图片来自网络,侵删!
参考文献:
1.Rashtak S, Rego R, Sweetser SR, Sinicrope FA: Sessile Serrated Polyps and Colon Cancer Prevention. Cancer Prev Res (Phila). 2017, 10:270-278
2.Gibson JA, Odze RD: Pathology of premalignant colorectal neoplasia. Dig Endosc. 2016, 28:312-323
3.Tanaka S, Saitoh Y, Matsuda T, et al.: Evidence-based clinical practice guidelines for management of colorectal polyps. J Gastroenterol. 2015, 50:252-260
4.Murino A, Hassan C, Repici A: The diminutive colon polyp: biopsy, snare, leave alone? Curr Opin Gastroenterol. 2016, 32:38-43

















 增生性息肉是最常见的锯齿状息肉,占锯齿状息肉的80%,并无恶性潜能,多位于左半结肠,直径多<5 mm,形态学上表现为隐窝拉长并伴有隐窝表面程度不等的锯齿状结构。根据形态学分类,HP又可分为3型:
增生性息肉是最常见的锯齿状息肉,占锯齿状息肉的80%,并无恶性潜能,多位于左半结肠,直径多<5 mm,形态学上表现为隐窝拉长并伴有隐窝表面程度不等的锯齿状结构。根据形态学分类,HP又可分为3型:

















共0条评论