作者:陶祥1,赵澄泉2
单位:1复旦大学附属妇产科医院病理科,上海,200011;2 美国匹兹堡大学医学院,匹兹堡,PA 15213,美国
来源:妇产科网
美国及欧洲发达国家60年宫颈癌筛查历史已充分证明宫颈细胞学是预防宫颈癌的有效手段。宫颈细胞学筛查的前提是在规范的质控基础上开展。然而与发达国家相比,尤其是美国由美国病理医师协会(the College of American Pathologists, CAP)主导的细胞学质量管理(包括质量控制、质量保证以及质量改进三个方面),国内目前仍有较明显的欠缺。国内各地区的发展不平衡,缺乏全国性的严格统一的宫颈细胞学质量控制和检查标准。美国宫颈细胞学液基仅有2种方法,即Hologic公司的ThinPrep和BD公司的SurePath 2种产品,而国内除此之外,还有近百种液基产品在市场上应用。目前,美国CAP对其所有认证的实验室必须严格执行其质量保证/检查的各项要求,每年均有TBS报告率的总结调查,且每个病理医生者必须参加CAP宫颈细胞学执业资质与技能测试。而国内缺乏一全国范围内TBS报告及宫颈细胞学一般状况的总结研究。自2018年初,我们开始考虑实施做一独立的全国范围内的宫颈细胞学现状调查。本次调查的目的在于广泛采集国内不同级别、不同类型的宫颈细胞学实验室的数据,汇总成具有一定代表性的细胞质控数据。同时提出一些已被欧美发达国家验证有效的、且操作性强的宫颈细胞学质控方法,以供参与或未参与此次调查的实验室进行室间质评时参考。
本次调查采用网络无记名形式,在河南、山东、辽宁、浙江、安徽、河北、山西、四川、上海、广东、内蒙古、福建、甘肃、重庆、江苏、广西、新疆、湖南、湖北、吉林、北京、云南、天津、江西24省市以及香港、澳门特别行政区展开。各省市、自治区、港澳均有一病理或妇科带头人帮助推动,总共收集了1,656份反馈,其中有效者1,572份,约占所调查省份总实验室的20-70%。收集时间自2018-4-1至2018-5-30,为各家实验室的2017年全年数据。
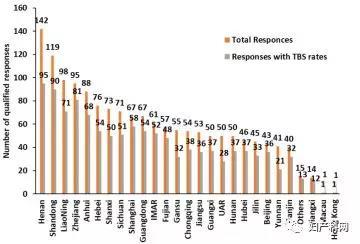
图1 各省市反馈调查表数量(橙色为总数,灰色为提交TBS报告率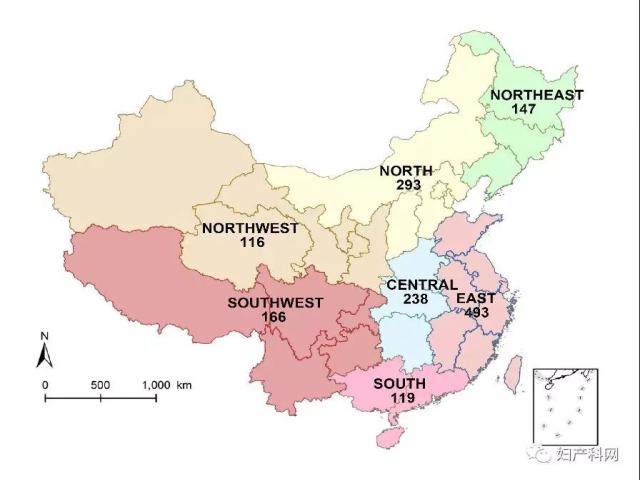
图2 反馈调查表的地区分布特征
采集的数据包括:所在的省份、医院性质、等级、开展科室、制片和染色方法、报告术语、HPV检测及DNA倍体检测有无、各类TBS报告率(液基和传统涂片分列)。为避免强迫答题而造成的结果不实,各题目均非必答题。因此文中以分数的分母、各表格中以n代表填写该题的实验室数目。
总结的调查结果论文被美国细胞病理学会(ASC)官方期刊美国细胞病理学杂志(JASC)接受,于2019年2月网上提前发表,英文题目为Nationwide Survey of Cervical Cytology Laboratory Practices in China,论文作者为:陶祥,R. Marshall Austin,孔令非,孙青,吕庆杰,徐海苗,孟刚,黄向华,郝敏,周桥,周先荣,王连唐,张越,许淑霞,石清芳,周琦,郭凌川,曾思恩,王玉兰,周建华,聂秀,田立祥,沈丹华,雷梓,刘易欣,梅金红,王锦詠,张雅贤,李娟,朱明华,赵澄泉。此文将结果简介如下:
基本信息:
1656个实验室的调查表,剔除不合格或重复提交的资料后共计1572份有效资料。1159份(73.7%)资料填写了TBS各判读比例的数据。提交份数排名前5位的省份为河南、山东、辽宁、浙江、安徽,分别有142、119、98、95和88份。
按医院的性质来分,综合医院1281家,占81.6%,其次为妇幼保健专科医院(12.0%)、其它医院(3.7%)和独立实验室(2.7%)。
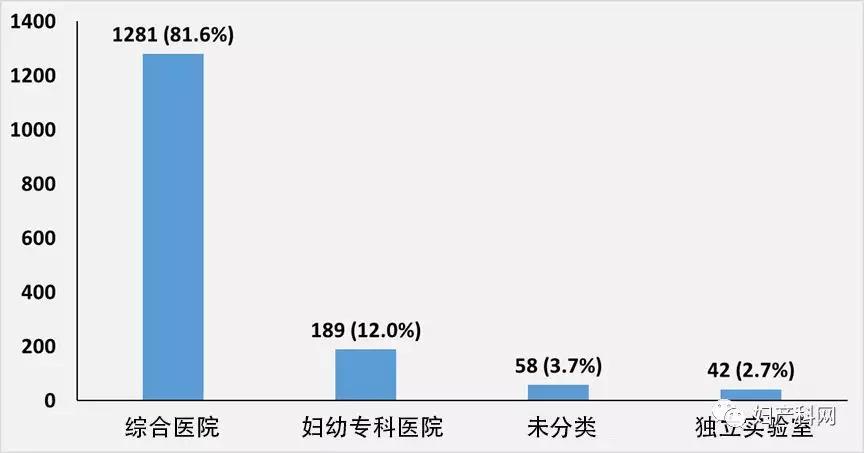
图1 开展的宫颈细胞学筛查的单位类型
按医院等级划分,三甲医院657家(41.9%),三乙医院200家(12.7%),二甲医院579家(36.9%),另有少量二乙、一级和未填写级别的单位。
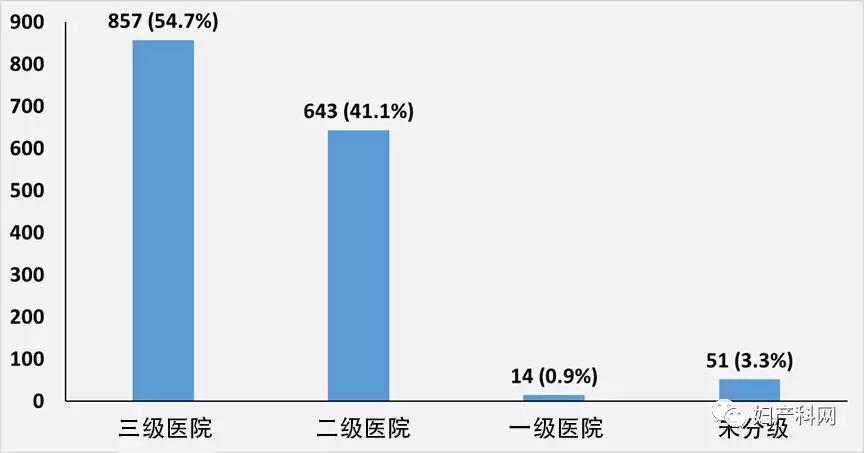
图2 开展宫颈细胞学的医院等级
细胞学所在科室从提交的表格来看,属于病理科业务的为1419家,占90.8%。2.4%(38/1562)属妇产科、3.9%(61/1562)属检验科,另有2.9%(45/1562)单位标本外送其它实验室。每间实验室2017年细胞学总量从小于100例至892142例不等,四分位数为5200 (2100,12424)例。按年宫颈细胞学量统计细胞学实验室数目,其中开展LBP的实验室规模在年1000~4999例的最多见(40.5%);开展传统涂片则最多见于年细胞学量<1000例(41.2%),各科室平均3.7位医师从事宫颈细胞病理诊断,其中1~2人规模占调查总科室的42.7%,3~5人占41.1%,6~9人占11.2%,10人以上占5.0%。从细胞学量和人员配备来看,细胞学实验室的总体规模较小。
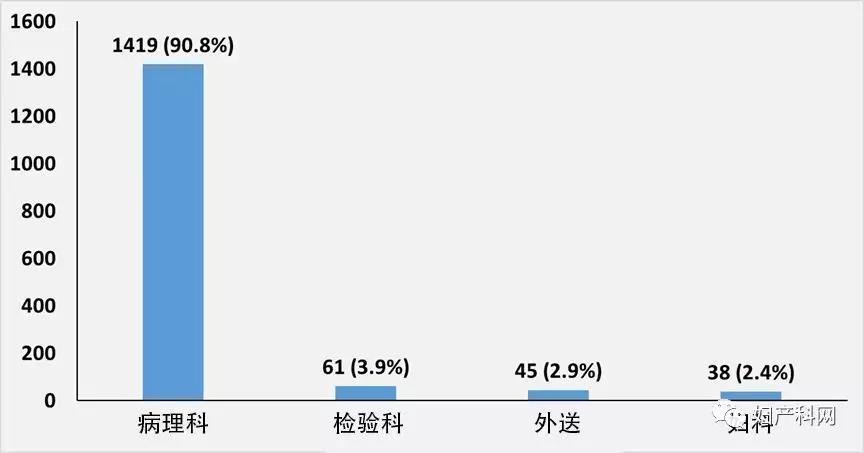
图3 开展宫颈细胞学的科室
细胞学染色方法选择上,63.7%(912/1431)的实验室仅有巴氏染色,19.5%(279/1431)的实验室仅有H&E染色。另有16.8%(240/1431)两种染色均使用。
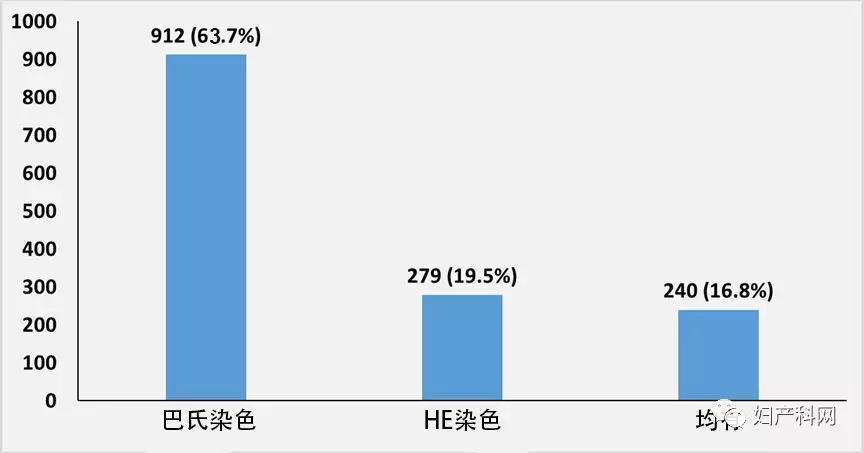
图4 细胞学的染色方法
LBP制片方法中,37%(548/1478)采用进口仪器,其中膜式制片(ThinPrep)占其中的75.7%(415/548),24.3%(133/548)为沉降式制片(SurePath)。国产方法占73.0%(1079/1431)。其中又以沉降式为多,占59.9%(646/1079)。另有8.5%(126/1478)单位选了其它制片方法。(表2)
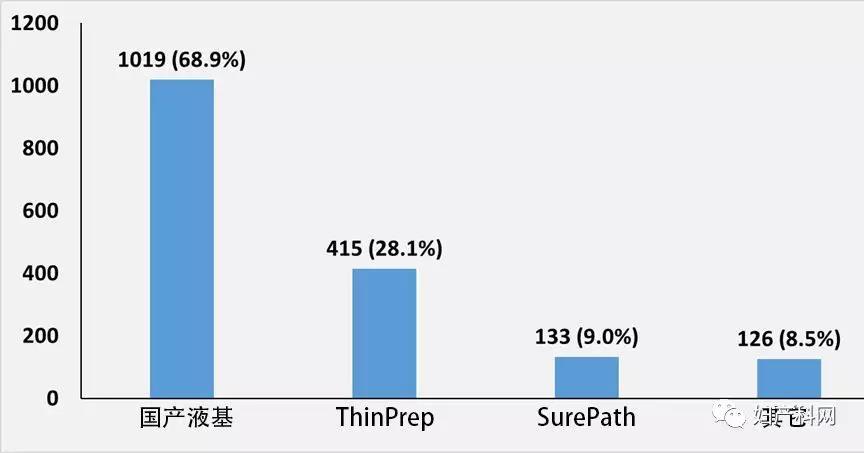
图5 液基细胞学制片设备
91.6%(1363/1488)的参与单位细胞学判读术语采用TBS判读,有4.4%(60/1488)仍采用巴氏5级判读标准。另有4%(65/1488)两种判读标准均采用,即8.4%的参与单位仍使用巴氏分级。
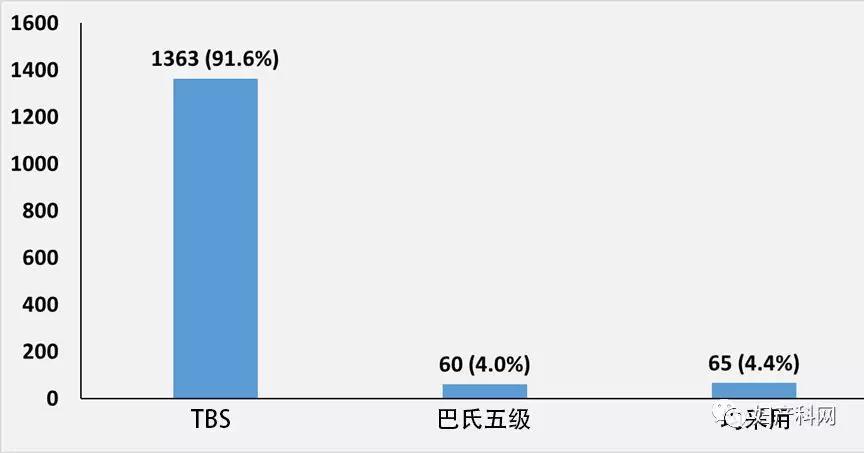
图6 宫颈细胞学的诊断术语
HPV开展的情况,此次提交的调查表中有86%(1307/1512)的单位开展。约一半在病理科开展(46.5%,609/1512),一半在其它科室开展(698/1512,46.2%)。
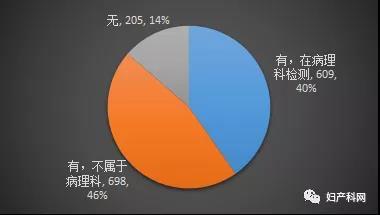
图7 HPV检测开展情况
DNA倍体检测有21%(319/1496)的参与单位开展。
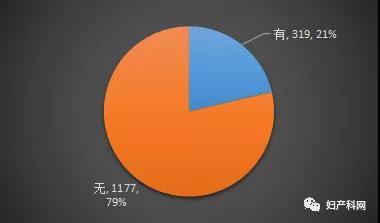
图8 DNA倍体检测开展情况
TBS报告率:
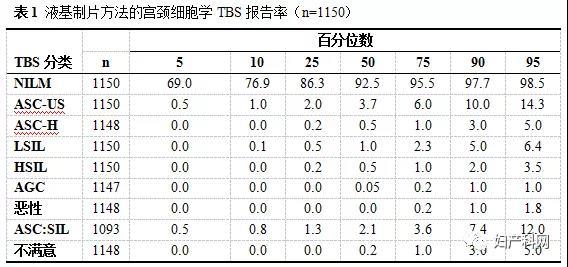
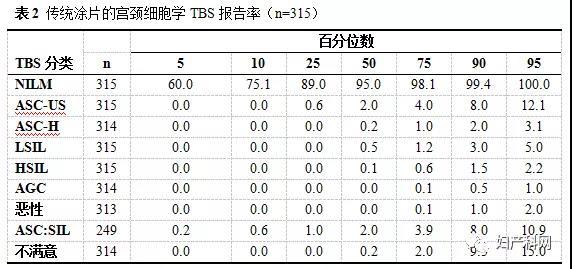
表1和表2分别列出了LBP和CP的TBS各判读类别的5、10、25、50、75、90和95百分位数的百分比,其中50百分位数值即中位数,25和75百分位数即下四分位数和上四分位数。结果显示,LBP和CP的阳性率(%,以下省略)分别为7.5(4.5,13.7)和5(1.9,11),两者之间存在显著差异(Wilcoxon符号秩检验,P<0.01)。LBP和CP的ASC-US判读率分别为3.7(2.0,6.0)和2.0(0.6,4.0),ASC-H判读率分别为0.5(0.2,1.0)和0.2(0.0,1.0),LSIL判读率为1.0(0.5,2.3),HSIL判读率为0.5(0.2,1.0),AGC判读率为0.1(0.0,0.2)和0.0(0.0,0.1)。各判读率的LBP与CP数据的差别均有统计学意义。
分层分析的TBS报告率:
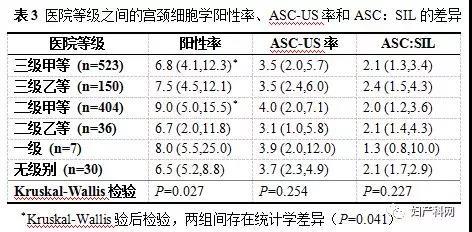
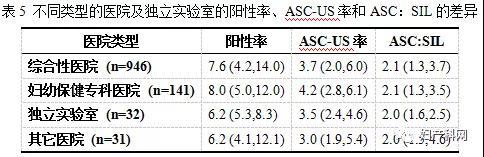
按医院等级划分,三级甲等与二级甲等的阳性率分别为6.8 (4.1,12.3)和9.0 (5.0,15.5),差异具有统计学意义(Kruskal-Wallis检验两两比较,P=0.041)(表3),而ASC-US率和ASC:SIL比值无统计学差异。
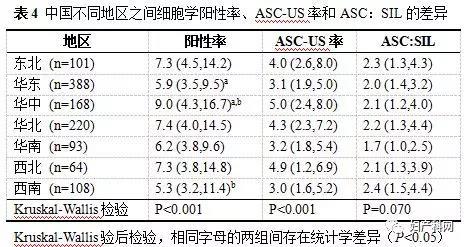
按照地区划分东北、华北、华东、华南、华中、西北和西南地区,阳性率分别为8.0 (5.0,15.5)、8.3 (4.6,15.0)、6.4 (4.0,10.7)、6.6 (4.1,10.1)、9.7 (5.0,18.4)、9.6 (4.5,19.3)和7.0 (4.0,13.5)。两两比较可见华东、华南和西南地区相对较低,而华中、东北和华北地区较高。其中华中地区实验室的阳性率与华东以及西南实验室的差异具有统计学意义(Kruskal-Wallis检验两两比较,P<0.05)。ASC-US率在华东地区判读率较低,且有统计学意义,而ASC:SIL各地区间无统计学差异。(表4)
TBS报告率已经被证实可以宏观地评估宫颈细胞学实验室的诊断质量。在美国,病理医师协会(CAP)负责认证各细胞学实验室的质控,收集各实验的TBS报告率也是其中重要的组成部分。CAP根据各实验室数据制出TBS各判读报告率的表格,方便各实验室参考。因为我们这次调查为2017年数据,所以在下述讨论中我们主要与美国2017年《CAP细胞学清单》的数据作比较(表6,7,8)。
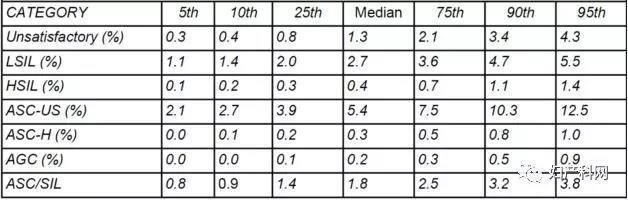
表6 CAP2017细胞学清单中的ThinPrep制片的TBS报告率
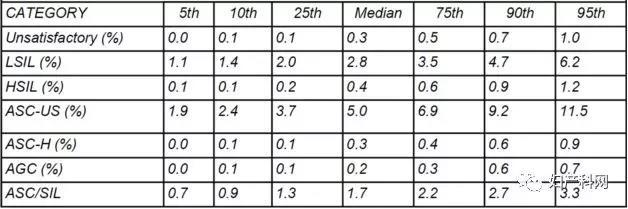
表7 CAP2017细胞学清单中的SurePath制片的TBS报告率
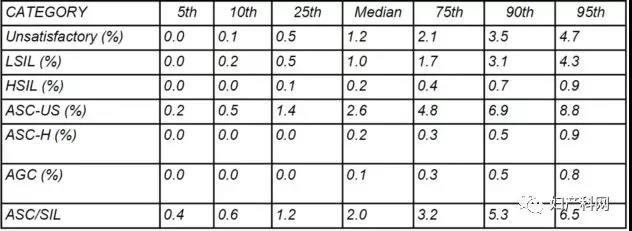
表8 CAP2017细胞学清单中的传统制片的TBS报告率
阳性率是ASC-US、ASC-H、AGC、SIL和恶性病变比例的总和。如果一个实验室的阳性率显著低于总体实验室的中位数水平,则意味着存在一定程度的漏诊率。同时,也要考虑到阳性率也受到具体筛查对象的影响,如高危人群,例如门诊病人的细胞学阳性率一定会高于普通筛查人群。通常会认为三级医院承担重病人的诊治,理应有更高的宫颈细胞学阳性检出率。然而在本次调研中,却发现二级甲等医院的阳性率中位数为9.0%,显著高于三级甲等医院的6.8%,一定程度上反映规模小的医院可能承担着相对高风险人群的筛查。还需要考虑到三甲医院质控相对严格,提高了异常判读的阈值,也可能造成这种差别出现的原因之一。按地域统计阳性率数据,可见华东和华南地区的阳性率中位数为6.4%和6.6%,低于其它地区,提示了发达地区由于筛查工作基础好,人群覆盖面广,人群的宫颈病变发生率可能较欠发达地区有所降低。提示我们的宫颈细胞学培训工作需要更多地向基层、向内陆地区倾斜。
ASC-US是不确定的宫颈细胞学判读,判读有一定主观性,不同实验室、不同病理医生对于ASC-US判读的阈值不同也可引起ASC-US报告率的差异。制片质量同样也会影响到ASC-US率。本调查结果中液基细胞与传统涂片ASC-US报告率中位数分别为3.7%和2%,与美国CAP2017公布细胞学质控清单列出的ASC-US率为5.4%(ThinPrep),5.0%(SurePath)和2.6%(CP)。相比略低,提示可以通过提高ASC-US的比例以增加细胞学筛查敏感性仍有一定的空间。因为宫颈细胞学的主要目的是筛查,在保证质控的基础上,可以提高ASC-US报告率以提高筛查的敏感性。美国的ASC-US的比例也存在逐年增高的趋势,以ThinPrep制片为例,2001年、2003年和2017年中位数分别为:2.5%、4.9%和5.4%,反映了逐渐普及的ASC-US反馈性检查HPV以及为提高检查敏感性、减少漏诊的观念对美国病理医生的影响。
ASC与SIL的比例是不确定判读与明确性判读之间的比例,反映了细胞诊断医生对鳞状上皮病变的识别能力,其优点在于比值并不会因受检人群的不同而受到影响,在不同实验室间相对恒定。美国的数据显示中位数比值为2左右,且建议高限设为3。在2017年CAP公布的数据中液基与传统涂片的中位数分别为2和1.8(ThinPrep)、1.8(SurePath)(表6,表7,表8)。我们的调查数据分别为2.1和2,非常接近于上述结果。但必须看到,我们的变异范围很大,在75百分位数的值已经超过3,而美国的液基细胞制片数据在90(ThinPrep)和95(SurePath)百分位数时才超过3。
本次调查数据中,LSIL、AGC和不满意率较低,反映出在这些疾病判读上仍旧存在困难。特别是LSIL病变,作为宫颈细胞学最易识别的病变,判读重复性理应最高,可能反映了相当比例的中国病理医生对LSIL判读标准掌握不稳,漏报了LSIL病例,或者是将很多LSIL低报为ASC-US。
腺上皮病变AGC识别较鳞状上皮病变更为困难,我们收集的数据中,液基制片的AGC判读率中位数仅为0.05%,传统涂片为中位数为0。远低于美国CAP2017报道的中位数数据:ThinPrep、SurePath和传统涂片均为0.3%。西方国家的AGC报告率在0.18%~0.74%之间。说明国内细胞学实验室对腺体病变的判读能力普遍不够。在美国一份3007例 AGC细胞学的活检随访中,仅1.9%的病例存在宫颈腺上皮病变,6.7%为内膜的不典型增生和内膜癌,20.7%为宫颈鳞状上皮病变,而70.5%活检为阴性。
不满意率低反映了国内病理医生对不满意标本的判读标准掌握不够,也可能由于不满意判读会导致医患关系的紧张。然而在不满意标本中作出阴性判读,可能会造成漏诊;即使是阳性判读,也可能诊断不足。
本次的调查,初次采集了来自全国大部分地区的宫颈细胞学现状的资料。当然,不足之处也很明显。包括填写不够仔细而造成的错误或用约数来填写导致一定程度的错误。虽然在数据整理和统计中尽可能地避免这些错误,如仔细核对、以及用中位数来避免极端值的影响。另外,未将肿瘤专科医院分开统计,因其患病人群更为集中,其TBS率与其它医院比较肯定有较大程度的偏离,所以没有相应体现。还有,本次调查主要是通过各省市的病理质控负责人推动的,一些由检验科和妇产科负责宫颈细胞学检查的单位没有得到覆盖,导致这一部分数据的缺失。总之,这是一次独立的网上问卷调查,虽然数据代表性上仍值得商榷,可能与实际情况存在偏差,但这是国内第一次的大规模、广覆盖的宫颈细胞学数据的总结,可供有兴趣的单位和个人参考。
1. 总的TBS报告率在美国CAP报告范畴之内,但LSIL、AGC和不满意率相对较低。
2. 不同地区、不同类型医院的异常细胞报告率不同。
3. 根据参与调查实验室结果看,国产液基占比最高。
4. 宫颈细胞学检查方法呈多样化趋势。液基细胞学为最主要的方法,而单纯传统涂片仅16家,占1.1%。
5. 染色方法中巴氏染色占比最高,但有36%实验室仅用HE染色或部分使用HE染色。
6. 21%参与实验室开展DNA倍体检查方法。
7. 8.4%参与调查实验室仍完全或部分采用传统巴氏5级判读术语。
8. HPV检查普遍开展,86%的参与调查单位开展HPV检测。
除了所有作者外,本次调查还得到许多热心病理医生的大力帮助,在此一并感谢。陈豹,丁永玲,郭晓静,何琼琼,胡爱侠,黄波,李建业,林静,刘爱军,刘东戈,梅平,平波,石丽华,王丽,王应霞,王志莲,吴美仙,杨开选,余俐,赵昀,张琳,张新莹,郑宝文。





























共0条评论