[导读] 编译整理:强子
PD1是表达于细胞毒性T细胞及前B细胞的表面受体,其相应配体PD-L1、PD-L2则表达于巨噬细胞、上皮细胞、其他正常细胞。正常情况下,PD1/PD-L1结合后会产生特异性构象改变,进而保护正常细胞免受免疫识别、抑制细胞毒性T细胞对其破坏。如果这一过程出现异常,则导致自身免疫,其结果就是细胞增殖和分化终止、出现程序性死亡或凋亡。
后续研究发现,某些肿瘤通过瘤细胞表面PD-L1表达的上调而使得肿瘤逃避了这种免疫监视:瘤细胞表面上调的PD-L1与活化T细胞的PD1结合,使其失活并耗竭,因此肿瘤细胞可以逃避“免疫检查点”的检查、进而继续增殖。如果阻断瘤细胞表面PD-L1与活化T细胞的PD1结合,则可以起到抑制肿瘤的作用。
目前,已批准上市、针对PD1/PD-L1通路的药物有5种:2种为针对PD-1的人源化IgG单克隆抗体,即纳武单抗(nivolumab)和派姆单抗(pembrolizumab);3种为针对PD-L1的人源化IgG单克隆抗体,即阿特珠单抗(atezolizumab)、德瓦鲁单抗(durvalumab)、阿维单抗(avelumab)。这些药物结合于相应靶点中的不同抗原表位,因此从临床角度来说,存在一定的适用病种;而从个体化角度来说,在应用之前应进行相关检测,确定具体病例是否可自相应治疗中获益。有鉴于此,病理诊断中引入了伴随诊断(companion diagnostics)和补充诊断(complementary diagnostics)的概念。
所谓伴随诊断,是告知患者可以进行某种方案的治疗,且明确患者具体适用于哪种药物。补充诊断则告知患者可自哪种治疗获益,以协助治疗决策。伴随诊断和补充诊断之间的关系有时可以相互转化,如美国食品药品管理局(Food and Drug Administration,FDA)批准的第一项伴随诊断检测是1998年提出需原位杂交检测HER2确定是否应用曲妥珠单抗,但那时候用的名称是补充诊断。由于前述PD1/PD-L1通路药物的应用中,需要根据相应标志物的表达水平来确定患者获益程度,同时不同药物对应不同的生物标志物、在不同的检测平台检测、具有不同的质控方案、评分方案等,因此目前FDA对于这类药物也均有伴随诊断的规定和要求。关于PD1/PD-L1相关免疫检查点治疗药物及相关检测要点信息,详见表1、表2。
表1. PD1/PD-L1相关免疫检查点治疗的药物、靶点、检测所用抗体
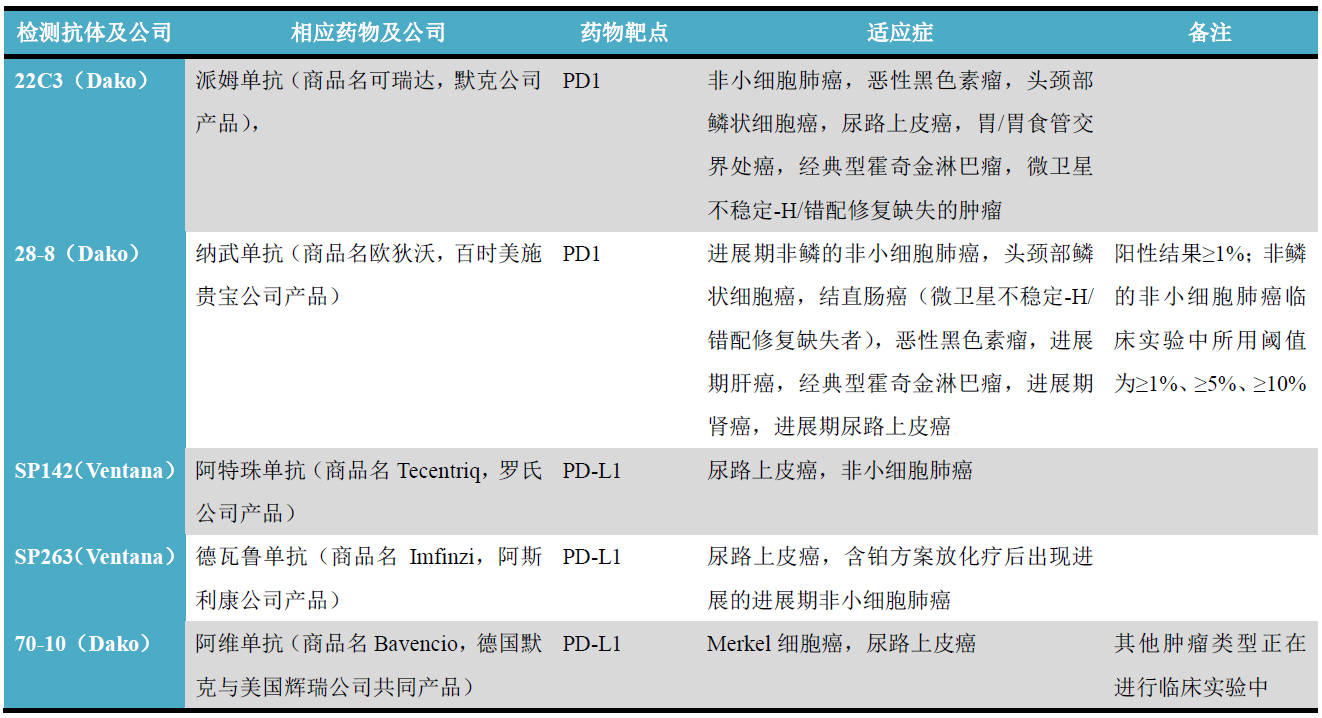
表2. PD-L1检测结果解读相关要点
 美国以癌症为重点的NeoGenomics实验室病理专家O’Malley等检索该实验室2017年1月至2018年5月数据,共计检出62896例进行了PD1/PD-L1检测的病例,排除资料不全、检测质量欠佳等情况后,作者对其余病例的检测结果、肿瘤部位、临床病史等进行了分析。文章发表于近期的美加病理学会(United States and Canadian Academy of Pathology)官方期刊《Modern Pathology》,感兴趣的同仁可以自行查阅。
美国以癌症为重点的NeoGenomics实验室病理专家O’Malley等检索该实验室2017年1月至2018年5月数据,共计检出62896例进行了PD1/PD-L1检测的病例,排除资料不全、检测质量欠佳等情况后,作者对其余病例的检测结果、肿瘤部位、临床病史等进行了分析。文章发表于近期的美加病理学会(United States and Canadian Academy of Pathology)官方期刊《Modern Pathology》,感兴趣的同仁可以自行查阅。
部分结果及图例赏析
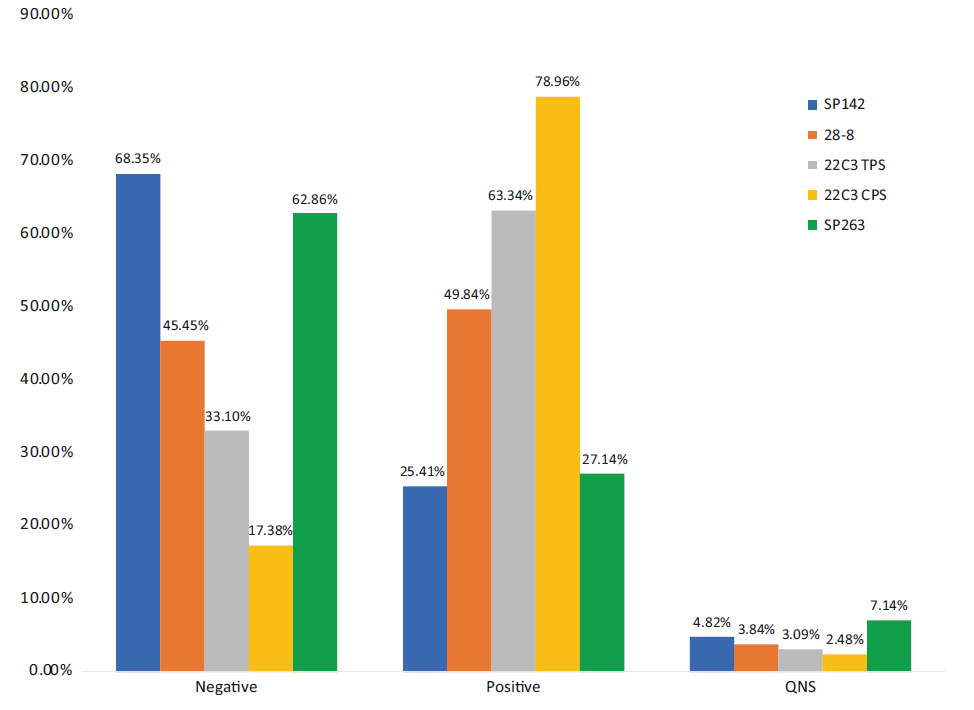 图1. 不同抗体中阴性(左列)、阳性(中间列)、质控不过关(右列)的相对比例。
图1. 不同抗体中阴性(左列)、阳性(中间列)、质控不过关(右列)的相对比例。
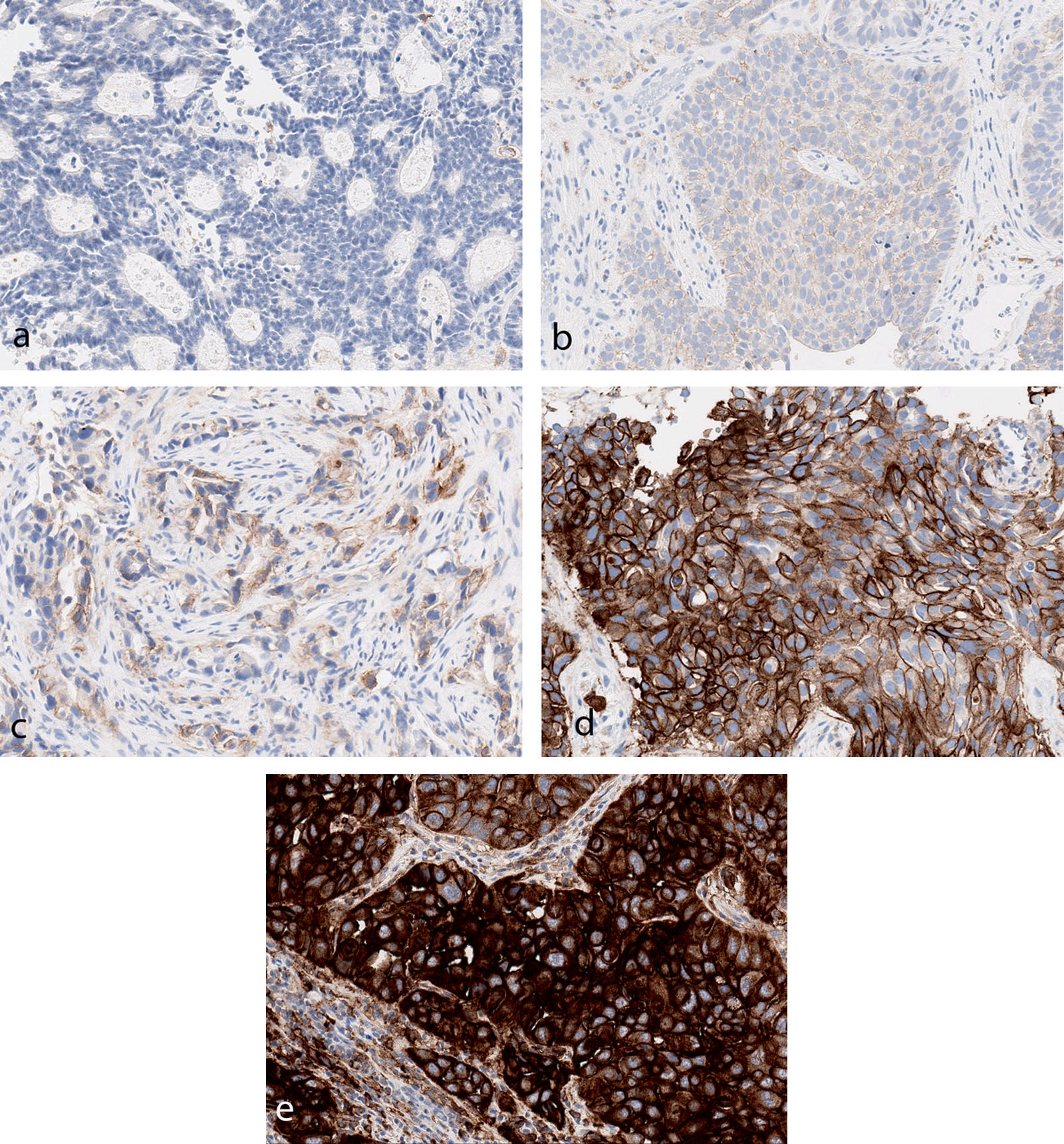 图2. 抗体22C3检测,不同结果的代表性区域着色强度:a为0,阴性;b为1+,弱阳性;c为2+,中等程度阳性;d为3+,强阳性;e也为3+,极强阳性,这种情况表现为细胞膜、胞质均一强阳性着色。尽管并不特异,但这一结果可能预示着肿瘤细胞PD-L1具有构成性过表达(constitutive overexpression)。
图2. 抗体22C3检测,不同结果的代表性区域着色强度:a为0,阴性;b为1+,弱阳性;c为2+,中等程度阳性;d为3+,强阳性;e也为3+,极强阳性,这种情况表现为细胞膜、胞质均一强阳性着色。尽管并不特异,但这一结果可能预示着肿瘤细胞PD-L1具有构成性过表达(constitutive overexpression)。
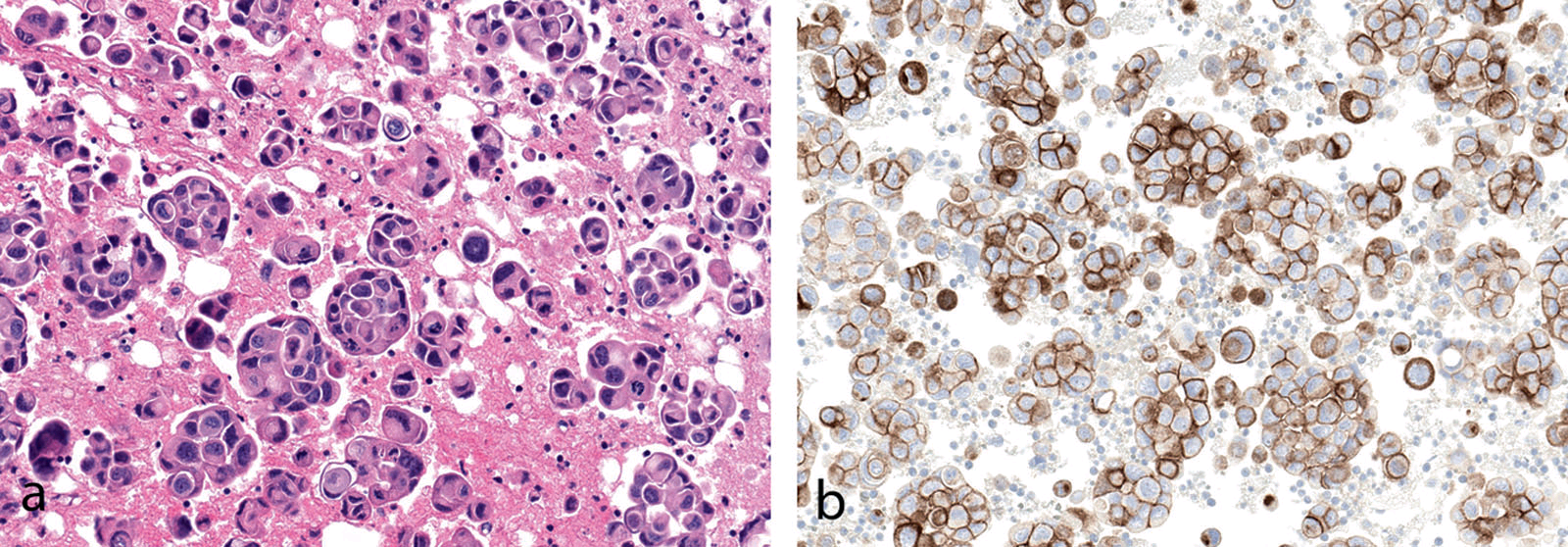 图3. 心包积液中的腺癌,抗体22C3检测,肿瘤细胞具有PD-L1的表达。
图3. 心包积液中的腺癌,抗体22C3检测,肿瘤细胞具有PD-L1的表达。
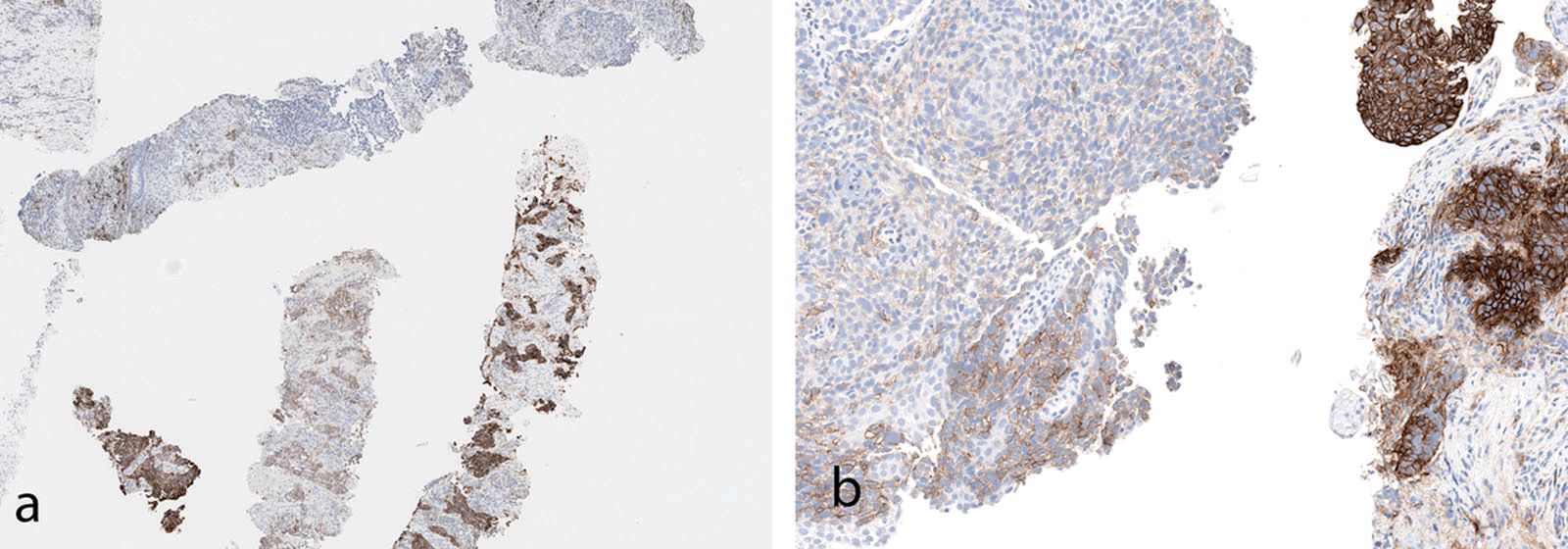 图4. 抗体22C3检测,肿瘤内PD-L1免疫着色强度不均一,该图中0至3+结果均有。
图4. 抗体22C3检测,肿瘤内PD-L1免疫着色强度不均一,该图中0至3+结果均有。
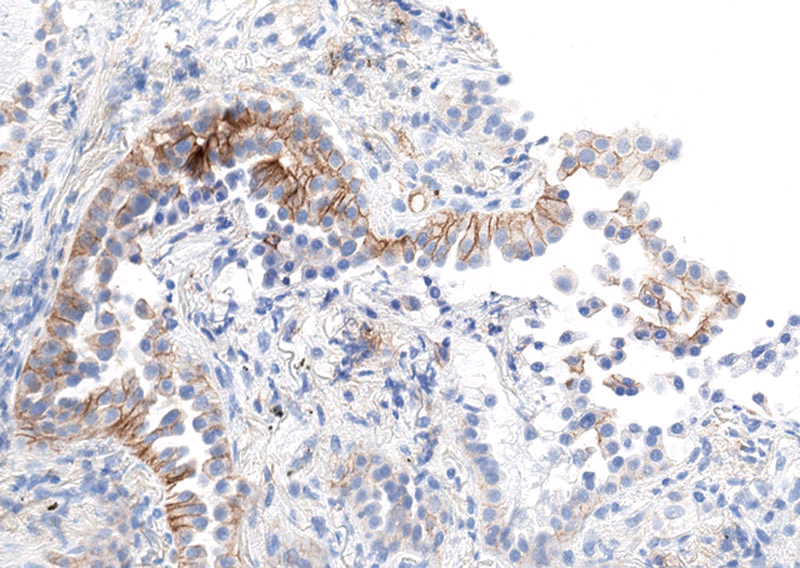 图5. PD-L1检测中,部分细胞膜着色,腔面并无着色,这种情况仍视为阳性。
图5. PD-L1检测中,部分细胞膜着色,腔面并无着色,这种情况仍视为阳性。
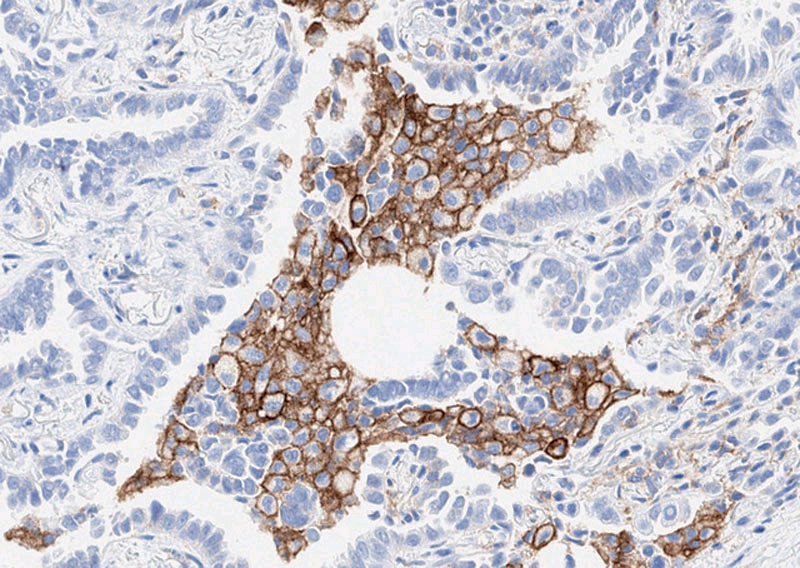 图6. PD-L1检测,腺腔内巨噬细胞具有3+的强阳性着色,而肿瘤性腺细胞并无着色;该图中所用抗体为22C3。
图6. PD-L1检测,腺腔内巨噬细胞具有3+的强阳性着色,而肿瘤性腺细胞并无着色;该图中所用抗体为22C3。
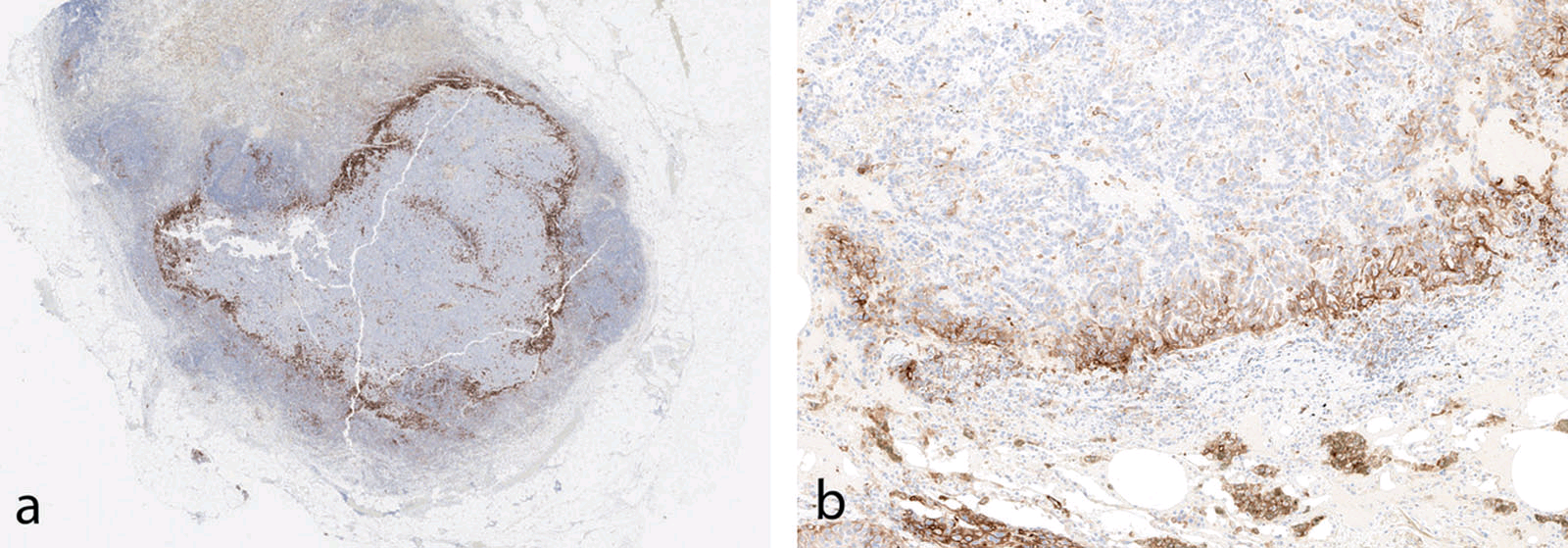 图7. 肿瘤转移至淋巴结时PD-L1染色结果,低倍镜下可见肿瘤与非肿瘤之间有分界,免疫细胞也有着色;高倍镜下仔细观察,可见交界处阳性为免疫细胞及肿瘤细胞,远离交界处的肿瘤细胞为阴性。该图中所用抗体为22C3。
图7. 肿瘤转移至淋巴结时PD-L1染色结果,低倍镜下可见肿瘤与非肿瘤之间有分界,免疫细胞也有着色;高倍镜下仔细观察,可见交界处阳性为免疫细胞及肿瘤细胞,远离交界处的肿瘤细胞为阴性。该图中所用抗体为22C3。
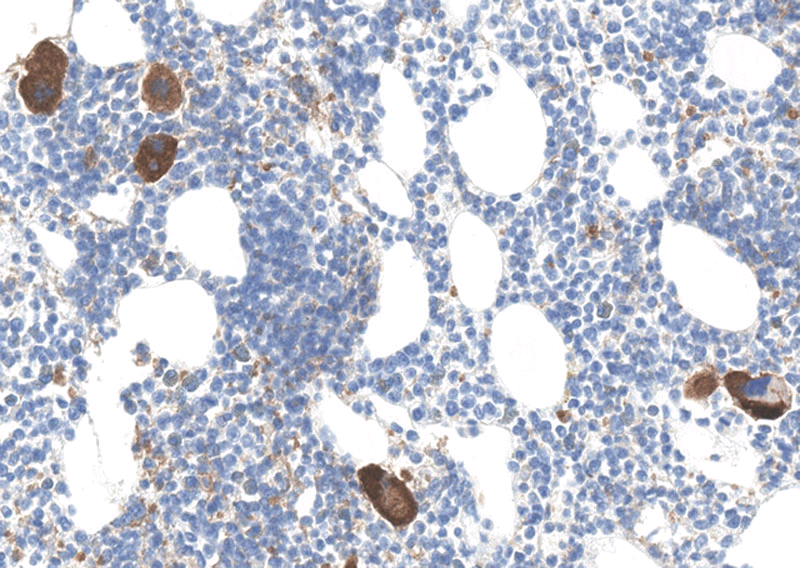 图8. PD-L1检测中巨核细胞呈胞质强阳性,该图中所用抗体为22C3,但所有抗体中均有此着色结果出现。
图8. PD-L1检测中巨核细胞呈胞质强阳性,该图中所用抗体为22C3,但所有抗体中均有此着色结果出现。
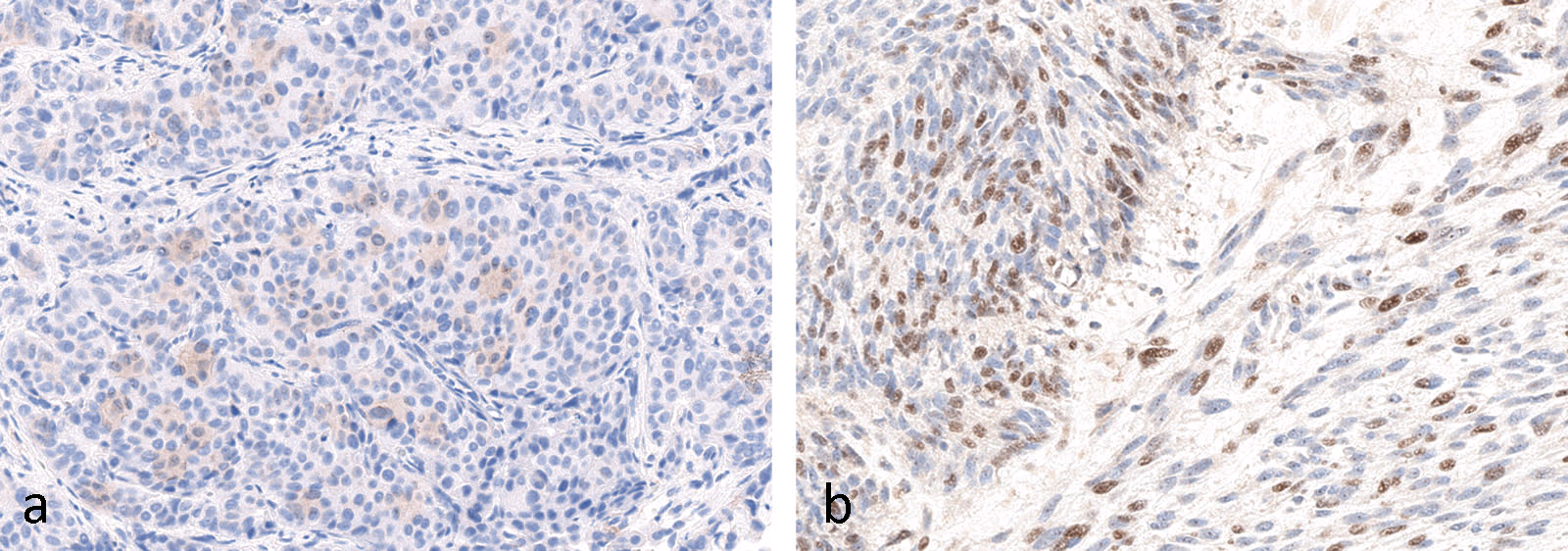 图9. a:乳腺癌中PD-L1呈胞质纤细着色,此时并不认为是真正的阳性;b:PD-L1检测中的细胞核着色,这在任何检测系统中,都不认为是真正的阳性着色。该图中所用抗体为22C3。
图9. a:乳腺癌中PD-L1呈胞质纤细着色,此时并不认为是真正的阳性;b:PD-L1检测中的细胞核着色,这在任何检测系统中,都不认为是真正的阳性着色。该图中所用抗体为22C3。
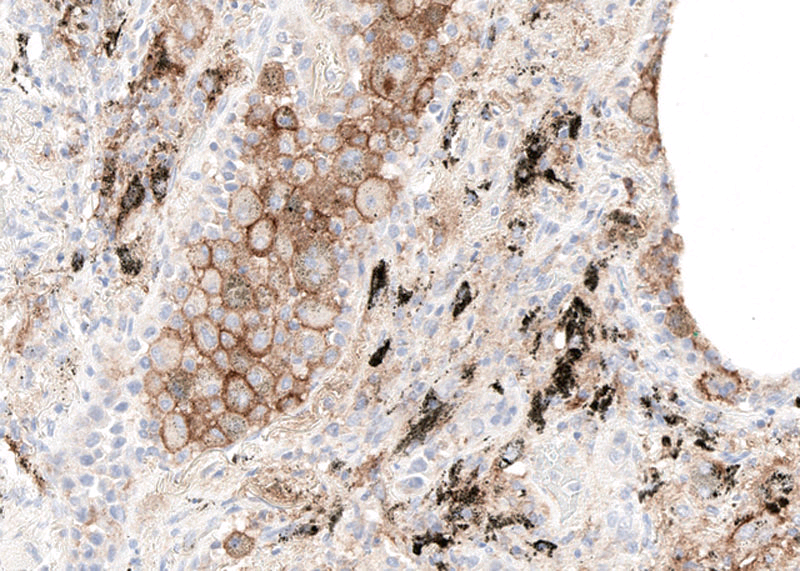 图10. PD-L1检测中,碳末(黑色所示)及巨噬细胞着色,肿瘤细胞并无着色;该图中所用抗体为22C3。
图10. PD-L1检测中,碳末(黑色所示)及巨噬细胞着色,肿瘤细胞并无着色;该图中所用抗体为22C3。
点击下载英文文献
参考文献
O'Malley DP,Yang Y,Boisot S,et al.Immunohistochemical detection of PD-L1 among diverse human neoplasms in a reference laboratory: observations based upon 62,896 cases[J].Modern Pathology ,2019.
DOI:10.1038/s41379-019-0210-3






 美国以癌症为重点的NeoGenomics实验室病理专家O’Malley等检索该实验室2017年1月至2018年5月数据,共计检出62896例进行了PD1/PD-L1检测的病例,排除资料不全、检测质量欠佳等情况后,作者对其余病例的检测结果、肿瘤部位、临床病史等进行了分析。文章发表于近期的美加病理学会(United States and Canadian Academy of Pathology)官方期刊《Modern Pathology》,感兴趣的同仁可以自行查阅。
美国以癌症为重点的NeoGenomics实验室病理专家O’Malley等检索该实验室2017年1月至2018年5月数据,共计检出62896例进行了PD1/PD-L1检测的病例,排除资料不全、检测质量欠佳等情况后,作者对其余病例的检测结果、肿瘤部位、临床病史等进行了分析。文章发表于近期的美加病理学会(United States and Canadian Academy of Pathology)官方期刊《Modern Pathology》,感兴趣的同仁可以自行查阅。 图1. 不同抗体中阴性(左列)、阳性(中间列)、质控不过关(右列)的相对比例。
图1. 不同抗体中阴性(左列)、阳性(中间列)、质控不过关(右列)的相对比例。 图2. 抗体22C3检测,不同结果的代表性区域着色强度:a为0,阴性;b为1+,弱阳性;c为2+,中等程度阳性;d为3+,强阳性;e也为3+,极强阳性,这种情况表现为细胞膜、胞质均一强阳性着色。尽管并不特异,但这一结果可能预示着肿瘤细胞PD-L1具有构成性过表达(constitutive overexpression)。
图2. 抗体22C3检测,不同结果的代表性区域着色强度:a为0,阴性;b为1+,弱阳性;c为2+,中等程度阳性;d为3+,强阳性;e也为3+,极强阳性,这种情况表现为细胞膜、胞质均一强阳性着色。尽管并不特异,但这一结果可能预示着肿瘤细胞PD-L1具有构成性过表达(constitutive overexpression)。 图3. 心包积液中的腺癌,抗体22C3检测,肿瘤细胞具有PD-L1的表达。
图3. 心包积液中的腺癌,抗体22C3检测,肿瘤细胞具有PD-L1的表达。 图4. 抗体22C3检测,肿瘤内PD-L1免疫着色强度不均一,该图中0至3+结果均有。
图4. 抗体22C3检测,肿瘤内PD-L1免疫着色强度不均一,该图中0至3+结果均有。 图5. PD-L1检测中,部分细胞膜着色,腔面并无着色,这种情况仍视为阳性。
图5. PD-L1检测中,部分细胞膜着色,腔面并无着色,这种情况仍视为阳性。 图6. PD-L1检测,腺腔内巨噬细胞具有3+的强阳性着色,而肿瘤性腺细胞并无着色;该图中所用抗体为22C3。
图6. PD-L1检测,腺腔内巨噬细胞具有3+的强阳性着色,而肿瘤性腺细胞并无着色;该图中所用抗体为22C3。 图7. 肿瘤转移至淋巴结时PD-L1染色结果,低倍镜下可见肿瘤与非肿瘤之间有分界,免疫细胞也有着色;高倍镜下仔细观察,可见交界处阳性为免疫细胞及肿瘤细胞,远离交界处的肿瘤细胞为阴性。该图中所用抗体为22C3。
图7. 肿瘤转移至淋巴结时PD-L1染色结果,低倍镜下可见肿瘤与非肿瘤之间有分界,免疫细胞也有着色;高倍镜下仔细观察,可见交界处阳性为免疫细胞及肿瘤细胞,远离交界处的肿瘤细胞为阴性。该图中所用抗体为22C3。 图8. PD-L1检测中巨核细胞呈胞质强阳性,该图中所用抗体为22C3,但所有抗体中均有此着色结果出现。
图8. PD-L1检测中巨核细胞呈胞质强阳性,该图中所用抗体为22C3,但所有抗体中均有此着色结果出现。 图9. a:乳腺癌中PD-L1呈胞质纤细着色,此时并不认为是真正的阳性;b:PD-L1检测中的细胞核着色,这在任何检测系统中,都不认为是真正的阳性着色。该图中所用抗体为22C3。
图9. a:乳腺癌中PD-L1呈胞质纤细着色,此时并不认为是真正的阳性;b:PD-L1检测中的细胞核着色,这在任何检测系统中,都不认为是真正的阳性着色。该图中所用抗体为22C3。 图10. PD-L1检测中,碳末(黑色所示)及巨噬细胞着色,肿瘤细胞并无着色;该图中所用抗体为22C3。
图10. PD-L1检测中,碳末(黑色所示)及巨噬细胞着色,肿瘤细胞并无着色;该图中所用抗体为22C3。







共0条评论