编译整理:强子
1979年,Agnatis及Rosen首次描述了间质伴破骨细胞样巨细胞的乳腺癌。该肿瘤约占乳腺癌的0.5-1.2%。其具体起源仍有一定争议,但免疫组化提示这些巨细胞为良性组织细胞来源。伴破骨细胞样巨细胞的浸润性乳腺癌大部分为浸润性导管癌,其他亚型也有个案报道,但浸润性小叶癌则极少。西班牙病理学家Peña-Jaimes等在《Diagnostic Pathology》报道了一例伴破骨细胞样巨细胞的乳腺多形性小叶癌,并结合文献进行了讨论。为拓宽大家对该类病变的视野,我们将该文编译介绍如下。
病例展示
患者女性,72岁,一月前发现左乳肿物并伴烧灼感入院。乳腺钼靶检查见左乳内上象限结节状密度增高影,考虑为恶性,BI-RADS-5。超声为低回声不规则包块,大小约23×14mm,境界不清。同侧腋窝淋巴结未见显著异常。粗针穿刺活检证实为恶性,行左乳肿物切除并前哨淋巴结活检。
大体检查,可见两个相邻病灶,合计约28×17mm。病变境界不清,灰白色,中央质软、棕红色。乳头及乳晕周围未见显著病变。组织学检查,两处病灶、取材6张切片,镜下表现一致。肿瘤富于细胞,细胞黏附性差,呈片状排列。胞质丰富,细胞核异型性显著。病灶中可见大量破骨巨细胞样多核细胞,其中的细胞核形态均一;可见吞噬含铁血黄素的巨噬细胞。间质疏松,血管丰富,局灶可见出血及慢性炎症细胞浸润。浸润性肿瘤周边可见部分原位癌区域。
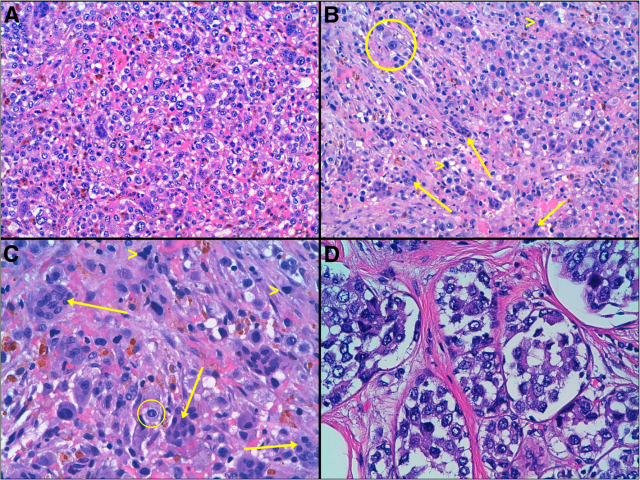
图1. (A)肿瘤富于细胞,间质血管丰富,可见出血、吞噬含铁血黄素的巨噬细胞及慢性炎症细胞浸润;(B)(C)高倍观,可见大量破骨细胞样巨细胞,形态及大小不一;(D)局灶可见原位癌成分。
术中常规检查前哨淋巴结共3枚,其中1枚行一步法核酸扩增检查,结果提示转移。因此行同侧腋窝淋巴结清扫,但清扫出的14枚淋巴结未见转移。
免疫组化证实肿瘤为上皮来源,瘤细胞表达AE1/AE3、CK19。由于肿瘤细胞黏附性差,因此做了E-cadherin,结果证实原位癌区域及浸润性癌区域均为表达缺失。巨细胞成分不表达CK,但组织细胞标记CD68强阳性。肿瘤中90%的细胞ER强阳性,PR阴性,HER2无过表达;Ki-67增殖指数约18%。同时本例进行了CDH1(编码E-cadherin蛋白)基因相关检测,证实有缺失突变(C. del866C)。
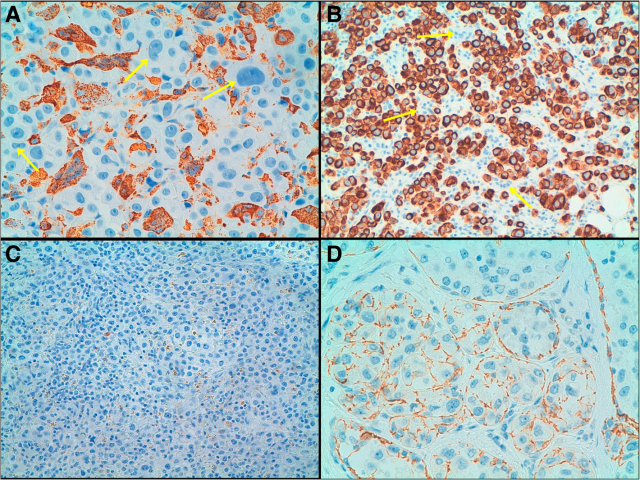
图2. 免疫组化。A:破骨细胞样巨细胞表达CD68,而肿瘤细胞不表达(箭头所示);B:肿瘤细胞表达AE1/AE3,而破骨细胞样巨细胞不表达(箭头所示)。浸润性成分(C)及原位癌成分(D)均为E-cadherin完全缺失。
综合上述结果,最终诊断为伴破骨细胞样巨细胞的浸润性多形性小叶癌,组织学分级3级。患者参与了一项绝经后女性乳腺癌患者术后他莫昔芬联合或不联合化疗的研究,并被随机分配至仅激素治疗组。术后2年随访,患者情况良好,未见复发或转移迹象。
讨论
本例由于肿瘤呈弥漫性生长,且伴大量炎症细胞及破骨细胞样巨细胞,因此鉴别诊断需考虑到淋巴系统肿瘤及间叶性肿瘤。因此CK表达证实该肿瘤为上皮源性对于确诊非常重要。原位癌成分和浸润性癌成分中E-cadherin表达均缺失,证实该肿瘤为小叶癌。巨细胞成分CD68阳性,则证实这些细胞为组织细胞来源。
伴破骨细胞样巨细胞的乳腺癌很少见,自首例报道以来仅约200余例,其中最多见的组织学亚型为浸润性导管癌,而浸润性小叶癌据作者所述,仅7例报道,其中5例为经典型浸润性小叶癌,2例为腺泡型浸润性小叶癌;2例为浸润性导管癌及浸润性小叶癌混合并伴破骨细胞样巨细胞;不过,需要指出的是此前报道均未通过免疫组化检测E-cadherin或基因检测CDH1的方法证实。
乳腺癌中伴破骨细胞样巨细胞的预后意义仍有争议,有研究者认为可能预后会差,而有作者认为这一现象并不影响预后、甚至预后会更好。不过,本文作者认为相关预后更多的取决于癌的类型,而并非破骨细胞样巨细胞的有无。
Tips:
Ø 间质伴破骨细胞样巨细胞的乳腺癌罕见;相关报道中多为浸润性导管癌,浸润性小叶癌者更是极为罕见
Ø 乳腺小叶癌的诊断,需结合细胞学特征、生长方式、免疫组化来综合判断
Ø 这种情况下破骨细胞样巨细胞的形成机制仍不清楚,但大部分报道均支持其非上皮性、间质组织细胞来源
Ø 破骨细胞样巨细胞对预后的影响仍有争议;本文作者及相关研究表明影响预后更显著的可能是癌的类型,而并非破骨细胞样巨细胞的有无
Ø 对该肿瘤的生物学行为、合适治疗方案等,仍需进一步研究
点击下载英文文献
参考文献
Peña-Jaimes L,González-García I,Reguero-Callejas ME,et al.Pleomorphic lobular carcinoma of the breast with osteoclast-like giant cells: a case report and review of the literature[J].Diagnostic pathology,2018,13(1):62.
DOI:10.1186/s13000-018-0744-6















共0条评论